肺隐球菌病(pulmonary cryptococcosis, PC)是通过吸入隐球菌孢子引起的亚急性或慢性肺真菌病[1]。近年来发病率逐年上升, 已成为仅次于白色念珠菌、曲霉菌的第三大类肺真菌病[2]。既往认为, PC常见于免疫功能低下的患者[3], 但近年来在免疫功能正常人群肺隐球菌病的发病率逐渐增加, 加之其临床症状无明显特异性、胸部影像学表现多样, 故常被误诊为细菌性肺炎、肺结核、肺癌等疾病, 往往需要通过有创检查如肺穿刺活检甚至手术后病理加特染、组织培养明确诊断, 但还会出现组织病理学与隐球菌抗原检测不一致、无法行有创检查获得组织病理的情况, 导致临床上肺隐球菌病常常被误诊或漏诊; 此外, 对肺隐球菌病指南尚无明确的诊断分级标准。因此, 提高对肺隐球菌病的认识、减少有创检查的诊断方法具有重要意义。本文回顾性分析24例肺隐球菌患者的临床特征, 探讨其诊断策略, 以期提高对肺隐球菌病的认识及临床诊断水平。
1 资料与方法收集本院2012年2月至2019年7月诊断的肺隐球菌病24例, 对患者临床特征(如年龄、性别、免疫状况、临床表现、影像学、隐球菌抗原、病理等)及诊断进行回顾性分析。
1.1 入选病例诊断标准参照2010年美国感染病学会更新的《隐球菌病治疗临床实践指南》[4]及2017年《肺隐球菌病诊治浙江省专家共识》[5], 肺隐球菌病的诊断要点包括:①临床症状、影像学; ②隐球菌抗原检测; ③病理组织学:HE、六胺银、AB/PAS染色; ④隐球菌病原学检测:痰、BALF培养、肺组织培养出隐球菌(金标准)。近年来, 二代测序(next generation sequencing, NGS)亦用于病原学检测[6]。
入选病例符合上述诊断要点①和其他要点1条及以上。符合全部肺隐球菌病诊断要点的即确诊; 临床特征及影像学需考虑肺隐球菌病, 隐球菌抗原阳性、病理组织学(含特染)发现圆形隐球菌菌体可临床诊断(即①+②+③); 临床特征及影像学需考虑肺隐球菌病, 对隐球菌抗原与病理组织学(含特染)仅有一项阳性时可拟诊(即①+②或①+③)。对于拟诊的患者给予氟康唑诊断性治疗(400 mg, 1次/d, 1~2周)。
1.2 影像学分析患者均行胸部CT检查。主要分析胸部CT的病灶分布、形态、边缘及伴随征象等。包括边缘是否光滑, 有无分叶及毛刺征象, 有无晕征及空洞, 有无胸膜受累等, 伴随征象包括胸腔积液、肺门或纵隔淋巴结肿大等。
1.3 隐球菌抗原检测及病理活检采用血液胶体金免疫层析法行隐球菌抗原检测; 采用经皮肺穿刺活检行组织病理检查(其中1例为手术后病理诊断), 加用AB/PAS染色或银染。
1.4 病原学检测痰、纤支镜肺泡灌洗液及组织培养。
2 结果 2.1 患者一般资料及主要临床表现本研究经医院伦理委员会核准, 入选对象均签署知情同意书。24例患者中男性14例, 女性10例; 年龄25~67岁, 平均46岁。无免疫功能抑制患者较多, 有20例(83.3%); 仅4例患者合并免疫抑制基础疾病, 其中1例合并系统性红斑狼疮, 1例可疑HIV感染, 1例为肾移植术后使用免疫抑制剂患者, 1例合并肺癌, 在EGFR-TKI靶向治疗过程中出现胸膜下新发结节疑肺癌进展经活检明确并抗隐球菌治疗病灶吸收。3例患者合并慢性基础病, 其中2例合并高血压, 1例合并慢性乙型病毒性肝炎。15例患者起病时有临床症状, 9例为咳嗽、干咳或少量白痰, 其中有3例分别合并胸痛、发热、气促; 3例仅表现为胸痛, 1例仅表现为发热, 1例仅表现为气促, 但症状较轻微; 9例无临床症状, 为体检发现。
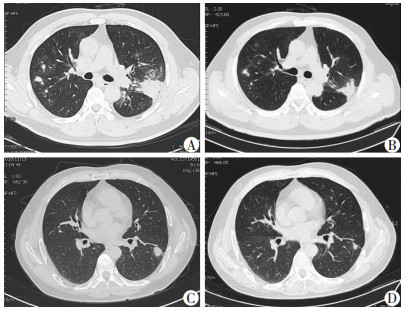
2.2 影像学特征24例肺隐球菌病患者胸部CT表现如下:①单发或多发结节或肿块多见, 有13例(54.1%), 病变多位于两中下肺, 其中单发结节8例, 多发结节5例, 其中2例结节内可见空洞, 部分结节可有晕征, 位于胸膜下(图 1); ②4例(16.7%)表现为单发或多发斑片影、片块影, 病变多分布在肺外带, 邻近或累及胸膜, 呈均匀中等程度强化, 外缘轻度膨隆, 2例合并有近端支气管充气征, 3例病变周围有晕征(图 2); ③7例(29.2%)表现混合性病灶, 为斑片实变影或片块影与结节混合, 3例在实变影或片块影同一病灶内出现空气支气管征和小局灶坏死区并存(图 3); ④2例(8.3%)合并少量胸腔积液(图 4)。
|
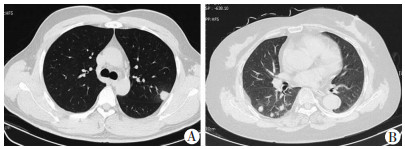
| A:左上肺单发结节; B:右下肺多发结节, 病灶多位于胸膜下, 晕征 图 1 肺隐球菌病胸部CT见单发结节与多发结节 |
|
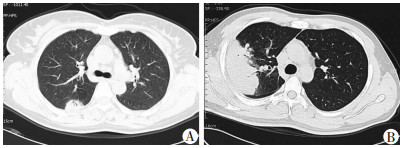
| A:右上肺近胸膜下斑片影; B:右上肺片块状高密度影, 累及胸膜, 边缘轻度膨隆, 可见近端支气管充气征 图 2 肺隐球菌病胸部CT见斑片影与片块影 |
|
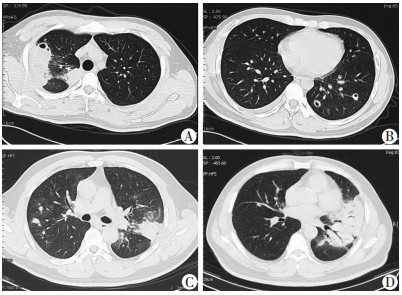
| A:右上肺斑片实变影边缘模糊, 内有小局灶坏死区; B:左下肺散在结节影, 部分结节内可见空洞; C:左下肺斑片、片状高密度影, 近端支气管充气征; D:右肺散在大小不等结节影; A、B及C、D分别为同一病例 图 3 肺隐球菌病胸部CT见斑片实变影或片块影与结节混合 |
|
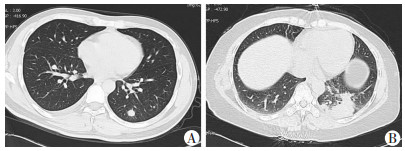
| A:右侧少量胸腔积液; B:双侧少量胸腔积液 图 4 肺隐球菌病胸部CT见胸腔积液 |
2.3 隐球菌抗原检测、病理及病原学 2.3.1 隐球菌抗原
24例患者中有21例行胶体金隐球菌抗原检测, 其中20例为阳性(95.2%, 20/21)。另有3例因就诊时医院未开展此项目故未行检测。
2.3.2 病理组织学24例患者中, 15例行病理检查, 其中14例行肺活检, 1例为手术后病理诊断。病理主要表现为慢性肉芽肿性炎伴坏死、纤维组织增生或多核巨细胞形成等, 仅8例见圆形隐球菌菌体(53%, 8/15)。12例病理加做碘酸雪夫(PAS)染色, 其中2例同时行银染, 结果9例PAS阳性(75%, 9/12, 其中2例PAS及六胺银染色均阳性)。病理组织学阳性率为80%(12/15)。
2.3.3 病原学检测本组24例患者, 仅有9例有咳嗽症状, 但多为干咳或少量白痰, 3例行纤支镜检查, 痰及肺泡灌洗液病原学检测均阴性; 1例患者肺穿刺活检组织培养出新型隐球菌。
2.4 诊断情况① 本组病例仅1例符合全部肺隐球菌病诊断要点, 即确诊; ②本组共有9例患者满足临床诊断条件; ③本组共有10例患者符合拟诊条件, 其中9例未行活检但隐球菌抗原阳性, 1例病理组织学阳性隐球菌抗原阴性, 均给予“氟康唑400 mg, 1次/d”诊断性治疗(病灶广泛、有临床症状者住院期间静脉滴注, 其余情况氟康唑胶囊口服), 1~2周后复查胸部CT即可观察到病灶吸收好转(图 5), 9例观察有效; ④位于结核好发部位病灶, PPD强阳性、γ-干扰素释放试验(IGRA)阳性, 病理为肉芽肿性炎, 但病理组织特染PAS阳性及隐球菌抗原支持肺隐球菌病时, 应仔细观察其影像表现, 如为胸膜下病灶、有晕征而无结核其他影像表现如纤维化、钙化灶时, 可采用氟康唑诊断性治疗(图 6)。本组有6例给予氟康唑诊断性治疗, 5例有效, 1例失访。
|
| A、B:未行病理活检, 隐球菌荚膜抗原阳性, 给予氟康唑400 mg/d静滴1周; C、D:病理活检示慢性肉芽肿性炎, PAS(-), 隐球菌荚膜抗原阳性, 氟康唑胶囊口服2周病灶明显吸收 图 5 仅病理或隐球菌抗原阳性氟康唑诊断性治疗前后肺隐球菌病胸部CT |

|
| A:2017年9月18日; B:2017年10月27日; 胸部CT可见左肺上叶后段胸膜下结节影, 可见晕征; PPD(+++)、IGRA阳性, 病理为肉芽肿性炎伴纤维组织增生, PAS阳性, 隐球菌抗原阳性; 口服氟康唑治疗2周后病灶明显吸收 图 6 同时具有肺结核及肺隐球菌病诊断依据时氟康唑诊断治疗前后肺隐球菌病胸部CT |
3 讨论
近年来肺隐球菌病发病率逐渐升高, 但由于其临床症状、胸部影像学无特异性, 关键诊断要点之一的病理组织学及组织病原学检查为有创检查, 增加了临床诊断难度。本研究回顾性分析了24例肺隐球菌病的临床特征及诊断方法, 探讨其诊断策略, 以期提高对肺隐球菌病的认知和诊断水平。
3.1 无免疫功能抑制的肺隐球菌病常见既往认为, 肺隐球菌病多发生在免疫功能抑制的患者, 但近年来免疫正常人群肺隐球菌病的病例逐渐增多[7]。本组24例患者中, 20例免疫功能均正常, 仅4例合并免疫功能抑制基础疾病, 提示我们在临床工作中不能因为无免疫抑制基础或免疫功能正常而放松对肺隐球菌病的警惕, 导致误诊或延迟诊断。
3.2 肺隐球菌病的临床症状无特异性且相对于影像表现轻微肺隐球菌病主要表现为咳嗽、少痰、胸痛、发热、咯血、气促少见, 且相对轻微。特别对于免疫正常人群, 文献报道[8]仅20%患者有症状, 且无明显体征。本组患者中, 15例起病时有临床症状, 但缺乏特异性, 且相对于肺部影像表现轻微, 9例为体检发现, 无临床症状。与文献报道一致。
3.3 胸部影像学表现在肺隐球菌的诊断中具有重要价值肺隐球菌病影像表现多样, 主要有:单发或多发结节或肿块; 单发或多发斑片影; 斑片实变影与结节肿块混合病灶; 晕征、近端支气管通气征等。病灶多位于肺野外带, 邻近或累及胸膜, 均匀中等程度强化[9]。姚克林等[10]认为混合型多形态病灶有一定特征性, 同一病灶内出现空气支气管征和小局灶坏死区并存的现象可能是肺隐球菌病的特征表现。本组患者中, 有13例仅表现为单发或多发结节, 此类患者多为体检时发现, 无免疫抑制基础疾病及临床症状, 这可能与患者免疫功能正常, 病变易形成肉芽肿而不易播散有关[11]; 4例表现为单发或多发斑片影、片块影, 病变多分布在肺外带, 邻近或累及胸膜, 呈均匀中等程度强化, 外缘轻度膨隆, 2例合并有近端支气管充气征, 有3例病变周围有晕征; 7例表现混合性病灶, 为斑片实变影或片块影与结节混合, 有3例在实变影或片块影同一病灶内出现空气支气管征和小局灶坏死区并存。综合文献及本组患者胸部CT表现, 我们认为:单发或多发胸膜下尤其是有晕征的结节, 位于肺外带邻近或累及胸膜、外缘轻度膨隆伴近端支气管通气征的片块影、混合型病灶是肺隐球菌病相对特异的影像表现。
3.4 隐球菌抗原检测对诊断具有重要意义, 阳性者可给予氟康唑诊断性治疗既往隐球菌抗原检测多采用乳胶凝集法或酶联免疫法, 其特异性及敏感性较低, 通过该方法临床诊断病例较少。近年来, 胶体金隐球菌抗原检测由于特异性及敏感性强、操作简单且无创、10 min即可出结果, 已广泛用于临床[12], 在临床及影像学考虑肺隐球菌病时可作为重要的筛查依据。我院自2017年开展胶体金层析法查隐球菌抗原, 本组24例患者中, 有20例是开展此项目后诊断的, 隐球菌抗原检测阳性率为95.2%(20/21)。对于临床疑诊肺隐球菌病的患者未行活检, 或病理未提示隐球菌感染但隐球菌抗原阳性, 给予氟康唑诊断性治疗有效可协助诊断。本组病例中9例未行肺穿刺病理检测, 隐球菌抗原阳性, 给予氟康唑诊断性治疗有效。《肺隐球菌病诊治浙江省专家共识》也有此推荐[5]。
3.5 组织病理学阳性者也可给予氟康唑诊断性治疗, 但其阳性率较隐球菌抗原低组织病理学检查是肺隐球菌病的重要诊断依据。无法排除肺部肿瘤的患者, 建议肺穿刺活检。肺隐球菌病组织病理学表现主要为慢性肉芽肿性炎伴坏死、纤维组织增生或多核巨细胞形成等。由于HE染色仅部分可看到隐球菌圆形菌体, 因此, 需加用特染如AB/PAS、六胺银染色等, 必要时行组织培养。本组24例患者中, 15例行病理检查, 仅8例HE染色见圆形隐球菌菌体(53%, 8/15), 12例行组织PAS染色, 结果9例PAS阳性(75%, 9/12), 1例同时组织培养为新型隐球菌[13]。组织病理阳性率明显低于隐球菌抗原检测阳性率(95.2%)。其中1例患者病理组织学阳性隐球菌抗原阴性, 给予氟康唑诊断性治疗有效。
综上, 我们认为肺隐球菌病可采取如下诊断策略:①不能因为无免疫抑制基础疾病或免疫功能正常而放松警惕, 导致误诊或延迟诊断; ②症状轻而肺部病变重、影像学具有肺隐球菌病相对特征表现, 或当抗炎、甚至抗结核治疗无效且又不支持肿瘤诊断时, 应警惕肺隐球菌病可能; ③临床及胸部影像学高度怀疑肺隐球菌病患者应筛查隐球菌抗原, 阳性者给予氟康唑治疗可协助诊断, 从而减少有创检查甚至避免手术; 隐球菌抗原阴性或影像学不能排除肺癌的患者, 行组织病理学及病原学检查明确诊断; ④仅病理学支持而隐球菌抗原阴性的患者, 可采用氟康唑诊断性治疗; ⑤对于结核好发部位病灶, 结核及隐球菌病诊断依据都较充分时, 只要胸部CT符合肺隐球菌病相对特征表现, 采用氟康唑诊断性治疗短期内即可鉴别。
| [1] |
HUNG M S, TSAI Y H, LEE C H, et al. Pulmonary cryptococcosis: Clinical, radiographical and serological markers of dissemination[J]. Respirology, 2008, 13(2): 247-251. DOI:10.1111/j.1440-1843.2007.01202.x |
| [2] |
GULLO F P, ROSSI S A, SARDI J D E C, et al. Cryptococcosis: epidemiology, fungal resistance, and new alternatives for treatment[J]. Eur J Clin Microbiol Infect Dis, 2013, 32(11): 1377-1391. DOI:10.1007/s10096-013-1915-8 |
| [3] |
YAMAKAWA H, YOSHIDA M, YABE M, et al. Correlation between clinical characteristics and chest computed tomography findings of pulmonary cryptococcosis[J]. Pulm Med, 2015, 2015: 703407. DOI:10.1155/2015/703407 |
| [4] |
PERFECT J R, DISMUKES W E, DROMER F, et al. Clinical practice guidelines for the management of cryptococcal disease: 2010 update by the infectious diseases society of America[J]. Clin Infect Dis, 2010, 50(3): 291-322. DOI:10.1086/649858 |
| [5] |
浙江省医学会呼吸病学分会. 肺隐球菌病诊治浙江省专家共识[J]. 中华临床感染病杂志, 2017, 10(5): 321-326. Respiratory Branch of Zhejiang Medical Association. Expert consensus on diagnosis and treatment of pulmonary cryptococcosis[J]. Chin J Clin Infect Dis, 2017, 10(5): 321-326. DOI:10.3760/cma.j.issn.1674-2397.2017.05.001 |
| [6] |
王芳, 马海畅, 王晓娟, 等. 脑脊液宏基因组测序技术在隐球菌性脑膜炎中的应用分析[J]. 河南医学研究, 2019, 28(15): 2718-2720. WANG F, MA H C, WANG X J, et al. Application analysis of CSF sequencing technology in cryptococcal meningitis[J]. Henan Med Res, 2019, 28(15): 2718-2720. DOI:10.3969/j.issn.1004-437X.2019.15.010 |
| [7] |
邸小青, 甘思远, 叶瑞芳, 等. 肺原发性隐球菌病患者临床病理及影像学特征分析[J]. 中国病原生物学杂志, 2019, 14(6): 639-642. DI X Q, GAN S Y, YE R F, et al. Clinicopathological and imaging features of patients with primary pulmonary cryptococcosis[J]. J Parasit Biol, 2019, 14(6): 639-642. DOI:10.13350/j.cjpb.190605 |
| [8] |
陈相猛, 段晓蓓, 郝以秀, 等. 非艾滋病患者不同免疫状态肺隐球菌病临床和CT表现对比分析[J]. 放射学实践, 2016, 31(11): 1047-1051. CHEN X M, DUAN X B, HAO Y X, et al. Pulmonary crytococcosis in non-AIDS patients with different immunology conditions: comparison of clinical and CT characteristics[J]. Radiol Pract, 2016, 31(11): 1047-1051. |
| [9] |
谢长浓, 杨春阳, 梁健华, 等. 肺隐球菌病的CT表现及临床分析[J]. 实用放射学杂志, 2017, 33(2): 203-205. XIE C N, YANG C Y, LIANG J H, et al. CT characteristics and clinical analysis of pulmonary cryptococcosis[J]. J Pract Radiol, 2017, 33(2): 203-205. DOI:10.3969/j.issn.1002-1671.2017.02.010 |
| [10] |
姚克林, 胡红杰, 夏瑞明, 等. HIV阴性患者肺隐球菌病的临床与CT影像分析[J]. 浙江临床医学, 2016, 18(5): 807-809. YAO K L, HU H J, XIA R M, et al. The clinical and CT imaging performance characteristics of HIV negative patients of Pulmonary Cryptococcosis[J]. Zhejiang Clin Med J, 2016, 18(5): 807-809. |
| [11] |
周新. 解读侵袭性肺部真菌感染的诊断标准与治疗原则(草案)[J]. 中华内科杂志, 2006, 45(9): 788-789. ZHOU X. Interpretation of diagnostic criteria and treatment principles for invasive pulmonary fungal infections (draft)[J]. Chin J Intern Med, 2006, 45(9): 788-789. DOI:10.3760/j.issn:0578-1426.2006.09.035 |
| [12] |
黄佳斯, 石磊, 唐爱国, 等. 胶体金免疫层析法检测血清隐球菌抗原在肺隐球菌病诊断中的应用价值[J]. 临床检验杂志, 2017, 35(7): 518-519. HUANG J S, SHI L, TANG A G, et al. Application value of colloidal gold immunochromatography in detecting cryptococcal antigen in diagnosis of pulmonary cryptococcosis[J]. Chin J Clin Lab Sci, 2017, 35(7): 518-519. |
| [13] |
付成凤, 唐春兰, 罗虎. 误诊为肺炎的青年肺隐球菌诊治1例并文献复习[J]. 临床肺科杂志, 2018, 23(8): 1541-1544. FU C F, TANG C L, LUO H. Diagnosis and treatment of cryptococcal pneumonia in young people misdiagnosed as pneumonia and literature review[J]. J Clin Pulm Med, 2018, 23(8): 1541-1544. DOI:10.3969/j.issn.1009-6663.2018.08.049 |



