肾细胞癌是最常见的肾恶性肿瘤,占全部成人恶性肿瘤的2%~3%,约占肾脏恶性肿瘤的90%,对人类健康造成严重的影响,并给全球医疗卫生系统带来沉重的负担[1]。根据肿瘤细胞基因改变和组织学特征的不同,WHO(2004版)将肾细胞癌分为透明细胞癌(clear cell renal cell carcinoma, ccRCC)、乳头状细胞癌(papillary renal cell carcinoma,PRCC)及嫌色细胞癌(chromophobe renal cell carcinoma,ChRCC)3个主要的亚型,其中乳头状细胞癌又分为Ⅰ、Ⅱ两种亚型。ccRCC约占全部肾细胞癌85%,其他类型肾细胞癌相对少见[2]。不同亚型肾细胞癌的生物学行为和预后截然不同,相较于其他亚型,ccRCC发生转移的倾向性更明显,约占全部肾癌转移的94%;同时,ccRCC的5年总生存率仅为44%~69%,明显低于PRCC(82%~92%)、ChRCC(78%~92%)[3]。不同亚型肾细胞癌需要选择不同的个体化治疗方案,以达到最佳治疗效果。因此提高术前不同亚型肾细胞癌鉴别诊断能力,有助于更好地选择适合的治疗方案,以改善患者预后。
CT增强检查对肾脏恶性肿瘤的检出及评价其周围浸润、转移发挥着重要作用。通过测量CT增强扫描病灶不同期相的CT绝对值,能对肿瘤的增强特征、血管密度进行评估,为肾癌的术前分型提供参考。但CT绝对值除了反应肿瘤的组织学特征,还受多种因素如体质量指数、心输出量及对比剂方案、扫描方案等[4]的影响,在其基础上进行肾癌亚型鉴别不够准确。故本研究尝试引入校正后CT增强参数,以提升RCC各亚型间鉴别的准确性。
1 资料与方法 1.1 一般资料收集2017年8月至2019年6月本院经穿刺或手术病理证实的肾细胞癌患者76例。其中ccRCC 28例,男性17例,女性11例,年龄33~83(58.1±10.9)岁。PRCC Ⅰ型24例,男性14例,女性10例,年龄17~ 71(52.5±14.4)岁。PRCCⅡ型6例,均为男性,年龄25~73(55.5±17.8)岁。ChRCC 18例,男性8例,女性10例,年龄34~75(54.8±11.1)岁。
1.2 检查方法患者均行肾脏CT平扫及增强多期扫描。分别采用GELightSpeed VCT 64层和SOMATOM Definition Flash双源CT。患者采取仰卧位,扫描范围为膈面至髂棘上方,患者深吸后闭气进行扫描。扫描参数:管电流分别为300 mA、280 mAs, 管电压120 kV,视野40,矩阵512×512,层厚5 mm,层距5 mm,重建层厚分别1.25 mm、1 mm。增强方式:采用高压注射器经肘静脉注入碘佛醇(320 mg/100 mL),用量80 mL,流速3.5 mL/s。注射对比剂后23 s进行皮髓质期(corticomedullary phase, CMP)扫描、60 s进行实质期(nephrographic phase,NP)扫描,180 s进行排泄期(excretory phase,EP)扫描。
1.3 图像分析所有图像质量达到诊断要求,由2名高年资放射科主治医师分析,测量肿瘤最大体积横径。于增强扫描各期中选择肿瘤强化最明显部分放置感兴趣区(region of interest, ROI)测量CT值,并在平扫及增强扫描其余各期相同位置放置ROI。ROI尽可能包含全部肿瘤实质部分,并避开坏死、瘢痕、钙化等。本研究参考RUPPERT-KOHLMAYR等[5]的方法,测量肿瘤平面腹主动脉各期CT值(Ax),各期选用恒定值(SAx)作为校准基础值,分别为CMP 250 Hu、NP 120 Hu、EP 90 Hu,以此得到标准化系数Fx(公式:Fx=SAx/Ax)。标准化系数Fx乘以病灶CT值Lx得到病灶矫正CT值cLx(公式:cLx=Fx×Lx)。并计算病灶相对强化率rEx=矫正CT值cLx/病灶平扫值(LU)。
1.4 统计学分析采用SPSS19.0统计软件进行分析,计量资料以x±s表示,应用Kolmogorov-Smirnov方法进行正态性检验,组间采用单因素方差分析(F检验),若有统计学意义且满足方差齐性,则继续进行多样本均数两两比较LSD(q检验)统计,若方差不齐,则采用Tamhane’s T2检验。绘制受试者工作特征(receiver operator characteristic, ROC)曲线,分析不同期相矫正CT值及矫正相对强化率对肾脏恶性肿瘤分型的敏感度和特异性,并基于尤登指数得出分型阈值。检验水准α=0.05。
2 结果 2.1 一般资料与CT平扫各组间性别、年龄及肿瘤大小等差异无统计学意义(P>0.05)。CT平扫各组间CT值及矫正CT值差异均无统计学意义(P>0.05)。
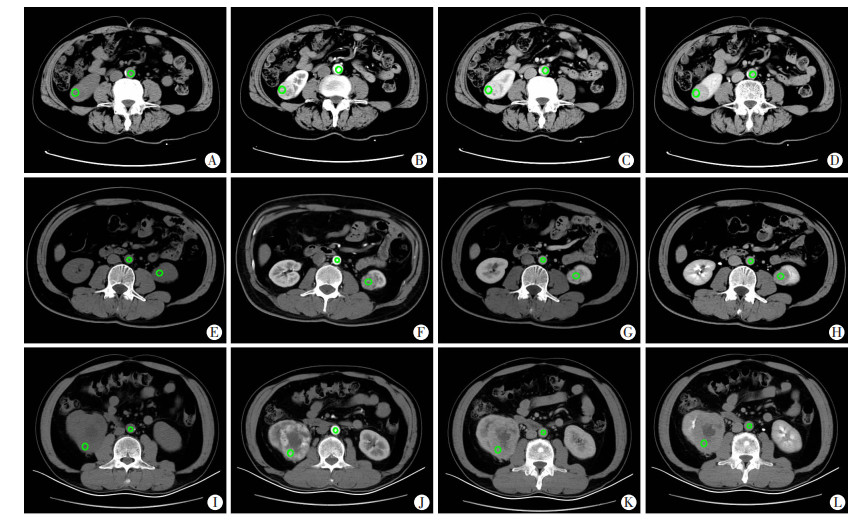
2.2 CT增强特征及矫正增强CT值ChRCC表现为边界清楚肿块,密度多均匀,增强扫描皮髓质期肿瘤较明显强化,实质期持续强化(图 1A~D)。PRCCⅠ型为乏血供肿瘤,增强扫描强化不明显,增强扫描各期均低于肾皮质(图 1E~H),PRCCⅡ型具有侵袭性,肿瘤密度不均;ccRCC内坏死多见,皮髓质期肿瘤实质部分强化显著,实质期快速消退,呈“快进快出”强化方式(图 1I~L)。
|
| A~D:ChRCC患者A:CT平扫示右肾下极占位;B~D:分别为皮髓质、实质期及排泄期;E~H:PRCCⅠ型患者E:CT平扫示左肾下极占位;F~H:分别为皮髓质、实质期及排泄期;I~L:ccRCC患者I:CT平扫示右肾占位;G~L:分别为皮髓质、实质期及排泄期;图中绿圈表示为测量各时相肿瘤及相应平面主动脉CT值的ROI 图 1 肾细胞癌不同亚型CT表现 |
ccRCC三期矫正CT值均高于其他组,其中皮髓质期与其余3组差异均有统计学意义(P < 0.01),实质期、排泄期ccRCC与PRCCⅠ、Ⅱ型间CT矫正值差异有统计学意义(P < 0.05),与ChRCC间差异无统计学意义(P>0.05)。PRCCⅠ型与PRCCⅡ型各期间CT矫正值差异均无统计学意义(P>0.05)。ChRCC各期矫正CT值介于ccRCC与PRCC之间,皮髓质期与PRCCⅡ型差异有统计学意义(P < 0.01),实质期与PRCCⅠ、Ⅱ型CT矫正值间差异有统计学意义(P < 0.05,表 1)。
| 肾癌亚型 | n | 肿瘤最大径/cm | LU | cLCMP | cLNP | cLEP |
| ChRCC | 18 | 5.87±3.58 | 39.45±4.95 | 63.43±11.61 | 84.54±21.38 | 65.68±11.69 |
| PRCCⅡ型 | 6 | 6.71±2.41 | 37.63±6.04 | 40.03±6.99a | 63.25±5.62b | 60.54±4.23 |
| PRCCⅠ型 | 24 | 6.37±3.48 | 38.83±9.35 | 49.12±21.96 | 60.01±20.77b | 52.86±17.19 |
| ccRCC | 28 | 5.97±3.01 | 35.34±8.24 | 110.68±45.62ace | 95.36±25.02de | 74.01±16.10e |
| a:P < 0.01,b:P < 0.05, 与ChRCC比较;c:P < 0.01,d:P < 0.05, 与PRCCⅡ型比较;e:P < 0.01,与PRCCⅠ型比较 | ||||||
2.3 矫正CT相对强化率
ccRCC皮髓质期强化明显,其皮髓质期相对强化率明显高于其余组(P < 0.01),实质期、排泄期强化消退,呈“快进快出”表现。实质期、排泄期ccRCC相对强化率较ChRCC、PRCCⅠ型和PRCCⅡ型高,实质期、排泄期ccRCC相对强化率与PRCCⅠ、Ⅱ型差异均有统计学意义(P < 0.05),排泄期ccRCC相对强化率与ChRCC差异有统计学意义,实质期差异无统计学意义。PRCCⅠ、Ⅱ型、ChRCC呈持续强化,强化峰值位于实质期。PRCCⅠ、Ⅱ型各期相对强化率无差异。ChRCC三期相对强化率均高于PRCCⅠ、Ⅱ型,皮髓质期与PRCCⅡ型差异有统计学意义(P < 0.05),实质期与PRCCⅠ型差异有统计学意义(P < 0.05),排泄期与PRCCⅠ、Ⅱ型差异无统计学意义(P>0.05)。详见表 2。
| 肾癌亚型 | n | rECMP | rENP | rEEP |
| ChRCC | 18 | 1.66±0.43 | 2.19±0.68 | 1.70±0.41 |
| PRCCⅡ型 | 6 | 1.07±0.11a | 1.71±0.24 | 1.64±0.24 |
| PRCCⅠ型 | 24 | 1.27±0.50 | 1.57±0.52a | 1.40±0.45 |
| ccRCC | 28 | 3.19±1.41abd | 2.82±1.03bd | 2.19±0.71acd |
| a:P < 0.01,与ChRCC比较;b:P < 0.01,c:P < 0.05, 与PRCCⅡ型比较;d:P < 0.01,与PRCCⅠ型比较 | ||||
2.4 矫正CT值/相对强化率ROC曲线
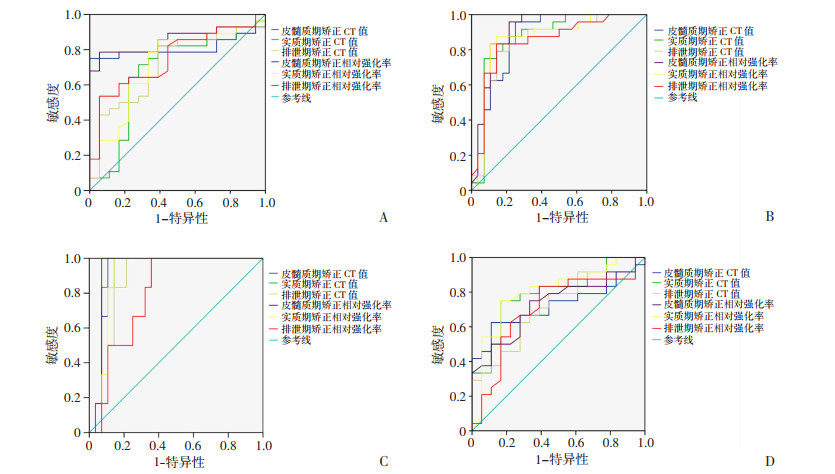
经计算发现相对强化率对于鉴别肾癌亚型价值最为显著。rECMP是鉴别ccRCC与其余肾癌亚型最敏感指标,鉴别ccRCC与ChRCC、PRCCⅠ型、PRCCⅡ型时ROC曲线下面积分别为0.855、0.908、0.935,当阈值分别为2.56、2.28、1.25时,其敏感性分别为78.6%、95.8%、100.0%, 特异性分别为94.4%、78.6%、92.9%。而rENP有助于鉴别ChRCC与PRCCⅠ型,其ROC曲线下面积为0.797,当rENP为1.64时,其敏感性、特异性分别为75.0%、83.3%。见图 2。
|
| A:ccRCC与ChRCC鉴别;B:ccRCC与PRCCⅠ型鉴别;C:ccRCC与PRCCⅡ型鉴别;D: ChRCC与PRCCⅠ型鉴别 图 2 各肾癌亚型间矫正后指标的ROC曲线分析 |
3 讨论
CT增强扫描时肿瘤强化程度及持续时间被认为反映了肿瘤内血管密度等组织学特性,有助于对肿瘤性质的鉴别,同时对肿瘤治疗方案选择及预后评估有着重要价值。既往研究证实:不同亚型肾细胞癌具有不尽相同的强化模式,基于CT皮髓质期的增强表现能对肾细胞癌亚型进行鉴别[6]。有研究进一步探讨多期相阈值对肾脏肿瘤分型的意义,发现相对于单期相而言,多期相强化表现能显著提高ccRCC与其余亚型鉴别诊断的准确性,具有更高的临床意义[7]。
CT增强成像中肿瘤强化表现取决于病灶内对比剂的相对浓度。这除了与肿瘤本身组织学特征如微血管密度、肿瘤微环境密切相关外,还受到多重内、外源因素的影响。对比剂剂量、速率及扫描延迟时间的变化,能显著改变肿瘤的CT强化表现。同时,体质量指数、心输出量及肾功能等因素的不同[5],同样会导致肿瘤内对比剂浓度峰值及持续时间的差异。因此,简单比较肾癌绝对CT值及其变化程度来鉴别肾癌亚型是不准确的。研究人员引进了矫正CT值的概念,以正常肾皮质CT值为对照,对肿瘤强化前后的CT值进行标准化,试图降低上述内、外源因素对强化方式的影响,得到了较好的效果[6]。但肾癌的恶性程度往往较高,易侵犯周围肾组织,使得被测定认为是正常的肾皮质组织往往存在潜在的肿瘤组织,导致结果存在误差。而由于高速血流的存在,肾癌组织几乎不可能在主动脉种植,使得主动脉腔CT值是一种比较理想的参照物。因此,本研究以主动脉的同期CT值为对比,通过公式对各期肿瘤组织CT值进行标准化,获得不同时相病灶的矫正CT值,并进一步计算矫正CT相对强化率,尽量摒除内、外源因素的干扰,基于其影像学表现对肾细胞癌进行亚型分型。
本研究发现,ccRCC皮髓质期矫正后CT值及相对强化率均显著高于其余各组,同时不同于其他亚型持续性强化表现,ccRCC强化峰值出现在皮髓质期,呈“快进快出”表现。这是由于ccRCC起源于近曲小管上皮,其间质内存在丰富的窦状血管,同时血管外周间隙增宽,血流通过速度增快,对比剂更容易从血管进入周围组织间隙[8]。研究表明皮髓质期CT值超过74 Hu, 诊断ccRCC的敏感性、特异性分别为79.0%、77.8%[9]。而本组中rECMP在鉴别ccRCC与其他亚型肾癌时表现更为敏感,提示皮髓质期快速、显著强化是其特征性表现,也符合其病理表现。实质期、排泄期ccRCC矫正后CT值与ChRCC无差异,考虑与ccRCC强化快速消退,而ChRCC呈持续强化,实质期、排泄期二者CT值出现一定重叠有关。高级别ccRCC总体强化程度反而低于低级别ccRCC,提示高级别ccRCC内更多非肉眼可见坏死及相应的血管减少[10]。
PRCC是一种起源于近曲小管上皮的嗜色细胞癌,具有乳头状或乳头小管状结构,基于免疫组化特征及基因表达差异被进一步分为PRCCⅠ型和PRCCⅡ型。由于缺乏VHL基因突变使血管内皮生长因子表达减少,PRCC为相对乏血供肿瘤,增强扫描强化多不明显,皮髓质期、实质期强化程度均低于肾皮质。虽然Ⅱ型较Ⅰ型恶性程度更高,但是二者在平扫、三期增强CT值以及相应CT增加值差异并无统计学意义[11]。国内学者[12]也发现Ⅱ型更易出现肾周侵犯、淋巴结转移及静脉癌栓等恶性征象,但Ⅱ型皮髓质期、实质期绝对CT值较Ⅰ型更高,且Ⅰ型表现为轻-中度渐进性持续强化,而Ⅱ型表现为皮髓质期、实质期渐进性强化、排泄期强化轻度消退。这可能与Ⅱ型更易出现乳头结节,同时乳头结节内对比剂充填有关。本组中PRCC三期增强扫描CT值最低,与其余亚型存在显著差异。但Ⅰ型和Ⅱ型间各期矫正后CT值及相对强化率均无差异。CT强化方式对于鉴别PRCCⅠ、Ⅱ型有一定难度,可能需要结合病灶侵袭表现帮助诊断。
ChRCC起源于肾集合管上皮细胞,瘤体多位于肾髓质,是一种相对少见的肾癌亚型,具有良好的预后,癌栓及转移等恶性征象罕见。肿瘤表现为均匀实性病灶,部分病灶内可见有“轮辐样”中央瘢痕,具有一定特征性[13]。ChRCC均匀强化率达69%~75%,有研究表明肿瘤内密度不均匀和中央瘢痕,提示肿瘤进展[14]。ChRCC间质血管丰富,皮髓质期肿瘤强化较明显,强化程度介于ccRCC与PRCC之间[2]。同时病灶各期强化程度均较肾皮质低[15]。本组中ChRCC表现为延迟强化,强化峰值位于实质期,同时其矫正CT值、相对强化率高于PRCCⅠ、Ⅱ型。当rENP为1.64时,其鉴别敏感性、特异性分别为75.0%、83.3%。可能与ChRCC内丰富的纤维组织增生,对比剂流出缓慢,实质期持续较明显强化,而PRCC间质内被大量泡沫细胞浸润,间质血管较少有关[16]。
综上,ccRCC、PRCCⅠ、Ⅱ型及ChRCC多期增强扫描强化方式有一定特点,通过矫正后CT值及相对强化率有助于摒除各种干扰因素影响,提高肾癌亚型间鉴别的准确性,尤其是皮髓质期、实质期的相对强化率,对于肾癌亚型的鉴别意义最为显著。ccRCC表现为典型“快进快出”强化,诊断一般不难。病灶表现为持续、均匀强化,强化程度介于ccRCC与PRCC之间,中央瘢痕及“反转”强化有助于ChRCC诊断。PRCCⅠ、Ⅱ型间强化方式重叠,鉴别二者可能需要更多的结合肿瘤形态学表现, 最后确诊仍需病理结果。
| [1] |
LOW G, HUANG G, FU W, et al. Review of renal cell carcinoma and its common subtypes in radiology[J]. World J Radiol, 2016, 8(5): 484-500. DOI:10.4329/wjr.v8.i5.484 |
| [2] |
CHING B C, TAN H S, TAN P H, et al. Differential radiologic characteristics of renal tumours on multiphasic computed tomography[J]. Singapore Med J, 2017, 58(5): 262-266. DOI:10.11622/smedj.2016081 |
| [3] |
OUYANG A M, WEI Z L, SU X Y, et al. Relative computed tomography (CT) enhancement value for the assessment ofmicrovascular architecture in renal cell carcinoma[J]. Med Sci Monit, 2017, 23: 3706-3714. DOI:10.12659/MSM.902957 |
| [4] |
ERTEKIN E, AMASYALI A S, EROL B, et al. Role of contrast enhancement and corrected attenuation values of renal tumors in predicting renal cell carcinoma (RCC) subtypes: protocol for atriphasic multi-slice computed tomography (CT) procedure[J]. Pol J Radiol, 2017, 82: 384-391. DOI:10.12659/PJR.901957 |
| [5] |
RUPPERT-KOHLMAYR A J, UGGOWITZER M, MEISSNITZER T, et al. Differentiation of renal clear cell carcinoma and renal papillary carcinoma using quantitative CT enhancement parameters[J]. Am J Roentgenol, 2004, 183(5): 1387-1391. DOI:10.2214/ajr.183.5.1831387 |
| [6] |
VELOSO GOMES F, MATOS A P, PALAS J, et al. Renal cell carcinoma subtype differentiation using single-phasecorticomedullary contrast-enhanced CT[J]. Clin Imaging, 2015, 39(2): 273-277. DOI:10.1016/j.clinimag.2014.09.007 |
| [7] |
YOUNG J R, MARGOLIS D, SAUK S, et al. Clear cell renal cell carcinoma: discrimination from other renal cell carcinoma subtypes and oncocytoma at multiphasic multidetector CT[J]. Radiology, 2013, 267(2): 444-453. DOI:10.1148/radiol.13112617 |
| [8] |
朱黎, 李迎春, 赵新湘. 不同亚型肾细胞癌的MRI及CT表现[J]. 临床放射学杂志, 2018, 37(5): 793-797. ZHU L, LI Y C, ZHAO X X. The performance of MRI and CT in the diagnosis of different subtypes of renal cell carcinoma[J]. J Clin Radiol, 2018, 37(5): 793-797. DOI:10.13437/j.cnki.jcr.2018.05.019 |
| [9] |
ŽOKALJ I, MAROTTI M, KOLARIĆ B. Pretreatment differentiation of renal cell carcinoma subtypes by CT: the influence of different tumor enhancement measurementapproaches[J]. Int Urol Nephrol, 2014, 46(6): 1089-1100. DOI:10.1007/s11255-013-0631-8 |
| [10] |
COY H, YOUNG J R, DOUEK M L, et al. Association of qualitative and quantitative imaging features on multiphasicmultidetector CT with tumor grade in clear cell renal cell carcinoma[J]. Abdom Radiol, 2019, 44(1): 180-189. DOI:10.1007/s00261-018-1688-8 |
| [11] |
BINDAYI A, MCDONALD M L, BEKSAC A T, et al. Can multiphase CT scan distinguish between papillary renal cell carcinoma type 1 and type 2?[J]. Turkish J Urol, 2018, 44(4): 316-322. DOI:10.5152/tud.2018.28938 |
| [12] |
王君广, 周赵霞, 张夏, 等. 不同亚型乳头状肾细胞癌CT影像鉴别与病理对照研究[J]. 实用放射学杂志, 2019, 35(3): 418-421. WANG J G, ZHOU Z X, ZHANG X, et al. Differential and pathological study of different subtypes of papillary renal cell carcinoma by CT imaging[J]. J Pract Radiol, 2019, 35(3): 418-421. DOI:10.3969/j.issn.1002-1671.2019.03.020 |
| [13] |
RAMAN S P, JOHNSON P T, ALLAF M E, et al. Chromophobe renal cell carcinoma: multiphase MDCT enhancement patterns and morphologic features[J]. Am J Roentgenol, 2013, 201(6): 1268-1276. DOI:10.2214/AJR.13.10813 |
| [14] |
KIM J H, BAE J H, LEE K W, et al. Predicting the histology of small renal masses using preoperative dynamic contrast-enhanced magnetic resonance imaging[J]. Urology, 2012, 80(4): 872-876. DOI:10.1016/j.urology.2012.06.001 |
| [15] |
张学勇, 王明杰, 李旭丹, 等. 肾脏嫌色细胞癌的影像学分析[J]. 医学影像学杂志, 2018, 28(5): 790-793. ZHANG X Y, WANG M J, LI X D, et al. Imaging analysis of chromophobe renal cell carcinoma[J]. J Med Imaging, 2018, 28(5): 790-793. |
| [16] |
刘学玲, 邹新农, 陈宏伟, 等. 多排螺旋CT动态增强扫描对乳头状肾细胞癌与嫌色细胞肾癌的鉴别诊断价值[J]. 中华肿瘤杂志, 2015, 37(1): 52-56. LIU X L, ZOU X N, CHEN H W, et al. Diagnostic value ofmult-detector CT for papillary renal cell carcinoma and chromophobe renal cell carcinoma[J]. Chin J Oncol, 2015, 37(1): 52-56. DOI:10.3760/cma.j.issn.0253-3766.2015.01.011 |



