儿童期自发性颅内出血(spontaneous intracranial hemorrhage, SICH)在病因、临床表现、并发症、治疗方法等方面都与成人有所不同, 预后也有较大差异。而即使在儿童期, 婴幼儿(≤3岁)与大龄儿童(>3岁)的SICH比较, 临床特点也有其独特性[1-2]。目前国内报道的儿童SICH病例组均以整个儿童期为研究目标, 年龄跨度较大, 不能体现各年龄段的差异性。为此, 本研究针对婴幼儿期(≤3岁)自发性颅内出血病例进行回顾性分析, 以期探索婴幼儿期SICH在诊断、治疗及预后等方面的特点, 为临床诊疗提供依据。
1 资料与方法 1.1 一般资料收集我科2011-2018年收治的住院SICH患儿131例。纳入标准:①年龄≤3岁; ②临床症状符合《小儿内科学》(第5版)颅内出血诊断标准[3], 且经头颅CT或MRI检查证实为颅内出血; ③既往无脑出血病史、产伤、窒息史; ④影像学及实验室检验明确出血病因, 其中脑血管病变、缺氧缺血性脑病、脑肿瘤卒中由增强CT/MRI、CTA证实, 凝血功能障碍及肺吸虫脑病由相关实验室检查确诊。排除标准:①本次患病前有明确外伤史; ②临床资料不完整。本组患儿男性91例, 女性40例, 男女比例:2.27 :1, 年龄范围:14 d~3岁, 平均0.47岁, 其中新生儿期(≤1个月)4例, 婴儿期(>1个月~1岁)109例, 幼儿期(>1~3岁)18例; 病程:5 h~20 d, 平均3.94 d。本研究获重庆医科大学附属儿童医院医学研究伦理委员会批准[(2019)年伦审(研)第(254)号]。
1.2 临床表现本组患儿均为急性或亚急性起病, 其中频繁呕吐、前囟膨隆、烦躁不安等高颅压症状103例(78.6%), 意识障碍71例(54.2%), 颅神经功能障碍67例(51.1%), 黄疸36例(27.1%), 病理征阳性34例(26.0%), 肢体瘫痪25例(19.1%), 颈阻阳性23例(17.6%)。
1.3 诊断方法本组患儿均行CT或MRI明确颅内出血诊断, 采取影像学、凝血功能、凝血因子、寄生虫抗体等检查进一步明确出血病因。其中34例行增强CT或MRI和CT血管造影(computed tomographic angiography, CTA)检查; 本组均未行数字减影血管造影(digital subtraction angiography, DSA)检查。
1.4 治疗方法本组患儿行手术治疗43例, 包括脑室/硬膜下外引流术23例、颅内血肿清除术13例、颅内血肿清除+脑室/硬膜下外引流术6例、神经导航下左额叶海绵状血管瘤切除+皮层脑电下癫痫灶皮层热灼术1例。3例脑肿瘤出血性卒中患儿中行肿瘤切除+颅内血肿清除术2例、1例肿瘤患儿拒绝手术。5例因术后再出血行二次手术, 非计划再次手术率为11.6%。其余88例为非手术治疗, 包括药物降颅压(甘露醇、高渗盐水等)、血凝酶等静滴止血、止惊、营养神经等对症、支持治疗, 凝血功能障碍的患儿予以成分输血和血液制品(冰冻血浆、凝血因子产品等)输注纠正, 肺吸虫患儿予以抗寄生虫治疗。
1.5 预后评估预后用出院时GOS评分(1~5)表示, GOS分值:5=恢复正常/良好; 4=轻度残疾; 3=重度残疾; 2=植物状态; 1=死亡。评分1~3分为预后不良组, 评分4~5分为预后良好组。
1.6 统计学分析采用SPSS 22.0软件进行统计学分析, 计数资料以率和构成比表示; 对并发症与预后的关系进行单因素卡方检验, 筛选自变量, 并发症用1代表存在, 0代表不存在; 运用二元Logistic回归进行多因素分析, 设定检验显著性水平为α=0.05。
2 结果 2.1 出血病因本组患儿颅内出血的病因以各种凝血功能障碍为主, 共98例, 占74.8%, 其中晚发型维生素K依赖因子缺乏72例(54.9%)、血友病15例(11.4%)、不明原因凝血功能障碍9例(6.9%)、急性白血病1例(0.8%)、嗜血细胞综合征1例(0.8%); 列出血病因第2位的是脑血管病变, 共24例, 占18.3%, 其中动静脉畸形16例(12.2%)、海绵状血管瘤5例(3.8%)、动脉瘤2例(1.5%)及颅面血管瘤1例(0.8%); 其他病因包括缺氧缺血性脑病4例(3.0%), 脑肿瘤卒中3例(2.3%), 肺吸虫脑病2例(1.5%)。
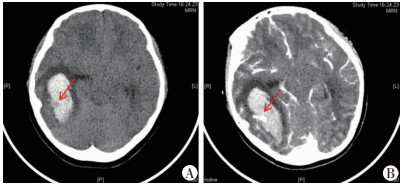
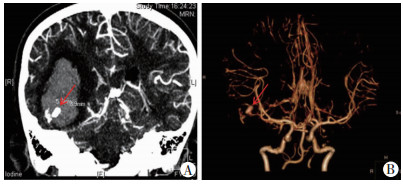
2.2 影像学检查本组颅内出血类型包括:脑内血肿(intracerebral hematoma, ICH)、硬膜下血肿(subdural hematoma, SDH)、脑室内出血(intraventricular hemorrhage, IVH)、蛛网膜下腔出血(subarachnoid hemorrhage, SAH), 以上类型单独出现或伴发出现, 发生比例由高到低为SAH>ICH>SDH>IVH(表 1)。本组疑诊脑血管病变患儿34例, 均行增强CT、MRI和CTA检查, 增强CT、MRI提示可疑脑血管病变8例(图 1), CTA发现脑血管病变24例(图 2), 术后病检结果均证实为脑血管畸形或动脉瘤。
| 出血类型/部位 | 例数(%) |
| 蛛网膜下腔出血(SAH) | 74(56.5) |
| 脑内血肿(ICH) | 72(54.9) |
| 颞叶 | 20(15.3) |
| 额叶 | 16(12.2) |
| 枕叶 | 9(6.9) |
| 顶叶 | 4(3.0) |
| 两个脑叶以上 | 23(17.5) |
| 硬膜下血肿(SDH) | 69(52.7) |
| 脑室内出血(IVH) | 37(28.2) |
|
| 箭头示血管畸形可能 图 1 SICH患儿术前CT平扫(A)及CT增强扫描(B)示血管畸形可能 |
|
| 箭头示畸形血管 图 2 SICH患儿术前CTA扫描成像(A)和三维立体成像(B)示脑血管畸形表现 |
2.3 并发症与预后
本组患儿并发症发生率由高到低依次为:抽搐/惊厥发作、贫血、继发感染、脑疝、脑水肿、脑梗塞、脑积水、呼吸衰竭、惊厥持续状态(表 2)。患儿的临床结局采用出院时GOS评分评估:恢复正常/良好为57例(43.5%); 轻度残疾和重度残疾分别为43例(32.8%)和25例(19.1%), 植物状态5例(3.8%)、死亡1例(0.8%)。
| 并发症 | 例数 | 预后良好 | 预后不良 | χ2值 | P值 |
| 抽搐/惊厥发作 | 18.30 | <0.01 | |||
| 有 | 86 | 55(63.9) | 31(36.1) | ||
| 无 | 45 | 44(97.7) | 1(2.3) | ||
| 贫血 | 0.55 | 0.45 | |||
| 有 | 77 | 57(74.0) | 20(26.0) | ||
| 无 | 54 | 43(79.6) | 11(20.4) | ||
| 继发感染 | 0.65 | 0.41 | |||
| 有 | 46 | 37(80.4) | 9(19.6) | ||
| 无 | 85 | 63(74.1) | 22(25.9) | ||
| 脑疝 | 35.3 | <0.01 | |||
| 有 | 32 | 12(37.5) | 20(62.5) | ||
| 无 | 99 | 88(88.8) | 11(11.2) | ||
| 脑水肿 | 7.26 | 0.07 | |||
| 有 | 28 | 16(57.1) | 12(42.9) | ||
| 无 | 103 | 84(81.5) | 19(18.5) | ||
| 脑梗塞 | 0.67 | 0.41 | |||
| 有 | 27 | 19(70.3) | 8(29.7) | ||
| 无 | 104 | 81(77.8) | 23(22.2) | ||
| 脑积水 | 0.35 | 0.55 | |||
| 有 | 26 | 21(80.7) | 5(19.3) | ||
| 无 | 105 | 79(75.2) | 26(24.8) | ||
| 呼吸衰竭 | 4.49 | 0.03 | |||
| 有 | 14 | 7(50.0) | 7(50.0) | ||
| 无 | 117 | 93(79.4) | 24(20.6) | ||
| 惊厥持续状态 | 0.26 | 0.60 | |||
| 有 | 9 | 8(88.8) | 1(11.2) | ||
| 无 | 122 | 92(75.4) | 30(24.6) |
并发症与预后的相关性采用单因素卡方检验分析, 结果显示:抽搐/惊厥发作、脑水肿、脑疝和呼吸衰竭在预后上的差异有统计学意义(表 2); 进一步对上述4个因素采用多因素二元Logistic回归分析, 最终脑水肿、脑疝和呼吸衰竭被纳入回归方程, 结果提示脑水肿、脑疝和呼吸衰竭是患儿预后不良的危险因素(P<0.05, 表 3)。
| 并发症 | OR | 95%CI | P值 |
| 脑水肿 | 5.794 | 1.921~17.476 | 0.002 |
| 脑疝 | 11.326 | 3.726~34.430 | <0.01 |
| 呼吸衰竭 | 8.028 | 1.878~34.327 | 0.005 |
3 讨论
有研究显示儿童期SICH的最常见病因是脑血管病变, 以动静脉畸形为主[4], 其占比可达84.7%[5]。但这些研究的病例组年龄多为0~14岁, 没有体现不同年龄段的差异。本研究针对婴幼儿期(≤3岁)的SICH进行病因分析, 结果显示各种疾病导致的凝血功能障碍为主要病因, 说明婴幼儿与大龄儿童不同, SICH的病因有其自身特点。在导致凝血功能障碍的疾病中以晚发性维生素K依赖因子缺乏症最为常见, 占比54.9%, 与国内外的报道相符[6-8]。该病是小婴儿自发性脑出血的重要病因, 此类患儿流行病学史较为一致, 均为出生后未注射维生素K、单纯母乳喂养、发病前有腹泻病史。出血原因是由于孕期母体维生素K不能进入胎儿体内[9], 出生后未补充外源性维生素K(肌注或从食物中摄取), 婴儿肠道内主要菌群乳酸杆菌又不能合成维生素K, 最终导致内源、外源性维生素K均极度缺乏, 维生素K依赖性凝血因子(Ⅱ、Ⅶ、Ⅸ、Ⅹ)合成障碍, 引发凝血功能障碍和出血倾向[7]。
本组第二位病因为脑血管病变, 以动静脉畸形最多见, 占66.6%(16/24), 低于儿童期自发性颅内出血病例组[5], 分析其原因可能是本组婴幼儿期患儿相对年龄较小, 动静脉畸形尚在病变早期, 相对体积较小; 病变出血后部分或完全破裂, 常规影像学检查往往不能发现病灶, 且病灶内微血栓形成, 造影剂无法进入, 血管造影(CTA)也很难发现AVM的特征影像[10]。此外, 由于本组患儿受年龄因素限制无法行DSA检查, 也存在部分AVM患儿漏诊的可能。有研究报道, 儿童自发性颅内出血病因中烟雾病为脑血管病变的第二大病因[5], 而本组未发现烟雾病病例, 原因可能为:烟雾病的成因——颈内动脉、大脑前、中动脉起始部狭窄或闭塞为渐进性发展, 在婴幼儿期病变不严重, 至大龄儿童期才出现临床症状。另有文献[11]报道颅面血管瘤综合征(sturge-weber syndrome, SWS)可导致出血性脑卒中发作, 本组亦发现1例, 表现为右侧海马区出血, 采用非手术治疗, 预后良好。值得一提的是本组发现2例脑型肺吸虫病致颅内出血, 在婴幼儿期较为罕见, 提示对婴幼儿自发性脑出血亦需要考虑到寄生虫感染的可能。
通常临床将DSA作为脑血管疾病诊断的金标准, 也有研究显示, 高场强下的磁共振血管造影(magnetic resonance angiography, MRA)对于脑血管成像的分辨力和准确度接近DSA, 明显优于CTA[12-13]。但在实际运用中CTA检查具有辐射量小、无创操作、耗时短、出血急性期实施较安全的特点[14]; 并且3D-CTA能够更清晰地显示血管病变周围结构的立体形态[15], 对血管病变的诊断准确率仍可达到90%以上[16]。本组24例脑血管病变均由CTA检出并经术后病检证实, 检出率为100%。由于婴幼儿SICH病情进展快, 患儿配合度差, 因此我们建议疑诊脑血管病变者, 将3D-CTA检查列为病因检查的首选。
有研究报道, 儿童SICH手术率为44.6%[17], 本组患儿手术率较儿童组低, 为32.8%。分析原因可能与出血病因不同有关:本组患儿以晚发性维生素K依赖因子缺乏症为主, 出血可以表现为蛛网膜下腔出血、硬膜下出血、脑室内出血、脑内血肿等多种形式, 部分患儿无需手术治疗; 儿童病例组的主要出血病因为动静脉畸形[17], 非手术治疗通常不能有效控制出血和根治疾病, 故手术治疗比率较大。此外, 婴儿颅骨骨缝未闭合, 对出血导致的颅内压增高有一定代偿作用, 患儿对高颅压的耐受能力强于大龄儿童, 故在确定治疗方式时更多病例选择非手术治疗。
本组患儿的并发症以抽搐/惊厥发作最多见, 文献报道抽搐/惊厥发作在新生儿脑出血中多见, 其发生率为67%[18], 而在全部儿童期病例中为15%~25%[2]。本组发生率为65.6%, 略低于新生儿但明显高于大龄儿童。原因可能是本组患儿年龄为婴儿期, 其大脑皮层发育不够成熟, 在颅内出血的刺激下更易兴奋[19]。本组并发症单因素分析结果提示抽搐/惊厥发作与患儿颅内出血的预后有相关性, 虽然不是预后的决定因素, 但惊厥发作发生率高, 急性期可能加重脑水肿并导致后期继发性癫痫的出现, 临床需高度重视并予以积极对症处理。多因素二元Logistic回归分析显示本组患儿预后不良的危险因素是脑水肿、脑疝和呼吸衰竭, 临床出现上述并发症时, 患儿预后不良的发生率分别为脑水肿(42.9%)、脑疝(62.5%)及呼吸衰竭(50.0%)。这三类并发症在病情衍变中有一定相关性:脑水肿是脑出血的重要继发性损伤[20], 脑水肿可导致颅内压增高, 造成神经功能障碍, 直接影响患儿预后, 严重者可形成脑疝, 部分患儿最终出现呼吸衰竭、死亡[21-22]。受年龄因素影响, 婴幼儿颅内出血症状较隐匿, 病情进展较快, 出现此类并发症时如不能及时救治往往预后较差。
有研究报道儿童SICH的病死率为4%~54%[2], 且儿童病例中重症的比例可达73%[23]。本组患儿病死率为0.8%, 致残率虽达51.9%, 但其中32.8%为轻瘫。提示婴儿期自发性颅内出血的病死率较低, 该年龄段总体预后明显优于大龄儿童。综上所述, 对于婴幼儿SICH的诊治, 应积极寻找病因, 早期积极对症治疗, 预防严重并发症, 个体化选择治疗方案以改善预后, 提高患儿生活质量。
| [1] |
MAJERSIK J J, COLE J W, GOLLEDGE J, et al. Recommendations from the international stroke genetics consortium, part 1: standardized phenotypic data collection[J]. Stroke, 2015, 46(1): 279-284. DOI:10.1161/STROKEAHA.114.006839 |
| [2] |
FERRIERO D M, FULLERTON H J, BERNARD T J, et al. Management of stroke in neonates and children: a scientific statement from the American heart association/American stroke association[J]. Stroke, 2019, 50(3): e51-e96. DOI:10.1161/STR.0000000000000183 |
| [3] |
薛辛东.新生儿颅内出血[M]//孙锟, 沈颖.小儿内科学.5版.北京: 人民卫生出版社, 2014: 54-58. XUE X D. Intracraninal hemorrhage of newborn[M]//SUN K, SHEN Y. Pediatric internal medicine. 5th ed.Beijing: People's Health Press, 2014: 54-58. |
| [4] |
LIU J F, WANG D R, LEI C Y, et al. Etiology, clinical characteristics and prognosis of spontaneous intracerebral hemorrhage in children: a prospective cohort study in China[J]. J Neurol Sci, 2015, 358(1/2): 367-370. DOI:10.1016/j.jns.2015.09.366 |
| [5] |
余云湖, 朱涛. 儿童期自发性颅内出血85例诊疗分析[J]. 中华神经外科杂志, 2012, 28(1): 13-16. YU Y H, ZHU T. Clinical analysis on spontaneous intracerebral hemorrhage in childhood, a report of 85 cases[J]. Chin J Neurosurg, 2012, 28(1): 13-16. DOI:10.3760/cma.j.issn.1001-2346.2012.01.005 |
| [6] |
魏中南, 张庆江, 詹江华, 等. 晚发性维生素K缺乏性颅内出血外科治疗316例[J]. 临床小儿外科杂志, 2016, 15(6): 594-597. WEI Z N, ZHANG Q J, ZHAN J H, et al. Surgical treatment for late vitamin K deficiency intracranial hemorrhage: a report of 316 cases[J]. J Clin Pediatr Surg, 2016, 15(6): 594-597. |
| [7] |
王丽杰, 孙莹, 颜卫源. 晚发性维生素K缺乏致颅内出血患儿的临床特征分析[J]. 中国医科大学学报, 2014, 43(10): 946-949. WANG L J, SUN Y, YAN W Y. Clinical characteristics of children with late vitamin K deficiency induced intracranial hemorrhage[J]. J China Med Univ, 2014, 43(10): 946-949. |
| [8] |
VOLPE J J. Intracranial hemorrhage in early infancy: renewed importance of vitamin K deficiency[J]. Pediatr Neurol, 2014, 50(6): 545-546. DOI:10.1016/j.pediatrneurol.2014.02.017 |
| [9] |
OZDEMIR M A, KARAKUKCU M, PER H, et al. Late-type vitamin K deficiency bleeding: experience from 120 patients[J]. Childs Nerv Syst, 2012, 28(2): 247-251. DOI:10.1007/s00381-011-1575-x |
| [10] |
张英俊, 出良钊, 余晖, 等. 四维CT血管造影在脑动静脉畸形诊断中的应用[J]. 中华神经外科杂志, 2014, 30(9): 880-883. ZHANG Y J, CHU L Z, YU H, et al. Application of 4D-CTA in diagnosis of cerebral arteriovenous malformations[J]. Chin J Neurosug, 2014, 30(9): 880-883. DOI:10.3760/cma.j.issn.1001-2346.2014.09.005 |
| [11] |
SUDARSANAM A, ARDERN-HOLMES S L. Sturge-Weber syndrome: from the past to the present[J]. Eur J Paediatr Neurol, 2014, 18(3): 257-266. DOI:10.1016/j.ejpn.2013.10.003 |
| [12] |
韩新生, 裘丽红, 许予明. CTA、MRA及DSA在脑血管疾病患者临床诊断中的意义[J]. 中国实验诊断学, 2014, 18(1): 33-36. HAN X S, QIU L H, XU Y M. Significance of clinical diagnosis with CTA, MRA and DSA in patients with cerebrovascular disease[J]. Chin J Lab Diagn, 2014, 18(1): 33-36. |
| [13] |
范影, 谢玉海, 李曼曼, 等. 单倍剂量三维对比增强MRA诊断脑动静脉畸形的临床价值[J]. 磁共振成像, 2014, 5(6): 455-458. FAN Y, XIE Y H, LI M M, et al. The clinical value of single-dose three-dimensional contrastenhanced MR angiography in diagnosis of cerebral arteriovenous malformation[J]. Chin J Magn Reson Imaging, 2014, 5(6): 455-458. DOI:10.3969/j.issn.1674-8034.2014.06.010 |
| [14] |
王磊, 裴昌军, 王琨, 等. MSCTA在自发性颅内出血病因诊断中的价值[J]. 中国临床医学影像杂志, 2017, 28(3): 162-165. WANG L, PEI C J, WANG K, et al. The value of MSCTA in the etiological diagnosis of spontaneous intracranial hemorrhage[J]. J China Clin Med Imaging, 2017, 28(3): 162-165. DOI:10.3969/j.issn.1008-1062.2017.03.003 |
| [15] |
于军, 王壮, 赵明明, 等. 3D-CTA与3D-DSA对颅内动脉瘤诊断价值比较[J]. 中华神经外科杂志, 2013, 29(3): 238-241. YU J, WANG Z, ZHAO M M, et al. Comparison of the value of 3D-CTA and 3D-DSA in the diagnosis of posterior communicating artery aneurysm[J]. J China Clin Med Imaging, 2013, 29(3): 238-241. DOI:10.3760/cma.j.issn.1001-2346.2013.03.007 |
| [16] |
汪五全, 刘心, 何金年. CTA、MRA诊断脑动静脉畸形:与DSA比较[J]. 中国介入影像与治疗学, 2012, 9(12): 854-857. WANG W Q, LIU X, HE J N. Comparison of CTA and MRA with DSA for diagnosis of arteriovenous malformations[J]. Chin J Interv Imaging Ther, 2012, 9(12): 854-857. |
| [17] |
赵雪灵, 梁平, 翟瑄, 等. 213例儿童自发性颅内出血的临床分析[J]. 重庆医科大学学报, 2020, 45(1): 134-138. ZHAO X L, LIANG P, ZHAI X, et al. Etiology and clinical features of children with spontaneous intracranial hemorrhage: a clinical analysis[J]. J Chongqing Med Univ, 2020, 45(1): 134-138. DOI:10.13406/j.cnki.cyxb.002197 |
| [18] |
COLE L, DEWEY D, LETOURNEAU N, et al. Clinical characteristics, risk factors, and outcomes associated with neonatal hemorrhagic stroke: a population-based case-control study[J]. JAMA Pediatr, 2017, 171(3): 230-238. DOI:10.1001/jamapediatrics.2016.4151 |
| [19] |
GLASS H C. Neonatal seizures: advances in mechanisms and management[J]. Clin Perinatol, 2014, 41(1): 177-190. DOI:10.1016/j.clp.2013.10.004 |
| [20] |
URDAY S, KIMBERLY W T, BESLOW L A, et al. Targeting secondary injury in intracerebral haemorrhage: perihaematomal oedema[J]. Nat Rev Neurol, 2015, 11(2): 111-122. DOI:10.1038/nrneurol.2014.264 |
| [21] |
WANG X, ARIMA H, YANG J, et al. Mannitol and outcome in intracerebral hemorrhage: propensity score and multivariable intensive blood pressure reduction in acute cerebral hemorrhage trial 2 results[J]. Stroke, 2015, 46(10): 2762-2767. DOI:10.1161/STROKEAHA.115.009357 |
| [22] |
LIM-HING K, RINCON F. Secondary hematoma expansion and perihemorrhagic edema after intracerebral hemorrhage:from bench work to practical aspects[J]. Front Neurol, 2017, 8: 74. DOI:10.3389/fneur.2017.00074 |
| [23] |
FOX C K, JOHNSTON S C, SIDNEY S, et al. High critical care usage due to pediatric stroke: results of a population-based study[J]. Neurology, 2012, 79(5): 420-427. DOI:10.1212/WNL.0b013e3182616fd7 |



