应激性溃疡(stress ulcer,SU)是机体在短时间内遭受强烈心理、生理等不良刺激(如创伤、感染、饥饿、寒冷、缺氧等)后发生的胃、十二指肠黏膜急性糜烂和溃疡,易合并出血,病情危重[1-3]。蹦极作为一种新兴的极限运动项目,被越来越多的人所熟悉和喜爱。极限高空运动还包括我们所熟知的高台跳水、高空跳伞、翼装飞行等。这些运动项目对人体会造成巨大的应激刺激。在这里将这些运动项目统称为高空悬跳。高空悬跳作为一种强烈的应激源和紧急情况,有引发胃溃疡的危险,而以往研究应激性溃疡的动物模型主要有束缚浸水、冷冻应激、旋转应激、枪声应激、力竭游泳等[4]。经典的束缚浸水模型主要研究的是束缚和冷水刺激对大鼠应激性溃疡形成的影响,而对于特异性应激高空悬跳与应激性溃疡是否有关尚不清楚。本研究通过大鼠高空悬跳刺激模拟人类高空应激事件,观察大鼠应激性溃疡发生情况,探讨该方法建立应激性溃疡模型的有效性,并采用药物、预适应不同预处理方式对应激过程进行干预,为防治高空运动引起应激性溃疡提供依据。
1 材料与方法 1.1 实验动物雄性SD大鼠88只,体质量180~220 g,购自兰州大学实验动物中心,许可证号:SCXK(甘:2018-0002)。常规饲料喂养,自由进水,室温18~20 ℃,湿度50%~60%,自然光照。
1.2 主要材料SOD、MDA测试盒购自南京建成公司,10%甲醛溶液、雷尼替丁购自江西汇仁公司,参苓白术散购自同仁堂,酸度计(SX-610)购自上海三信公司。
1.3 方法 1.3.1 建立高空悬跳致应激性溃疡模型48只大鼠按随机数字表法分为6组(n=8):束缚浸水组(RWIS组)、悬跳17 m 30 min组(H17-30组)、悬跳17 m 40 min组(H17-40组)、悬跳17 m 50 min组(H17-50组)、悬跳34 m 40 min组(H34-40组)和悬跳46 m 40 min组(H46-40组)。RWIS组选用经典束缚浸水应激法(restraint water-immersion stress,RWIS) [1-2]复制SU模型,大鼠禁食不禁水24 h后,将四肢固定于木板直立浸入温度21~23 ℃的水中,保持水面至大鼠胸骨剑突处,浸泡7 h后取出。
高空悬跳大鼠禁食不禁水24 h后,实验当天,室外温度15 ℃,风速1~2级,分别将大鼠双后肢用橡皮筋一端固定。大鼠从17 m(5楼)高分别悬跳30 min(悬跳15 min后,休息5 min,再次重复1次)、40 min(悬跳20 min后,休息5 min,再次重复1次)、50 min(悬跳25 min后,休息5 min,再次重复1次);自34 m(10楼)和46 m(14楼)高悬跳,连续悬跳20 min后,休息5 min,再次重复1次,共计悬跳40 min。大鼠所用橡皮筋,材质相同,弹性系数相同。
1.3.2 预处理干预实验40只大鼠按随机数字表法分为5组(n=8):正常对照组(C组)、模型组(H17-40组)、雷尼替丁组(R组)、参苓白术散组(S组)、悬跳预适应组(P组)。
R组:大鼠每天以2.4 mg/100 g雷尼替丁灌胃;H17-40组:大鼠每天给予1 mL生理盐水灌胃;S组:大鼠每天给予1.2 g/kg参苓白术散水液灌胃。以上3组灌胃3 d后,禁食24 h,自由饮水,进入高空17 m悬跳40 min。P组禁食24 h,自由饮水,在高空悬跳前于1 m高度进行适应性悬跳, 每次持续5 min,连续悬跳3次后,再进入高空17 m悬跳40 min(悬跳20 min后,休息5 min,再次重复1次)。C组不做特殊处理。
1.3.3 胃内pH值测定实验完成后,取下大鼠,用10%水合氯醛,0.35 mL/100 g麻醉。沿腹部中线纵行打开腹腔,找到胃,分别结扎贲门和幽门下方一段十二指肠后剪断胃与食管及十二指肠连接处,取出胃。为避免针头造成的创伤被误认为溃疡,用小灌胃针从十二指肠端注入生理盐水2 mL,轻轻震荡后取出胃液,离心,1 000 r/min,5 min,取上清液进行pH值测定。
1.3.4 胃壁观察及损伤程度测定取出全胃后,沿胃大弯剪开并展平, 用棉签轻轻将胃黏液及血凝块擦除,观察胃黏膜损伤的形态和程度。胃黏膜在解剖显微镜下见溃疡灶,光镜下见变性坏死组织为实验模型制作成功的判断标准。评价胃黏膜溃疡的发生率和溃疡指数。溃疡指数(ulcer index,溃疡指数)的判定参考Goth的方法,即以黏膜损伤长度计算:< 1 mm为1分,1~ < 2 mm为2分,2~ < 3 mm为3分,以此类推,损伤宽度超过2 mm,分数加倍。
1.3.5 病理切片制作以溃疡部位为中心修剪胃壁组织,以溃疡平行于胃长轴方向的最长径中心取材,切取含溃疡边缘约3 mm组织在内的溃疡组织块,迅速置于10%甲醛中固定24 h,石蜡包埋,5 μm厚度切片,作HE染色。
1.3.6 SOD活性及MDA含量测定大鼠麻醉后采集大鼠心血1 mL,离心取上清,按测试盒说明操作检测SOD活性和MDA含量。
1.4 统计学分析采用SPSS 18.0统计软件,计量资料以x±s表示,两组间比较采用独立样本t检验,两两比较采用SNK法,计数资料行χ2检验,以P < 0.05为差异具有统计学意义。
2 结果 2.1 SU大鼠模型的建立 2.1.1 高空悬跳时间对大鼠致应激性溃疡的影响大鼠自17 m高空分别悬跳30、40、50 min,均可发生胃溃疡;与RWIS组比较,溃疡指数差异无统计学意义(表 1),并随时间增加,溃疡指数逐渐增大,H17-40组溃疡指数与束缚浸水组最为接近。
| 组别 | 发生溃疡[例(%)] | 溃疡指数(x±s) |
| RWIS组 | 8(100.0) | 11.00±3.29 |
| H17-30组 | 8(100.0) | 8.13±3.52 |
| H17-40组 | 8(100.0) | 11.63±3.78 |
| H17-50组 | 8(100.0) | 16.25±2.70 |
2.1.2 高空悬跳高度对大鼠致应激性溃疡的作用
大鼠分别从17、34、46 m高度悬跳40 min,均可发生胃溃疡;与束缚浸水组比较,H17-40组溃疡指数差异无统计学意义,但H34-40组、H46-40组溃疡指数显著升高(P < 0.05,表 2)。
| 组别 | 发生溃疡[例(%)] | 溃疡指数(x±s) |
| RWIS组 | 8(100.0) | 11.00±3.29 |
| H17-40组 | 8(100.0) | 11.63±3.78 |
| H34-40组 | 8(100.0) | 16.75±2.60a |
| H46-40组 | 8(100.0) | 19.13±2.53a |
| a: P < 0.05,与RWIS组比较 | ||
2.1.3 各组大鼠溃疡指数比较
与RWIS组比较,H17-30组大鼠溃疡指数下降;H17-50组、H34-40组、H46-40组溃疡指数升高,其中H34-40组、H46-40组差异有统计学意义(P < 0.05,表 1、2)。H17-40组溃疡指数与束缚浸水组最为接近,提示如果以RWIS组为标准参照,在17 m高悬跳40 min为最合适的成模条件。
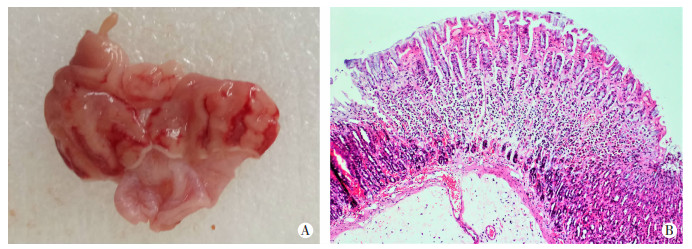
2.1.4 大鼠应激性溃疡的病理学特点束缚浸水组和高空悬跳组溃疡部位的病理检查未见明显差异。肉眼可见呈点状或条索状的出血或糜烂,多位于黏膜的皱折处,以胃体部多见,且大多与胃的纵轴平行。镜下见部分黏膜完整性破坏,上皮细胞坏死或脱落,黏膜内有充血、出血,表层水肿明显,有炎性细胞浸润(图 1)。
|
| A:肉眼观,见条索状出血;B:镜下观,见灶性出血及炎症反应(HE ×400) 图 1 高空悬跳大鼠应激性胃溃疡形态观察 |
2.2 预处理的干预效果 2.2.1 胃液pH值变化及胃黏膜溃疡指数
胃液pH值:与C组比较,H17-40组胃内pH值降低(P < 0.05);与H17-40组比较,R组、S组和P组胃内pH值增加(P < 0.05)。R组、S组和P组组间两两比较,差异无统计学意义。溃疡指数:与H17-40组比较,R组、S组和P组溃疡指数减小(P < 0.05)。R组、S组和P组组间两两比较,差异无统计学意义,见表 3。
| 组别 | pH值 | 溃疡指数 | SOD/U·mL-1 | MDA/nmol·mL-1 |
| C组 | 5.74±0.61 | 0 | 163.62±21.35 | 12.30±2.55 |
| H17-40组 | 3.28±0.76a | 11.75±3.65 | 13.73±4.74a | 38.48±4.78a |
| R组 | 4.89±0.67b | 7.13±1.13b | 74.30±24.44b | 18.97±3.27b |
| S组 | 4.47±0.76b | 8.13±2.10b | 60.90±11.15b | 28.20±8.11b |
| P组 | 4.73±0.40b | 7.25±1.83b | 63.47±14.87b | 20.51±6.92b |
| a:P < 0.05,与C组比较;b:P < 0.05,与H17-40组比较 | ||||
2.2.2 血清SOD和MAD的变化
血清SOD活性:与C组比较,H17-40组血清SOD活性降低(P < 0.05);与H17-40组比较,R组、S组和P组血清SOD活性增加(P < 0.05)。R组、S组和P组组间两两比较,差异无统计学意义。血清MDA含量:与C组比较,H17-40组血清MDA含量增加(P < 0.05);与H17-40组比较,R组、S组和P组血清MDA含量降低,差异有统计学意义(P < 0.05)。R组、S组和P组间两两比较,差异无统计学意义,见表 3。
3 讨论应激性胃溃疡是机体在应激状态下引起的胃黏膜急性损伤。高空悬跳作为一种强烈的应激源和紧急情况,有引发胃溃疡的危险。本研究采用大鼠高空悬跳方式,模拟人类高空应激事件,结果证明大鼠在17 m悬跳40 min溃疡的发生率及严重程度与经典的束缚浸水应激性溃疡无明显差异,并随着悬跳时间和悬跳高度增加,说明大鼠高空悬跳建立应激性溃疡动物模型的方法是有效、可靠的,该方法可简便、快速地建立特异性因素诱导的应激性溃疡动物模型。
应激性溃疡的发生机制普遍认为是机体对各种应激性刺激的全身性非特异性反应[5]。高空悬跳引起应激性溃疡的可能机制主要有:①高空悬跳应激时交感肾上腺髓质系统强烈兴奋,胃黏膜供血相对减少。②盐酸产生增加。一方面由于倒置,盐酸进入到肠道减少,使得胃内盐酸进一步聚集,加重胃黏膜损伤;另一方面可能与胃泌素增加有关,被公认的高强度跳伞应激研究结果显示:跳伞应激时,血清胃泌素随应激强度的增加和应激时间的延长而增加[6]。③大鼠悬跳倒置时,胆汁、胰液会逆流入胃,在胃内积存,损伤胃黏膜表面细胞。胆汁中的胆盐可降低胃黏膜的电位差,增加胃黏膜的通透性,使H+更容易通过胃黏膜;并且胆盐对黏膜上皮细胞膜的脂质有溶解作用,导致胃黏膜损伤。除阿司匹林和酒精外,胆盐是造成胃黏膜损害排行第3位的物质。④高空冷刺激也参与了溃疡的形成[7]。研究发现低温导致胃运动加强,并已经证实应激性溃疡的形成与胃运动异常有关。⑤在本研究中,高空悬跳大鼠SOD活性降低,MDA含量增加,表明氧自由基对黏膜上皮的损伤也发挥了一定的作用。
雷尼替丁属H2受体拮抗剂,主要通过阻滞胃壁细胞分泌胃酸,提高十二指肠上皮细胞的增殖,降低患者体内胃蛋白酶的活性,以降低溃疡的发生。大量研究[8]已经证实雷尼替丁用于预防应激性溃疡的有效性。在2018版防治指南中明确雷尼替丁可作为应激性溃疡的预防药物[9]。本研究结果也显示雷尼替丁对高空悬跳致应激性溃疡大鼠预防性使用是有效的,主要通过降低盐酸和减少氧自由基生成发挥预防或减轻溃疡程度的效果。参苓白术散对治疗应激性溃疡出血临床有效率达96.87%[10]。有研究显示参苓白术散对乙酸诱导大鼠胃溃疡有保护作用[11]。本研究也证实对可预见的应激性溃疡预防性使用参苓白术散,可达到预防或减轻溃疡程度的效果,与胃酸的降低和氧自由基的减少有关。预适应训练可有效激活体内内源性保护物质,研究者发现低氧预适应具有明显预防低氧应激性溃疡的作用[12],预适应可有效减轻海水浸泡束缚大鼠应激性溃疡[13]。本研究尝试在高空悬跳前给予低空悬跳预适应(短暂多次的低空1 m悬跳)训练后,预适应组溃疡指数较直接应激组显著改善,表明低空悬跳预适应训练对预防应激性溃疡是有效的。
本研究通过高空悬跳应激刺激成功建立了大鼠应激性胃溃疡模型,发现溃疡程度与悬跳持续时间和高度有关;给予雷尼替丁、参苓白术散、低空悬跳预处理可有效预防或减轻溃疡程度,其发生机制与降低胃酸分泌和减少氧自由基形成有关。提示在高空运动中保暖、减少悬跳持续时间及适当控制高度,加强科学的训练方法及适度的药物预防,可有效减少应激性溃疡的发生。
| [1] |
STANGHELLINI V, CHAN F K L, HASLER W L, et al. Gastroduodenal disorders[J]. Gastroenterology, 2016, 150(6): 1380-1392. DOI:10.1053/j.gastro.2016.02.011 |
| [2] |
RANASINGHE N, DEVANARAYANA N M, RAJINDRAJITH S, et al. Functional gastrointestinal diseases and psychological maladjustment, personality traits and quality of life[J]. BMC Gastroenterol, 2018, 18(1): 33. DOI:10.1186/s12876-018-0760-8 |
| [3] |
TOEWS I, GEORGE A T, PETER J V, et al. Interventions for preventing upper gastrointestinal bleeding in people admitted to intensive careunits[J]. Cochrane Database Syst Rev, 2018, 6: CD008687. DOI:10.1002/14651858.CD008687.pub2 |
| [4] |
尹斌, 刘真, 贾赤宇. 应激性溃疡动物模型建立的研究进展[J]. 中华损伤与修复杂志(电子版), 2015, 10(5): 431-433. YIN B, LIU Z, JIA C Y. Research progress on the establishment of the animal model of stressulcer[J]. Chin J Inj Repair Wound Heal (Electron Ed), 2015, 10(5): 431-433. DOI:10.3877/cma.j.issn.1673-9450.2015.05.014 |
| [5] |
杨韵然, 臧林泉. 应激诱导溃疡损伤的研究进展[J]. 世界最新医学信息文摘, 2019, 19(32): 32-33. YANG Y R, ZANG L Q. Research progress of stress-induced ulcerinjury[J]. World Latest Med Inf, 2019, 19(32): 32-33. DOI:10.19613/j.cnki.1671-3141.2019.32.016 |
| [6] |
张莉, 郝文平, 路长林, 等. 空降兵新兵跳伞应激对血浆心钠素、血管紧张素Ⅱ、内皮素及胃泌素含量的影响[J]. 中华航空航天医学杂志, 2002, 13(2): 94-97. ZHANG L, HAO W P, LU C L, et al. Effect of parachute jumping stress on plasma ANP, AngⅡ, ET and SHG levels in newly recruited parachutists[J]. Chin J Aerosp Med, 2002, 13(2): 94-97. DOI:10.3760/cma.j.issn.1007-6239.2002.02.007 |
| [7] |
张玉玉, 祝文兴, 孙一耕, 等. 大鼠束缚-浸水应激模型体温降低与应激性胃溃疡的关系[J]. 生物医学工程研究, 2007, 26(3): 282-284, 290. ZHANG Y Y, ZHU W X, SUN Y G, et al. The relationship between hypothermia and gastric ulcers induced by restraint water-immersion stress in rats[J]. J Biomed Eng Res, 2007, 26(3): 282-284, 290. DOI:10.19529/j.cnki.1672-6278.2007.03.016 |
| [8] |
邢晓璇, 白向荣, 褚燕琦, 等. 药物预防应激性溃疡的系统综述[J]. 实用药物与临床, 2017, 20(4): 475-480. XING X X, BAI X R, CHU Y Q, et al. A systematic review of drugs for stress ulcer prophylaxis[J]. Pract Pharm Clin Remedies, 2017, 20(4): 475-480. DOI:10.14053/j.cnki.ppcr.201704029.ppcr.201704029 |
| [9] |
柏愚, 李延青, 任旭, 等. 应激性溃疡防治专家建议(2018版)[J]. 中华医学杂志, 2018, 98(42): 3392-3395. BAI Y, LI Y Q, REN X, et al. Expert advice on prevention and treatment of stress ulcer (2018)[J]. Natl Med J China, 2018, 98(42): 3392-3395. DOI:10.3760/cma.j.issn.0376-2491.2018.42.003 |
| [10] |
董得刚. 参苓白术散加减治疗慢性糜烂性胃炎、胃溃疡伴幽门螺旋杆菌感染心得体会[J]. 临床医药文献电子杂志, 2017, 4(71): 14013. DONG D G. Experience in the treatment of chronic erosive gastritis and gastric ulcer with Helicobacter pylori infection with Shenling Baizhu powder[J]. J Clin Med Lit, 2017, 4(71): 14013. DOI:10.16281/j.cnki.jocml.2017.71.133 |
| [11] |
陈宇宁, 曹辉琼, 张毅. 参苓白术散对乙酸诱导大鼠胃溃疡的保护作用[J]. 中国医药指南, 2014, 12(16): 92-93. CHEN Y N, CAO H Q, ZHANG Y. Protective effect of Shenling Baizhu powder on gastric ulcer induced by acetic acid in rats[J]. Guid China Med, 2014, 12(16): 92-93. DOI:10.15912/j.cnki.gocm.2014.16.161 |
| [12] |
NARYZHNAYA N V, MASLOV L N, VYCHUZHANOVA E A, et al. Effect of hypoxic preconditioning on stress reaction inrats[J]. Bull Exp Biol Med, 2015, 159(4): 450-452. DOI:10.1007/s10517-015-2988-4 |
| [13] |
施斌斌, 傅继华, 骆益宙. 不同预适应对海水浸泡束缚大鼠应激性溃疡的影响[J]. 第二军医大学学报, 2008, 29(10): 1193-1196. SHI B B, FU J H, LUO Y Z. Effect of different preconditionings on stress ulcer induced by seawater immersion and restriction in rats[J]. Acad J Second Mil Med Univ, 2008, 29(10): 1193-1196. DOI:10.3321/j.issn:0258-879X.2008.10.012 |



