2019年12月发生于武汉的不明原因肺炎[1],现已迅速蔓延至我国其他省市地区,世界范围内也已有5大洲24国家报道发现确诊病例[2]。2020年2月11日WHO将该疾病更名为COVID-19(coronavirus disease 2019),并将该病毒正式命名为SARS-CoV-2,认定该病毒为SARS冠状病毒的姊妹病毒[3]。有学者针对武汉海鲜市场暴露人群患者的临床病例研究显示,疫区患者的主要临床特点为发热、干咳、呼吸困难、肌痛、疲劳、白血病数减少及肺CT影响异常,其中危重病多集中在老年人[4]。目前研究多集中在疫区地区病例研究[4-6]。但随着疫情发展,不排除有病毒第2、3代传播,并扩大到非疫区,防控及治疗任务非常严峻。深入了解病毒在非疫区传播特点,掌握传播规律,为防控政策的科学制定提供参考。本研究收集南京市公共卫生中心出院的非疫区57例临床诊断COVID-19肺炎患者资料,分析流行病学及临床特点,以加深对该疾病的认识,为该疾病识别及诊治提供参考。
1 资料与方法 1.1 一般资料2020年1月23日开始南京市公共卫生中心集中收治、确诊患者。本研究回顾性分析已出院的57例诊断为COVID-19肺炎的患者资料。其中男性29例(50.9%),女性28例(49.1%),年龄5~97岁,中位年龄37岁。入院后详细追问流行病学病史,完善相关实验室及CT检查。
1.2 诊断标准临床诊断标准采用收治当期最新版COVID-19诊疗指南[7]。
1.3 观察项目患者入院前流行病学调查(疫区旅居史、密切接触人员、活动轨迹、暴露时间、发病时间);入院时完善相关检查(血常规、肝肾功、心肌酶、电解质及CT影像学检查),潜伏期、发病时间、住院时间。
1.4 治疗方案及出院标准入院后治疗方案均按指南结合病情,给予重组干扰素α1b 50 μg雾化,2次/d;洛匹那韦利托那韦片(克立芝)500 mg口服每日2次;阿比多尔及达芦那韦考比司他片抗病毒治疗,视病情变化考虑给予免疫球蛋白0.2~0.4 g/(kg·d)输注提高免疫力,甲强龙40 mg静脉滴注每日1次抗感染治疗,其余给予止咳、止泻、补钾、营养等对症及支持治疗。在体温恢复正常3 d以上,呼吸道症状明显好转基础上,肺部影像学显示炎症吸收,连续2次呼吸道病原核酸检测阴性(采样时间间隔至少1 d),可解除隔离出院,或根据病情转至相应科室治疗其他疾病。
2 结果 2.1 流行病学情况57例COVID-19患者中,54例在南京发病,最小年龄5岁,最大年龄97岁。
5~20岁4例(7.02%),21~30岁10例(17.54%),31~40岁18例(31.58%),41~50岁9例(15.79%),51~60岁6例(10.53%),61~100岁10例(17.54%)。最短潜伏期1 d,最长潜伏期21 d,平均7.4 d;发病后最短于1 d入院,平均6.8 d;无症状感染者13例,占总数22.8%;住院时间最短4 d,最长26 d,平均住院时间10.1 d;57例COVID-19患者发病至出院时间平均15.6 d。所有病例中轻症15例占26.3%,普通型42例占73.7%;明确的疫区长居史8例(14.0%),无疫区旅居史而与COVID-19患者(有武汉经历)有明确接触史的共35例(61.4%);所有病例中因聚集性疫情而染病的患者32例(56.1%),其中主要以探亲聚集14例(24.6%)、出差至武汉10例(17.5%)为主;有明确汉口菜市场暴露史共2例(3.5%)。
2.2 临床症状患者主要临床症状见表 1。发热、咳嗽为主要症状,分别占59.7%、52.6%;其中23例以发热为首发症状,占40.4%;咳嗽以干咳为主,占52.6%,其中以干咳为首发症状占26.6%,少数伴白痰;其余以乏力全身酸痛(35.1%)、胸痛(1.8%)为首发症状,10.5%的患者在发病或住院期间均有腹泻。
| 症状 | 例数 | 百分比(%) |
| 发热(首发) | 23 | 40.4 |
| < 38 ℃ | 15 | 26.3 |
| 38~39 ℃ | 12 | 21.1 |
| 39~39.9 ℃ | 7 | 12.3 |
| 咳嗽 | 30 | 52.6 |
| 干咳(首发) | 14 | 26.6 |
| 乏力、全身酸痛 | 20 | 35.1 |
| 乏力全身酸痛(首发) | 5 | 8.8 |
| 胸痛(首发) | 1 | 1.8 |
| 鼻塞咽痛 | 4 | 7 |
| 腹泻 | 6 | 10.5 |
| 胸闷气短 | 8 | 14 |
| WBC | ||
| < 4×109/L | 15 | 26.3 |
| (4~10)×109/L | 42 | 73.7 |
| EOS < 0.02×109/L | 19 | 33.3 |
| LYMPH < 0.8×109/L | 14 | 24.6 |
| PMV > 11fl | 15 | 26.3 |
| AST > 40 U/L | 4 | 7 |
| ALT > 40 U/L | 9 | 15.8 |
| Th/Ts | ||
| < 0.68 | 5 | 8.8 |
| 0.68~2.47 | 24 | 42.1 |
| > 2.47 | 6 | 10.5 |
| CD4+ | 12 | 21.1 |
| CD8+ | 10 | 17.5 |
| LDH > 245 U/mL | 15 | 26.3 |
| CKMB > 4.87 g/mL | 3 | 5.3 |
| CRP > 10 mg/L | 20 | 35.1 |
| 超敏C > 3 mg/L | 26 | 45.6 |
| K < 3.5mmo/L | 23 | 40.4 |
2.3 实验室检查
白细胞计数(WBC)、淋巴细胞绝对值(LYMPH)、嗜酸性粒细胞绝对值(EOS)、平均血小板体积(MPV)、丙氨酸转氨酶(ALT)、谷草转氨酶(AST)、乳酸脱氢酶(HLD)、肌酸激酶同工酶(CKMB)、血钾、CRP及超敏CRP结果见表 1。结果表明新型冠状病毒可导致部分患者WBC(15%)、LYMPH(24.6%)及EOS(19%)降低,其中白细胞正常者占73.7%,心肌(CKMB 5.3%)、肝脏(AST 4%, ALT 9%, LDH23.6%)及血液系统均有累及,病毒感染后普遍引起炎性反应(CRP或超敏CRP 80.7%),血钾降低占有较大比例(40.4%)。
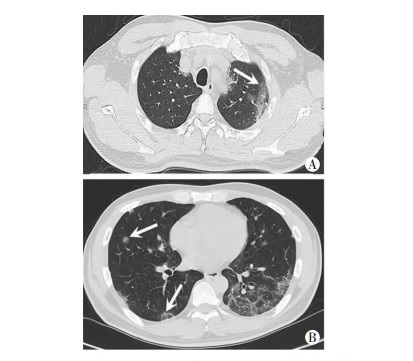
2.4 胸部CT表现57例患者入院均行胸部CT检查,均有不同程度的斑片状磨玻璃影,呈间质性改变,部分病例可呈大片阴影。双肺或单肺肺部炎症渗出病变常延支气管树累及多叶、散在分布胸膜下,双侧病变占68.4%,双中下肺占22.8%,双上肺占14.0%,单侧中下肺占26.3%。典型胸部CT表现见图 1~3。
|
| A:上肺单侧斑片状磨玻璃影;B:下肺胸膜下多发散在斑片状磨玻璃影 图 1 COVID-19典型病例1胸部CT表现(患者男性,42岁) |
|
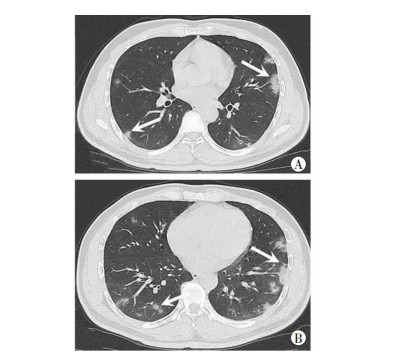
| A:两肺中叶胸膜下磨玻璃影;B:下肺胸膜下多发散在斑片状磨玻璃影 图 2 COVID-19典型病例2胸部CT表现(患者男性,37岁) |
|
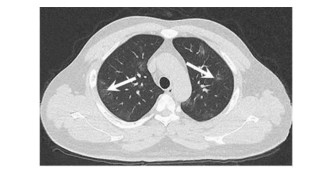
| 图 3 COVID-19典型病例3胸部CT表现(患者男性,35岁。双上肺多发散在斑片状磨玻璃影) |
2.5 治疗情况
患者分为轻型及普通型,入院后主要接受重组干扰素α1b(57例),并多采用口服克立芝(47例)、阿比多尔(18例)抗病毒治疗,少量患者使用达芦那韦考比司他片(8例),抗病毒同时应用乙酰半胱氨酸预防肺部纤维化、激素抗炎平喘。经隔离、充分休息、营养支持及维持电解质稳定等综合治疗后,57例患者均好转出院,见表 2。
| 类型 | 抗病毒 | 抗感染 | 临床结局 | |||||
| 干扰素α1b | 克立芝 | 达芦那韦考比司他片 | 阿比多尔 | 甲泼尼龙 | 乙酰半胱氨酸(片或针剂) | 好转 | 恶化 | |
| 轻型 | 13 | 8 | 2 | 3 | 0 | 13 | 13 | 0 |
| 普通型 | 44 | 39 | 6 | 15 | 8 | 44 | 44 | 0 |
| 合计 | 57 | 47 | 8 | 18 | 8 | 57 | 57 | 0 |
3 讨论
目前COVID-19作为一种新型冠状病毒肺炎,已被证实为人传人。研究发现男性较女性更易感MERS-CoV和SARS-CoV病毒[8-9],而本研究57例回顾性研究病例中,男性29例,占50.9%,女性28例,占49.1%,不同于疫区相关研究提出的男性多于女性[6],本地区性别分布未见明显差异。本研究中患者年龄在5~97岁,其中21~50岁患者共37例,占总数的64.91%。可能同该年龄段人群活动范围广、接触人群多、致感染机会增加有关。非疫区疫情发生主要以探亲、旅居及因公出差返当地后,多在当地区发病为主。明确有疫区(武汉)史占14.1%,而无疫区接触史,但通过流行病学调查获知其同确诊患者(近期有武汉经历)密切接触的占47.3%,其中1例患者回顾同确诊患者共处半小时后,于4 d后发病。上述表现反映各年龄段人群均易感,无性别倾向,疫情预防控制应着重关注该类人群。
本研究中COVID-19肺炎平均潜伏期为7.4 d,平均住院时间为10.1 d,而发病至出院时间平均15.6 d。其中13例(22.8%)患者因意识到或调查得知有明确接触史后,行核酸检查阳性收治入院隔离治疗,观察其在整个病程中无明显临床表现,此类患者属无症状感染者,该现象给疫情防控带来较大难度,因此加强接触者流行性病学调查追踪及群众宣传尤为必要。本研究57例患者中,共发生16起聚集性疫情,共涉及此病例中32人,占56.1%。所有病例中轻症占24.7%,普通型占75.3%,反映疫区外患者多以普通型为主,病情具有一定自限性。但有研究发现具有基础疾患的老年人或免疫力低下人群[8-11],易感性较强,且易进展为危重症,致死率较高,该类人群仍需重点关注。
57例确诊患者多以发热(40.4%)、干咳(26.6%)、乏力全身酸痛(8.8%)为首发症状,少数为腹泻、头痛不典型表现。该结果同WANG[5]和CHEN[6]的疫区住院患者特点相似。实验室检查中,白细胞、淋巴细胞绝对值减少明显,且80.7%患者C反应蛋白或超敏C反应蛋白升高,反映出COVID-19肺炎病毒引起机体炎症反应,且攻击人类T淋巴细胞免疫[12]造成抵抗力下降。对淋巴细胞亚群进一步检测,发现Th/Ts正常者占多数(42.1%),但其中仍有一定比例患者的CD4+、CD8+绝对值不同程度下降,10.5%患者Th/Ts升高,提示以CD8+淋巴细胞下降幅度较大,反映CD8+在病毒感染中耗损较重。有研究[13]证实CD8+主要通过细胞-细胞依赖性抑制或分泌抑制性炎症细胞因子如IL-10、TGFβ1来抑制抗原特异性或非特异性免疫反应,诱导免疫耐受,而COVID-19肺炎的部分患者迅速发展至感染性休克或呼吸窘迫综合征等危重疾病,除与病毒载量较多有关,可能同该病毒通过ACE2受体进入人体后损伤免疫淋巴细胞有关[14],导致自身免疫系统失调,严重时可引起炎症风暴导致多器官功能衰竭。因此,早期应用免疫球蛋白可能有助于提高抵抗力、抗炎及改善预后[4],但须进一步研究证实。本研究中多为普通型患者,病情好转时复测淋巴细胞较入院时明显升高。有研究推荐淋巴细胞绝对值可作为COVID-19诊断参考标准[6]。
嗜酸性粒细胞绝对值降低多见于烧伤、大手术等应激状态,临床意义较小,但此次COVID-19肺炎患者中,嗜酸性粒细胞绝对值降低比例占33.3%,为该疾病特点之一。同时,在入院时或住院中,患者心肌酶升高,ALT或AST升高,血钾多有降低,分别占5.3%、22.8%及40.4%,血小板平均体积升高占26.3%,故在临床治疗管理中,密切监测心肌酶、肝功能、电解质及凝血功能变化,尤其对于患有心功能不全、冠心病、心律失常、肝病等基础疾病的老年人,需引起关注。
COVID-19患者的CT典型表现多为两肺胸膜下(外周带)多发斑片状磨玻璃影[15],上中下叶均可累及。本研究中发现部分患者出院时核酸阴性时,复查CT病灶局部吸收,但患者临床症状已明显好转,故建议患者宜居家隔离14d,期间病情若有反复,需就近就诊排查是否复发可能。57例患者以轻型及普通型为主,入院后多采用重组干扰素α1b雾化,单独口服克立芝或联合阿比多尔抗病毒治疗,并应用乙酰半胱氨酸抗肺纤维化、纠正电解质紊乱及营养支持等治疗后好转,未有转为危重病例,考虑可能同病毒载量较少、感染人群以中青年为主、基础病少、抵抗力较强及就诊及时等有关。
综上所述,目前防疫严峻阶段,在接诊发热、干咳等类似上呼吸症状患者时,应详细询问疫区史、密切接触史,行胸部CT检测,结合实验室检查,综合判断,有利于减少漏诊率。对可疑患者,严格行流行病学调查,避免疏漏无症状感染者,做到应收尽收,应治尽治,将对控制传染源起到一定作用。本研究仍存在局限性,如样本量较少,单中心研究,危重患者资料有待进一步纳入分析,后期随访资料有待完善。
| [1] |
TANG J W, TAMBYAH P A, HUI D S C. Emergence of a novel coronavirus causing respiratory illness from Wuhan, China[J]. J Infect, 2020, 80(3): 350-371. DOI:10.1016/j.jinf.2020.01.014 |
| [2] |
HUI D S, I AZHAR E, MADANI T A, et al. The continuing 2019-nCoV epidemic threat of novel coronaviruses to global health—The latest 2019 novel coronavirus outbreak in Wuhan, China[J]. Int J Infect Dis, 2020, 91: 264-266. DOI:10.1016/j.ijid.2020.01.009 |
| [3] |
新冠病毒被定义为SARS姊妹病毒命名为SARS-CoV-2[EB/OL]. [2020-02-13]. |
| [4] |
HUANG C L, WANG Y M, LI X W, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China[J]. Lancet, 2020, 395(10223): 497-506. DOI:10.1016/S0140-6736(20)30183-5 |
| [5] |
WANG D W, HU B, HU C, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China[J]. JAMA, 2020. DOI:10.1001/jama.2020.1585 |
| [6] |
CHEN N S, ZHOU M, DONG X, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptivestudy[J]. Lancet, 2020, 395(10223): 507-513. DOI:10.1016/S0140-6736(20)30211-7 |
| [7] |
World Health Organization. Clinical management of severe acute respiratory infection when novel coronavirus (nCoV) infection is suspected: interim guidance, 25 January 2020[R]. WHO, 2020.
|
| [8] |
BADAWI A, RYOO S G. Prevalence of comorbidities in the Middle East respiratory syndrome coronavirus (MERS-CoV): a systematic review and meta-analysis[J]. Int J Infect Dis, 2016, 49: 129-133. DOI:10.1016/j.ijid.2016.06.015 |
| [9] |
CHANNAPPANAVAR R, FETT C, MACK M, et al. Sex-based differences in susceptibility to severe acute respiratory syndrome coronavirus infection[J]. J Immunol, 2017, 198(10): 4046-4053. DOI:10.4049/jimmunol.1601896 |
| [10] |
MOXLEY G, POSTHUMA D, CARLSON P, et al. Sexual dimorphism in innateimmunity[J]. Arthritis Rheum, 2002, 46(1): 250-258. DOI:10.1002/1529-0131(200201)46:1<250::AID-ART10064>3.0.CO;2-T |
| [11] |
DRYDEN M, BAGUNEID M, ECKMANN C, et al. Pathophysiology and burden of infection in patients with diabetes mellitus and peripheral vascular disease: focus on skin and soft-tissueinfections[J]. Clin Microbiol Infect, 2015, 21. DOI:10.1016/j.cmi.2015.03.024 |
| [12] |
LIU W J, ZHAO M, LIU K F, et al. T-cell immunity of SARS-CoV: Implications for vaccine development against MERS-CoV[J]. Antiviral Res, 2017, 137: 82-92. DOI:10.1016/j.antiviral.2016.11.006 |
| [13] |
李秀秀, 邱继花, 闵亚楠, 等. CD8+调节性T细胞在ITP发病中的意义及大剂量地塞米松的影响[J]. 临床血液学杂志, 2016, 29(3): 375-378. LI X X, QIU J H, MIN Y N, et al. The role of CD8+ regulatory T cell and the effect of high-dose dexamethasone in patients with immune thrombocytopenia[J]. J Clin Hematol, 2016, 29(3): 375-378. DOI:10.13201/j.issn.1004-2806.2016.05.007 |
| [14] |
XU X T, CHEN P, WANG J F, et al. Evolution of the novel coronavirus from the ongoing Wuhan outbreak and modeling of its spike protein for risk of humantransmission[J]. Sci China Life Sci, 2020, 1-4. DOI:10.1007/s11427-020-1637-5 |
| [15] |
LEI J Q, LI J F, LI X, et al. CT imaging of the 2019 novel coronavirus (2019-nCoV) pneumonia[J]. Radiology, 2020, 200236. DOI:10.1148/radiol.2020200236 |



