Notch信号属五大基础发育信号,经典Notch信号主要由Notch配体(Jag1,Jag2,Delta-like1、3、4)及Notch受体(Notch1~4)组成[1-2],在细胞增殖、分化、迁移、凋亡等生理过程中具有重要作用[3-6]。Notch配体结合膜受体经furin样转化酶(furin-like convertase)、金属蛋白酶(metalloprotease, ML)/肿瘤坏死因子-α转换酶(TNF-α converting enzyme, TACE)及r-分泌酶(r-secretase)水解后形成可溶性Notch胞内结构域(NICD)转移至细胞核,上调下游Hes家族及Hey家族靶基因的表达激活Notch信号[7-8]。
骨髓间充质干细胞/基质细胞(bone marrow stromal cells, BMSCs)具有强大的增殖及多向分化的潜能,可形成成纤维细胞克隆集落(CFU-F)或骨、软骨类似聚集体[9],被广泛用于骨组织工程基础及临床研究。骨细胞由间充质干细胞/基质细胞经历成骨细胞分化而来,占骨骼细胞的90%~95%[10],形成能及时响应激素和机械变化的特殊网管结构,动态调控骨微环境影响BMSCs成骨分化[11-12]。近年来大量研究证实,骨细胞亦具有分泌功能,其本身及分泌的生物因子能产生特定微环境直接或间接影响骨髓基质细胞成骨分化及部分骨科疾病的发生发展[13-16]。
激活骨细胞Notch信号突变鼠表型不一:有研究发现激活骨细胞Notch信号导致骨髓基质细胞成骨分化成熟障碍导致骨量增加[17-18];另有研究发现激活骨细胞Notch信号可抑制祖细胞向成骨分化导致骨量降低[19-22]。为了明确激活骨细胞Notch对BMSCs成骨分化的影响,本研究在体外利用Ad-Cre激活Notch信号的骨细胞与BMSCs共培养观察其对成骨分化的影响,并探究潜在的机制。
1 材料与方法 1.1 实验材料 1.1.1 实验小鼠4~6周龄野生C57BL/6小鼠购自重庆医科大学实验动物中心;4~6周龄RosaNotch小鼠购自美国Jackson实验室,由重庆医科大学实验动物中心代养繁殖。RosaNotch老鼠携带靶向构建编码NICD的DNA序列的Rosa26基因座,前部携带可经Cre工具酶作用后缺失导致可溶性Notch胞内结构域(NICD)组成型表达的双侧loxP位点修饰的STOP盒。实验过程中所有动物实验操作符合重庆医科大学动物实验中心伦理及操作要求。
1.1.2 主要试剂完全培养基:10%胎牛血清(FBS,Gibco)+89% α-MEM/DMEM/F12-DMEM/DMEM(HyClone)+1%青霉素-链霉素(PS,HyClone);0.25%胰蛋白酶(HyClone);Ad-Cre、Ad-GFP(重庆德诺和生物科技);BCIP/NBT碱性磷酸酶显色及碱性磷酸酶检测试剂盒、BCA蛋白浓度测定试剂盒(上海碧云天);TRIzol (Invitrogen);逆转录试剂盒、Syber Green Supermix(大连宝生物公司),Vit C、β-磷酸甘油、地塞米松、茜素红(塞米克)、qPCR引物由上海生工设计并由武汉金斯瑞生物科技有限公司合成,具体引物序列见表 1、2。
| 基因 | 正义链(5′→3′) | 反义链(5′→3′) |
| GAPDH | GCACAGTCAAGGCCGAGAAT | GCCTTCTCCATGGTGGTGAA |
| Hes1 | TACCCCAGCCAGTGTCAACA | TCCATGATAGGCTTTGATGACTTTC |
| Hey1 | CACTGCAGGAGGGAAAGGTTAT | CCCCAAACTCCGATAGTCCAT |
| HeyL | GAAGCGCAGAGGGATCATAGA | CCAATCGTCGCAATTCAGAA |
| Jag1 | TGGCCGAGGTCCTACACTT | GCCTTTTCAATTATGCTATCAGG |
| Jag2 | TCCTCCTGCTGCTTTGTGAT | TTGCAGGGCTGAAAGACAC |
| Dll1 | GGGACAGAGGGGAGAAGATG | TCCATGTTGGTCATCACACC |
| Dll3 | GGGGGCAGCTGTAGTGAA | ACATCGAAGCCCGTAGAATC |
| Dll4 | AGGTGCCACTTCGGTTACAC | GGGAGAGCAAATGGCTGATA |
| 基因 | 正义链(5′→3′) | 反义链(5′→3′) |
| DMP1 | CATTCTCCTTGTGTTCCTTTGG | TCAGTATTGTGGTATCTGGCAACT |
| Sost | CGTGCCTCATCTGCCTACTTGTG | CCGGTTCATGGTCTGGTTGTTCTC |
| ALP | ACACCAATGTAGCCAAGAATGTCA | GATTCGGGCAGCGGTTACT |
| Runx2 | CCGGTCTCCTTCCAGGAT | GGGAACTGCTGTGGCTTC |
| Osterix | CCCTTCTCAAGCACCAATGG | AAGGGTGGGTAGTCATTTGCATA |
| VEGF | AGCACAGCAGATGTGAATGC | AATGCTTTCTCCGCTCTGAA |
| HIF1α | AGTTCCGCAAGCCCTGAAAGC | TCAGTGGTGGCAGTGGTAGTGG |
| CD31 | GCCTAGTGTGGAAGCCAACA | GAGCCTTCCGTTCTCTTGGT |
| EMCN | CCACAGTGAGGACGGCAAAGATG | CGATGCCTGGTATTGTGACAGAGG |
1.1.3 实验仪器
37 ℃ 5%CO2细胞培养箱(Thermo Fisher),常温高速、低速离心机(平凡仪器),低温高速离心机(Sigma),倒置荧光显微镜(Nikon)。
1.1.4 实验细胞人胚肾293细胞(human embryonic kidney-293, HEK 293)购自ATCC公司,野生C57BL/6小鼠BMSCs,RosaNotch小鼠骨细胞于重庆医科大学生命科学研究院细胞培养室培养。
1.2 方法 1.2.1 基因型鉴定采集出生后14 d左右新生鼠耳部组织于含0.1 mg/mL蛋白酶K消化液中56 ℃消化过夜,提取DNA进行普通PCR扩增后于1.5%琼脂糖凝胶中进行凝胶电泳分离,并采集图像分析鉴定。
1.2.2 骨髓基质细胞及骨细胞的分离培养取4~6周龄RosaNotch小鼠提取骨细胞[23],即无菌条件下去除双侧股骨、胫骨肌肉组织及干骺端后剪至1~2 mm3,1 mg/mL Ⅰ型胶原酶37 ℃ 120 r/min消化3次,5 mmol/L EDTA和1 mg/mL Ⅰ型胶原酶溶液37 ℃、120 r/min交替消化各3次;收集每次处理后消化液并加入等体积含10%FBS的α-MEM完全培养基中和置冰上保存。合并前3次消化所得细胞称f1-3,合并中间3次细胞称f4-6,合并最后3次细胞称f7-9,骨碎片生长出细胞称BC。f1-3、f4-6、f7-9及BC各组细胞以2×105/孔铺板,α-MEM完全培养基37 ℃ 5%CO2孵箱中培养5 d后进行ALP染色、ALP生化定量检测,qPCR检测成骨细胞标志物ALP及骨细胞标志物DMP1、Sost mRNA转录水平。1 mL无菌注射器冲出4~6周龄野生C57BL/6小鼠骨髓腔内细胞[24],800 r/min离心5 min重悬后加入F12/DMEM完全培养基,置37 ℃ 5%CO2孵箱中培养。骨碎片中生长出的细胞经形态学观察及特异性标志物[25]检测后鉴定为骨细胞(图 1)。
|
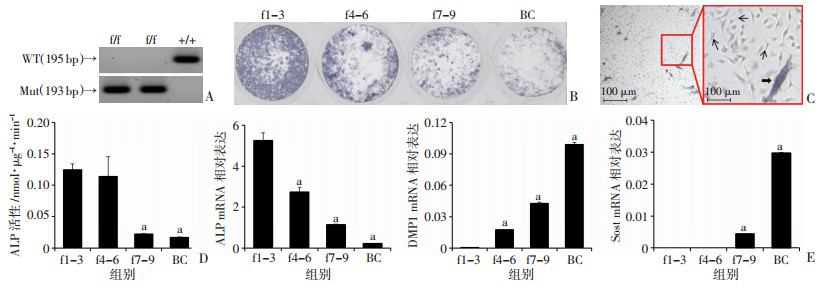
| A:PCR扩增后凝胶电泳鉴定小鼠基因型;B、D:对f1-3、f4-6、f7-9、BC中的细胞进行ALP染色及ALP生化定量检测;C:显微镜下观察骨细胞形态,粗箭头代表成骨细胞,细箭头代表骨细胞;E:qPCR检测成骨分化标志物ALP及骨细胞标志物DMP1、Sost(n=3);a:P < 0.05,与f1-3比较 图 1 小鼠基因型鉴定 |
1.2.3 腺病毒扩增及感染滴度测定
实验过程中所用到的病毒均由HEK293细胞(DMEM完全培养基中培养)利用Ad-Easy系统扩增,并利用按照绿色荧光蛋白标记法进行滴度测定[26],滴度测定结果分别为:Ad-GFP: 2.07×1011 GFU/mL,Ad-Cre: 1.83×1011GFU/mL。骨细胞按照2×104/孔铺板(24孔板)贴壁后,分别加入稀释10倍后的Ad-GFP及Ad-Cre 2、4、8、16、32、64 μL进行感染(n=3),倒置荧光显微镜下观察最佳感染滴度,最终本实验中Ad-GFP及Ad-Cre病毒原液的使用量均为1.6 μL/2×104。
1.2.4 骨细胞与BMSCs共培养骨细胞以2×104/孔铺板,贴壁后加入相应腺病毒作用24 h后,无菌PBS缓冲液清洗后分别向Blank组、Ad-GFP组及Ad-Cre组中加入8×104/孔野生C57BL/6小鼠BMSCs共培养,共培养5 d后进行ALP染色,提取ALP生化定量样本及RNA样本进行后续操作(n=3)。
1.2.5 ALP染色细胞培养5 d后按照BCIP/NBT碱性磷酸酯酶显色试剂盒说明书进行ALP染色,去离子水清洗后显微镜下观察并采集图像(n=3)。
1.2.6 ALP活性测定BCA蛋白浓度测定:培养5 d后每孔加入300 μL 50 mmol/L pH=7.4 Tris-HCl,超声破碎仪破碎细胞后离心收集上清,按BCA蛋白浓度测定试剂盒操作检测λ=592 nm处光密度值,并根据标准曲线计算样品蛋白量。ALP含量及活性测定:根据碱性磷酸酶测定试剂盒操作测定λ=405 nm处光密度并记录作用时间,根据标准底物浓度曲线计算ALP物质的量;根据蛋白量与ALP物质的量及作用时间计算ALP相对活性(n=3)。
1.2.7 细胞总RNA提取、逆转录及qPCR共培养5 d后,Trizol提取总RNA,按照TaKaRa逆转录试剂盒操作说明于冰上依次加入相应试剂制备cDNA,产物5倍稀释后采用qPCR技术测定相应目的基因mRNA的转录水平。所有基因转录水平均以GAPDH基因表达量作为对照(n=3)。引物序列见表 1、2。
1.2.8 茜素红染色(钙盐沉积实验)共培养3 d后将α-MEM完全培养基更换为含50 mg/L Vit C、0.1 μmol/L地塞米松及10 mmol/L β-磷酸甘油的成骨诱导培养基,37 ℃、5%CO2条件下培养21 d后按照茜素红染色试剂盒说明书进行染色,去离子水清洗后普通光学显微镜下观察并采集图像(n=3)。
1.2.9 统计学分析使用SPSS17.0对实验数据进行分析,结果以x±s表示;采用单因素方差分析比较多组间差异,student t检验比较两组间差异。检验水准α=0.05。
2 结果 2.1 RosaNotch小鼠基因型及骨细胞鉴定提取RosaNotch小鼠DNA扩增后分别对WT和Mut序列进行PCR扩增及鉴定,仅表达Mut序列(flox序列)不表达WT基因者为RosaNotch小鼠(f/f),仅表达WT基因不表达Mut序列者为野生型小鼠(+/+)(图 1A)。
f1-3、f4-6、f7-9及BC各组细胞以2×105/孔铺板,5 d后进行ALP染色、ALP生化定量及qPCR检测。ALP染色结果显示BC组展示最弱ALP染色强度(图 1B);普通光学显微镜下观察骨细胞突触多、体积小,成骨细胞突触少、体积大(图 1C);ALP生化定量显示f7-9 ALP活性相较f1-3、f4-6显著降低(P < 0.05),BC组ALP活性较f7-9显著降低(P < 0.05,图 1D);qPCR结果显示成骨分化标志物ALP mRNA转录水平在各组中的表达相继降低(P < 0.05),该结果与ALP染色及ALP生化定量结果相符;骨细胞特异性标志物DMP1、Sost在BC中高度表达(P < 0.05),而在f1-3、f4-6中未检测到(图 1E)。以上结果提示BC组生长出的细胞绝大部分为骨细胞,可用于后续实验。
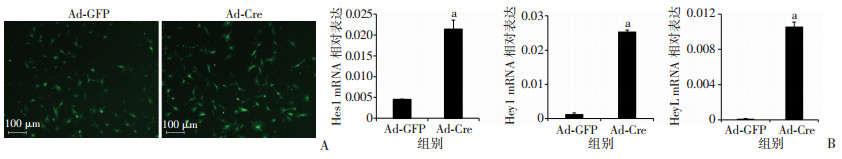
2.2 Ad-Cre激活RosaNotch骨细胞Notch信号RosaNotch小鼠骨细胞以2×105/孔铺板至24孔板,贴壁后分别加入Ad-GFP及Ad-Cre腺病毒,24 h后于倒置荧光显微镜下观察骨细胞中绿色荧光蛋白表达情况,光镜下显示细胞状态良好,转染效率高于50%(图 2A)。5 d后提取mRNA检测Notch信号特异性靶基因表达。qPCR结果显示Ad-Cre组Notch信号特异性靶基因Hes1、Hey1、HeyL相较Ad-GFP组显著增高(P < 0.05,图 2B),提示骨细胞Notch信号成功激活。
|
| A:荧光观察Ad-GFP、Ad-Cre感染RosaNotch小鼠骨细胞;B:qPCR检测骨细胞Notch信号靶基因Hes1、Hey1、HeyL表达情况(n=3);a:P < 0.05,与Ad-GFP组比较 图 2 Ad-Cre激活RosaNotch小鼠骨细胞Notch信号 |
2.3 激活骨细胞Notch信号抑制BMSCs成骨分化标志物表达及钙盐沉积水平
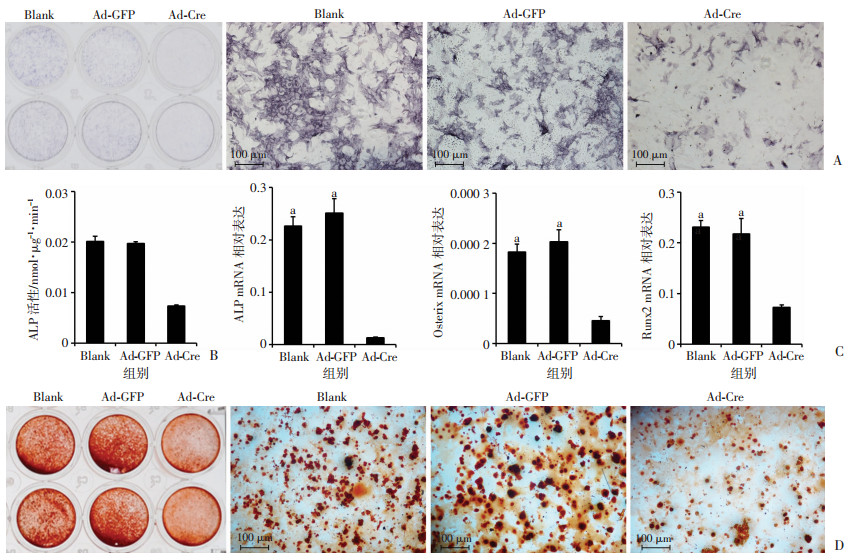
根据实验设计检测共培养5 d后进行ALP染色、ALP生化定量、成骨分化标志物及钙盐沉积水平检测。ALP染色结果显示Blank组与Ad-GFP组无显著差异,Ad-Cre组相较Blank组及Ad-GFP组显著降低(图 3A);该结果与ALP生化定量及ALP mRNA转录水平(图 3B、C)相符。qPCR结果显示Ad-Cre组共培养物成骨标志物Runx2及Osterix mRNA转录水平相较Ad-GFP组及Blank组显著降低(P < 0.05)。茜素红染色结果显示成骨诱导培养基共培养21 d后Ad-Cre组钙盐沉积水平显著低于Blank组及Ad-GFP组,Blank组与Ad-GFP组间未见统计学差异(图 3C、D)。因此,激活骨细胞Notch信号可抑制BMSCs成骨分化及钙盐沉积水平。
|
| A、B:ALP染色及ALP生化定量检测Ad-GFP和Ad-Cre作用RosaNotch骨细胞后与BMSCs共培养ALP表达水平;C:qPCR检测激活Notch信号骨细胞与野生型C57BL/6小鼠BMSCs共培养成骨分化标志物ALP、Osterix、Runx2 mRNA转录水平(n=3);D:茜素红染色检测21 d钙盐沉积水平;a:P < 0.05,与Ad-Cre组比较 图 3 激活骨细胞中Notch信号对BMSCs成骨分化标志物转录水平及钙盐沉积的影响 |
2.4 激活骨细胞中Notch信号对Notch配体表达的影响
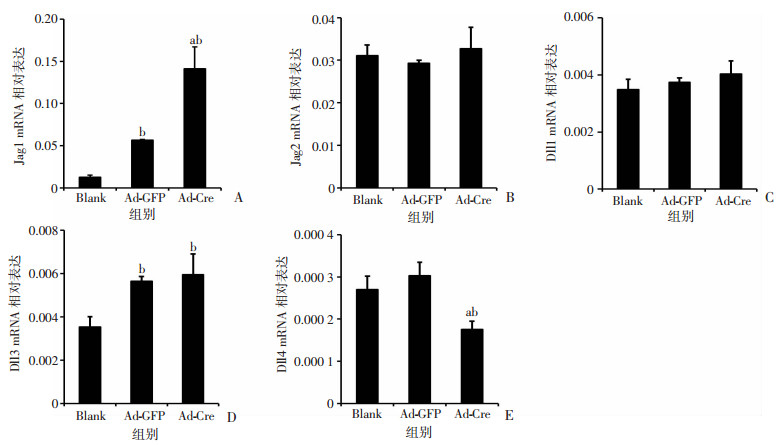
进一步检测激活Notch信号骨细胞与BMSCs共培养后Notch配体表达情况,qPCR结果显示Jag1 mRNA转录水平较Blank组及Ad-GFP组显著升高(P < 0.05,图 4A),Jag2、Dll1 mRNA转录水平较Ad-GFP及Blank组无统计学差异(图 4B、C);Ad-GFP组及Ad-Cre组中Dll3的表达较Blank组均显著增高(P < 0.05,图 4D);Dll4 mRNA转录水平较Blank组及Ad-GFP组显著降低(P < 0.05,图 4E)。
|
| A~E:qPCR检测激活Notch信号骨细胞与BMSCs共培养产物中Notch配体Jag1、Jag2、Dll1、Dll3、Dll4 mRNA转录水平;a:P < 0.05,与Ad-GFP组比较;b:P < 0.05,与Blank组比较 图 4 激活Notch信号骨细胞与BMSCs共培养物Notch配体表达情况(n=3) |
2.5 激活骨细胞Notch信号对成血管因子表达的影响
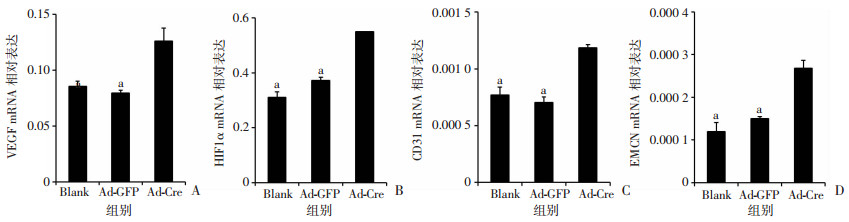
Notch配体与血管生成紧密相关,本研究进一步检测成血管相关标志物VEGF、CD31、HIF1α、EMCN mRNA转录水平。qPCR结果显示激活骨细胞Notch信号后共培养物VEGF、CD31、HIF1α、EMCN mRNA转录水平较Blank组及Ad-GFP组显著增高(P < 0.05),而Blank组与Ad-GFP组间无显著差异(图 5)。
|
| A~D:分别为VEGF、HIF1α、CD31、EMCN mRNA转录水平;a:P < 0.05,与Ad-Cre组比较 图 5 激活Notch信号骨细胞与野生型小鼠BMSCs共培养物成血管因子表达情况(n=3) |
3 讨论
Notch信号是高度保守的信号传导通路,研究显示激活同一细胞谱系不同分化状态细胞可造成不同影响[21, 27-28]:激活2.3 kb Ⅰ型胶原启动子通过直接结合Runx2抑制反式激活功能抑制早期成骨细胞的分化发育,刺激早期成骨细胞增殖[27],导致成骨细胞成熟障碍和功能异常的编织骨沉积,造成骨量增加和生长迟缓;激活3.6 kb Ⅰ型胶原启动子控制的NICD通过抑制干细胞/祖细胞的成骨分化导致成骨细胞数量减少、骨量减少[21]。
CANALIS等[19]利用DMP1-10kb-Cre激活骨细胞经典Notch信号可导致骨质疏松症,但该研究过程中同时激活突变鼠骨细胞及成骨细胞中Notch信号,因此该结果不能证实仅激活骨细胞Notch信号对BMSCs成骨分化的影响。本研究利用Ad-Cre体外激活骨细胞Notch信号后与野生C57BL/6小鼠BMSCs共培养观察对BMSCs成骨分化的影响,结果显示野生C57BL/6 BMSCs与激活Notch信号骨细胞共培养ALP染色及21 d细胞外基质矿化水平相较Ad-GFP组及Blank组显著降低;qPCR结果显示成骨分化标志物(ALP、Osterix、Runx2)表达相较Ad-GFP组及Blank组显著降低(P < 0.05),因此激活骨细胞Notch信号可抑制BMSCs早期成骨分化及晚期细胞外基质矿化水平。过去大量Notch信号过表达小鼠模型研究产生争议的原因可能系同时激活多阶段成骨细胞系细胞Notch信号,祖细胞、骨细胞Notch信号活性低,未产生显著抑制表型,而骨髓基质细胞或成骨细胞中Notch活性较强,可观察到骨量发生显著增加[29]。TU等[30]的研究发现激活骨细胞Wnt信号小鼠骨量显著增高,Notch信号受体及配体亦处于过表达状态,在此基础上利用DAPT抑制Notch信号可抑制由激活骨细胞Wnt信号促进的成骨分化[31];WANG等[32]的研究发现激活Notch信号导致Runx2和早期成骨分化因子下调但不影响p-Smad 1/5/8的表达,DAPT阻断Notch信号后通过过表达p-Smad 1/5/8影响成骨分化,故激活骨细胞Wnt信号及成骨细胞Notch信号的强大成骨作用将激活骨细胞内Notch信号的抑制成骨作用抵消,最终表现为高骨量表型。Notch信号在血管内皮发育过程中亦发挥重要作用[33],研究显示Dll4负调节血管内皮生长因子介导的血管发芽和分支[34];且Notch配体Dll4与Jag1在调节血管生成中的作用相反[35]。基于以上研究基础,本研究进一步检测血管生成标志物及Notch配体的表达情况,qPCR结果显示成血管标志物VEGF、HIF1α、CD31、EMCN及Notch配体Jag1 mRNA转录水平显著增高(P < 0.05),Dll4 mRNA转录水平显著降低(P < 0.05)。因此,研究结果提示激活骨细胞Notch信号可能通过增高Jag1、降低Dll4促进BMSCs成血管因子及内皮细胞因子表达从而降低成骨分化。
激活不同分化阶段成骨谱系细胞Notch信号可对成骨分化产生不同影响,本研究证实体外激活骨细胞Notch信号抑制BMSCs成骨分化。接下来本研究将进一步明确具体作用机制,同时利用DMP1-8kb-Cre工具鼠与RosaNotch小鼠构建激活骨细胞Notch信号的转基因小鼠,进行动、静态骨组织变化检测及转录组测序,进一步明确具体作用分子及作用机制。
| [1] |
BI P P, KUANG S H. Notch signaling as a novel regulator of metabolism[J]. Trends Endocrinol Metab, 2015, 26(5): 248-255. DOI:10.1016/j.tem.2015.02.006 |
| [2] |
CAMPBELL D P, CHRYSOSTOMOU E, DOETZLHOFER A. Canonical Notch signaling plays an instructive role in auditory supporting cell development[J]. Sci Rep, 2016, 6: 19484. DOI:10.1038/srep19484 |
| [3] |
CHEUNG L, LE TISSIER P, GOLDSMITH S G, et al. NOTCH activity differentially affects alternative cell fate acquisition and maintenance[J]. Elife, 2018, 7: e33318. DOI:10.7554/eLife.33318 |
| [4] |
COLOMBO M, THVMMLER K, MIRANDOLA L, et al. Notch signaling drives multiple myeloma induced osteoclastogenesis[J]. Oncotarget, 2014, 5(21): 10393-10406. DOI:10.18632/oncotarget.2084 |
| [5] |
KUSHWAH R, GUEZGUEZ B, LEE J B, et al. Pleiotropic roles of Notch signaling in normal, malignant, and developmental hematopoiesis in the human[J]. EMBO Rep, 2014, 15(11): 1128-1138. DOI:10.15252/embr.201438842 |
| [6] |
WAHI K, BOCHTER M S, COLE S E. The many roles of Notch signaling during vertebrate somitogenesis[J]. Semin Cell Dev Biol, 2016, 49: 68-75. DOI:10.1016/j.semcdb.2014.11.010 |
| [7] |
COLOMBO M, GALLETTI S, GARAVELLI S, et al. Notch signaling deregulation in multiple myeloma: a rational molecular target[J]. Oncotarget, 2015, 6(29): 26826-26840. DOI:10.18632/oncotarget.5025 |
| [8] |
ZANOTTI S, CANALIS E. Notch signaling and the skeleton[J]. Endocr Rev, 2016, 37(3): 223-253. DOI:10.1210/er.2016-1002 |
| [9] |
NG A H, BAHT G S, ALMAN B A, et al. Bone marrow stress decreases osteogenic progenitors[J]. Calcif Tissue Int, 2015, 97(5): 476-486. DOI:10.1007/s00223-015-0032-3 |
| [10] |
BONEWALD L F. The role of the osteocyte in bone and nonbone disease[J]. Endocrinol Metab Clin N Am, 2017, 46(1): 1-18. DOI:10.1016/j.ecl.2016.09.003 |
| [11] |
ANSARI N, HO P W, CRIMEEN-IRWIN B, et al. Autocrine and paracrine regulation of the murine skeleton by osteocyte-derived parathyroid hormone-related protein[J]. J Bone Miner Res, 2018, 33(1): 137-153. DOI:10.1002/jbmr.3291 |
| [12] |
TOKARZ D, MARTINS J S, PETIT E T, et al. Hormonal regulation of osteocyte perilacunar and canalicular remodeling in the hyp mouse model of X-linked hypophosphatemia[J]. J Bone Miner Res, 2018, 33(3): 499-509. DOI:10.1002/jbmr.3327 |
| [13] |
DELGADO-CALLE J, ANDERSON J, CREGOR M D, et al. Bidirectional notch signaling and osteocyte-derived factors in the bone marrow microenvironment promote tumor cell proliferation and bone destruction in multiple myeloma[J]. Cancer Res, 2016, 76(5): 1089-1100. DOI:10.1158/0008-5472.CAN-15-1703 |
| [14] |
JÄHN K, KELKAR S, ZHAO H, et al. Osteocytes acidify their microenvironment in response to PTHrP in vitro and in lactating mice in vivo[J]. J Bone Miner Res, 2017, 32(8): 1761-1772. DOI:10.1002/jbmr.3167 |
| [15] |
LIU W, WANG Z Y, YANG J, et al. Osteocyte TSC1 promotes sclerostin secretion to restrain osteogenesis in mice[J]. Open Biol, 2019, 9(5): 180262. DOI:10.1098/rsob.180262 |
| [16] |
NAKASHIMA T, HAYASHI M, FUKUNAGA T, et al. Evidence for osteocyte regulation of bone homeostasis through RANKL expression[J]. Nat Med, 2011, 17(10): 1231-1234. DOI:10.1038/nm.2452 |
| [17] |
CANALIS E, ADAMS D J, BOSKEY A, et al. Notch signaling in osteocytes differentially regulates cancellous and cortical bone remodeling[J]. J Biol Chem, 2013, 288(35): 25614-25625. DOI:10.1074/jbc.M113.470492 |
| [18] |
XU Y, SHU B, TIAN Y, et al. Notch activation promotes osteoblast mineralization by inhibition of apoptosis[J]. J Cell Physiol, 2018, 233(10): 6921-6928. DOI:10.1002/jcp.26592 |
| [19] |
CANALIS E, BRIDGEWATER D, SCHILLING L, et al. Canonical Notch activation in osteocytes causes osteopetrosis[J]. Am J Physiol Endocrinol Metab, 2016, 310(2): E171-E182. DOI:10.1152/ajpendo.00395.2015 |
| [20] |
ZANOTTI S, CANALIS E. Activation of Nfatc2 in osteoblasts causes osteopenia[J]. J Cell Physiol, 2015, 230(7): 1689-1695. DOI:10.1002/jcp.24928 |
| [21] |
ZANOTTI S, SMERDEL-RAMOYA A, STADMEYER L, et al. Notch inhibits osteoblast differentiation and causes osteopenia[J]. Endocrinology, 2008, 149(8): 3890-3899. DOI:10.1210/en.2008-0140 |
| [22] |
DEREGOWSKI V, GAZZERRO E, PRIEST L, et al. Notch 1 overexpression inhibits osteoblastogenesis by suppressing wnt/β-catenin but not bone morphogenetic protein signaling[J]. J Biol Chem, 2006, 281(10): 6203-6210. DOI:10.1074/jbc.m508370200 |
| [23] |
SHAH K M, STERN M M, STERN A R, et al. Osteocyte isolation and culture methods[J]. Bonekey Rep, 2016, 5: 838. DOI:10.1038/bonekey.2016.65 |
| [24] |
MARIDAS D E, RENDINA-RUEDY E, LE P T, et al. Isolation, culture, and differentiation of bone marrow stromal cells and osteoclast progenitors from mice[J]. J Vis Exp, 2018(131): 56750. DOI:10.3791/56750 |
| [25] |
ISO T, KEDES L, HAMAMORI Y. HES and HERP families: multiple effectors of the Notch signaling pathway[J]. J Cell Physiol, 2003, 194(3): 237-255. DOI:10.1002/jcp.10208 |
| [26] |
KRATZER R F, KREPPEL F. Production, purification, and titration of first-generation adenovirus vectors[J]. Methods Mol Biol, 2017, 1654: 377-388. DOI:10.1007/978-1-4939-7231-9_28 |
| [27] |
ENGIN F, YAO Z Q, YANG T, et al. Dimorphic effects of Notch signaling in bone homeostasis[J]. Nat Med, 2008, 14(3): 299-305. DOI:10.1038/nm1712 |
| [28] |
HILTON M J, TU X L, WU X M, et al. Notch signaling maintains bone marrow mesenchymal progenitors by suppressing osteoblast differentiation[J]. Nat Med, 2008, 14(3): 306-314. DOI:10.1038/nm1716 |
| [29] |
SHAO J, ZHOU Y H, XIAO Y. The regulatory roles of Notch in osteocyte differentiation via the crosstalk with canonical Wnt pathways during the transition of osteoblasts to osteocytes[J]. Bone, 2018, 108: 165-178. DOI:10.1016/j.bone.2018.01.010 |
| [30] |
TU X L, DELGADO-CALLE J, CONDON K W, et al. Osteocytes mediate the anabolic actions of canonical Wnt/β-catenin signaling in bone[J]. Proc Natl Acad Sci USA, 2015, 112(5): E478-E486. DOI:10.1073/pnas.1409857112 |
| [31] |
任磊, 代光明, 林枭, 等. 骨细胞Wnt/β-Catenin通过Notch信号促进BMSCs成骨分化[J]. 中国骨质疏松杂志, 2018, 24(5): 600-605. REN L, DAI G M, LIN X, et al. Wnt/β-Catenin induces osteoblastic differentiation of BMCS via Notch signaling pathway by osteocytes[J]. Chin J Osteoporos, 2018, 24(5): 600-605. DOI:10.3969/j.issn.1006-7108.2018.05.008 |
| [32] |
WANG N, LIU W, TAN T, et al. Notch signaling negatively regulates BMP9-induced osteogenic differentiation of mesenchymal progenitor cells by inhibiting JunB expression[J]. Oncotarget, 2017, 8(65): 109661-109674. DOI:10.18632/oncotarget.22763 |
| [33] |
BIGAS A, ROBERT-MORENO A, ESPINOSA L. The Notch pathway in the developing hematopoietic system[J]. Int J Dev Biol, 2010, 54(6/7): 1175-1188. DOI:10.1387/ijdb.093049ab |
| [34] |
FRASER H M, HASTINGS J M, ALLAN D, et al. Inhibition of delta-like ligand 4 induces luteal hypervascularization followed by functional and structural luteolysis in the primate ovary[J]. Endocrinology, 2012, 153(4): 1972-1983. DOI:10.1210/en.2011-1688 |
| [35] |
BENEDITO R, ROCA C, SÖRENSEN I, et al. The notch ligands Dll4 and Jagged1 have opposing effects on angiogenesis[J]. Cell, 2009, 137(6): 1124-1135. DOI:10.1016/j.cell.2009.03.025 |



