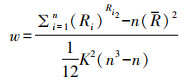2. 400038 重庆,陆军军医大学(第三军医大学):第一附属医院放射科;
3. 441003 湖北 襄阳,解放军第991医院精神科
2. Department of Radiology, First Affiliated Hospital, Army Medical University (Third Military Medical University), Chongqing, 400038;
3. Department of Psychiatry, No. 991 Hospital of PLA, Xiangyang, Hubei Province, 441003, China
目前,我国癌症发病率持续上升,随着现代医学的进步以及癌症诊疗手段的提高,癌症幸存者数量同样呈快速上升趋势,癌症幸存者对治疗后续的康复随访、提高生活质量的需求成为影响整个社会公共卫生领域的重要问题。乳腺癌已成为女性的头号杀手,并且在我国5年内诊断为癌症且存活的癌症患者中,女性乳腺癌患者最多[1]。虽然乳腺癌早期诊断和治疗水平的提高大大延长了患者的生命期限,但是乳腺癌幸存者(breast cancer survivor, BCS)长期处于慢性心理应激状态中,容易产生恐惧、焦虑等负性情绪[2],对癌症的复发恐惧(fear of cancer recurrence, FCR)成为其最突出的情绪特征,也是癌症复发的重要诱因。
癌症复发恐惧是指癌症患者针对癌症原发部位的发展情况、复发或是转移等情况产生恐惧心理[3]。据研究报道,55%~90%的乳腺癌幸存者存在对癌症复发的恐惧,过度的癌症复发恐惧与担忧不仅会降低患者参与治疗的依从性,影响疾病的预后,从而增加复发风险,还会影响其人际关系和生活质量,导致乳腺癌幸存者的幸福感降低[4]。此外,研究显示高癌症复发恐惧的癌症幸存者会有更多的就医行为,从而占用更多的医疗资源[5]。
作为一类非侵入式脑功能技术,静息态脑功能成像能够直接呈现脑功能激活区域、大小与确切位置,在空间分辨率上表现良好,具备可重复、无创性等优势。已有研究表明负性情绪会对大脑功能产生重要影响[6],本研究拟通过局部一致性(regional homogeneity, ReHo)脑成像数据处理技术指标,探讨乳腺癌幸存者的癌症复发恐惧的机制,以期寻找降低癌症复发恐惧,提高生存质量的有效方法。这对于乳腺癌幸存者的癌症康复具有重要意义。
1 资料与方法 1.1 研究对象2017年5-7月按照自愿报名的形式,对陆军军医大学第一附属医院乳腺甲状腺外科就诊的癌症复发恐惧乳腺癌幸存者进行招募,在试验前完成癌症复发恐惧量表与知情同意书的填写。按照癌症复发恐惧量表的划界分12分进行分组[7],得分12分以下的被试作为低癌症复发恐惧组,得分12分以上的被试作为高癌症复发恐惧组。参加正式试验的被试还需满足以下条件:①年龄在18周岁以上;②学历为初中及以上文化程度;③右利手;④视力或矫正视力在1.0以上;⑤无精神疾病、认知障碍和脑外伤;⑥未服用过作用于精神系统的相关药物。本研究于2016年9月获得陆军军医大学伦理委员会批准。
1.2 量表癌症复发恐惧量表(Fear of Cancer Recurrence Inventory, FCRI):该量表一共有42个题目,包括诱因、严重性、心理压力、应对策略、功能损害、自我认知和安心感共7个因子[8]。由于严重性因子与癌症复发恐惧总分呈高的正相关,因此在许多研究中直接将严重性因子作为短版的检测工具[9],共包括9个题目,它评估与FCR相关的侵入性思维的存在和严重性。每个项目都按照Likert等级进行评级,从0(“根本没有”或“从来”)到4(“很多”或“一直”)。更高的分数表示更高水平的FCR。本研究中Cronbach’s α系数为0.865。
1.3 图像采集每个被试的扫描工作均借助3T MRI(德国西门子产品)仪器完成。此工具将32通道头线圈当作射频信号接收机,同时通过海绵对待测人员头部加以固定,从而避免运动伪影的产生。在扫描期间,被试人员不需要进行任何操作,仅需呈仰卧位、两眼闭合、静止不动且保持清醒即可。在本试验中实施常规临床T1加权以及T2加权MRI扫描,并由2名曾进行过大量实践操作的放射科诊断医生进行现场诊断,从而确定存在器质性颅脑异常与否,明确无此异常方能够继续扫描。接着实施Resting-state Functional MRI (R-fMRI)数据采集,扫描序列的采集采用平面回波EPI序列完成。扫描EPI序列相关参数设置如下:重复时间TR为2 000 ms, 回波时间TE为30 ms, 翻转角为90°,视野FOV为192 mm×192 mm, 像素大小为3 mm×3 mm×3 mm,数据矩阵为64×64, 图像数合计量为240,扫描层数为轴位36层,层厚为3 mm。
1.4 数据预处理R-fMRI(静息态功能磁共振)数据于西门子工作站在光盘作用下被导出到配套的MATLAB平台。利用此平台的专属软件SPM8来预处理R-fMRI数据,借助软件DPARSF实施标准的预处理操作。具体流程为:删除前10个时间的图像,由于初始扫描阶段,磁共振仪器要接受匀场校准处理,从而将无均匀性的磁场干扰排除掉。因在整个扫描过程中被试者存在轻微的头动问题,需将全部图像于空间上对齐,然后把功能图像统一标准化处理至MNI空间内。ReHo的平滑是在预处理后的数据通过带通滤波(频率为0.01~0.08 Hz)处理后求解所得ReHo值,接着借助半高全宽(FWHM)的高斯核(4 mm)实施平滑处理。因大脑内脑白质、头动、脑脊液信号等因素对进一步分析可能存在一定干扰性,所以把此信号与6个方向的头动参数当作协变量回归,从而降低其干扰性,促进结果准确性提升。最后确定全部波段内0.01~0.08 Hz范围内信号,从而避免低频信号与高频信号的干扰。接着通过标准化处理至相应MNI模板上。
1.5 指标计算通过肯德尔和谐系数(KCC)对局部一致性状况进行度量,通过下述公示来求解给定体素的ReHo值:
w为k个体素的KCC值,即ReHo值,此体素时间序列KCC值的取值区间为0~1,本研究中,k取值等于27,即表示体素簇由目标体素和其邻近的26个体素总和构成;n为总秩次数,本研究中n=190;Ri为第i个时间点的秩和。KCC值用来对邻近体素时间序列的一致性以及相似性进行度量,此值愈趋于1,说明此类时间序列一致性愈高,反之则一致性愈差。
借助FWHM的高斯核(4 mm)平滑处理图像,从而促进其信噪比提升。最后,实施均值标准化(归一化)处理,从而使受试人员间差异性下降。通过对相关系数实施Fisher Z变换,能够使其与正态分布相符。
组间ReHo差异分析:在获得了两组被试的ReHo脑图后,采用SPSS 22.0统计软件,两组间比较采用独立样本t检验,P < 0.05被认为有统计学差异,并通过高斯随机场GRF(Gaussian random field)进行多重比较校正(P < 0.01, Z>2.32)。为研究ReHo值是否与癌症复发恐惧的相关性,采用Pearson相关系数对双方相关程度进行度量;当明确高癌症复发恐惧组与低癌症复发恐惧组具有组间差异的脑区后,将差异脑区作为感兴趣区(ROI),提取患者ROI内ReHo值,最后度量其与癌症复发恐惧的相关性。
2 结果 2.1 乳腺癌幸存者的人口学资料本研究招募被试62例,因3例低复发恐惧被试未完成全部实验被剔除,最终得到59例被试,其中低癌症复发恐惧组28例,高癌症复发恐惧组31例,人口学资料见表 1。
| 变量 | 低癌症复发恐惧组(n=28) | 高癌症复发恐惧组(n=31) |
| 年龄/岁 | ||
| 30~~ < 40 | 3(10.71) | 6(19.36) |
| 40~ < 50 | 19(67.86) | 11(35.48) |
| ≥50 | 6(21.43) | 14(45.16) |
| 婚姻状况 | ||
| 未婚 | 2(7.14) | 1(3.23) |
| 已婚 | 18(64.29) | 29(93.54) |
| 离异 | 7(25.00) | 1(3.23) |
| 丧偶 | 1(3.57) | 0(0.00) |
| 受教育程度 | ||
| 小学 | 0(0.00) | 0(0.00) |
| 中学 | 10(35.71) | 8(25.81) |
| 高中/中专 | 8(28.58) | 9(29.03) |
| 大学及以上 | 10(35.71) | 14(45.16) |
| 就业情况 | ||
| 工作 | 4(14.29) | 12(38.71) |
| 无业 | 13(46.43) | 7(22.58) |
| 退休 | 11(39.28) | 12(38.71) |
| 家庭年收入/万元 | ||
| <5 | 3(10.71) | 0(0.00) |
| 5~ < 10 | 10(35.71) | 8(25.81) |
| 10~ < 30 | 8(28.58) | 9(29.03) |
| ≥30 | 7(25.00) | 14(45.16) |
| 患病时间/年 | ||
| <2 | 12(42.86) | 17(54.84) |
| 2~ < 5 | 12(42.86) | 13(41.94) |
| 5~ < 10 | 3(10.71) | 1(3.22) |
| ≥10 | 1(3.57) | 0(0.00) |
| 癌症分级 | ||
| Ⅰ | 5(17.86) | 6(19.36) |
| Ⅱ | 21(75.00) | 24(77.42) |
| Ⅲ | 2(7.14) | 1(3.22) |
| Ⅳ | 0(0.00) | 0(0.00) |
| 手术方式 | ||
| 乳房切除术 | 27(96.43) | 27(87.10) |
| 保守治疗 | 0(0.00) | 1(3.23) |
| 乳房切除+乳房重建 | 1(3.57) | 3(9.67) |
2.2 高/低癌症复发恐惧乳腺癌幸存者ReHo值差异
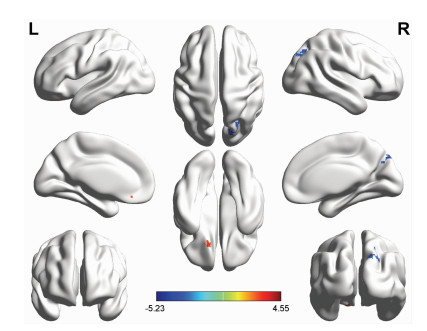
与低癌症复发恐惧组比较,高癌症复发恐惧组乳腺癌幸存者在静息状态下脑的BOLD信号的ReHo增高部位为左侧尾状核,ReHo降低部位为右侧楔前叶(P < 0.01,图 1、表 2)。
|
| 红色区域为高癌症复发恐惧组比低癌症复发恐惧ReHo值增高部位,蓝色区域为ReHo值降低部位 图 1 高/低癌症复发恐惧乳腺癌幸存者ReHo值存在差异的脑区图 |
| 脑区位置 | BA | MNI坐标 | t值 | 体素/mm3 | ||
| x | y | z | ||||
| 左侧尾状核 | 47 | -12 | 21 | -27 | 4.55 | 99 |
| 右侧楔前叶 | 7 | 21 | -78 | 36 | -5.23 | 93 |
| BA: Broadmann脑区;MNI坐标:大脑三维坐标系统 | ||||||
2.3 差异脑区与癌症复发恐惧相关性分析
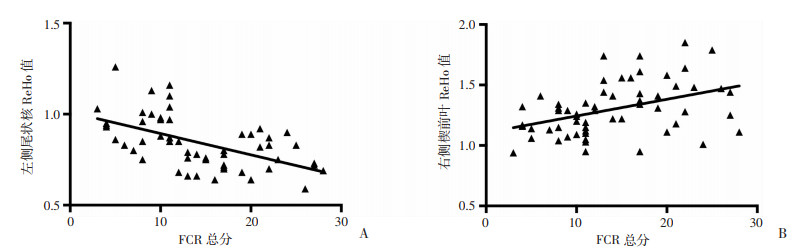
将上述具有ReHo值显著差异的脑区作为ROI,提取出被试的每个感兴趣区的平均ReHo值,最后计算其与癌症复发恐惧的相关关系。结果发现,左侧尾状核与癌症复发恐惧呈显著负相关(r=-0.501,P < 0.05);右侧楔前叶与癌症复发恐惧呈显著正相关(r=0.505,P < 0.05),见图 2。
|
| 图 2 左侧尾状核(A)与右侧楔前叶(B)的ReHo值与癌症复发恐惧的相关性分析 |
3 讨论
本研究采集了31例高癌症复发恐惧乳腺癌幸存者和28例低癌症复发恐惧的大脑功能磁共振成像数据,采用ReHo方法来研究两组被试的差异。通过ReHo的方法发现,两组被试存在显著差异的脑区主要位于尾状核和楔前叶部位。提示:癌症复发恐惧可能导致左侧尾状核脑区神经元活动的时间一致性增强,而右侧楔前叶脑区神经元活动的时间一致性降低。
局部一致性被认为是一类具备高重测信度、以数据驱动为基础的方法[10]。此方法能够对局部脑区神经元自发性行为的瞬间变化进行逐一体素的测定,可避免不同任务范式的混杂因素干扰。通过该方法发现高癌症复发恐惧乳腺癌幸存者的左侧尾状核的ReHo值增强。尾状核作为纹状体的重要结构,是基底神经节的关键构成单元,在控制随意运动中起到重要的作用,同时也参与了程序学习、联想学习、情感以及睡眠等重要功能的调节[11]。在情感、学习、注意与记忆,尤其在信息加工以及反馈分析方面,近期尾状核的关键价值开始受到各位研究人员的高度关注。尾状核对各种情绪刺激发生非特异性反应,例如对奖赏的事件或者信号做出反应而对不带奖赏性质的信号则没有反应。因此,已有研究认为尾状核是确保个体灵活应对环境的重要区域[12]。此外,研究者们发现尾状核还是情绪调控环路的重要组成结构,在皮层-纹状体-苍白球-丘脑这一神经调控环路形成中发挥一定作用,而此环路同边缘系统-前额叶这一环路互相配合,协作调控机体应对来自外部的正向或负向刺激,使机体情绪反射保持正常,所以,若尾状核相关功能与结构等发生异常,可导致情绪调控系统异常,导致负性情绪的发生[13]。在对动物的实验中也得到了类似的结果,研究者通过动物的磁共振成像研究发现尾状核控制情绪决策和悲观情绪,并且尾状核异常活动可能在某种程度上干扰了多巴胺活跃性[14]。本研究发现处于高复发恐惧状态的乳腺癌幸存者,对癌症相关情绪刺激出现敏感反应,容易导致情绪调控失衡,出现焦虑、恐惧等情绪失调状况。因此,尾状核的异常活动可能是高低癌症复发恐惧的乳腺癌幸存者的重要差异。
通过ReHo这一方法还发现楔前叶是两组被试存在显著差异的脑区。楔前叶作为大脑默认网络的重要组成部分,分布在头顶叶内侧范围,为DMN的构成节点,同超强的认知机能、工作记忆以及情绪处理相关,是静息状态下神经元最为活跃的脑区之一[15-16]。与这些研究一致的是,本研究发现高癌症复发恐惧患者的左右侧楔前叶的ReHo值相对低癌症复发恐惧患者增加。楔前叶作为DMN的关键脑区,若楔前叶与DMN其他脑区功能协同性减弱,会对DMN内部、DMN同其他脑网络间的机能协同(或资源分配)产生干扰,导致患者癌症复发恐惧情绪的出现。
本研究采用因ReHo法只体现局部脑组织的机能连接状况,因此,在今后的研究中, 还应进一步借助以体素水平为基础的对称体素同伦连接法评价ReHo值不正常脑区同相应侧半球同一范围的机能不正常状态。其次,采用静息态脑功能成像技术是一种理想的状态,在试验中只能要求被试尽量不做任何思维活动,也只是尽可能地接近静息状态,有可能会对数据造成影响。此外,本研究对象未排除用药因素,对脑功能成像的结果可能有一定的影响,因此,还有待今后深入的研究。
综上所述,本研究应用ReHo脑成像数据分析方法,发现高癌症复发恐惧乳腺癌幸存者局部脑功能活动不正常脑区,提示癌症复发恐惧患者大脑两半球功能明显异常;同时,从客观上证明了不同癌症复发恐惧的乳腺癌幸存者之间存在明显差异。本研究通过探索癌症复发恐惧对乳腺癌幸存者脑功能活动的影响,为筛选高癌症复发恐惧的风险人群提供了客观依据,并为临床工作者尽早对患者进行心理干预提供了参考,这对于癌症幸存者的疾病康复具有重要的意义。
| [1] |
CHEN W Q, ZHENG R S, BAADE P D, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132. DOI:10.3322/caac.21338 |
| [2] |
ALMEIDA S N, ELLIOTT R, SILVA E R, et al. Fear of cancer recurrence: a qualitative systematic review and meta-synthesis of patients' experiences[J]. Clin Psychol Rev, 2019, 68: 13-24. DOI:10.1016/j.cpr.2018.12.001 |
| [3] |
VICKBERG S M. The Concerns About Recurrence Scale (CARS): a systematic measure of women's fears about the possibility of breast cancer recurrence[J]. Ann Behav Med, 2003, 25(1): 16-24. DOI:10.1207/S15324796ABM2501_03 |
| [4] |
HALBACH S M, ENDERS A, KOWALSKI C, et al. Health literacy and fear of cancer progression in elderly women newly diagnosed with breast cancer: a longitudinal analysis[J]. Patient Educ Couns, 2016, 99(5): 855-862. DOI:10.1016/j.pec.2015.12.012 |
| [5] |
SARKAR S, SAUTIER L, SCHILLING G, et al. Anxiety and fear of cancer recurrence and its association with supportive care needs and health-care service utilization in cancer patients[J]. J Cancer Surviv, 2015, 9(4): 567-575. DOI:10.1007/s11764-015-0434-2 |
| [6] |
CHAURET M, SUFFREN S, PINE D S, et al. Fear conditioning and extinction in anxious youth, offspring at-risk for anxiety and healthy comparisons: an fMRI study[J]. Biol Psychol, 2019, 148: 107744. DOI:10.1016/j.biopsycho.2019.107744 |
| [7] |
PENG L, HUANG W R, ZHANG W M, et al. Psychometric properties of the short form of the fear of cancer recurrence inventory (FCRI) in Chinese breast cancer survivors[J]. Front Psychiatry, 2019, 10: 537. DOI:10.3389/fpsyt.2019.00537 |
| [8] |
SIMARD S, SAVARD J. Fear of Cancer Recurrence Inventory: development and initial validation of a multidimensional measure of fear of cancer recurrence[J]. Support Care Cancer, 2009, 17(3): 241-251. DOI:10.1007/s00520-008-0444-y |
| [9] |
SIMARD S, SAVARD J. Screening and comorbidity of clinical levels of fear of cancer recurrence[J]. J Cancer Surviv, 2015, 9(3): 481-491. DOI:10.1007/s11764-015-0424-4 |
| [10] |
ZANG Y F, JIANG T Z, LU Y L, et al. Regional homogeneity approach to fMRI data analysis[J]. Neuroimage, 2004, 22(1): 394-400. DOI:10.1016/j.neuroimage.2003.12.030 |
| [11] |
VILLABLANCA J R. Why do we have a caudate nucleus?[J]. Acta Neurobiol Exp (Wars), 2010, 70(1): 95-105. |
| [12] |
ZINK C F, PAGNONI G, MARTIN-SKURSKI M E, et al. Human striatal responses to monetary reward depend on saliency[J]. Neuron, 2004, 42(3): 509-517. DOI:10.1016/s0896-6273(04)00183-7 |
| [13] |
FILIPOVIC B R, DJUROVIC B, MARINKOVIC S, et al. Volume changes of corpus striatum, thalamus, Hippocampus and lateral ventricles in posttraumatic stress disorder (PTSD) patients suffering from headaches and without therapy[J]. Cent Eur Neurosurg, 2011, 72(3): 133-137. DOI:10.1055/s-0030-1253349 |
| [14] |
AMEMORI K I, AMEMORI S, GIBSON D J, et al. Striatal microstimulation induces persistent and repetitive negative decision-making predicted by striatal beta-band oscillation[J]. Neuron, 2018, 99(4): 829-841. DOI:10.1016/j.neuron.2018.07.022 |
| [15] |
DECO G, JIRSA V K, MCINTOSH A R. Emerging concepts for the dynamical organization of resting-state activity in the brain[J]. Nat Rev Neurosci, 2011, 12(1): 43-56. DOI:10.1038/nrn2961 |
| [16] |
CAVANNA A E, TRIMBLE M R. The precuneus: a review of its functional anatomy and behavioural correlates[J]. Brain, 2006, 129(Pt 3): 564-583. DOI:10.1093/brain/awl004 |