Aminopeptidase N(APN,EC 3.4.11.2)含967个氨基酸残基,相对分子质量为150×103,与CD13的序列完全一样,是细胞表面跨膜糖蛋白和锌依赖性外肽酶,属于M1家族金属蛋白酶,其编码基因位于15号染色体的长臂q25~26位置[1],在内皮细胞、小肠和肾近端小管的刷状缘膜上高度表达[2],在肝肿瘤、乳腺肿瘤、前列腺肿瘤等多种肿瘤细胞中高度表达,参与肿瘤细胞的增殖、浸润和肿瘤血管的生成[3-5],另外有研究表明APN参与肿瘤细胞的耐药[6],因此APN是肿瘤治疗的潜在靶点。
胶质瘤是原发性神经上皮细胞神经系统恶性肿瘤,约占成年人颅内系统肿瘤的一半,可以发生在神经系统的任何部位[7]。目前胶质瘤的标准治疗方法是手术切除术后放化疗,但胶质瘤患者的预后不佳,经过标准化、综合治疗的生存期为12~15个月,5年生存率只有不到5%[8]。由于胶质瘤的恶性程度高,预后不良,因此急需寻找更加有效的治疗方法。APN在众多肿瘤中作为促癌基因,可以作为潜在的肿瘤治疗靶点。我们此前的预实验发现APN在胶质瘤组织中高表达,但是APN在胶质瘤中的作用还未知。因此, 本实验旨在探究APN在胶质瘤中的作用,并试图探究其作用机制,以探索胶质瘤治疗的新靶点。
1 材料与方法 1.1 材料与试剂人胶质瘤细胞株U251购于上海生命科学院细胞库,高糖DMEM培养基、胎牛血清购于美国Gibco公司,青霉素、链霉素购于重庆蒙博生物科技有限公司。APN干扰序列由上海吉凯基因化学技术有限公司合成,APN:前链: 5′-CCCTCTTCATTCACTTCAGAA-3′;后链: 5′-TTCTGAAGTGAATGAAGAGGG-3′。阴性对照、嘌呤霉素购于上海吉凯基因化学技术有限公司,RNAiso Plus、Primescript RT reagent Kit、TB green购于TaKaRa公司,抗APN、抗p-STAT3、抗t-STAT3、抗Bcl-2、抗MMP-2和β-actin购于Abcam,辣根过氧化物酶标记山羊抗兔、羊抗鼠二抗购于北京中山金桥生物技术有限公司,Matrigel购于Corning公司。
1.2 细胞培养、慢病毒转染U251细胞培养于含10%和1%青-链霉素的高糖DMEM培养基中,在37 ℃、5%CO2孵箱中培养,细胞融合度达80%~100%时进行细胞传代和细胞处理。将U251分为Blank(空白对照)、NC-siRNA、APN-siRNA 3组,Blank组不进行病毒转染,NC-siRNA组进行阴性对照病毒转染,APN-siRNA组进行阳性病毒转染,U251融合度在25%~30%进行慢病毒转染,转染时间为24 h,慢病毒转染48 h后加入嘌呤霉素杀死未转染病毒的U251细胞,进行细胞筛选,慢病毒转染72 h后在荧光倒置显微镜下观察转染效率。
1.3 RT-qPCR检测各组U251细胞用RNAiso Plus试剂按厂家使用说明提取总RNA,提取到总RNA后用Primescript RT reagent Kit进行cDNA逆转录,然后进行RT-qPCR,APN前链为5′-CCAGGCAGTGACACGACGAT-3′,后链为5′-CACCCACTTGATGTTGGCTTTC-3′,β-actin前链为5′-CCACGAAACTACCTTCAACTCC-3′,后链为5′-GTGATCTCCTTCTGCATCCTGT-3′。PCR反应程序为第一步,95 ℃ 30 s;第二步95 ℃15 s,60 ℃45 s重复40次;然后用2-ΔΔCt方法评估mRNA的表达变化。
1.4 Western blot检测各组U251细胞用含1%的PMSF的RIPA解液在冰上裂解细胞,收取裂解后的细胞液在4 ℃离心机12 000 r/min离心15 min,离心后取上清,加入20%上样缓冲液,在100 ℃条件下煮10 min,然后放-20 ℃备用。等量的蛋白样本被SDS-PAGE分离,转移到PVDF膜上,含有蛋白的PVDF膜用5%脱脂牛奶在水平摇床上室温下封闭60 min,分别用APN(1 :1 000)、p-STAT3(1 :2 000)、t-STAT3(1 :5 000)、Bcl-2(1 :1 000)、MMP-2(1 :1 000)和β-actin(1 :1 000)一抗在4 ℃条件下孵育过夜;用辣根过氧化物酶标记山羊抗兔和羊抗鼠二抗(1 :5 000)在水平摇床上室温孵育60 min;膜用TBST洗涤3次,每次10 min,用增强化学发光试剂进行曝光,利用图像实验室软件对每个条带的蛋白质含量进行定量分析。
1.5 细胞周期检测用70%预冷乙醇对1×106个不同组的U251细胞进行固定,用50 mg/mL碘化丙钠(PI)和50 mg/mL RNase在37 ℃下孵育30 min,用流式细胞仪分析细胞周期。
1.6 细胞凋亡检测1×106个各组U251细胞重悬在500 μL PBS中,用25 μg/mL propidium iodide和25 μg/mL Fluorescein isothiocyanate在37 ℃和暗室条件下孵育30 min,流式细胞仪分析细胞凋亡。
1.7 CCK-8检测分别在慢病毒转染24、48、72 h和96 h后,在96孔板中每孔加入10 μL CCK-8继续培养30 min,在酶标仪上450 nm处检测光密度值[D(450)]。
1.8 Transwell实验将Matrigel原液用无血清培养基以1 :2的比例稀释,每个24孔板的小室用60 μL稀释后的Matrigel包被,然后放入37 ℃培养箱中约30 min使Matrigel凝固,待Matrigel凝固后每孔加入不同处理的用无血清培养基重悬的不同组U251细胞约3×104个,下室每孔加入600 μL完全培养基,然后继续培养24 h,用棉签擦拭小室内残留的细胞和Matrigel,用甲醇固定15 min,再用0.1%结晶紫染色20 min,用双蒸水清洗3次,倒置显微镜随机选取上中下5个视野拍照计数(400×)。
1.9 细胞划痕实验将各组U251细胞进行6孔板铺板,待各组细胞融合度达90%~95%时用200 μL枪头作“十”字刮痕,PBS清洗细胞碎片,然后每孔加入无血清培养基并在倒置显微镜下拍照记录,继续培养24 h后在倒置显微镜下拍照对比迁移情况(40×)。
1.10 统计学分析采用SPSS 21.0软件进行数据处理分析,数据均用x±s表示,两组比较采用t检验,P < 0.05认为差异有统计学意义。
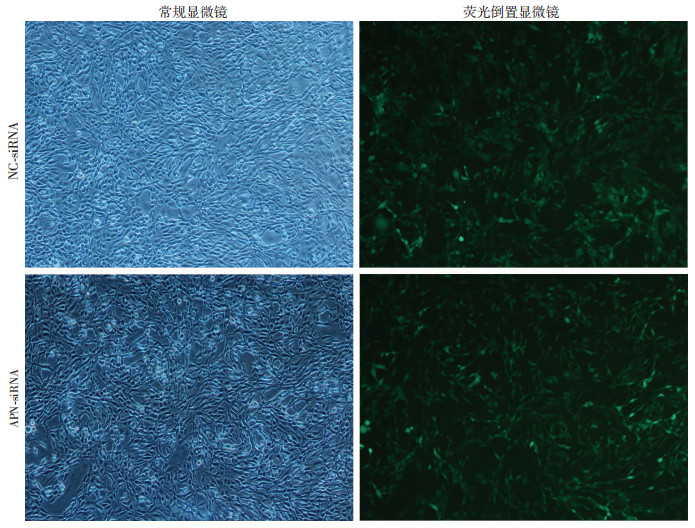
2 结果 2.1 APN-siRNA慢病毒载体感染人胶质瘤U251细胞将APN-siRNA和NC-siRNA的慢病毒转染进入U251细胞中培养72 h后,荧光倒置显微镜下观察发现80%以上的细胞都可见荧光(图 1),提示慢病毒转染成功。
|
| 图 1 U251细胞转染慢病毒72 h后荧光倒置显微镜观察 (×40) |
2.2 APN-siRNA抑制U251中APN的表达
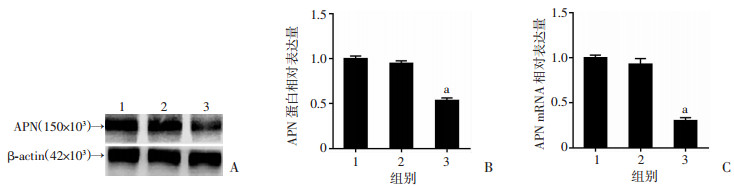
转染慢病毒72 h后,将转染率在80%以上的细胞进行Western blot和RT-qPCR实验。Western blot结果显示:与空白对照组相比, APN-siRNA组的APN蛋白表达水平明显下调,差异有统计学意义(P < 0.05),而NC-siRNA组与空白对照组相比无明显差别(图 2A、B);RT-qPCR显示:与空白对照组相比,APN-siRNA组的APN mRNA表达量降低, 差异有统计学意义(P < 0.01),而NC-siRNA组与空白对照组相比无明显差别(图 2C)。
|
| A:Western blot检测APN蛋白表达;B:APN蛋白半定量分析;C: APN mRNA表达 1:空白对照组;2:NC-siRNA组;3:APN-siRNA组;a: P < 0.01,与空白对照组比较 图 2 RNA干扰后APN在U251中的表达变化 |
2.3 沉默APN能抑制U251的增殖
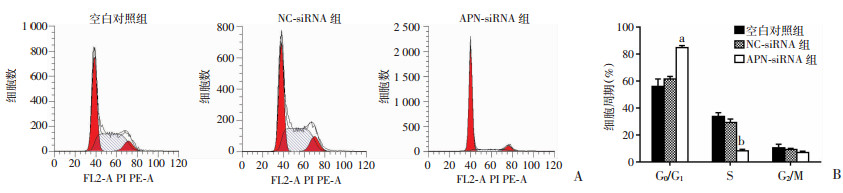
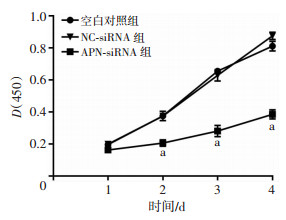
利用流式细胞仪检测各组细胞周期,结果显示与空白对照组相比,APN-siRNA组的S期比例明显减低,G0/G1期比例明显升高,差异有统计学意义(P < 0.05),NC-siRNA组与空白对照组相比无明显差别(图 3)。采用CCK-8在慢病毒转染后24、48、72 h和96 h时检测各组细胞的增殖活性,结果显示与空白对照组相比,NC-siRNA的活性无明显改变,而APN-siRNA组细胞与空白对照组相比在48、72 h和96 h增殖活性明显下降(P < 0.01,图 4)。
|
| A:流式细胞仪检测细胞周期;B:细胞周期的分布 a: P < 0.05,b: P < 0.01,与空白对照组比较 图 3 流式细胞仪检测沉默U251细胞APN后对细胞周期的影响 |
|
| a: P < 0.01,与空白对照组比较 图 4 不同处理组U251细胞的CCK-8增殖曲线 |
2.4 沉默APN能降低U251的迁移和侵袭能力
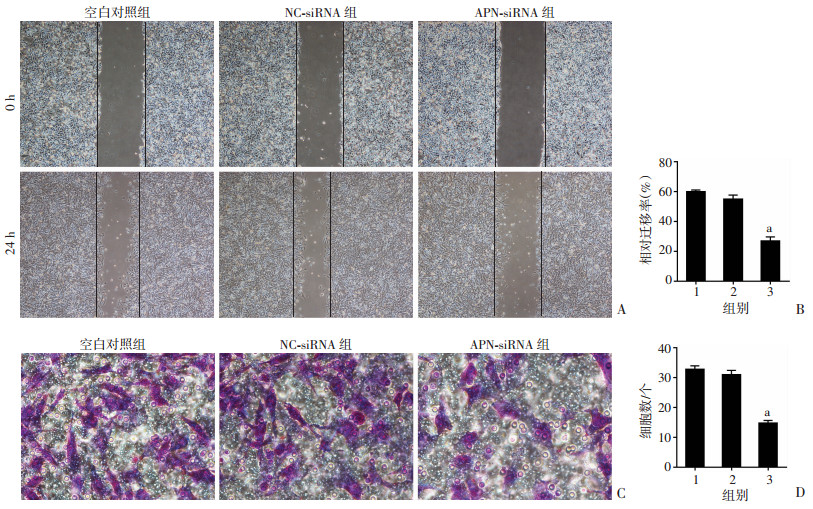
采用划痕实验来检测APN对胶质瘤细胞U251的迁移能力,结果表明APN-siRNA组的迁移能力比空白对照组明显减弱,差异有统计学意义(图 5A、B,P < 0.01);用Transwell的方法来检测各组U251细胞的侵袭能力,结果表明与空白对照组相比,APN-siRNA组的细胞显著减少(P < 0.05),NC-siRNA组与空白对照组无明显差异(P>0.05, 图 5C、D)。
|
| A、B:划痕实验检测U251细胞迁移能力的变化(×40);C、D:Transwell实验检测U251细胞侵袭能力的变化(×400) 1:空白对照组;2:NC-siRNA组;3:APN-siRNA组;a: P < 0.01,与空白对照组比较 图 5 沉默U251细胞APN后对其迁移、侵袭能力的影响 |
2.5 沉默APN能诱导U251凋亡
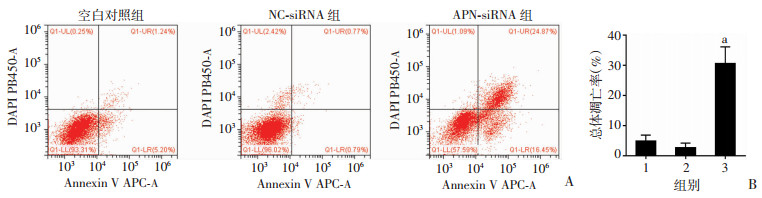
采用流式细胞仪检测沉默胶质瘤细胞U251中APN的表达对凋亡的影响,结果显示:APN-siRNA组与空白对照组的凋亡率差异有统计学意义(P < 0.01),NC-siRNA组与空白对照组的凋亡率无明显差异(P>0.05, 图 6)。
|
| A:流式细胞仪检测;B:细胞凋亡率分析 1:空白对照组;2:NC-siRNA组;3:APN-siRNA组;a: P < 0.01,与空白对照组比较 图 6 流式细胞仪检测沉默U251细胞APN后对其凋亡的影响 |
2.6 沉默APN抑制STAT3信号通路的激活
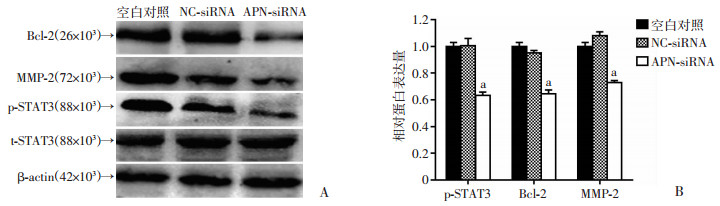
采用Western blot检测沉默U251细胞中APN的表达后STAT3及下游蛋白Bcl-2、MMP-2的表达变化,结果显示:与空白对照组相比,APN-siRNA组p-STAT3、Bcl-2、MMP-2的蛋白表达水平明显降低(P < 0.05),NC-siRNA组与空白对照组相比,p-STAT3、Bcl-2、MMP-2的蛋白表达水平没有明显变化(图 7)。
|
| A:Western blot检测STAT3通路蛋白的变化;B: STAT3信号途径蛋白半定量分析 a: P < 0.05,与空白对照组比较 图 7 沉默U251细胞中APN后对STAT3细胞通路的影响 |
3 讨论
胶质瘤占神经系统肿瘤的一半左右,由于胶质瘤生长在颅内,所以胶质瘤是国内外最棘手的肿瘤类型,探究胶质瘤的形成机制对于寻找有效的治疗方法有重要的意义。研究发现胶质瘤的发生发展与IDH的突变、1p/19q染色体的缺失、MGMT启动子的甲基化、TERT启动子的突变、EGFRvⅢ基因的突变等因素有关,其中这些基因的突变与缺失往往同时存在[9],基于对胶质瘤发生、发展过程中的认识研究者为胶质瘤的治疗不断开辟新的治疗方法。免疫疗法治疗肿瘤具有广阔的前景,免疫检查点抑制剂帕博利珠单抗和纳武利尤单抗已运用于恶性黑色素瘤、非小细胞肺癌、膀胱癌和霍奇金淋巴瘤等恶性肿瘤的治疗[10-11],但有研究表明免疫检查点抑制剂在胶质瘤的治疗中没有明显的效果[12],需要进一步的探索和寻找其他的有效治疗方法;CAR-T细胞疗法目前在血液系统肿瘤如急性淋巴细胞白血病[13]、B细胞淋巴瘤[14]、非小细胞肺癌[15]和胰腺癌[16]等肿瘤治疗中取得了不错的治疗效果,因此有学者运用CAR-T细胞疗法治疗胶质瘤,其用CAR-T细胞疗法靶向IL13Rα2、EGFRvⅢ和HER2[17]治疗胶质瘤取得了一定的治疗成果,表明CAR-T细胞疗法用于胶质瘤的治疗存在理论上的可行性。但是由于胶质瘤的复杂性和神经系统的特殊性,目前的治疗方法对于胶质瘤的治疗效果存在很大的局限性,因此需要不断地探究新的胶质瘤靶向治疗方法。
研究发现APN在许多肿瘤中扮演着促癌作用的角色,被认为是促癌基因。研究表明抑制急性淋巴细胞白血病肿瘤细胞的APN活性能通过PI3K或AKT信号途径诱导肿瘤细胞的凋亡[18],在膀胱癌肿瘤细胞中抑制APN活性通过AKT信号途径诱导膀胱癌细胞自噬凋亡[19];肿瘤细胞的增殖能力是肿瘤良恶性的关键,APN对某些肿瘤细胞增殖起着关键作用,在卵巢癌和肺癌细胞中APN的表达显著增加[20],研究发现Notch和Wnt/β-catenin是APN促进肿瘤细胞增殖的机制之一[21]。肿瘤细胞的远处转移和侵袭能力是判断肿瘤恶性程度的关键因素之一,研究发现在恶性肿瘤如肝癌、胃癌等细胞中存在APN的高表达,通过靶向抑制APN的活性能够抑制肝癌、胃癌细胞的运动能力[22]。学者们对APN在肝癌、胃癌、肺癌、白血病等肿瘤类型中的角色研究得出APN具有促进恶性肿瘤进程的作用,因此本研究探究胶质瘤细胞中APN的表达及其对于胶质瘤细胞的作用,为胶质瘤的治疗探寻新的靶向治疗方法。
为了寻找胶质瘤潜在的治疗靶点,我们在前期的实验中发现APN在胶质瘤组织标本中高表达,本研究试图探究胶质瘤细胞U251中APN的表达量,结果显示U251细胞中存在APN的表达。采用RNA干扰方法沉默U251中APN的表达来检测APN对胶质瘤细胞U251增殖活性、细胞周期、迁移和侵袭能力的影响,结果显示:沉默U251中APN的表达后U251的细胞活力明显下降;流式细胞显示细胞周期G1期的比例增加,S期的比例下降,并且U251细胞的凋亡比例明显增加;沉默APN后U251细胞的迁移能力或侵袭能力也明显受到抑制。本研究结果表明APN具有促进胶质瘤细胞U251增殖、迁移和侵袭能力的作用。
本研究发现STAT3信号途径参与肿瘤的发生、发展过程,STAT3在Tyr705位点磷酸化,然后通过诱导下游抗凋亡、促增殖侵袭蛋白的表达从而促进肿瘤进程[23]。本研究发现沉默U251细胞中APN的表达后STAT3的磷酸化水平明显降低,引起其下游抑制凋亡蛋白Bcl-2的表达下调,从而诱导了U251的凋亡,同时侵袭相关蛋白MMP-2的表达下调,抑制了胶质瘤U251的迁移和侵袭能力。
综上所述,APN在胶质瘤细胞U251中可通过STAT3信号通路促进胶质瘤的发展,因此靶向APN及其STAT3信号通路可能是胶质瘤治疗潜在的方法之一。
| [1] |
DIXON J, KAKLAMANIS L, TURLEY H, et al. Expression of aminopeptidase-n (CD 13) in normal tissues and malignant neoplasms of epithelial and lymphoid origin[J]. J Clin Pathol, 1994, 47(1): 43-47. DOI:10.1136/jcp.47.1.43 |
| [2] |
RESHEQ Y J, MENZNER A K, BOSCH J, et al. Impaired transmigration of myeloid-derived suppressor cells across human sinusoidal endothelium is associated with decreased expression of CD13[J]. J Immunol, 2017, 199(5): 1672-1681. DOI:10.4049/jimmunol.1600466 |
| [3] |
YAMANAKA C, WADA H, EGUCHI H, et al. Clinical significance of CD13 and epithelial mesenchymal transition (EMT) markers in hepatocellular carcinoma[J]. Jpn J Clin Oncol, 2018, 48(1): 52-60. DOI:10.1093/jjco/hyx157 |
| [4] |
MARTÍNEZ J M, PRIETO I, RAMÍREZ M J, et al. Aminopeptidase activities in breast cancer tissue[J]. Clin Chem, 1999, 45(10): 1797-1802. DOI:10.1093/clinchem/45.10.1797 |
| [5] |
ISHⅡ K, USUI S, SUGIMURA Y, et al. Aminopeptidase N regulated by zinc in human prostate participates in tumor cell invasion[J]. Int J Cancer, 2001, 92(1): 49-54. |
| [6] |
ZHANG J, FANG C Y, QU M H, et al. CD13 inhibition enhances cytotoxic effect of chemotherapy agents[J]. Front Pharmacol, 2018, 9: 1042. DOI:10.3389/fphar.2018.01042 |
| [7] |
AFFRONTI M L, HEERY C R, HERNDON J E 2nd, et al. Overall survival of newly diagnosed glioblastoma patients receiving carmustine wafers followed by radiation and concurrent temozolomide plus rotational multiagent chemotherapy[J]. Cancer, 2009, 115(15): 3501-3511. DOI:10.1002/cncr.24398 |
| [8] |
LIAO A H, CHOU H Y, HSIEH Y L, et al. Enhanced therapeutic epidermal growth factor receptor (EGFR) antibody delivery via pulsed ultrasound with targeting microbubbles for glioma treatment[J]. J Med Biol Eng, 2015, 35(2): 156-164. DOI:10.1007/s40846-015-0032-9 |
| [9] |
WELLER M, WICK W, ALDAPE K, et al. Glioma[J]. Nat Rev Dis Primers, 2015, 1: 15017. DOI:10.1038/nrdp.2015.17 |
| [10] |
HAMID O, ROBERT C, DAUD A, et al. Safety and tumor responses with lambrolizumab (anti-PD-1) in melanoma[J]. N Engl J Med, 2013, 369(2): 134-144. DOI:10.1056/NEJMoa1305133 |
| [11] |
BALAR A V, WEBER J S. PD-1 and PD-L1 antibodies in cancer: current status and future directions[J]. Cancer Immunol Immunother, 2017, 66(5): 551-564. DOI:10.1007/s00262-017-1954-6 |
| [12] |
FILLEY A C, HENRIQUEZ M, DEY M. Recurrent glioma clinical trial, CheckMate-143: the game is not over yet[J]. Oncotarget, 2017, 8(53): 91779-91794. DOI:10.18632/oncotarget.21586 |
| [13] |
GRUPP S A, KALOS M, BARRETT D, et al. Chimeric antigen receptor-modified T cells for acute lymphoid leukemia[J]. N Engl J Med, 2013, 368(16): 1509-1518. DOI:10.1056/NEJMoa1215134 |
| [14] |
SCHUSTER S J, SVOBODA J, CHONG E A, et al. Chimeric antigen receptor T cells in refractory B-cell lymphomas[J]. N Engl J Med, 2017, 377(26): 2545-2554. DOI:10.1056/nejmoa1708566 |
| [15] |
WEI X R, LAI Y X, LI J, et al. PSCA and MUC1 in non-small-cell lung cancer as targets of chimeric antigen receptor T cells[J]. Oncoimmunology, 2017, 6(3): e1284722. DOI:10.1080/2162402x.2017.1284722 |
| [16] |
HECKLER M, DOUGAN S K. Unmasking pancreatic cancer: epitope spreading after single antigen chimeric antigen receptor T-cell therapy in a human phase Ⅰ trial[J]. Gastroenterology, 2018, 155(1): 11-14. DOI:10.1053/j.gastro.2018.06.023 |
| [17] |
陈峰, 郑晓红, 李文斌. 脑胶质瘤免疫治疗进展[J]. 首都医科大学学报, 2019, 40(6): 966-971. CHEN F, ZHENG X H, LI W B. Immunotherapy for the treatment of glioma[J]. J Cap Med Univ, 2019, 40(6): 966-971. DOI:10.3969/j.issn.1006-7795.2019.06.028 |
| [18] |
PIEDFER M, DAUZONNE D, TANG R P, et al. Aminopeptidase-N/CD13 is a potential proapoptotic target in human myeloid tumor cells[J]. FASEB J, 2011, 25(8): 2831-2842. DOI:10.1096/fj.11-181396 |
| [19] |
WANG X Q, LIU Y, LIU W, et al. Ubenimex, an APN inhibitor, could serve as an antitumor drug in RT112 and 5637 cells by operating in an Aktassociated manner[J]. Mol Med Rep, 2018, 17: 4531-4539. DOI:10.3892/mmr.2018.8402 |
| [20] |
TERAUCHI M, KAJIYAMA H, SHIBATA K, et al. Inhibition of APN/CD13 leads to suppressed progressive potential in ovarian carcinoma cells[J]. BMC Cancer, 2007, 7: 140. DOI:10.1186/1471-2407-7-140 |
| [21] |
WANG R, SUN Q, WANG P, et al. Notch and Wnt/β-catenin signaling pathway play important roles in activating liver cancer stem cells[J]. Oncotarget, 2016, 7(5): 5754-5768. DOI:10.18632/oncotarget.6805 |
| [22] |
SAIKI I, FUJⅡ H, YONEDA J, et al. Role of aminopeptidase N (CD13) in tumor-cell invasion and extracellular matrix degradation[J]. Int J Cancer, 1993, 54(1): 137-143. DOI:10.1002/ijc.2910540122 |
| [23] |
BRANTLEY E C, BENVENISTE E N. Signal transducer and activator of transcription-3: a molecular hub for signaling pathways in gliomas[J]. Mol Cancer Res, 2008, 6(5): 675-684. DOI:10.1158/1541-7786.mcr-07-2180 |



