2. 110000 沈阳,锦州医科大学北部战区总医院:超声科
2. Department of Ultrasonography, General Hospital of Northern Theater Command, Jinzhou Medical University, Shenyang, Liaoning Province, 110000, China
东北地区及高海拔地区冬季严寒,夜晚温度更低,在此地区野外巡逻、站岗的战士长时间暴露在低温环境中,如果防护不当会造成急性冻伤[1],心脏也是受累器官之一。二维斑点追踪显像(two-dimensional speckle tracking imaging,2D-STI)是一种敏感而可靠的跟踪左心室(left ventricular,LV)重塑并评估心肌功能受损的技术[2-3]。本研究应用二维斑点追踪技术观测低温条件下兔左心室收缩功能随着时间的变化,以期为下一步低温条件下作业和站岗人员左心室收缩功能的评估提供一种无创伤性的方法,也为相关研究奠定实验基础。
1 材料与方法 1.1 实验动物健康新西兰兔30只,雌雄不限,体质量3~3.5 kg,由北部战区总医院实验动物中心提供。分成3组,对照组、低温4 h组(A组)和低温8 h组(B组),每组10只。对照组置于室温22~25 ℃,A、B组分别置于-25 ℃的冷冻柜内4、8 h。用8%硫化钡脱去兔躯体及四肢体毛,穿定制仿军大衣连体外套,放入冷冻柜中, 冷冻柜留有一定空隙,保证实验兔所需氧气。
1.2 超声检查选用GE Vivid 7彩色超声显像仪,10 s探头(10 MHz),所有家兔均采用戊巴比妥钠麻醉(1.5%,2 mL/kg),连接同步心电图后,左侧卧位。标准左心室长轴切面测量收缩末期左心房内径(LAESd)、舒张末期左心室内径(LVEDd)。双平面Simpson法测量左心室射血分数(left ventricular enjection fraction,LVEF)。TDI记录二尖瓣环室间隔侧运动频谱,测量收缩期峰值运动速度(peak systolic velocity, Sm)、舒张早期峰值运动速度(peak early diastolic velocity, Em)、舒张晚期峰值运动速度(peak end diastolic velocity, Am)。于心尖部采集四、三、二腔心及左室短轴基底段、中间段和心尖段各5个心动周期二维动态图像,于EchoPAC工作站脱机分析,选择清晰图像,手动勾画ROI,调节ROI直径至各节段均显示满意,得到各节段心肌纵向应变峰值(longitudinal strain, SL)、圆周应变峰值(circumferential strain, SC)、径向应变峰值(radial strain, SR)及曲线,记录整体及各水平SL、SC、SR,结果取5个心动周期平均值。
1.3 检验指标与组织学观察每组随机选取5只兔,行超声引导下股静脉穿刺,抽取静脉血进行检测。检测指标为血清天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、血清磷酸肌酸激酶(creatine kinase,CK)、血清磷酸肌酸激酶同工酶(creatine kinase isozyme,CK-MB)、高敏肌钙蛋白T(high-sensitivity cardiac troponin T,HS-TNT)。
检查及检验结束后,对所有家兔实施耳静脉空气栓塞安乐死,取左室前乳头肌及室壁心肌,进行固定、脱水、包埋、切片及HE染色。
1.4 统计学分析采用SPSS 21.0统计软件,计量资料以x±s表示。组间各参数比较采用单因素方差分析,组间两两比较采用LSD法,P < 0.05认为差异有统计学意义。
2 结果 2.1 常规超声参数及TDI比较与对照组比较,B组的LAESd、LVEDd、LVEF、Sm、Em、Am差异均有统计学意义(P < 0.05);与A组比较,B组的LAESd、LVEF差异有统计学意义(P < 0.05)。见表 1。
| 组别 | LAESd/mm | LVEDd/mm | LVEF/% | Sm/cm·s-1 | Em/cm·s -1 | Am/cm·s-1 |
| 对照组 | 8.80±1.39 | 12.80±1.39 | 82.00±4.73 | 4.80±0.63 | 6.26±1.13 | 8.28±1.24 |
| A组 | 9.00±1.05 | 13.40±1.17 | 78.80±3.79 | 4.40±0.69 | 5.96±1.01 | 7.88±1.07 |
| B组 | 10.10±0.56ab | 14.30±1.05a | 71.20±4.26ab | 3.80±1.03a | 4.83±1.17a | 6.90±1.52a |
| F值 | 4.33 | 3.83 | 16.77 | 3.88 | 4.59 | 3.00 |
| P值 | 0.023 | 0.034 | < 0.001 | 0.033 | 0.019 | 0.066 |
| a:P < 0.05,与对照组比较;b:P < 0.05,与A组比较 | ||||||
2.2 二维应变参数比较
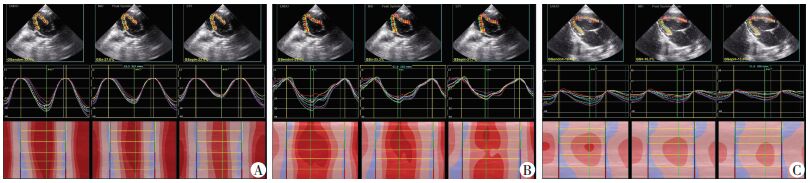
3组兔心尖三腔心切面左室心肌纵向应变曲线见图 1。随低温时间的延长,纵向应变曲线峰值延后、减低,曲线低平。与对照组比较,A组心尖段及整体SL、SC、SR显著减低(P < 0.05),B组基底段、中间段、心尖段及整体SL、SC、SR均显著减低(P < 0.05);与A组比较,B组基底段、中间段、心尖段及整体SL、SR均显著减低(P < 0.05)。见表 2~4。
|
| A:对照组;B:低温4 h组(A组);C:低温8 h组(B组) 图 1 各组兔心尖三腔心切面左室心肌纵向应变曲线图 |
| 组别 | 基底段 | 中间段 | 心尖段 | 整体 |
| 对照组 | -20.65±1.87 | -18.77±1.53 | -17.47±1.27 | -18.97±1.52 |
| A组 | -19.28±1.70 | -17.64±1.51 | -16.06±0.94a | -17.66±1.30a |
| B组 | -15.73±1.43ab | -14.31±1.17ab | -13.00±1.20ab | -14.35±1.23ab |
| F值 | 22.77 | 26.69 | 39.73 | 30.66 |
| P值 | < 0.001 | < 0.001 | < 0.001 | < 0.001 |
| a:P < 0.05,与对照组比较;b:P < 0.05,与A组比较 | ||||
| 组别 | 基底段 | 中间段 | 心尖段 | 整体 |
| 对照组 | -18.30±4.16 | -18.86±3.73 | -19.60±3.06 | -18.92±2.00 |
| A组 | -15.29±4.19 | -15.67±4.99 | -15.80±4.29a | -15.59±2.88a |
| B组 | -13.62±3.74a | -12.72±3.53a | -13.89±4.71a | -13.41±1.26ab |
| F值 | 3.43 | 5.48 | 5.07 | 16.57 |
| P值 | 0.047 | 0.010 | 0.013 | < 0.001 |
| a:P < 0.05,与对照组比较;b:P < 0.05,与A组比较 | ||||
| 组别 | 基底段 | 中间段 | 心尖段 | 整体 |
| 对照组 | 32.83±3.33 | 39.33±4.62 | 44.62±3.93 | 38.92±2.82 |
| A组 | 30.42±3.39 | 36.25±5.14 | 39.52±4.99a | 35.39±3.73a |
| B组 | 25.75±1.93ab | 31.02±3.69ab | 33.63±4.75ab | 30.13±3.18ab |
| F值 | 14.681 | 8.626 | 14.376 | 18.298 |
| P值 | < 0.001 | 0.001 | < 0.001 | < 0.001 |
| a:P < 0.05,与对照组比较;b:P < 0.05,与A组比较 | ||||
2.3 血液学检测指标比较
与对照组比较,A、B组的AST、CK、CK-MB、HS-TNT均增高,且B组增高更明显,差异均有统计学意义(P < 0.05);与A组比较,B组的AST、CK、CK-MB、HS-TNT均显著增高(P < 0.05,表 5)。
| 组别 | AST /U·L1 |
CK /U·L1 |
CK-MB /U·L1 |
HS-TNT /ng·mL1 |
| 对照组 | 106.27±3.46 | 1 147.00±46.61 | 636.80±28.52 | 0.01±0.00 |
| A组 | 132.14±2.99a | 1 614.20±100.69a | 855.40±46.63a | 0.12±0.02a |
| B组 | 208.13±3.50ab | 2 155.00±117.75ab | 1 237.80±49.33ab | 0.24±0.02ab |
| F值 | 1 262.49 | 145.81 | 255.99 | 163.81 |
| P值 | < 0.001 | < 0.001 | < 0.001 | < 0.001 |
| a:P < 0.05,与对照组比较;b:P < 0.05,与A组比较 | ||||
2.4 病理结果比较
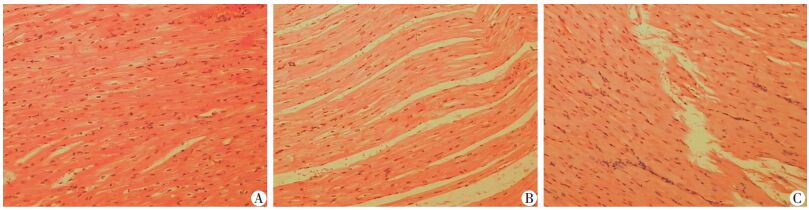
对照组:心肌纤维排列规则,胞浆粉染,核膜完整,细胞间隙正常(图 2A);A组:心肌纤维间隙增宽,心肌细胞轻度变性,局部可见炎性细胞聚集(图 2B);B组:心肌纤维部分断裂,心肌细胞崩解,胞核溶解,染色质淡染,可见大量炎性细胞(图 2C)。
|
| A:对照组;B:低温4 h组(A组);C:低温8 h组(B组) 图 2 HE染色观察3组兔心肌病理学形态(×100) |
3 讨论
心脏的主要功能是为肝、肾、脑等器官及组织提供充足的血流量以及氧和营养物质,是一个高耗能器官。心肌的供血主要来源于冠状动脉细小分支,做功所需的主要能量来源于ATP。长时间暴露于深低温环境称为意外性低温[4],而意外性低温造成的心肌损伤目前尚不清楚。本研究应用2D-STI探讨随低温时间延长,心肌不同程度受损,左心室收缩功能的改变。
低温造成心肌损伤的机制为:血液粘滞度增加[5],血管内血小板聚集、淤滞阻塞冠状动脉,心肌组织供血不足[6],随后循环血量减少,心腔内压力升高,左心室前、后负荷增加[7-8],进而心功能减低。有研究报道,低温15 ℃环境下5 h,大鼠循环血流量减少65%[9]。心肌缺血缺氧可造成心肌细胞酸中毒[8],可使心肌膜对Na+/K+-ATPase抑制,游离在胞质中的Ca2+清除率降低,细胞内Ca2+超负荷,抑制肌浆网对Ca2+的摄取和释放,从而导致ATP合成障碍[10],进而使细胞内活性氧(ROS)增多,过高水平的ROS诱导细胞氧化应激,损害心肌细胞线粒体生物能,诱导心肌细胞凋亡,最终出现整体心肌功能减低[11]。低温还可使皮肤血管收缩、儿茶酚胺释放和交感神经系统的兴奋,加重心肌缺氧缺血,引发心血管反射调节紊乱。
本研究显示,与对照组比较,低温B组LAESd、LVEDd、Sm、Em、Am、LVEF差异均有统计学意义(P < 0.05),说明低温时间延长会导致左室收缩功能减低。低温A组的LVEF较对照组差异无统计学意义(P>0.05)。很多研究也证明, 早期心脏病患者LVEF仍在正常范围[12-13]。2D-STI通过识别并连续追踪二维超声灰阶图像,能够定量评价局部及整体心肌运动,灵敏度明显高于常规超声心动图。既往研究也显示,STI可在亚临床早期发现左室功能的细微变化[14-15]。本研究显示,与对照组比较,A组心尖段及整体SL、SC、SR显著减低(P < 0.05),B组基底段、中间段、心尖段及整体SL、SC、SR均显著减低(P < 0.05)。随低温时间的延长,纵向应变曲线峰值延后、减低,曲线低平(图 1B、C),并与病理和检验结果相对应(图 2B、C)。
综上所述,本研究显示,随着低温时间的延长,心肌呈不同程度受损,应用2D-STI技术能够准确地评价低温环境下左室心肌收缩功能,可以尽早发现左室收缩功能减低及病变受累程度,指导临床医师及时进行干预治疗,对临床诊断及治疗具有重要意义。
| [1] |
毕名森, 曹军英, 张筠, 等. 声触诊组织定量技术评价低温条件下兔肝脏改变的初步研究[J]. 中国超声医学杂志, 2017, 33(7): 639-642. BI M S, CAO J Y, ZHANG Y, et al. Preliminary study of virtual touch tissue quantification technique estimating the change of liver in rabbits in low temperature condition[J]. Chin J Ultrasound Med, 2017, 33(7): 639-642. DOI:10.3969/j.issn.1002-0101.2017.07.020 |
| [2] |
SEO Y, ISHIZU T, ENOMOTO Y, et al. Validation of 3-dimensional speckle tracking imaging to quantify regional myocardial deformation[J]. Circ Cardiovasc Imaging, 2009, 2(6): 451-459. DOI:10.1161/CIRCIMAGING.109.858480 |
| [3] |
FU Q, XIE M X, WANG J, et al. Assessment of regional left ventricular myocardial function in rats after acute occlusion of left anterior descending artery by two-dimensional speckle tracking imaging[J]. J Huazhong Univ Sci Tech (Med Sci), 2009, 29(6): 786-790. DOI:10.1007/s11596-009-0623-1 |
| [4] |
FILSETH O M, HOW O J, KONDRATIEV T, et al. Post-hypothermic cardiac left ventricular systolic dysfunction after rewarming in an intact pig model[J]. Crit Care, 2010, 14(6): R211. DOI:10.1186/cc9334 |
| [5] |
GUTIERREZ G, WARLEY A R, DANTZKER D R. Oxygen delivery and utilization in hypothermic dogs[J]. J Appl Physiol, 1986, 60(3): 751-757. DOI:10.1152/jappl.1986.60.3.751 |
| [6] |
TVEITA T, YTREHUS K, SKANDFER M, et al. Changes in blood flow distribution and capillary function after deep hypothermia in rat[J]. Can J Physiol Pharmacol, 1996, 74(4): 376-381. DOI:10.1139/y96-028 |
| [7] |
MORLEY D, YAMANE K, O'MALLEY R, et al. Rewarming for accidental hypothermia in an urban medical center using extracorporeal membrane oxygenation[J]. Am J Case Rep, 2013, 14: 6-9. DOI:10.12659/AJCR.883728 |
| [8] |
MINE T, SATO I, KISHIMA H, et al. Left ventricular systolic dysfunction in a patient with accidental hypothermia: a case report[J]. J Med Case Rep, 2012, 6(1): 429. DOI:10.1186/1752-1947-6-429 |
| [9] |
KONDRATIEV T V, FLEMMING K, MYHRE E S, et al. Is oxygen supply a limiting factor for survival during rewarming from profound hypothermia?[J]. Am J Physiol Heart Circ Physiol, 2006, 291(1): H441-H450. DOI:10.1152/ajpheart.01229.2005 |
| [10] |
BOLLI R, MARBÁN E. Molecular and cellular mechanisms of myocardial stunning[J]. Physiol Rev, 1999, 79(2): 609-634. DOI:10.1152/physrev.1999.79.2.609 |
| [11] |
吴丽珍, 杜兴华, 雷艳, 等. 急性低温暴露对家兔心肝肾功能的影响[J]. 昆明医科大学学报, 2013, 34(5): 43-49. WU L Z, DU X H, LEI Y, et al. Effects of acute cold exposure on rabbit heart, liver and renal function[J]. J Kunming Med Univ, 2013, 34(5): 43-49. DOI:10.3969/j.issn.1003-4706.2013.05.011 |
| [12] |
范苗, 任卫东, 宋光, 等. 三维面积应变评价射血分数保留心力衰竭患者左心室收缩功能变化[J]. 中国医学影像技术, 2018, 34(7): 998-1002. FAN M, REN W D, SONG G, et al. Three-dimensional area strain in evaluatinon on changes of left ventricular myocardial contractional function in heart failure patients with preserved ejection fraction[J]. Chin J Med Imaging Technol, 2018, 34(7): 998-1002. DOI:10.13929/j.1003-3289.201710125 |
| [13] |
YAMADA M, TAKAHASHI K, KOBAYASHI M, et al. Mechanisms of left ventricular dysfunction assessed by layer-specific strain analysis in patients with repaired tetralogy of fallot[J]. Circ J, 2017, 81(6): 846-854. DOI:10.1253/circj.CJ-16-1162 |
| [14] |
LIPIEC P, SZYMCZYK E, MICHALSKI B, et al. Echocardiographic quantitative analysis of resting myocardial function for the assessment of viability after myocardial infarction: comparison with magnetic resonance imaging[J]. Kardiol Pol, 2011, 69(9): 915-922. DOI:10.1111/j.1651-2227.1958.tb07860.x. |
| [15] |
KUSUNOSE K, YAMADA H, NISHIO S, et al. Validation of longitudinal peak systolic strain by speckle tracking echocardiography with visual assessment and myocardial perfusion SPECT in patients with regional asynergy[J]. Circ J, 2011, 75(1): 141-147. DOI:10.1253/circj.cj-10-0551 |



