2. 400037 重庆,陆军军医大学(第三军医大学)第二附属医院:胸外科
2. Department of Thoracic Surgery, Second Affiliated Hospital, Army Medical University (Third Military Medical University), Chongqing, 400037, China
尽管胸腔镜肺叶切除术是一种微创手术,但其脏器内部创伤依然较大,可引起强烈的术中应激反应和剧烈的术后疼痛,因此,如何最大程度控制术中应激反应和术后疼痛是目前胸腔镜手术围术期管理的重点和难点[1]。区域镇痛技术是有效控制术中应激及术后多模式镇痛的关键部分[2],胸部硬膜外镇痛(thoracic epidural analgesia, TEA)被视为胸科手术术后疼痛处理的金标准,胸椎旁阻滞(thoracic paravertebral block, TPV)也被认为是开胸术后缓解疼痛的第2好方法[3]。然而,TEA和TPVB是一种相对侵入性的技术,伴有严重并发症的风险,如:气胸,脊髓损伤,交感神经阻滞和低血压。近年来,新型区域镇痛技术如单纯竖脊肌平面阻滞(erector spinae plane block, ESPB)、单纯前锯肌平面阻滞(serratus anterior plane block,SAPB)被应用于胸科手术围术期镇痛[5],但仍不理想。目前两者联合应用于胸腔镜手术却鲜有报道,我们采用随机、双盲、对照临床研究方法,观察超声引导下SAPB联合ESPB在VAST肺叶切除术术中及术后镇痛效果,期望为临床应用提供新的支撑证据。
1 资料与方法 1.1 一般资料本研究经陆军军医大学第二附属医院伦理委员会审核同意(2018-研第051-02),所有受试者本人均签署书面知情同意书。纳入2018年10月-2019年3月于陆军军医大学第二附属医院胸外科接受胸腔镜下肺叶切除术的患者120例。男性58例,女性62例,年龄(51.7±10.2)岁。
纳入标准:年龄20~70岁;ASA Ⅰ~Ⅱ级;体质量指数(BMI)为18~30 kg/m2;确诊为“肺结节”或肺癌的患者。排除标准:凝血功能障碍者, 穿刺部位感染者;对局麻药过敏者;拒绝行区域阻滞者;慢性疼痛、精神病史者;严重心脑血管疾病、肝肾功能不全者;慢性支气管炎、慢性阻塞性肺疾病(chronic obstructive pulmonary diseases,COPD)疾病病史者;术中转开胸或术后出现严重并发症者。
1.2 研究设计本研究设计为单中心平行(分配比1:1:1:1)随机对照研究,由独立的统计员进行简单随机化,计算机产生随机化序列按1:1:1:1将受试者分为4组,每组肺叶切除术30例,其中竖脊肌平面阻滞组(E组) 1例因非计划再次手术终止研究;前锯肌平面阻滞组(S组) 1例因术中转开胸,1例因严重肺部感染退出研究;竖脊肌联合前锯肌平面阻滞组(SE组)及对照组(G组)均无患者退出或终止研究。由1名麻醉医生负责病例纳入和术中麻醉管理;另1名麻醉医生完成所有的神经阻滞操作;1名有经验的麻醉护士负责术后随访;数据收集是由训练有素的不参与患者管理的统计人员进行;术后由胸外科专家评估术后肺部并发症;除神经阻滞操作的麻醉医生外所有受试者和研究人员,包括参与手术和病房管理的人,在治疗期间对患者的分组均不知情。
1.3 麻醉方法所有患者入室后建立静脉通道,监测心率、血氧饱和度、无创血压等,并静脉注射地塞米松注射液10 mg。所有患者采用双腔气管插管全身麻醉,麻醉诱导依次给予咪达唑仑0.1 mg/kg、丙泊酚1.5 mg/kg、罗库溴铵0.6 mg/kg、舒芬太尼0.5 μg/kg,成功后完成双腔支气管导管气管插管(男37F/女35F),纤维支气管镜完成定位。手术开始前10 min行单肺通气。术中监测有创血压、心率、呼气末二氧化碳(PETCO2),脑电双频谱指数(BIS),动脉血气分析、气道压(paw)等。通气参数:FiO2 100%,潮气量4~6 mL/kg,呼吸频率14~18次/min,PEEP 4~6 cmH2O, PETCO2 35~45 mmHg。麻醉维持:七氟烷0.6~1.3 MAC,BIS 40~60, 根据心率、有创血压调节瑞芬太尼用量,间断给予罗库溴铵维持肌松。缝合手术切口前手控通气,直视下判断萎陷肺组织完全复张后行双肺通气。手术结束前10 min所有患者静脉注射雷莫司琼0.3 mg,术毕4组链接静脉自控镇痛泵(PCIA),(北京科联升华医疗科技有限公司,国械注准0153540995),镇痛配方:盐酸氢吗啡酮注射液0.18 mg/kg+氟比洛芬酯注射液3 mg/kg+雷莫司琼0.6 mg+生理盐水稀释至200 mL, 流速4 mL/h,单次PCA剂量1 mL,锁定时间15 min。补救措施:术后静息疼痛VAS>4分,由不知分组的病房医生给予氟比洛芬酯注射液50 mg补救镇痛。
1.4 神经阻滞方法麻醉成功后E、S、SE组患者更换侧卧完成神经阻滞,具体操作如下:①E组选择正中矢状位扫描T5棘突, 探头外移4~5 cm显现T5横突,识别T5表面的竖脊肌、菱形肌和斜方肌,常规消毒皮肤,固定探头(高频线阵,深圳华声医疗有限公司)采用一次性无菌注射针针(0.7×80 TWLB,上海康德莱集团)平面内进针,针尖指向头侧到达T5横突表面或触及T5横突骨质时回抽无血无气后注入0.5%盐酸罗哌卡因注射液20 mL;②S组高频线阵探头纵轴放置术侧腋中线第5肋,辨识背阔肌、前锯肌、第5肋及其深面胸膜,常规消毒皮肤,固定探头,使用一次性无菌注射针, 平面内进针, 针尖指向头侧,突破背阔肌和前锯肌后到达肋骨表面回抽无血无气后注射0.5%盐酸罗哌卡因注射液20 mL;③ES组同时使用E组、S组操作方法完成阻滞; ④G组无任何阻滞。所有患者均在全身麻醉后进行神经阻滞操作,且操作部位不留任何标识;所有操作均由负责神经阻滞的同一麻醉医生完成,且该麻醉医生不参与病例纳入、麻醉管理、数据输入分析及术后随访。
1.5 观察指标分别记录术中阿片类药物用量,PACU停留时间,PACU Riker镇静烦躁评分(SAS),观察比较术后0、6、12、24、48 h患者疼痛VAS评分及恶心、呕吐发生率;记录平均住院日及肺部并发症等指标。
疼痛VAS评分标准0分为无痛;1~3分为轻度疼痛;4~6分为中度疼痛;7~10分为重度疼痛[6]。镇静躁动评分采用Riker镇静躁动评分量表[7]评估:1分:对恶性刺激无或仅有轻微反应;2分:对躯体刺激有反应,不能交流及服从指令,有自主运动;3分:语言刺激或轻轻摇动可唤醒并服从简单指令,但又讯即入睡;4分:安静合作,服从指令;5分:焦虑或身体躁动,经言语劝阻可安静;6分:需要保护性束缚并反复语言劝阻,咬气管插管;7分:拉拽气管内插管,试图拔除各种导管,翻越窗栏,攻击医护人员,在床上辗转挣扎。
肺部并发症:采用MGS评分标准[8]评估:①T>38 ℃; ②WBC计数上升(>11.2×109/L); ③胸部X线片表现或肺不张; ④咳嗽、咯脓性痰; ⑤痰培养结果阳性; ⑥临床诊断肺炎; ⑦呼吸室内空气时SpO2 < 90%(PO2 < 60 mmHg伴或不伴PCO2>50 mmHg); ⑧延长住院或监护治疗时间, 患者满足4条及以上定义为出现术后肺部并发症。
1.6 统计学分析变量分别用x±s(SEM)、计数(百分比)来表示。正态分布的计量数据组间比较采用单因素方差分析,两两比较采用LSD法,其中采用重复测量方差分析比较不同时间点不同组别的疼痛VAS评分、镇痛泵消耗量;非正态分布数据采用非参数检验的Kruskal-Wallis法;计数资料的比较采用χ2检验。所有统计分析均通过SPSS 22.0统计软件进行,以双侧检验P < 0.05判断有统计学意义。
2 结果 2.1 患者一般情况比较4组患者年龄、性别、身高、体质量、BMI、手术时间、麻醉时间等比较差异无统计学意义(P>0.05,表 1)。
| 组别 | 性别(男/女) | 年龄/岁 | 身高/cm | 体质量/kg | BMI | 手术时间/min | 麻醉时间/min |
| S组 | 12/18 | 52. 23±9.97 | 162. 87±6. 60 | 60. 21±8.62 | 22.64±0.53 | 127.87±51.32 | 158.73±52.12 |
| E组 | 16/14 | 53.70±6.82 | 164. 42±6. 28 | 63. 35±7.44 | 23.47±0.78 | 116.63±35.30 | 144.30±37.17 |
| SE组 | 16/14 | 51.70±11.57 | 163 42±7 43 | 62. 97±10. 07 | 23.53±0.04 | 110.43±32.86 | 137.93±34.59 |
| G组 | 14/16 | 50 70±9 42 | 161 47±8 10 | 61.71±8.46 | 23.62±2.30 | 123.57±30.66 | 151.03±32.54 |
| F/x2 | 1.468 | 0 149 | 0.401 | 0.664 | 0.857 | 1.197 | 1.507 |
| P值 | 0.69 | 0 938 | 0 722 | 0.632 | 0.494 | 0.3 | 0.186 |
2.2 镇痛效果比较
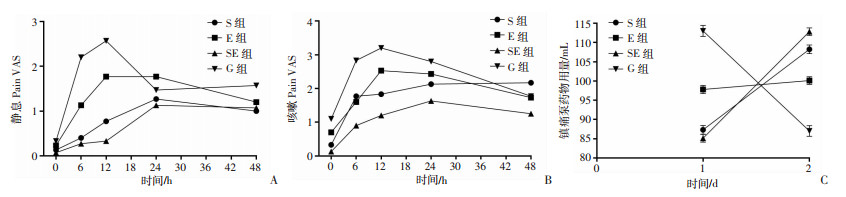
利用重复测量方差分析比较,术后不同时间点疼痛VAS评分分组、时间及分组和时间的交互效应差异具有统计学意义(P < 0.001, P < 0.001, P < 0.001, 表 2);疼痛VAS评分随时间变化趋势不一致(图 1A、B)。
| 变异来源 | 静息疼痛VAS | 咳嗽疼痛VAS | 镇痛泵消耗量 | |||||
| F | P | F | P | F | P | |||
| 时间效应 | 42.38 | < 0.001 | 88.63 | < 0. 001 | 2192 | < 0. 001 | ||
| 分组效应 | 9.08 | < 0.001 | 7.72 | < 0. 001 | 13.28 | < 0. 001 | ||
| 时间*分组效应 | 27.3 | < 0.001 | 13.57 | < 0. 001 | 112.44 | < 0. 001 | ||
|
|
S组:前锯肌组;E组:竖脊肌组;SE组:前锯肌+竖脊肌组;G组:对照组 A:静息疼痛VAS;B:咳嗽疼痛VAS;C:术后镇痛泵药物用量 图 1 各组各项指标水平随时间变化趋势图 |
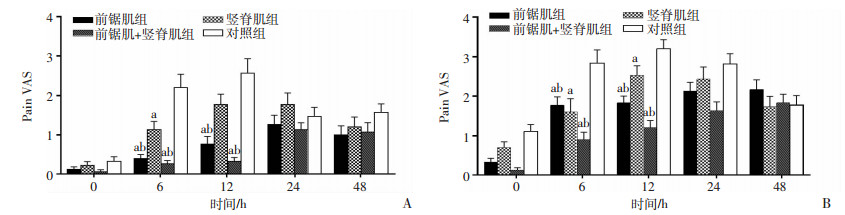
术后6 h,E组(1.13±0.21)、S组(0.40±0.10)、SE组(0.27±0.08)静息疼痛VAS评分均显著低于G组(2.20±0.34;P=0.001,P < 0.001,P < 0.001, 图 2A);术后6 h,E组(1.60±0.34)、S组(1.77±0.21)、SE组(0.90±0.00)咳嗽疼痛VAS评分也显著低于G组(2.83±0.34;P=0.002, P=0.008, P < 0.01, 图 2B);术后12 h, S组(0.77±0.19)、SE组(0.33±0.01)的静息疼痛VAS评分显著低于G组(2.57±0.36; P=0.012, P < 0.01,P < 0.01, 图 2A), E组(1.77±0.26)与G组(2.57±0.36)之间差异无统计学意义(P=0.06,图 2A); 术后12 h, E组(2.53±0.24)、S组(1.83±0.17)、SE组(1.20±0.18)咳嗽疼痛VAS评分低于G组(2.57±0.36; P=0.006,P < 0.001, P < 0.001, 图 2B)。术后6、12 h, SE组(6 h 0.27±0.08;12 h 0.33±0.01)静息疼痛VAS评分均显著低于E组(6 h 1.13±0.21;12 h 1.77±0.26;P=0.02, P=0.001, 图 2A),术后12 h, SE组(1.20±0.18)咳嗽疼痛VAS评分均显著低于E组(2.53±0.24; P < 0.01, 图 2B)。术后6、12 h,SE组(静息0.27±0.08,咳嗽0.90±0.00)与S组(静息0.40±0.10,咳嗽1.77±0.21)静息和咳嗽VAS评分之间差异均无统计学意义(静息6 h P=0.97, 12 h P=0.61;咳嗽6 h P=0.13, 12 h P=0.15, 图 2A, B)。术后0、24、48 h静息和咳嗽疼痛VAS评分4组比较差异均无统计学意义(P=0.07, P=0.26, P=0.53,图 2A、B)。
|
| a: P < 0.01, 与对照组比较,b: P < 0.05,与竖脊肌组比较; A:静息状态; B:咳嗽状态 图 2 各组患者不同时间点疼痛VAS评分 |
2.3 患者术中阿片类药物用量,镇痛泵药物用量,PACU停留时间、PACU Riker镇静烦躁评分(SAS)比较 2.3.1 术中阿片类药物用量比较
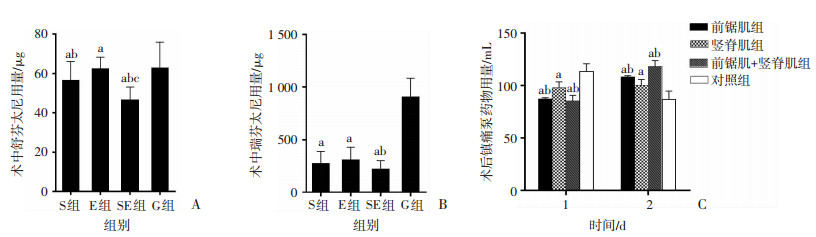
舒芬太尼用量,与G(62.81±1.07)组相比,E组(62.50±1.29)、S组(56.50±1.75)和SE组(46.33±1.24)明显减少(P < 0.01, P < 0.01, P < 0.01, 图 3A);SE组(46.33±1.24)明显少于S组(56.50±1.75)、E组(62.50±1.29)(P < 0.01,P < 0.01, 图 3A); S组(56.50±1.75)少于E组(62.50±1.29)(P < 0.01,图 3A);瑞芬太尼用量,与G组(907.67±32.17)相比, E组(307.61±14.11)、S组(275.40±20.65)和SE组(218.79±14.82)同样明显减少(P < 0.01,P < 0.01,P < 0.01,图 3B),SE组(218.79±14.82)用量明显少于E组(307.61±14.11)(P < 0.05,图 3B); S组(275.40±20.65)与E组(307.61±14.11)、SE组(218.79±14.82)之间差异无统计学意义(P=0.98, P=0.17,图 3B)。
|
| a: P < 0.01, 与对照组比较,b: P < 0.05,与竖脊肌组比较,c: P < 0.01,与前锯肌组比较;S组:前锯肌组,E组:竖脊肌组,SE组:前锯肌+竖脊肌组,G组:对照组A:术中舒芬太尼用量;B:术中瑞芬太尼用量;C:术后镇痛泵药物用量 图 3 各组术中阿片类药物及术后镇痛泵药物用量比较 |
2.3.2 镇痛泵药物用量比较
利用重复测量方差分析比较,术后不同时间镇痛泵用量分组、时间及分组和时间的交互效应差异具有统计学意义(P < 0.001, P < 0.001, P < 0.001, 见表 2);镇痛泵用量随时间变化趋势不一致(见图 1C)。术后第1天用量,与G组(113.00±1.41)相比,E组(97.80±1.03)、S组(87.30±1.12)和SE组(85.11±1.01)明显减少(P < 0.001, P < 0.001, P < 0.001, 图 3C);S组(87.30±1.12)、SE组(85.11±1.01)优于E组(97.80±1.03) (P < 0.01, P < 0.01, 图 3C); S组(87.30±1.12)、SE组(85.11±1.01)之间差异无统计学意义(P=0.935, 图 3C);术后第2天用量,与G组(87.0±1.40)相比,E组(100.10±1.02)、S组(108.23±1.14)和SE组(112.83±1.00)明显增多(P < 0.001, P < 0.001, P < 0.001, 图 3C), SE组(112.83±1.00)较E组(100.10±1.02)、S组(108.23±1.14)用量稍增加(P=0.02, P < 0.01, 图 3C), S组(108.23±1.14)也较E组(100.10±1.02)增多(P < 0.01, 图 3C)。
2.3.3 PACU停留时间与G组相比,E组、S组和SE组明显缩短(P < 0.01, P < 0.01, P < 0.01,表 3),且SE组明显优于S组和E组(P=0.005, P < 0.01,表 3), S组与E组之间差异无统计学意义(P=0.36,表 3)。2.3.4PACU Riker镇静烦躁评分SE组为(4.07±0.25),S组为(4.30±0.53),E组为(4.77±0.77),G组为(5.13±1.01), SE组明显低于其他3组(P < 0.05, 表 3)。
| 组别 | PACU停留时间/min | PACU镇静烦躁评分/(Riker) | 住院时间/d |
| S组 | 41.50±1.05ab | 4.30±0.10 | 12.83±1.01 |
| E组 | 45.20±1.07ab | 4.77±0.14b | 13.87±0.91 |
| SE组 | 36.90±0.86a | 4.07±0.05a | 11.80±0.88a |
| G组 | 53.43±0.82ab | 5.13±0.18b | 15.73±0.83 |
| χ2 | 69.7 | 31.47 | 15.24 |
| P值 | < 0.001 | < 0.001 | 0.002 |
| a: P < 0.05, 与G组相比, b: P < 0.05, 与SE组相比 | |||
2.4 恶心、呕吐发生率比较
术后0、24、48 h四组患者恶心、呕吐发生均为0例;术后6 h,发生率分别为:S组10%(3/30)、E组10%(3/30)、SE组10%(3/30)、G组26.7%(8/30);术后12 h发生率分别为:S组6.7%(2/30)、E组13.3%(4/30)、SE组、10%(3/30)、G组、26.7%(8/30);4组术后6、12 h恶心、呕吐发生率组间比较差异无统计学意义(P=0.952)。
2.5 平均住院时间比较SE组较G组明显缩短(P=0.014, 表 3), S、E、G组组间比较差异均无统计学意义(P=0.85, P=0.12, P=0.47, 表 3)。G组平均住院时间显著高于E组、S组和SE组(P < 0.05, 表 3)。
2.6 术后肺部并发症比较肺部感染发生率分别为,S组3.33%(1/30)、E组3.33%(1/30)、SE组3.33%(1/30)、G组6.67%(2/30);肺不张发生率分别:S组3.33%(1/30)、E组6.67%(2/30)、SE组3.33%(1/30)、G组3.33%(1/30);呼吸衰竭发生率:S、E、SE组均为0,G组3.33%(1/30);4组肺部并发症发生率组间比较差异无统计学意义(P=0.931)。
3 讨论本研究以SAPB+ESPB为主,PCIA为辅的多模式镇痛,不仅突破了胸科手术以强阿片类药物为主要镇痛药物的治疗常规,同时也减少了术中及术后阿片类药物用量,增强了PCIA镇痛效果,降低了术后疼痛VAS评分,PACU烦躁的发生,加快了胸腔镜肺叶切除患者早期术后康复。
超声引导下SAPB与ESPB分别由BLANCO等[9]和FORERO等[10]提出,因其操作简单、安全、并发症少,使其在围手术期镇痛及疼痛诊疗中有广阔前景;该两种阻滞大大降低硬膜外血肿,脊髓、神经损伤,气胸和中央感染等不良事件的风险[11]。目前仅单独应用于胸腔镜手术,联合应用却少见报道。从两种阻滞方法的解剖学基础及作用机制来看,ESPB的局麻药通过肋横突孔向前扩散到椎旁间隙作用于脊神经后支[12],对交感神经纤维产生阻滞效应,从而缓解内脏痛;SAPB似乎是通过阻断肋间神经的外侧皮支及其前后分支来介导的,仅对前外侧胸壁的浅表疼痛[13]及胸管部位疼痛[14]有效, 因此ESPB与SAPB联合能够相互补充产生更广泛的镇痛效应区域。
本研究中SE组在术后6、12 h疼痛VAS评分、术中阿片类药物用量以及术后第1天镇痛泵药物用量优于S组、E组和G组,同时也表明ESPB联合SAPB不仅能有效管理早期术后疼痛,同时也降低了术中应激反应,提高了围术期患者的镇痛质量,促进早期术后恢复。E组主要描述为胸管部位疼痛,S组近一半患者描述胸管部位疼痛及呼吸时胸管所致不适,SE组仅有1例患者描述胸管相关不适,这可能是由于位于前锯肌平面的胸长神经及胸背神经被阻滞[14],且同时竖脊肌阻滞增强了并扩大了该作用。除此之外,S组、E组、SE组3组患者在术后第2天镇痛泵消耗量明显多于G组。JACQUES等[15]认为患者在接受区域神经阻滞后12~24 h内会遭受严重的疼痛,对镇痛药物的需求明显增加,可能与下列因素相关:①区域神经阻滞阻止了信号传导,当阻滞作用消失后,保留的伤害感受性信号记忆被放大;②局麻药固有促炎特性可能导致区域阻滞后痛觉过敏;③易感患者区域阻滞的机械和化学作用引起周围神经损伤了某些机制[15]。然而,研究中患者并未遭受文献中所描述的严重疼痛,这可能与多模式镇痛相关。当然,这需要更多或更大样本的临床随机研究来证实。
本研究显示SE组在PACU停留时间及镇静烦躁评分方面明显优于其他3组,本研究躁动发生率36.6%(44/120), 低于文献报道的常规术后镇痛患者的躁动发生率43.5%[17]。其中SE组躁动发生率6.67%,ESPB联合SAPB不仅有效控制了早期术后疼痛;同时也减少了疼痛刺激的传入,从而降低交感神经兴奋,血浆皮质醇分泌减少,细胞免疫抑制减少,从而增加了患者的抗应激能力,从而降低了烦躁的发生。
术后恶心呕吐(postoperative nausea and vomiting, PONV)是术后常见的并发症,其发生与术后疼痛、阿片类药物剂量、创伤、麻醉及病人等因素相关[18]。本研究中4组之间恶心呕吐差异无统计学意义,可能的原因有:①本研究中多模式的镇痛方式不仅提供了完善的镇痛,同时也减少了阿片类药物的用量,从而降低了恶心呕吐的发生;②本研究中地塞米松作为一种术前用药,以降低双腔气管导管所致的黏膜水肿,地塞米松也被证实具有相当的止吐功能[19];③雷莫司琼的预防作用。本研究肺部并发症发生率9.1%, 低于文献报道16%的发生率[6];可能是由于:①低剂量阿片类药物降低了细胞免疫功能被抑制的风险[20];②联合阻滞更有效降低应激、外科创伤引起的早期炎症反应;③竖脊肌、前锯肌平面阻滞并不影响膈肌及呼吸功能或影响甚微[21],具体原因需进一步研究。
虽然超声引导下SAPB+ESPB在胸腔镜肺叶切除术早期疼痛管理及有效控制术中应激方面优于单纯竖脊肌或前锯肌平面阻滞,但本研究仍存在一些局限性,如多种止痛技术的联合应用可能干扰我们研究结果;竖脊肌、前锯肌平面阻滞属于新型筋膜阻滞,单次注射用药方式、容量、浓度及起效时间均是影响筋膜阻滞效果的因素;因手术周转的影响并未测量阻滞范围来证实是否存在叠加或互补。因此,我们需要进一步制定创新的方案来探索前锯肌联合竖脊肌平面对胸腔镜肺叶切除术患者早期康复的影响。
| [1] |
UMARI M, CARPANESE V, MORO V, et al. Postoperative analgesia after pulmonary resection with a focus on video-assisted thoracoscopic surgery[J]. Eur J Cardiothorac Surg, 2018, 53(5): 932-938. DOI:10.1093/ejcts/ezx413 |
| [2] |
WARDHAN R, CHELLY J. Recent advances in acute pain management: understanding the mechanisms of acute pain, the prescription of opioids, and the role of multimodal pain therapy[J]. F1000Res, 2017, 6: 2065. DOI:10.12688/f1000research.12286.1 |
| [3] |
WANG L P, WANG Y, ZHANG X, et al. Serratus anterior plane block or thoracic paravertebral block for postoperative pain treatment after uniportal video-assisted thoracoscopic surgery: a retrospective propensity-matched study[J]. J Pain Res, 2019, 12: 2231-2238. DOI:10.2147/JPR.S209012 |
| [4] |
顾楠, 张析哲, 周琪. 超声引导下竖脊肌平面阻滞在胸科手术的临床应用进展[J]. 世界最新医学信息文摘, 2019, 19(62): 44,46. GU N, ZHANG X Z, ZHOU Q. The clinical application of ultrasound-guided spinal muscle block in thoracic surgery[J]. World Latest Med Inf, 2019, 19(62): 44,46. DOI:10.19613/j.cnki.1671-3141.2019.62.024 |
| [5] |
骆艺菲, 何开华. 前锯肌平面阻滞镇痛的临床应用进展[J]. 山东医药, 2019, 59(8): 103-106. LUO Y F, HE K H. Progress in clinical application of serratus anterior plane block analgesia[J]. Shandong Med J, 2019, 59(8): 103-106. DOI:10.3969/j.issn.1002-266X.2019.08.030 |
| [6] |
闫光明, 陈杰, 杨贵英, 等. 两种非甾体类抗炎药联合氢吗啡酮在胸腔镜手术患者术后镇痛中的应用:一项随机、双盲、对照临床研究[J]. 第三军医大学学报, 2018, 40(11): 1011-1016. YAN G M, CHEN J, YANG G Y, et al. Analgesic effects of 2 nonsteroidal anti-inflammatory drugs respectively combined with hydromorphone in postoperative analgesia after thoracic surgery: a randomized, double blind, controlled clinical study[J]. J Third Mil Med Univ, 2018, 40(11): 1011-1016. DOI:10.16016/j.1000-5404.201803125 |
| [7] |
RIKER R R, PICARD J T, FRASER G L. Prospective evaluation of the Sedation-Agitation Scale for adult critically ill patients[J]. Crit Care Med, 1999, 27(7): 1325-1329. DOI:10.1097/00003246-199907000-00022 |
| [8] |
AGOSTINI P, CIESLIK H, RATHINAM S, et al. Postoperative pulmonary complications following thoracic surgery: are there any modifiable risk factors?[J]. Thorax, 2010, 65(9): 815-818. DOI:10.1136/thx.2009.123083 |
| [9] |
BLANCO R, PARRAS T, MCDONNELL J G, et al. Serratus plane block: a novel ultrasound-guided thoracic wall nerve block[J]. Anaesthesia, 2013, 68(11): 1107-1113. DOI:10.1111/anae.12344 |
| [10] |
FORERO M, ADHIKARY S D, LOPEZ H, et al. The erector spinae plane block: a novel analgesic technique in thoracic neuropathic pain[J]. Reg Anesth Pain Med, 2016, 41(5): 621-627. DOI:10.1097/AAP.0000000000000451 |
| [11] |
EL-BOGHDADLY K, PAWA A. The erector spinae plane block: plane and simple[J]. Anaesthesia, 2017, 72(4): 434-438. DOI:10.1111/anae.13830 |
| [12] |
IVANUSIC J, KONISHI Y, BARRINGTON M J. A cadaveric study investigating the mechanism of action of erector spinae blockade[J]. Reg Anesth Pain Med, 2018, 43(6): 567-571. DOI:10.1097/AAP.0000000000000789 |
| [13] |
MAYES J, DAVISON E, PANAHI P, et al. An anatomical evaluation of the Serratus anterior plane block[J]. Anaesthesia, 2016, 71(9): 1064-1069. DOI:10.1111/anae.13549 |
| [14] |
CHU G M, JARVIS G C. Serratus anterior plane block to address postthoracotomy and chest tube-related pain: a report on 3 cases[J]. A A Case Rep, 2017, 8(12): 322-325. DOI:10.1213/XAA.0000000000000502 |
| [15] |
JACQUES N, KAROUTSOS S, AUBRY K, et al. Peripheral nerve block efficacy on refractory neuralgia complicating Ramsay hunt syndrome: a case report[J]. A A Pract, 2019. DOI:10.1213/XAA.0000000000001035 |
| [16] |
NOBRE L V, CUNHA G P, DE SOUSA P C C B, et al. Bloqueio de nervos periféricos e dor rebote: revisão de literatura[J]. Braz J Anesthesiol, 2019, 69(6): 587-593. DOI:10.1016/j.bjan.2019.05.001 |
| [17] |
YU D H, CHAI W, SUN X D, et al. Emergence agitation in adults: risk factors in 2, 000 patients[J]. J Can D'anesthesie, 2010, 57(9): 843-848. DOI:10.1007/s12630-010-9338-9 |
| [18] |
RÜSCH D, EBERHART L H, WALLENBORN J, et al. Nausea and vomiting after surgery under general anesthesia: an evidence-based review concerning risk assessment, prevention, and treatment[J]. Dtsch Arztebl Int, 2010, 107(42): 733-741. DOI:10.3238/arztebl.2010.0733 |
| [19] |
APFEL C C, KORTTILA K, ABDALLA M, et al. A factorial trial of six interventions for the prevention of postoperative nausea and vomiting[J]. N Engl J Med, 2004, 350(24): 2441-2451. DOI:10.1056/NEJMoa032196 |
| [20] |
CONNOLLY C, MADDEN S F, BUGGY D J, et al. Expression of anaesthetic and analgesic drug target genes in excised breast tumour tissue: Association with clinical disease recurrence or metastasis[J]. PLoS ONE, 2017, 12(5): e0177105. DOI:10.1371/journal.pone.0177105 |
| [21] |
KHALIL A E, ABDALLAH N M, BASHANDY G M, et al. Ultrasound-guided Serratus anterior plane block versus thoracic epidural analgesia for thoracotomy pain[J]. J Cardiothorac Vasc Anesth, 2017, 31(1): 152-158. DOI:10.1053/j.jvca.2016.08.023 |



