骨与软组织肉瘤是一种起源于间叶组织的原发性恶性肿瘤,占成人恶性肿瘤的5%,儿童肿瘤的20%[1]。尽管相对罕见,但其致死率高,根据美国国家卫生统计中心的最新估计,仅在美国每年有5 800多骨与软组织肉瘤患者死亡,占新发患者的40%[1]。对于无转移的骨与软组织肉瘤患者而言,70%的患者可获得较长的生存期,而一旦发生转移或复发,其5年生存率仅有20%左右[1]。有10%~20%的骨与软组织肉瘤患者在确诊时已发生远处转移或微转移,且多为肺内转移[2]。目前检测复发或转移的方法主要依赖于临床检查、影像学检查和正电子发射断层扫描(positron emission computed tomography,PET-CT),以确定肿瘤的生长区域或代谢活动的增加。检测复发和转移的新方法可能改变骨与软组织肉瘤的诊断、筛查和治疗方式。
循环肿瘤细胞(circulating tumor cell,CTC)是来源于原发肿瘤或转移灶的肿瘤细胞,在特定条件下释放入外周循环血中。它们具有肿瘤的生物学特性,是肿瘤远处转移的种子。因此,CTC被认为是肿瘤复发和远处转移的重要原因之一[3]。研究表明,CTC计数与恶性肿瘤患者的分期、转移及预后密切相关[4-5]。通过检测外周血CTC,可为肿瘤转移、复发机制的研究、治疗方案的选择、疗效的评判及预后的预测等提供可靠依据。CTC的检测较影像学方法更能早期提示肿瘤细胞的复发和微转移,可用于监测肿瘤的发展状况,评估患者的预后。对CTC的检测已经在许多肿瘤类型中被研究,最常见的是在乳腺和结肠等上皮性肿瘤以及黑色素瘤中[6],但在间叶组织恶性肿瘤中CTC的研究相对较少。
同源盒基因(homeobox genes,HOX)是控制细胞增殖和分化的主要基因之一,其编码的转录因子通过作用于黏附分子、生长因子及膜蛋白受体等在肿瘤的进展、转移中发挥重要作用[7],同时参与调控肿瘤的自我更新、无限增殖等恶性生物学行为。目前在肺癌、胃癌、结肠癌及乳腺癌等多种肿瘤中均可检测到HOX基因的异常表达[8]。其中,位于第17号染色体的HOXB7已被证实属于癌基因的范畴[9]。HOXB7参与相关蛋白的DNA修复,其过度表达可能促使某些细胞的恶性转化[10-11]。因此,HOXB7在癌变过程中起着关键作用,与肿瘤的侵袭转移和疾病进展相关,并有望可作为治疗骨与软组织肉瘤的治疗靶点。
本研究检测骨与软组织肉瘤患者外周血循环肿瘤细胞,分析循环肿瘤细胞的数量、类型以及HOXB7基因的表达和骨与软组织肉瘤患者转移及预后中的关系,为骨与软组织肉瘤的诊治提供新的策略和依据。
1 资料与方法 1.1 研究对象纳入本院2017年5月至2019年7月有完整临床治疗及随访资料的新发骨与软组织肉瘤患者。纳入标准:①病理确诊为骨肉瘤或软组织肉瘤,ECOG评分0~2;②既往未接受过化疗、放疗、手术治疗及其他抗肿瘤治疗;③治疗前有CTC检测结果。排除标准:①合并其他恶性肿瘤病史者;②不接受治疗及依从性差者;③拒绝签署知情同意书者。
1.2 方法 1.2.1 收集资料收集患者基线资料和临床病理参数信息,包括年龄、性别、Enneking分期、肿瘤位置、大小、肿瘤类型等相关资料。
1.2.2 外周血循环肿瘤细胞富集与鉴定病理确诊后治疗开始前1周检测患者外周血CTC。所有样本检测采用CanPatrolTM二代CTC检测技术(广州益善科技)[12-14]。使用EDTA抗凝采血管采集5 mL外周血,上下颠倒混匀10次。加入红细胞裂解液裂解外周血中的红细胞,离心后去除上清液,在沉淀物中加入含4%甲醛的PBS重新悬浮细胞,转移至过滤管中加压过滤,压力≥0.08 MPa,过滤后回收滤膜上的细胞进行进一步鉴定分型。分型鉴定采用多重mRNA原位分析(multiple mRNA in situ analysis,MRIA)方法,对分离的CTC进行核酸定位并分型[12]。使用蛋白酶处理细胞后用上皮标记探针、间质标记及白细胞标记探针进行杂交,依次加入预扩增液、预扩增探针进行孵育。含有上皮型标志物CK8、CK18、CK19及EpCAM基因的RNA探针标记上皮型CTC,含有间质型标志物Vimentin和Twist基因的RNA探针标记间质型CTC,含有针对白细胞的CD45探针标记白细胞,同时还检测了HOXB7基因。孵育后加入Alexa Fluor 594红色荧光二抗检测上皮型探针,Alexa Fluor 488绿色荧光二抗检测间质型探针,Alexa Fluor 750白色荧光二抗检测白细胞,Alexa Fluor 647紫色荧光二抗检测CTC中的HOXB7基因。
1.2.3 结果分析红色荧光信号表示上皮型CTC,绿色荧光信号表示间质型CTC,同时显示红色及绿色信号的为混合型CTC,白色信号为白细胞,紫色信号表示CTC内的HOXB7基因表达阳性。
1.3 统计学分析采用SPSS 22.0统计学软件进行分析。资料的正态性检验使用Shapiro-Wilk检验,不同患者CTC计数不满足正态性检验,CTC数量与年龄、性别、肿瘤位置、大小等临床资料关系之间的比较使用Mann-Whitney U非参数检验,比较肿瘤类型、不同分期CTC数量之间的分布差异,采用Kruskal-Wallis H非参数检验,各分型CTC中HOXB7表达阳性的细胞数采用χ2检验。双侧检验,检验水准α=0.05。
2 结果 2.1 临床病理特征本研究共纳入40例患者,其中男性19例,女性21例;年龄6~68(31.28±17.05)岁;发生在肢体的肿瘤33例,非肢体的肿瘤7例;Ennecking Ⅰ期7例,Ennecking Ⅱ期27例,Ennecking Ⅲ期6例;肿瘤直径≤5 cm的7例,>5 cm的33例;骨肉瘤患者19例(47.5%),尤文肉瘤或原始神经外胚层瘤4例(10%),软组织肉瘤17例(42.5%)。在40例患者中检测了外周血循环肿瘤细胞,其阳性率为37/40(92.5%),分析循环肿瘤细胞与年龄、性别、肿瘤位置、大小以及肿瘤类型之间的关系,结果显示均无统计学意义(表 1)。
| 临床参数 | n | CTC阳性例数 | P |
| 年龄/岁 | |||
| <18 | 11 | 10 | 0.976 |
| ≥18 | 29 | 27 | |
| 性别 | |||
| 女性 | 21 | 20 | 1.000 |
| 男性 | 19 | 17 | |
| 肿瘤部位 | |||
| 肢体 | 33 | 30 | 0.626 |
| 非肢体 | 7 | 7 | |
| Enneking分期 | |||
| Ⅰ | 7 | 6 | |
| Ⅱ | 27 | 25 | 0.002 |
| Ⅲ | 6 | 6 | |
| 肿瘤长径 | |||
| ≤5 cm | 7 | 7 | 0.972 |
| >5 cm | 33 | 30 | |
| 肿瘤类型 | |||
| 骨肉瘤 | 19 | 18 | |
| 尤文肉瘤或原始神经外胚层瘤 | 4 | 3 | 0.066 |
| 软组织肉瘤 | 17 | 16 |
2.2 CTC分型
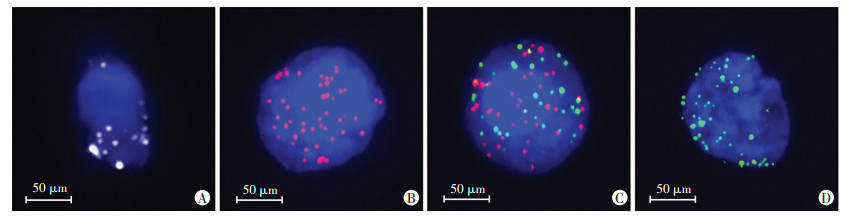
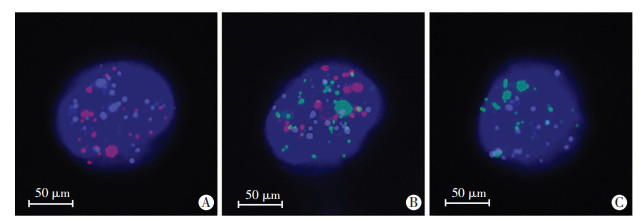
通过对滤过膜上的循环肿瘤细胞进行多重RNA原位杂交标记,对循环肿瘤细胞进行分型。其中上皮型标志物CK8、CK18、CK19及EpCAM基因表达阳性的为上皮型,表现为红色荧光;间质型标志物Vimentin和Twist基因表达阳性的为间质型,表现为绿色荧光;上皮型和间质型均表达阳性的为混合型,表现为红绿相间荧光;白细胞标志物CD45表达阳性者为白细胞,表现为白色荧光(图 1);HOXB7基因表达阳性的CTC,表现为紫色荧光(图 2)。
|
| A:白细胞;B:上皮型CTC;C:混合型CTC;D:间质型CTC 图 1 白细胞及3种CTC免疫荧光图像 |
|
| A:HOXB7阳性上皮型CTC;B:HOXB7阳性混合型CTC;C:HOXB7阳性间质型CTC 图 2 HOXB7阳性的3种CTC免疫荧光图像 |
2.3 CTC分型与肿瘤类型的关系
40例患者中,19例骨肉瘤患者共检测出795个CTC,17例软组织肉瘤患者共检测出430个CTC,4例尤文肉瘤或原始神经外胚层瘤患者共检测出31个CTC,其不同CTC分型见表 2。各瘤种CTC总数量分布差异无统计学意义(P=0.065),不同瘤种间上皮型、混合型及间质型CTC分布差异均无统计学意义(P>0.05,表 2)。
| CTC分型 | 肿瘤类型 | P | ||
| 骨肉瘤 | 尤文肉瘤或原始神经外胚层瘤 | 软组织肉瘤 | ||
| 上皮型 | 162 | 11 | 63 | 0.523 |
| 混合型 | 525 | 17 | 340 | 0.070 |
| 间质型 | 108 | 3 | 27 | 0.365 |
| 合计 | 795 | 31 | 430 | 0.065 |
2.4 CTC分型与肿瘤分期的关系
40例患者中,37例患者外周血CTC检测结果阳性(92.5%)。分析CTC计数与肿瘤分期的关系,结果显示,Ennecking Ⅰ期患者7例,其外周血CTC为36个,其中上皮型8个,混合型27个,间质型1个;均低于Ennecking Ⅱ期和Ⅲ期患者(表 3)。各分期CTC平均数量分布不同,差异具有统计学意义(H=12.918,P=0.002,表 3);Ennecking Ⅲ期患者CTC平均计数明显高于Ⅰ期(调整后的P=0.001)和Ⅱ期(调整后的P=0.024)患者。各分期上皮型CTC平均数量分布不同,差异具有统计学意义(H=12.454,P=0.002,表 3);Ennecking Ⅲ期患者上皮型CTC平均数量明显高于Ⅰ期(调整后的P=0.004)和Ⅱ期(调整后的P=0.004)患者。各分期混合型CTC数量分布不同,差异具有统计学意义(H=6.367,P=0.041,表 3),但校正显著性水平的事后两两比较无统计学意义。各分期间质型CTC数量分布不同,差异具有统计学意义(H=18.277,P < 0.001,表 3);Ennecking Ⅲ患者间质型CTC平均数量明显高于Ⅰ期(调整后的P < 0.001)和Ⅱ期(调整后的P=0.001)患者。
| CTC分型 | Enneking分期 | P | ||
| Ⅰ(n=7) | Ⅱ(n=27) | Ⅲ(n=6) | ||
| 上皮型 | 8 | 112 | 116 | 0.002 |
| 混合型 | 27 | 701 | 154 | 0.041 |
| 间质型 | 1 | 45 | 92 | < 0.001 |
| 合计 | 36 | 858 | 362 | 0.002 |
2.5 CTC中HOXB7的表达水平与肿瘤分期的关系
通过RNA原位杂交技术检测40例患者外周血CTC中HOXB7基因的表达,不同Ennecking分期间HOXB7阳性率差异有统计学意义(χ2=11.672,P=0.003,表 4)。同时检测19例骨肉瘤患者外周血CTC中HOXB7的表达水平,骨肉瘤Ennecking Ⅱ期患者HOXB7阳性率显著低于Ⅲ期患者(χ2=4.992,P=0.025,表 5)。
| Enneking分期 | n | HOXB7阳性 | HOXB7阴性 | 合计 |
| Ⅰ | 7 | 15(41.7) | 21(58.3) | 36 |
| Ⅱ | 27 | 400(46.6) | 458(53.4) | 858 |
| Ⅲ | 6 | 206(56.9) | 156(43.1) | 362 |
| χ2=11.672,P=0.003 | ||||
| Enneking分期 | n | HOXB7阳性 | HOXB7阴性 | 合计 |
| Ⅱ | 13 | 212(49.0) | 221(51.0) | 433 |
| Ⅲ | 6 | 206(56.9) | 156(43.1) | 362 |
| χ2=4.992,P=0.025 | ||||
3 讨论
CTC是原发肿瘤脱落到血管系统并在血流中循环的细胞[15]。这些细胞因其在早期诊断和监测抗癌药物治疗反应中的潜在作用而受到关注。基于细胞表面抗原或CTC的物理性质,研究者们开发了不同的CTC分离和表征技术[16]。基于细胞表面抗原的方法,如上皮标志物,是应用最广泛的CTC检测策略[17]。因此,现有的CTC研究主要集中于上皮来源肿瘤如乳腺癌、肺癌、胃癌等,而肉瘤等间质来源肿瘤由于缺乏特异性标记物[18],限制了骨与软组织肉瘤CTC的相关研究[6]。然而,这些上皮抗原为基础的方法很可能忽略了CTC细胞亚群的上皮间质转化(epithelial-mesenchymal transition,EMT)。EMT是一个多步骤的过程,在转移和癌症进展中起着重要的作用,具有EMT表型的CTCs被认为参与了肿瘤的传播和转移[19-20]。本研究采用CanPatrolTM CTC富集技术对骨肉瘤患者中无法表达上皮抗原的CTC进行分离和鉴定[12]。
通过对40例骨与软组织肿瘤患者外周血CTC的检测,37例患者外周血中检测出CTC细胞,阳性率为92.5%,如此高的阳性率反映了骨与软组织肉瘤是一类非常容易发生远处转移的肿瘤。对不同分期肉瘤患者进行CTC检测,结果表明,治疗前的CTC细胞计数与肿瘤的分期和转移显著相关,分期越晚,CTC计数越多。同时对不同分期CTC的类型进行分析,结果显示,间质型CTC与肉瘤患者的分期显著相关,分期越晚,间质型CTC比例越大。这说明上皮间质转化与肉瘤的进展、转移有关。目前对肉瘤患者复发、转移的检测及疗效的评估主要依靠影像学检查,尽管传统的TNM分期及Enneking分期在肉瘤的预后评估中起到了重要作用,但也有其局限性。肉瘤患者的转移与其组织学分级密切相关,尽管有些肿瘤体积较小,但可发生转移,说明按照解剖学特征的分期系统不足以充分反映肉瘤的预后。因此CTC计数可以作为影像学检查的补充,辅助临床医师对肉瘤患者病情的评估及预后的判定。对于CTC计数较多,间质型CTC比例较大等预后不良因素的患者进行针对性的干预处理。
研究表明,HOXB7可通过上调碱性成纤维细胞生长因子(basic fibroblast growth factor, bFGF),激活Ras/Rho蛋白通路,从而促进乳腺细胞发生EMT,促使肿瘤的转移[21]。最新研究发现骨肉瘤组织和细胞与相邻的非肿瘤骨组织和成骨细胞相比HOXB7的表达被上调[22]。HOXB7敲除显著抑制细胞存活、增殖、迁移和上皮间充质转移。相反HOXB7的下调显著抑制了骨肉瘤细胞的体外增殖,同时抑制了体内异种移植瘤的生长,下调HOXB7也抑制了骨肉瘤细胞的迁移和侵袭[23]。因此为了检测HOXB7在肉瘤中的作用,本研究检测了不同分期CTC中HOXB7基因的表达情况。结果显示,肿瘤分期越晚,HOXB7表达的阳性率越高,对骨肉瘤进行亚组分析,也可得出同样的结果。说明HOXB7可以通过增加CTC的侵袭和转移,进而增加肿瘤的转移,影响骨与软组织肉瘤患者的预后。因此,HOXB7可以作为预测骨肉瘤预后的潜在靶点。
综上所述,本研究通过研究骨与软组织肉瘤患者外周血CTC计数、分型及HOXB7基因表达与骨与软组织肿瘤的分期及转移之间的关系,结果表明,CTC计数、间质型CTC及HOXB7基因高表达与骨与软组织肉瘤的远处转移密切相关,可以作为常规影像学检查的补充,在预测肿瘤转移、疗效及预后中发挥辅助作用。未来需要多中心、大样本的临床试验进一步验证目前的结论。
| [1] |
CHANG L, ASATRIAN G, DRY S M, et al. Circulating tumor cells in sarcomas: a brief review[J]. Med Oncol, 2015, 32(1): 430. DOI:10.1007/s12032-014-0430-9 |
| [2] |
MEYERS P A, SCHWARTZ C L, KRAILO M D, et al. Osteosarcoma: the addition of muramyl tripeptide to chemotherapy improves overall survival—a report from the Children's Oncology Group[J]. J Clin Oncol, 2008, 26(4): 633-638. DOI:10.1200/JCO.2008.14.0095 |
| [3] |
KIM M Y, OSKARSSON T, ACHARYYA S, et al. Tumor self-seeding by circulating cancer cells[J]. Cell, 2009, 139(7): 1315-1326. DOI:10.1016/j.cell.2009.11.025 |
| [4] |
ZHONG X, ZHANG H, ZHU Y, et al. Circulating tumor cells in cancer patients: developments and clinical applications for immunotherapy[J]. Mol Cancer, 2020, 19(1): 15. DOI:10.1186/s12943-020-1141-9 |
| [5] |
PAOLETTI C, HAYES D F. Circulating tumor cells[J]. Adv Exp Med Biol, 2016, 882: 235-258. DOI:10.1007/978-3-319-22909-6_10 |
| [6] |
CABEL L, PROUDHON C, GORTAIS H, et al. Circulating tumor cells: clinical validity and utility[J]. Int J Clin Oncol, 2017, 22(3): 421-430. DOI:10.1007/s10147-017-1105-2 |
| [7] |
WELLIK D M. Hox genes and vertebrate axial pattern[J]. Curr Top Dev Biol, 2009, 88: 257-278. DOI:10.1016/S0070-2153(09)88009-5 |
| [8] |
LIAO W T, JIANG D, YUAN J, et al. HOXB7 as a prognostic factor and mediator of colorectal cancer progression[J]. Clin Cancer Res, 2011, 17(11): 3569-3578. DOI:10.1158/1078-0432.CCR-10-2533 |
| [9] |
原薇薇, 谭艳, 杜敏, 等. HOXB7基因在肺腺癌中的表达及其临床意义[J]. 临床肿瘤学杂志, 2014, 19(11): 987-991. YUAN W W, TAN Y, DU M, et al. Expression of HOXB7 in human lung adenocarcinoma and its clinical significance[J]. Chin Clin Oncol, 2014, 19(11): 987-991. |
| [10] |
BITU C C, CARRERA M, LOPES M A, et al. HOXB7 expression is a prognostic factor for oral squamous cell carcinoma[J]. Histopathology, 2012, 60(4): 662-665. DOI:10.1111/j.1365-2559.2011.04102.x |
| [11] |
RUBIN E, WU X, ZHU T, et al. A role for the HOXB7 homeodomain protein in DNA repair[J]. Cancer Res, 2007, 67(4): 1527-1535. DOI:10.1158/0008-5472.CAN-06-4283 |
| [12] |
WU S, LIU S, LIU Z, et al. Classification of circulating tumor cells by epithelial-mesenchymal transition markers[J]. PLoS ONE, 2015, 10(4): e0123976. DOI:10.1371/journal.pone.0123976 |
| [13] |
LI M, LU Y, LONG Z, et al. Prognostic and clinicopathological significance of circulating tumor cells in osteosarcoma[J]. J Bone Oncol, 2019, 16: 100236. DOI:10.1016/j.jbo.2019.100236 |
| [14] |
WU Z J, TAN J C, QIN X, et al. Significance of circulating tumor cells in osteosarcoma patients treated by neoadjuvant chemotherapy and surgery[J]. Cancer Manag Res, 2018, 10: 3333-3339. DOI:10.2147/CMAR.S176515 |
| [15] |
GUPTA G P, MASSAGUE J. Cancer metastasis: building a framework[J]. Cell, 2006, 127(4): 679-695. DOI:10.1016/j.cell.2006.11.001 |
| [16] |
CHEN X X, BAI F. Single-cell analyses of circulating tumor cells[J]. Cancer Biol Med, 2015, 12(3): 184-192. DOI:10.7497/j.issn.2095-3941.2015.0056 |
| [17] |
YU M, BARDIA A, WITTNER B S, et al. Circulating breast tumor cells exhibit dynamic changes in epithelial and mesenchymal composition[J]. Science, 2013, 339(6119): 580-584. DOI:10.1126/science.1228522 |
| [18] |
李明辉, 鲁亚杰, 张浩强, 等. 骨肉瘤外周血循环肿瘤细胞检测的临床意义[J]. 中华骨科杂志, 2018, 38(6): 330-337. LI M H, LU Y J, ZHANG H Q, et al. Clinical significance of peripheral blood circulating tumor cells detection in osteosarcoma patients[J]. Chin J Orthop, 2018, 38(6): 330-337. DOI:10.3760/cma.j.issn.0253-2352.2018.06.002 |
| [19] |
THIERY J P, ACLOQUE H, HUANG R Y, et al. Epithelial-mesenchymal transitions in development and disease[J]. Cell, 2009, 139(5): 871-890. DOI:10.1016/j.cell.2009.11.007 |
| [20] |
KANG Y, PANTEL K. Tumor cell dissemination: emerging biological insights from animal models and cancer patients[J]. Cancer Cell, 2013, 23(5): 573-581. DOI:10.1016/j.ccr.2013.04.017 |
| [21] |
WU X, CHEN H, PARKER B, et al. HOXB7, a homeodomain protein, is overexpressed in breast cancer and confers epithelial-mesenchymal transition[J]. Cancer Res, 2006, 66(19): 9527-9534. DOI:10.1158/0008-5472.CAN-05-4470 |
| [22] |
YANG Y, CHEN J, CHEN Q. Upregulation of HOXB7 promotes proliferation and metastasis of osteosarcoma cells[J]. Mol Med Rep, 2017, 16(3): 2773-2778. DOI:10.3892/mmr.2017.6906 |
| [23] |
YANG L, XIE F, LI S. Downregulation of Homeobox B7 inhibits the tumorigenesis and progression of osteosarcoma[J]. Oncol Res, 2017, 25(7): 1089-1095. DOI:10.3727/096504016X14784668796788 |



