2. 400037 重庆,陆军军医大学(第三军医大学)第二附属医院:妇产科
2. Department of Obstetrics and Gynecology, Second Affiliated Hospital, Army Medical University (Third Military Medical University), Chongqing, 400037, China
血管翳(Pannus)是人工瓣膜功能障碍常见的并发症之一。血管翳由纤维组织及慢性相关炎症细胞组成,常覆盖于人工瓣膜周围,导致瓣膜功能障碍,发生率1.6%~2%[1-2]。传统方法是通过经胸超声心动图、X-线透视及CT等方法评估人工瓣膜血管翳,传统方法诊断敏感性低且测值不准确,不能精确判断人工瓣膜梗阻程度。近年来,随着矩阵探头的发展,RT-3DTEE可提供独特的可视化效果和心脏空间结构定位,并对瓣膜和心室功能进行精确测量[3]。为了解决传统方法诊断人工瓣膜血管翳灵敏度低下的问题,本研究采用RT-3DTEE去诊断血管翳,旨在提高人工瓣血管翳诊断敏感性及特异性,定量瓣膜梗阻程度,以指导临床心血管外科下一步治疗方案选择。
1 资料与方法 1.1 研究对象选择2017年9月-2019年9月我院心血管外科收治人工主动脉瓣置换术后瓣膜梗阻患者89例,其中男性27例,女性62例,年龄31~68(49.8±9.1)岁,身高(1.63±0.08)m, 体质量(57.1±7.2)kg, 体表面积(1.56±0.12)m2,换瓣年限(8.1±4.3)年,术前单主动脉瓣置换患者19例,主动脉瓣及二尖瓣双瓣置换患者70例,所有患者均住院行二次换瓣手术,其中51例由手术标本及病理确诊为人工主动脉瓣血管翳。纳入标准:人工主动脉瓣口平均跨瓣压差≥30 mmHg[4],临床高度怀疑血管翳致使瓣膜梗阻;TTE、二维TEE及RT-3DTEE资料完整;手术及病理资料完整。排除标准:人工主动脉瓣口平均跨瓣压差 < 30 mmHg;因各种原因未手术治疗患者;相关病例资料不全。本研究经我院伦理委员会审核同意(2018-研第091-01),所有患者均知情同意。
1.2 仪器与方法使用GE vivid E9及E95彩色多普勒超声诊断仪,经胸M5Sc探头,频率1.7~3.3 MHz,经食管6VT-D探头,频率4~8 MHz。经胸探查:患者取左侧卧位,连接心电图,测量常规心脏数据后,在大动脉短轴及左室长轴等切面仔细观察人工主动瓣膜,显示并测量血管翳厚度及跨瓣压差。经食管探查:检查前确认患者禁食4~6 h,检查患者一般情况包括体温、脉搏、呼吸与血压,签署经食管超声心动图知情同意书,吞咽盐酸丁卡因胶浆麻醉剂5~6 g,患者取左侧卧位,经口腔轻柔插入食管探头,深度25~40 cm,采用进退、旋转探头,调节晶片角度,尖端屈曲等多方法结合,清晰显示人工主动脉瓣血管翳图像,观察瓣叶开放节律及最大开放角度,然后测量血管翳厚度。二维测量完成后,调整至主动脉瓣短轴切面(角度45~60°左右),启用RT-3DTEE模式,通过转动角度及切割等方式调整至显示血管翳最佳切面,观察血管翳位置,测量血管翳厚度、圆周范围及面积。全程同步Ⅱ导联心电图监视。
1.3 评价指标采用敏感性(sensitivity)、特异性(specificity)来评价RT-3DTEE的诊断水平;用阳性预测值(positive predictive value,PPV)、阴性预测值(negative predictive value,NPV)来反映RT-3DTEE在本组病例中的诊断效能。
1.4 统计学分析采用SPSS 22.0统计软件,计量资料以x±s表示,3种方法所测血管翳厚度行t检验对比,相关性比较均采用Pearson相关分析法,计数资料采用百分比(%)表示,行χ2检验。检验水准: α=0.05。
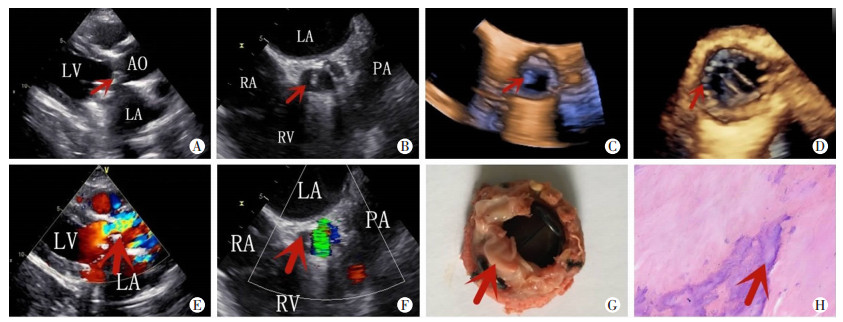
2 结果 2.1 3种方法诊断血管翳对比经手术标本及病理确诊血管翳患者51例,RT-3DTEE诊断血管翳敏感性、特异性、阳性预测值、阴性预测值分别为84.3%(43/51)、92.1%(35/38)、93.5%(43/46)、81.4%(35/43),经胸超声的敏感性、特异性、阳性预测值、阴性预测值分别41.1%(21/51)、89.5%(34/38)、84%(21/25)、53.1%(34/64),经食管超声的敏感性、特异性、阳性预测值、阴性预测值分别为64.1%(33/51)、89.5%(34/38)、89.2%(33/37)、64.4%(34/52), RT-3DTEE的敏感性、特异性、阳性预测值及阴性预测值均高于经胸超声及经食管超声心动图,差异有统计学意义(P < 0.05)。血管翳图像见图 1。
|
| A、E:TTE左室长轴图像,人工主动脉瓣瓣架周围软组织影像,血流通过此处梗阻(红色箭头示);B、F:TEE短轴切面45°,瓣架周围软组织影像,血流通过此处梗阻(红色箭头示);C:RT-3DTEE,三维显示瓣架周围血管翳影像,呈浅蓝色(红色箭头示);G:术中血管翳标本(红色箭头示),血管翳围绕瓣架及瓣柱不规则生长,与RT-3DTEE有较好的相关性;D:RT-3DTEE显示二次换瓣术后,血管翳清除,两个瓣叶活动自如(红色箭头示);H:血管翳病理HE染色结果,血管翳成分以纤维组织为主,部分可见钙化(红色箭头示)LA=Left atrium, 左房;LV=Left ventricle, 左室;AO=aorta,主动脉;RA=Right atrium,右房;RV=Right ventricle, 右室;PA=Pulmonary artery,肺动脉 图 1 血管翳超声图像与术中标本、病理比较 |
2.2 3种方法测量血管翳厚度的对比
3种方法测量人工主动脉瓣血管翳厚度值见表 1,RT-3DTEE测量的血管翳厚度较经胸及二维食管超声测值差异均有统计学意义。
| RT-3DTEE/mm | TTE/mm | TEE/mm | |
| 血管翳厚度 | 6.2±1.2 | 5.1±1.2a | 5.5±1.3a |
| a:P < 0.05, 与RT-3DTEE比较 | |||
2.3 RT-3DTEE在定量血管翳所致梗阻程度的价值
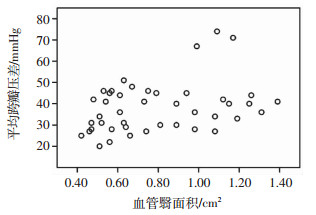
RT-3DTEE成功显示血管翳43例,从外科视野观察,血管翳位于右前象限最多见(右前象限者20例,右后象限者6例,左前象限者12例,左后象限者5例),厚度(6.2±1.2) mm,圆周范围(18.4±5.2) mm,面积(0.79±0.28) cm2,人工主动脉瓣平均跨瓣压差(38±12)mmHg,血管翳面积与人工瓣平均跨瓣压差具有一定相关性(r=0.34,P < 0.05),图 2。
|
| 图 2 血管翳面积与人工主动脉瓣平均跨瓣压差相关性分析 |
3 讨论
人工主动脉瓣置换是常见的心脏外科手术之一,人工瓣膜功能障碍的风险为每年0.1%~4%[5],血管翳形成是造成瓣膜功能障碍的重要原因之一,血管翳能干扰跨瓣血流,导致瓣膜功能不全或狭窄,部分患者可能需要二次心脏手术[6-8]。血管翳的组织学结构包括:内皮细胞、肌纤维母细胞、胶原巨噬细胞、淋巴细胞、巨细胞、浆细胞和乳突细胞组成的慢性炎症细胞及胶原、弹性纤维。大多数学者认为其发生机制为:瓣环周围心肌组织受损瘢痕修复、假体材料存在异物样炎症反应等[1]。传统诊断工具为经胸超声心动图、X-线透视及CT等方法,然而,受机械瓣声影、混响、增益等影响,血管翳检出率很低,术前诊断几乎是不可能的[8]。通常情况下,二尖瓣主要功能是舒张期血流通过左房到达左室,主动脉瓣主要功能是收缩期血流从左室喷射至主动脉,主动脉瓣承受的压力远高于二尖瓣,主动脉瓣瓣环却又小于二尖瓣瓣环,这就造成人工主动脉瓣血管翳的发生率及影响程度高于人工二尖瓣,这与大多数作者观点相符合[9-10],所以本研究选择我院临床诊断人工主动脉瓣梗阻患者89例为研究对象,通过比较RT-3DTEE与TTE和二维TEE三种方法的差异,旨在提高血管翳显示成功率及定量分析血管翳对人工瓣膜的梗阻程度,指导临床下一步治疗及手术方案选择。
RT-3DTEE与TTE相比的优势在于缩短超声探查路径,避开肋骨、肺组织及金属瓣架干扰,运用多切面超声数据实时重建图像,大大提高了超声心动图对人工瓣血管翳的显像成功率及图像分辨率,RT-3DTEE显示血管翳特点为:人工主动脉瓣架周围软组织团块,凸向瓣口内,导致梗阻,无明显活动度,伴或不伴瓣叶活动障碍。TTE与二维TEE往往显示血管翳图像质量不高,其声像图特点为:人工主动脉瓣架下方低回声软组织团块,部分可阻塞瓣叶活动或影响其开放角度,团块可致血流梗阻。本研究中RT-3DTEE诊断血管翳敏感性为84.3%,与BARBETSEAS等[5]评价RT-3DTEE诊断人工瓣功能障碍的敏感性为83%基本一致。RT-3DTEE不仅能提高诊断敏感性,对定量血管翳亦有重大价值。从表 1中可以看出,RT-3D TEE所测厚度值与TTE及二维TEE相比,差异有统计学意义,根据我们的经验,三者测值差异的原因,可能与图像显示角度有关,血管翳本身形状不规则及金属瓣架遮挡,TTE和二维TEE仅获取血管翳图像的某一切面,很难显示全貌,故TTE及二维TEE常常低估血管翳厚度,RT-3D TEE则收集多切面二维超声信息,能更精确测量血管翳厚度,与标本厚度相关性良好(P < 0.01)。
从RT-3DTEE显像与术中血管翳的对照中,我们总结人工主动脉瓣血管翳的一些特点:①血管翳常生长于人工瓣膜缝合环周围,呈不规则、非对称性、顶部偏向主动脉侧;②从主动脉侧观察,血管翳以右上及左上象限明显,血管翳常附着于瓣柱,并凸向瓣架内,可影响瓣叶的开放角度,甚至阻碍瓣叶活动;③血管翳组织较韧,表面光滑,不易脱落,基本无明显摆动。结合TESHIMA等[1]研究,我们考虑人工瓣血管翳形成是机体对人工瓣膜材料的免疫性修复过程,血管翳形成可能与左室流出道结构、瓣周炎症发生的轻重、个体免疫反应及左室流出道收缩期高速湍流有关。
本研究还通过Pearson相关分析法比较血管翳面积与人工主动脉瓣平均跨瓣压差的关系,结果显示二者具有一定相关性(P < 0.05),这与文献[11-12]报道的研究相符合。临床可根据血管翳面积和人工瓣膜平均压差两项指标共同评估瓣膜阻塞程度,降低左室大小、左室心功能、体表指数、心率及代谢的影响,更准确评估人工主动脉瓣功能,指导下一步治疗方式选择。对于伴有血管翳形成的人工瓣膜严重梗阻患者,手术是唯一的治疗选择,本研究中51例经手术确诊为人工瓣膜血管翳,手术标本形态、大小与术前RT-3DTEE显示血管翳较为符合,进一步验证了RT-3DTEE对人工瓣膜血管翳形成的诊断价值,值得在临床工作中推广应用。
本研究存在一定局限性:①这是一项回顾性观察研究,涉及单一机构患者,所有数据测量可能并非同一医生,这可能会到影响到真实数据,而且既往忽略了血管翳与主动脉瓣开放角度的关系,以后研究中会准确测量人工主动脉瓣叶开放角度,了解两者的关联性;②RT-3DTEE通过切割、旋转、测量等手段,偶尔出现拼接方位错误,三维假象等,需时刻结合二维图像,做出正确诊断;③RT-3DTEE依赖于二维TEE图像清晰度及分辨率,只有清晰的二维图像,才能切割出完整、高分辨率的三维图像。
综上所述,RT-3D TEE可准确诊断并定位、定量人工主动脉瓣血管翳形成,对血管翳所致人工瓣膜功能障碍的早期诊断有重要意义,为临床治疗决策提供充足的支持,具有重要临床价值。
| [1] |
TESHIMA H, HAYASHIDA N, YANO H, et al. Obstruction of St Jude Medical valves in the aortic position: histology and immunohistochemistry of pannus[J]. J Thorac Cardiovasc Surg, 2003, 126(2): 401-407. DOI:10.1016/s0022-5223(03)00702-5 |
| [2] |
RIZZOLI G, GUGLIELMI C, TOSCANO G, et al. Reoperations for acute prosthetic thrombosis and pannus: an assessment of rates, relationship andrisk[J]. Eur J Cardiothorac Surg, 1999, 16(1): 74-80. DOI:10.1016/s1010-7940(99)00124-4 |
| [3] |
LANG R M, MOR-AVI V, SUGENG L, et al. Three-dimensional echocardiography: the benefits of the additional dimension[J]. J Am Coll Cardiol, 2006, 48(10): 2053-2069. DOI:10.1016/j.jacc.2006.07.047 |
| [4] |
唐红, 蒲岷. 经食管实时三维超声心动图图谱[M]. 北京: 人民卫生出版社, 2010: 63-64. TANG H, PU M. Transesophageal real-time three-dimensional echocardiography[M]. Beijing: People's Medical Publishing House, 2010: 63-64. |
| [5] |
BARBETSEAS J, NAGUEH S F, PITSAVOS C, et al. Differentiating thrombus from pannus formation in obstructed mechanical prosthetic valves: an evaluation of clinical, transthoracic and transesophageal echocardiographic parameters[J]. J Am Coll Cardiol, 1998, 32(5): 1410-1417. DOI:10.1016/s0735-1097(98)00385-4 |
| [6] |
KIM G H, YANG D H, KANG J W, et al. Subvalvular Pannus and thrombosis in a mitral valve prosthesis[J]. J Cardiovasc Comput Tomogr, 2016, 10(2): 191-192. DOI:10.1016/j.jcct.2015.09.004 |
| [7] |
SUH Y J, LEE S, IM D J, et al. Added value of cardiac computed tomography for evaluation of mechanical aortic valve: Emphasis on evaluation of pannus with surgical findings as standardreference[J]. Int J Cardiol, 2016, 214: 454-460. DOI:10.1016/j.ijcard.2016.04.011 |
| [8] |
CHUNG M S, YANG D H, KIM D H, et al. Subvalvular pannus formation causing aortic stenosis in patient with a normal prosthetic aortic valve: computed tomography finding[J]. Eur Heart J Cardiovasc Imaging, 2015, 16(4): 458. DOI:10.1093/ehjci/jeu285 |
| [9] |
王建德, 焦盼晴, 吴金涛, 等. 人工机械瓣功能异常52例超声心动图回顾分析[J]. 中华超声影像学杂志, 2014, 23(4): 297-301. WANG J D, JIAO P Q, WU J T, et al. Retrospective evaluation of echocardiography in mechanical prosthesis valvedysfunction[J]. Chin J Ultrasonol, 2014, 23(4): 297-301. DOI:10.3760/cma.j.issn.1004-4477.2014.04.006 |
| [10] |
VITALE N, RENZULLI A, AGOZZINO L, et al. Obstruction of mechanical mitral prostheses: analysis of pathologicfindings[J]. Ann Thorac Surg, 1997, 63(4): 1101-1106. DOI:10.1016/s0003-4975(96)01391-4 |
| [11] |
LEE S, LEE S P, PARK E A, et al. Real-time 3D TEE for diagnosis ofsubvalvular pannus formation in mechanical aortic valves: comparison with multidetector CT and surgical findings[J]. JACC Cardiovasc Imaging, 2015, 8(12): 1461-1464. DOI:10.1016/j.jcmg.2014.12.036 |
| [12] |
HA H, KOO H J, HUH H K, et al. Effect of Pannus formation on the prosthetic heart valve: In vitro demonstration using particle imagevelocimetry[J]. PLoS ONE, 2018, 13(6): e0199792. DOI:10.1371/journal.pone.0199792 |



