皮肤瘢痕是创伤后组织过度纤维化的结果。瘢痕的形成不仅影响患者外观、伴随的瘙痒和疼痛会严重影响患者的生活质量;而瘢痕的挛缩和增生更会引起关节活动度降低甚至关节畸形,从而导致患者肢体功能障碍[1-2]。目前针对瘢痕的客观评估和诊断仍是难点。病理检查虽是临床瘢痕诊断的金标准,但因其是有创检查,且耗时较长、需要病理专家解读等原因致使临床应用受限。而目前临床常规使用的瘢痕评估指标仍然大都是主观指标,如温哥华瘢痕评定量表和患者与观察者瘢痕评估量表,对评测人的专业水平和主观依赖很大,难以准确、客观地评价瘢痕的特征,且增生性瘢痕与瘢痕疙瘩量表评分相差较小。因此,临床医师尤其需要一种客观、无创的工具来精准地评估和诊断瘢痕。
超声检查在医学中早已广泛应用,但使用超声检查皮肤病变以及瘢痕还在不断发展的阶段。早期超声由于分辨率较低,不足以精确地区分各皮肤亚层,这使得超声在皮肤病变诊断方面受到限制。近年来,高频超声的出现和应用则解决了这一重大难题。高频超声(high-frequency ultrasound,HF-US)是指中心频率为10~30 MHz的超声,同时具有高分辨率和高穿透率,可在有效观察皮肤全层的同时清楚地分辨皮肤的精细结构[3-4]。高频超声的主要优点包括组织在体的实时成像、皮肤形态和生理结构的测量、使用非电离介质的安全性等,并且高频超声所获得皮肤声像图与病理学之间有很好的相关性[5-7]。这使得高频超声应用于皮肤厚度的测量、皮肤声像图研究、皮肤疾病诊断成为可能。20 MHz高频超声能清晰区分皮肤表皮、真皮及皮下组织层次结构与界面[8],是目前诊断皮肤病变较佳的新型皮肤检测设备。然而,目前使用20 MHz高频超声对不同类型的瘢痕如增生性瘢痕、瘢痕疙瘩和萎缩性瘢痕进行较深入的比较分析和定量分析研究尚少。
因此,本研究使用20 MHz高频超声检测增生性瘢痕、瘢痕疙瘩和萎缩性瘢痕等不同类型瘢痕与正常皮肤的厚度、回声强度和超声声像图的差异,以探讨高频超声对瘢痕的诊断及临床应用价值。
1 资料与方法 1.1 研究对象本研究招募68例18~60(43.4±5.6)岁参与者,其中增生性瘢痕患者20名、瘢痕疙瘩患者18名、萎缩性瘢痕患者10名,为2018-2019年在本院就诊的瘢痕患者;正常皮肤志愿者20名,为泸州市区正常皮肤志愿者。已进行了其他瘢痕治疗或对超声专用凝胶过敏者除外。本研究通过西南医科大学附属医院伦理委员会批准(KY2019090)。
1.2 皮肤全层厚度检测所有参与者使用高频超声检测瘢痕部位,检测前先清洗患者瘢痕皮肤,由医师于瘢痕正中处涂抹超声专用凝胶,探头与皮肤表面垂直,轻微接触皮肤,避免探头加压,每个部位使用皮肤超声仪采集3张图片,每张图片检测3处瘢痕皮肤全层厚度,并取平均值。仪器为MEDA魅力MD-310S高端彩超仪(天津迈达医学科技股份有限公司),探头频率20 MHz,参与者均由同1名医师进行图片采集和数据测量工作。
1.3 皮肤回声强度检测将瘢痕皮肤和正常皮肤超声声像图导入DFY-Ⅰ型超声图像定量分析诊断软件[9],对采集的参与者瘢痕部位超声声像图进行定量分析,每张超声声像图于真皮层手动选择3处相同面积区域进行回声强度检测,并取平均值。
1.4 统计学分析用SPSS 17.0统计软件,数据以x±s表示,采用单因素方差分析比较各组瘢痕厚度与瘢痕回声强度差异性,检验水准α=0.05。
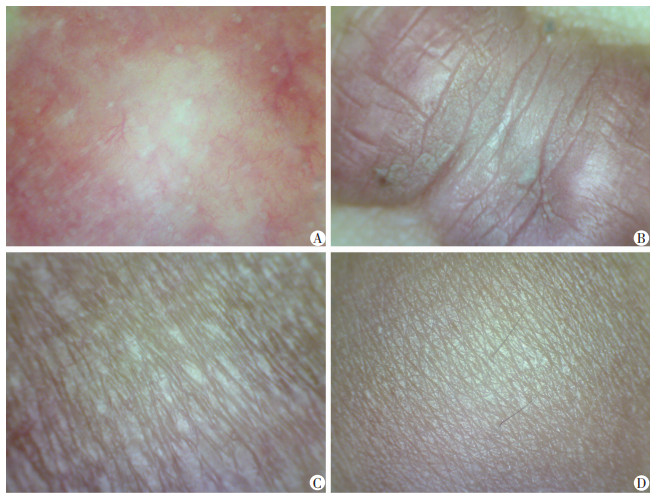
2 结果 2.1 不同瘢痕皮肤光学图特点通过MEDA魅力MD-310S高端彩超仪设备自带的皮肤显微镜检测瘢痕皮肤及正常皮肤,增生性瘢痕皮肤于皮肤显微镜下显示皮肤肤色偏红,瘢痕处血供明显偏高,存在大量的增生性毛细血管(图 1A);瘢痕疙瘩皮肤边缘明显隆起,高于正常皮肤表面,质地较硬韧,肤色偏红,常成结节状或片状肿块(图 1B);萎缩性瘢痕皮肤色素不均一,皮肤血供较差,皮肤表面出现较多细小褶皱(图 1C);而正常皮肤显微镜下显示表面光滑,纹里细腻,质地柔软,血供正常,且存在健康毛囊和汗毛(图 1D)。
|
| A:增生性瘢痕;B:瘢痕疙瘩;C:萎缩性瘢痕;D:正常皮肤 图 1 皮肤显微镜观察不同类型瘢痕皮肤的光学特点 |
2.2 不同瘢痕皮肤超声声像图具有特征性表现
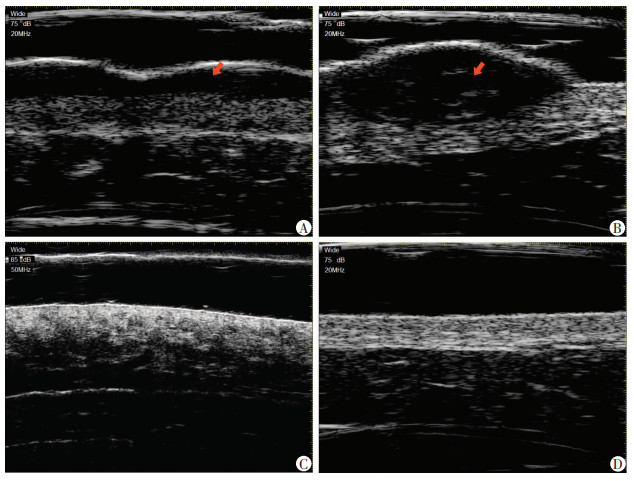
从皮肤全层厚度比较,增生性瘢痕与瘢痕疙瘩皮肤全层较厚,而萎缩性瘢痕和正常皮肤全层厚度较薄。从真皮层回声强度比较,增生性瘢痕与瘢痕疙瘩的真皮层回声强度均呈现低回声状态,增生性瘢痕的低回声区为真皮上层的一条低回声带,而瘢痕疙瘩的低回声区为表皮下一较集中的椭圆形低回声区域;而萎缩性瘢痕与正常皮肤真皮层回声强度较增生性瘢痕与瘢痕疙瘩的真皮层高,正常皮肤真皮回声强度较均一,而萎缩性瘢痕真皮层回声强度不均一。从组织结构排列比较,正常皮肤各层组织结构完整,分界清楚,依次为表皮层-高回声层、真皮层-不同强度的分散回声、皮下组织-无回声或低回声层,有时可观察到因间隔存在的增强回声结构;增生性瘢痕与瘢痕疙瘩表皮不平整,向上隆起,真皮层和皮下组织分界较清楚;而萎缩性瘢痕皮肤表皮虽较平整,但真皮层和皮下组织分界不清楚(图 2)。
|
| A:增生性瘢痕;B:瘢痕疙瘩;C:萎缩性瘢痕;D:正常皮肤;箭头示低回声区域 图 2 20 MHz高频超声检测不同类型瘢痕皮肤的声像图特点 |
2.3 不同瘢痕皮肤厚度差异
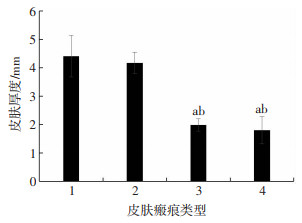
通过高频超声检测不同瘢痕皮肤和正常皮肤厚度。增生性瘢痕和瘢痕疙瘩皮肤厚度明显厚于萎缩性瘢痕和正常皮肤厚度(P < 0.05),而增生性瘢痕和瘢痕疙瘩皮肤厚度没有明显差异(P>0.05),萎缩性瘢痕和正常皮肤厚度没有明显差异(P>0.05)。见图 3。
|
| 1:增生性瘢痕;2:瘢痕疙瘩;3:萎缩性瘢痕;4:正常皮肤;a:P < 0.05,与增生性瘢痕比较;b:P < 0.05,与瘢痕疙瘩比较 图 3 不同瘢痕皮肤和正常皮肤厚度差异 |
2.4 不同瘢痕皮肤真皮层回声强度差异
与正常皮肤真皮层回声强度比较,增生性瘢痕与瘢痕疙瘩真皮层回声强度明显低于正常皮肤(P < 0.05),而萎缩性瘢痕与正常皮肤的真皮层回声强度没有明显差异(P>0.05)。而不同类型瘢痕皮肤真皮层回声强度之间比较,增生性瘢痕与瘢痕疙瘩均明显低于萎缩性瘢痕(P < 0.05);而瘢痕疙瘩真皮层回声强度又明显低于增生性瘢痕(P < 0.05,图 4)。

|
| 1:增生性瘢痕;2:瘢痕疙瘩;3:萎缩性瘢痕;4:正常皮肤; a:P < 0.05,与增生性瘢痕比较;b:P < 0.05,与瘢痕疙瘩比较 图 4 不同瘢痕皮肤和正常皮肤回声强度差异 |
3 讨论
高频超声系统是利用18 MHz以上的超声频率获取具有可接受分辨率的皮肤结构图像[10]。其中50 MHz的甚高频超声虽能获得更为精细的皮肤超声影像,但其穿透深度浅(5~6 mm),难以穿透厚而致密的增生性瘢痕。相比之下,20 MHz的高频超声则既能详细地显示皮肤结构亚结构,又具有更好的穿透深度(接近1 cm)[11-12],是诊断瘢痕的良好影像学方式。目前已有研究报道可通过高频超声客观评估瘢痕,观察激光治疗增生性瘢痕的效果[13-14]。然而,目前尚未有研究使用高频超声对不同类型的瘢痕如增生性瘢痕、瘢痕疙瘩和萎缩性瘢痕进行较深入的比较分析和定量分析。
不同类型的瘢痕具有不同的病理生理结构、组织学特征和细胞功能等,但目前临床对瘢痕的诊断常依靠临床表现来主观判断。尤其针对增生性瘢痕与瘢痕疙瘩的鉴别诊断仍是难点,常依靠其是否具有侵袭性、是否位于张力线[15]等特征来主观判断,大量研究也将增生性瘢痕与瘢痕疙瘩归为一类瘢痕进行研究,但其不但具有相似性还具有差异性[16]。因此本研究使用高频超声客观观察不同类型瘢痕皮肤表现出的声像学特点。
本研究结果表明:与正常皮肤相比,不同类型的瘢痕具有特征性的超声表现。正常皮肤的表皮层、真皮层与皮下组织分界清楚,厚度为(1.80±0.48)mm,真皮层回声强度为98.35±17.22;而增生性瘢痕和瘢痕疙瘩皮肤厚度明显厚于正常皮肤(P < 0.05),真皮层回声强度却明显低于正常皮肤(P < 0.05);萎缩性瘢痕皮肤厚度和回声强度与正常皮肤虽没有明显差异,但各皮肤亚层分界不清楚,排列紊乱。
增生性瘢痕与瘢痕疙瘩相比,虽两者真皮层回声均呈低回声模式,但因其胶原分布排列、细胞外基质含量、血供情况等不同,使得高频超声观察增生性瘢痕与瘢痕疙瘩的真皮层回声具有不同特征性的表现。瘢痕疙瘩真皮层总体回声强度明显低于增生性瘢痕(P < 0.05),并且存在一较集中的椭圆形低回声区域;而增生性瘢痕则在真皮上层表现为一条状低回声带。HSU等[17]研究发现瘢痕疙瘩真皮层胶原束以特定的方向排列,一般与皮肤张力线平行[15, 18-19],且瘢痕长轴的横切面呈结节状;而胶原纤维具有吸水性能,胶原的存在会影响皮肤水分的均匀性,水分的空间分布也可能与胶原组织有关[17],并且水在超声声像图中表现为低回声,因此本研究推测瘢痕疙瘩因胶原束以特定的方向排列组成的结节状病理结构而形成特殊的真皮层椭圆形回声缺乏区域。而增生性瘢痕病变的特点为胶原代谢异常和细胞外基质成分丰富,且真皮层中胶原纤维排列紊乱[20],这与瘢痕疙瘩有序排列的胶原束不同。
萎缩性瘢痕与正常皮肤相比,虽两者皮肤全层厚度和真皮层回声强度并无差异,但萎缩性瘢痕表皮菲薄,且其真皮层、皮下组织与深部组织如肌肉、神经等紧密粘连[21],使得高频超声观察萎缩性瘢痕各皮肤亚层分界不清楚,排列紊乱;并且萎缩性瘢痕真皮层回声强度不均一,真皮上层回声强度高于真皮下层。而正常皮肤的表皮层、真皮层与皮下组织分界很清楚,且真皮层回声强度均一。
综上所述,本研究通过20 MHz高频超声对不同类型瘢痕皮肤和正常皮肤声像学的研究发现,不同类型瘢痕组织之间的超声声像图有特征性的表现,组织生理结构、真皮层回声强度和厚度均有明显的差异。本研究结果可指导临床对不同类型瘢痕组织的客观诊断与鉴别诊断,可快速、有效并客观地区分瘢痕疙瘩与增生性瘢痕。其中使用超声声像图结合病理切片对瘢痕组织的胶原排列、分型及含量等进行更精准的定位和定量等问题有待进一步的研究。
| [1] |
FRIEDSTAT J S, HULTMAN C S. Hypertrophic burn scar management: what does the evidence show? A systematic review of randomized controlled trials[J]. Ann Plast Surg, 2014, 72(6): S198-S201. DOI:10.1097/SAP.0000000000000103 |
| [2] |
BOMBARO K M, ENGRAV L H, CARROUGHER G J, et al. What is the prevalence of hypertrophic scarring following burns?[J]. Burns, 2003, 29(4): 299-302. DOI:10.1016/s0305-4179(03)00067-6 |
| [3] |
BHATTA A K, KEYAL U, LIU Y Q. Application of high frequency ultrasound in dermatology[J]. Discov Med, 2018, 26(145): 237-242. |
| [4] |
POLAŃSKA A, DAŃCZAK-PAZDROWSKA A, JAŁOWSKA M, et al. Current applications of high-frequency ultrasonography in dermatology[J]. Postepy Dermatol Alergol, 2017, 34(6): 535-542. DOI:10.5114/ada.2017.72457 |
| [5] |
唱文娟, 张淼, 康春松, 等. 皮肤及皮神经超声检测的实验研究[J]. 山西医科大学学报, 2003, 34(6): 497-498. CHANG W J, ZHANG M, KANG C S, et al. Experimental research on skin and cutaneous nerve by ultrasonography[J]. J Shanxi Med Univ, 2003, 34(6): 497-498. DOI:10.3969/j.issn.1007-6611.2003.06.006 |
| [6] |
SCHMID-WENDTNER M H, DILL-MVLLER D. Ultrasound technology in dermatology[J]. Semin Cutan Med Surg, 2008, 27(1): 44-51. DOI:10.1016/j.sder.2008.01.003 |
| [7] |
WALLER J M, MAIBACH H I. Age and skin structure and function, a quantitative approach (Ⅰ): blood flow, pH, thickness, and ultrasound echogenicity[J]. Skin Res Technol, 2005, 11(4): 221-235. DOI:10.1111/j.0909-725X.2005.00151.x |
| [8] |
BESSONART M N, MACEDO N, CARMONA C. High resolution B-scan ultrasound of hypertrophic scars[J]. Skin Res Technol, 2005, 11(3): 185-188. DOI:10.1111/j.1600-0846.2005.00118.x |
| [9] |
王志刚, 邹建中, 廖翠容, 等. 超声图像定量诊断研究:附123例分析[J]. 上海生物医学工程, 1995, 16(1): 22-26. WANG Z G, ZOU J Z, LIAO C R, et al. Research of US qualitative evaluation[J]. Shanghai J Biomed Eng, 1995, 16(1): 22-26. |
| [10] |
LEE K C, DRETZKE J, GROVER L, et al. A systematic review of objective burn scar measurements[J]. Burns Trauma, 2016, 4: 14. DOI:10.1186/s41038-016-0036-x |
| [11] |
ZMUDZINSKA M, CZARNECKA-OPERACZ M, SILNY W. Principles of dermatologic ultrasound diagnostics[J]. Acta Dermatovenerol Croat, 2008, 16(3): 126-129. |
| [12] |
VAN DEN KERCKHOVE E, STAES F, FLOUR M, et al. Reproducibility of repeated measurements on post-burn scars with Dermascan C[J]. Skin Res Technol, 2003, 9(1): 81-84. DOI:10.1034/j.1600-0846.2003.00375.x |
| [13] |
MADNI T D, LU K R, NAKONEZNY P A, et al. Treating hypertrophic burn scar with 2940-nm Er: YAG laser fractional ablation improves scar characteristics as measured by noninvasive technology[J]. J Burn Care Res, 2019, 40(4): 416-421. DOI:10.1093/jbcr/irz056 |
| [14] |
ELREFAIE A M, SALEM R M, FAHEEM M H. High-resolution ultrasound for keloids and hypertrophic scar assessment[J]. Lasers Med Sci, 2019. DOI:10.1007/s10103-019-02830-4 |
| [15] |
OGAWA R, OKAI K, TOKUMURA F, et al. The relationship between skin stretching/contraction and pathologic scarring: the important role of mechanical forces in keloid generation[J]. Wound Repair Regen, 2012, 20(2): 149-157. DOI:10.1111/j.1524-475X.2012.00766.x |
| [16] |
KÖSE O, WASEEM A. Keloids and hypertrophic scars: are they two different sides of the same coin?[J]. Dematol Surg, 2008, 34(3): 336-346. DOI:10.1111/j.1524-4725.2007.34067.x |
| [17] |
HSU C K, TZENG S Y, YANG C C, et al. Non-invasive evaluation of therapeutic response in keloid scar using diffuse reflectance spectroscopy[J]. Biomed Opt Express, 2015, 6(2): 390-404. DOI:10.1364/BOE.6.000390 |
| [18] |
EHRLICH H P, DESMOULIÈRE A, DIEGELMANN R F, et al. Morphological and immunochemical differences between keloid and hypertrophic scar[J]. Am J Pathol, 1994, 145(1): 105-113. |
| [19] |
KISCHER C W, BRODY G S. Structure of the collagen nodule from hypertrophic scars and keloids[J]. Scan Electron Microsc, 1981(Pt 3): 371-376. |
| [20] |
徐静静.人瘢痕组织脱细胞真皮基质的组织结构和生物力学性能[D].西宁: 青海大学, 2015. XU J J. Structural and biomechanical properties of accelular dermal matrix derived from human scar tissue[D]. Xining: Qinghai University, 2015. |
| [21] |
张秀丽, 唐正东. 瘢痕研究进展[J]. 中国中西医结合皮肤性病学杂志, 2012, 11(4): 268-270. ZHANG X L, TANG Z D. The research progress of scar[J]. Chin J Dermatovenereol Integr Tradit West Med, 2012, 11(4): 268-270. DOI:10.3969/j.issn.1672-0709.2012.04.035 |



