贲门失弛缓症是一种少见的原发性食管运动功能障碍性疾病,其病因尚不明确,一般认为是由于食管肌层内神经节的变性、减少或缺如导致食管蠕动的缺乏和食管下括约肌的松弛缺陷。该病临床症状多表现为吞咽困难、反流以及胸痛、体质量下降等。贲门失弛缓症目前尚无根治性治疗手段,现有的治疗多是通过降低食管下括约肌压力来达到改善食管排空和缓解患者吞咽困难的目的[1]。腹腔镜下Heller手术(laparoscopic heller myotomy,LHM)结合部分胃底折叠术(Dor)是目前公认的外科治疗贲门失弛缓症的金标准[2],已广泛开展。INOUE等[3]于2010年首次报道经口内镜下肌切开术(peroral endoscopic myotomy,POEM)治疗贲门失弛缓症,该技术迅速被广大内镜医师接受,甚至成为部分医院治疗贲门失弛缓症的首选。不少研究表明:POEM与LHM相比,安全性与近期疗效相近,但远期疗效需要进一步验证[4-5]。POEM手术在切开贲门上下食管肌层后缺乏有效的抗反流手段,部分学者担心该术式可能导致术后胃食管反流(gastroesophageal reflux disease,GERD)并发症的发生。本研究回顾性分析我院自2012年10月至2017年4月经手术治疗并完成随访的贲门失弛缓症患者的临床资料,比较LHM和POEM两种治疗方法在中远期症状改善、食管动力学改善、GERD并发症等方面的差异,探讨POEM术后GERD并发症的治疗策略,为临床治疗的选择提供依据。
1 资料与方法 1.1 研究设计采用回顾性队列研究,收集我科2012年10月至2017年4月共61例经治疗并完成随访的贲门失弛缓症患者的临床病理资料。男性32例,女性29例,年龄13~76岁。其中30例行腹腔镜Heller手术加部分胃底折叠术(Dor),设为腹腔镜组(LHM组);31例行经口内镜下肌切开术,设为内镜组(POEM组)。本研究通过我院医学伦理委员会审批,批号为医研伦审(2018)第111号。两组患者术前分别签署Heller手术和POEM手术知情同意书。
1.2 纳入标准和排除标准 1.2.1 纳入标准① 经上消化道造影、高分辨食管测压明确诊断为贲门失弛缓症,且芝加哥分型为Ⅰ型或Ⅱ型;②有明显的胸痛、吞咽困难甚至呕吐等临床症状;③全身重要脏器功能良好,可耐受手术;④患者及家属同意手术。
1.2.2 排除标准① 诊断为贲门失弛缓症芝加哥Ⅲ型;②小儿贲门失弛缓症;③其他疾病导致的食管功能性吞咽梗阻;④既往LHM或POEM手术治疗复发者。
1.3 手术方法 1.3.1 LHM结合部分胃底折叠术(Dor)术晨留置胃管,全麻气管插管后取平卧位,脐上1 cm切口为腔镜观察孔,建立气腹;取两侧锁骨中线与脐水平线交叉点为操作孔。剑突下腹腔穿刺针穿入后;用丝线缝合肝三角韧带,牵引肝左叶显露食管裂孔部,游离腹段食管后,用超声刀剪开下端食管前壁肌层,切开纵行肌和环形肌,长度6~10 cm,胃端越过胃食管交界部2 cm,剥离肌层至食管周径的3/4,使食管黏膜膨出,置入电子纤维胃镜,充气观察食管下括约肌松弛程度及是否损伤食管黏膜。然后行胃底前壁180°折叠术,即Dor术(图 1)。术后观察有无腹痛、腹胀、黑便、恶心、呕吐等症状,给予胃肠减压、肠外营养支持、保护胃黏膜、抑酸等治疗。48 h后开始进流质饮食2~3 d,逐渐过渡到半流质、软食。复查碘水造影后出院。
|
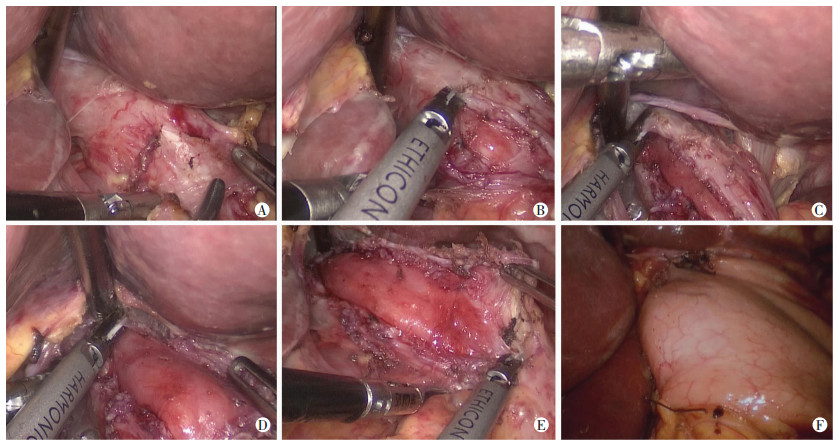
| A:游离下段食管;B:切开食管前壁肌层暴露黏膜层;C:切开增厚的食管肌层6~10 cm;D:充分膨出食管黏膜层;E:切开胃食管结合部肌层至胃端2 cm;F:胃底前壁180°折叠 图 1 贲门失弛缓症LHM+Dor手术过程 |
1.3.2 POEM手术
术晨禁食水,全麻气管插管后取左侧卧位,奥硝唑注射液20 mL冲洗食管,胃镜下取贲门上方8~10 cm处食管前壁黏膜为切口,注射生理盐水10 mL,用KD-650L高频DL型切开刀切开黏膜层约3 cm,扩张后内镜进入隧道,向下扩张至贲门下2~3 cm,纵行切开环形肌层,当食管下段及贲门下环形肌层与纵行肌层分界不明显时,切开固有肌层全层;隧道内充分止血后钛夹关闭黏膜入口(图 2)。术后复查胸片,监测生命体征,术后应用保护胃黏膜、抑酸、营养支持等治疗。术后24~48 h复查碘水造影,无异常则开始进食流质饮食,2~3 d后逐渐转变为半流质、软质饮食。无特殊情况发生则出院。
|
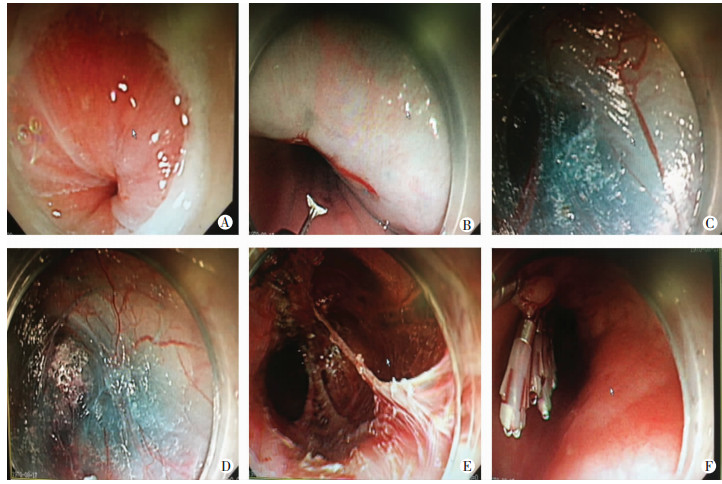
| A:确认齿状线位置;B:取齿状线上方8~10 cm食管前壁为切口;C:扩张后内镜进入隧道;D:扩张至贲门下2~3 cm;E:纵行切开环形肌层;F:金属夹关闭黏膜入口 图 2 贲门失弛缓症POEM手术过程 |
1.4 观察指标
① 患者临床基本资料:性别、年龄、病程、芝加哥分型、术前Ecardt评分、术前下段食管静息压(lower esophageal sphincter pressure, LES)测定值、既往治疗史;②手术资料:手术时间、失血量、手术相关并发症、住院日、住院费用;③术后随访资料:Ecardt评分(≤3分为治疗有效)、LES压力测定值、GERD自评量表(7分判定为有明显GERD症状)、24 h pH值测定、胃镜检查、临床相关GERD(病理性酸反流与GERD症状或食管炎相关)。
1.5 随访所有患者术后通过面对面随访或电话随访,随访至2019年4月。随访期间至少完成1次高分辨食管测压、24 h pH值测定和胃镜检查。
1.6 统计学分析采用SPSS 24.0统计软件,正态分布的计量资料用x±s表示,组间比较采用独立样本t检验;非正态分布的计量资料用M(P25,P75)表示,采用秩和检验;计数资料以样本数、率或百分比表示,组间比较采用χ2检验。P < 0.05为差异具有统计学意义。
2 结果 2.1 患者基本临床特征两组患者在性别、年龄、病程、芝加哥分型、既往治疗史方面,差异无统计学意义;LHM组术前Ecardt评分为6(5, 7)分,LES压力为(36.2±7.4)mmHg,POEM组术前Ecardt评分为6(5, 7)分,LES压力为(38.8±5.4)mmHg,两组间差异无统计学意义(表 1)。
| 组别 | n | 男/女(例) | 年龄/岁(x±s) | 病程/月 (x±s) |
芝加哥分型 (Ⅰ/Ⅱ,例) |
术前Ecardt评分 [M(P25, P75)] |
术前LES压力/mmHg (x±s) |
既往治疗史 (例) |
| LHM组 | 30 | 14/16 | 44.1±14.8 | 72.3±35.4 | 11 /19 | 6(5, 7) | 36.2±7.4 | 3 |
| POEM组 | 31 | 18/13 | 45.4±14.6 | 76.9±28.7 | 14 /17 | 6(5, 7) | 38.8±5.4 | 5 |
| P值 | 0.373 | 0.702 | 0.580 | 0.500 | 0.643 | 0.089 | 0.478 |
2.2 Heller组和POEM组患者的手术资料
两组患者在手术时间、失血量、住院日、住院费用方面差异无统计学意义。LHM组30例,出现手术相关并发症3例,发生率10%,其中术中食管黏膜破损2例,经一期修补术后恢复良好;胃黏膜出血1例,术后胃肠减压出约200 mL血性液体,经局部应用止血药物后好转。POEM组31例,发生手术相关并发症6例,发生率19.4%,其中皮下气肿3例,1例经皮下插入针头排气后好转,2例经保守治疗后好转;纵膈气肿1例,经保守治疗后痊愈;气胸1例,经胸腔穿刺抽气后痊愈出院;发生术后严重胸痛1例,给予静脉镇痛药物后缓解。两组手术相关并发症比较差异均无统计学意义(表 2)。
| 组别 | n | 手术时间/min (x±s) |
失血量/mL (x±s) |
并发症 (例) |
住院日/d (x±s) |
住院费用/万元 (x±s) |
| LHM组 | 30 | 112.5±19.7 | 27.2±17.4 | 3 | 8.1±3.2 | 4.2±0.9 |
| POEM组 | 31 | 126.3±57.3 | 37.6±9.9 | 6 | 8.3±2.3 | 4.0±0.6 |
| P值 | 0.217 | 0.051 | 0.303 | 0.793 | 0.277 |
2.3 随访情况
截至2019年4月28日,LHM组和POEM组中位随访时间分别为40.0(24.0,76.0)个月和35.0(27.0,77.0)个月,两组治疗有效率(Ecardt评分≤3分)分别为86.7%(26/30)和90.3%(28/31),差异无统计学意义。LHM组和POEM组比较,术后中位Ecardt评分、术后LES压力的差异均无统计学意义,但与术前相比,均有明显下降(P < 0.05)。POEM组在术后胃食管反流症状、病理性酸反流、食管炎发生率方面高于LHM组,且存在更高的临床相关GERD(P < 0.05,表 3)。
| 组别 | n | 术后Ecardt评分 [M(P25,P75)] |
术后LES压力/mmHg (x±s) |
胃食管反流症状(例) | 异常酸反流 (例) |
食管炎 (例) |
临床相关GERD (例) |
| LHM组 | 30 | 1(0, 2) | 14.5±6.3 | 3 | 4 | 2 | 1 |
| POEM组 | 31 | 1(0, 2) | 15.7±4.8 | 11 | 12 | 9 | 7 |
| P值 | 0.976 | 0.407 | 0.018 | 0.024 | 0.023 | 0.026 |
3 讨论
贲门失弛缓症是一种原发性食管运动功能障碍性疾病,传统的治疗方法有药物治疗、内镜下肉毒素注射、球囊扩张术及外科或内镜下手术。药物治疗因疗效差、副作用多,目前已很少应用。内镜下肉毒素注射治疗,多数患者在2年内复发,且需要反复多次注射,仅适用于不能耐受手术的患者[6];内镜下球囊扩张也需要多次扩张且效果难以持久,更因有食管穿孔的风险,已逐渐被LHM手术及POEM手术所取代[7]。
腹腔镜下LHM+Dor是目前公认的手术治疗贲门失弛缓症的金标准,术后5年、10年的吞咽困难缓解率可达85%、76.1%,该手术对胸骨后疼痛的缓解率为71%~89%,并能有效提高患者的营养状况及生活质量[8-10]。近年来,POEM手术因无体表切口、创伤小,近期疗效与LHM手术相当,越来越被内镜医生及患者所接受。LI等[11]在2013年报道了121例POEM手术患者,症状缓解率为95%,术后食管反流率为16.5%。目前多数研究显示POEM在安全性及近期疗效上与LHM相近,但缺乏远期疗效的评价[12-14]。本研究中,LHM组与POEM组手术时间、失血量、手术相关并发症、住院日、住院费用差异均无统计学意义,两者安全性相当,与文献报道相符。分析手术相关并发症,POEM组主要为气体并发症,多经保守治疗可以痊愈;LHM组主要为食管黏膜破损,在腔镜的高清视野和术中胃镜的支持下,多可及时发现,术中一期缝合修补即可痊愈。两种术式较为严重的并发症分别为食管穿孔引起的纵隔炎、腹膜炎,在本组病例中虽无发生,一旦发生常引起严重感染甚至休克,危及患者生命,应引起足够重视。本研究术后随访时间较长,LHM组和POEM组中位随访时间分别为40.0(24.0,76.0)个月和35.0(27.0,77.0)个月,两组治疗有效率分别为86.7%(26/30)和90.3%(28/31),差异均无统计学意义,说明两种治疗方法的中远期疗效相当,均可有效缓解吞咽困难的症状,同时使下食管括约肌压力明显下降,手术效果较为确切。
GERD是POEM术后主要的远期并发症,越来越受到手术医师的关注,但国内相关文献报道较少。REPICI等[15]的一项荟萃分析显示:POEM术后胃食管反流症状、异常酸暴露和食管炎的发生率均显著高于LHM手术(19.0% vs 8.8%、39% vs 16.8%、29.4% vs 7.6%)。SANAKA等[16]报道的一组贲门失弛缓症患者POEM术后病理性酸反流发生率显著高于LHM手术患者(48.4% vs 13.6%,P < 0.001),异常DeMeester积分比例为54.8% vs 17.4%(P < 0.001)。POEM是内镜下在食管黏膜层及固有肌层之间建立隧道,然后在隧道内切开肌层的微创技术,切开环形肌或全部食管肌层,松解了引起吞咽困难的解剖结构,使食管下段括约肌压力明显降低,改善患者症状效果明显。但正如该技术开始兴起时外科医生所担心的一样,与LHM+Dor相比,POEM手术缺乏有效的抗反流手段,术后易引起胃食管反流。贺德志等[17]发现:POEM手术切开食管全层肌比切开环形肌可导致术后更高的GERD发生率。LHM手术由食管外膜开始逐层切开食管全部肌层,暴露食管黏膜层并使之充分膨出,因为有部分胃底折叠术的抗反流措施,术后GERD并发症发生率显著低于POEM手术。本研究也证实:POEM组术后胃食管反流症状(P=0.018)、病理性酸反流(P=0.024)、食管炎(P=0.023)以及临床相关GERD(P=0.026)的发生率均显著高于LHM组。部分学者认为,POEM术后长期的胃食管反流、食管酸暴露可能引起更严重的并发症,如食管狭窄、Barrett食管甚至食管恶性肿瘤[18],但目前这方面的文献报道较少。我们认为:鉴于POEM术后GERD发生率较高,潜在的远期不良后果尚不明确,术后长期密切的随访和检查是必要的;对于存在术后GERD的患者,无论是否有明显临床症状,建议口服质子泵抑制剂进行治疗。POEM手术可用于治疗LHM失败或者复发的贲门失弛缓症病例,KRISTENSEN等[19]报道了采用POEM治疗LHM手术失败或复发病例的经验,手术难度明显增加,但长期疗效满意。我们认为:对于POEM术后发生严重GERD的患者,在口服药物治疗效果不佳或患者不能耐受长期服药的情况下,补充性的腹腔镜胃底折叠手术或许是一个可行的治疗方法,值得探索。
POEM和LHM在治疗贲门失弛缓症的安全性和临床疗效相当,但由于POEM术后较高的GERD发生率,术前应对该类并发症的发生风险进行充分的告知,并做好术后长期随访。
| [1] |
VAEZIM F, PANDOLFINO J E, VELA M F. ACG clinical guideline: diagnosis and management of achalasia[J]. Am J Gastroenterol, 2013, 108(8): 1238-1249. DOI:10.1038/ajg.2013.196 |
| [2] |
PANDOLFINOJ E, GAWRON A J. Achalasia: a systematic review[J]. JAMA, 2015, 313(18): 1841-1852. DOI:10.1001/jama.2015.2996 |
| [3] |
INOUE H, MINAMI H, KOBAYASHI Y, et al. Peroral endoscopic myotomy (POEM) for esophageal achalasia[J]. Endoscopy, 2010, 42(4): 265-271. DOI:10.1055/s-0029-1244080 |
| [4] |
KUMAGAI K, TSAIJ A, THORELL A, et al. Per-oral endoscopic myotomy for achalasia. Are results comparable to laparoscopic Heller myotomy?[J]. Scand J Gastroenterol, 2015, 50(5): 505-512. DOI:10.3109/00365521.2014.934915 |
| [5] |
DE PASCALE S, REPICI A, PUCCETTI F, et al. Peroral endoscopic myotomy versus surgical myotomy for primary achalasia: single-center retrospective analysis of 74 patients[J]. Dis Esophagus, 2017, 30(8): 1-7. DOI:10.1093/dote/dox028 |
| [6] |
ANNESE V, BASSOTTI G, COCCIA G, et al. A multicentre randomised study of intrasphincteric botulinum toxin in patients with oesophageal achalasia. GISMAD Achalasia Study Group[J]. Gut, 2000, 46(5): 597-600. DOI:10.1136/gut.46.5.597 |
| [7] |
ZANINOTTO G, BENNETT C, BOECKXSTAENS G, et al. The 2018 ISDE achalasia guidelines[J]. Dis Esophagus, 2018, 31(9). DOI:10.1093/dote/doy071 |
| [8] |
ZANINOTTO G, COSTANTINI M, RIZZETTO C, et al. Four hundred laparoscopic myotomies for esophageal achalasia: a single centre experience[J]. Ann Surg, 2008, 248(6): 986-993. DOI:10.1097/SLA.0b013e3181907bdd |
| [9] |
CHEN Z, BESSELLJ R, CHEW A, et al. Laparoscopic cardiomyotomy for achalasia: clinical outcomes beyond 5 years[J]. J Gastrointest Surg, 2010, 14(4): 594-600. DOI:10.1007/s11605-010-1158-2 |
| [10] |
COSTANTINI M, ZANINOTTO G, GUIRROLI E, et al. The laparoscopic Heller-Dor operation remains an effective treatment for esophageal achalasia at a minimum 6-year follow-up[J]. Surg Endosc, 2005, 19(3): 345-351. DOI:10.1007/s00464-004-8941-7 |
| [11] |
LI Q L, CHEN W F, ZHOU P H, et al. Peroral endoscopic myotomy for the treatment of achalasia: a clinical comparative study of endoscopic full-thickness and circular muscle myotomy[J]. J Am Coll Surg, 2013, 217(3): 442-451. DOI:10.1016/j.jamcollsurg.2013.04.033 |
| [12] |
MARANO L, PALLABAZZER G, SOLITO B, et al. Surgery or peroral esophageal myotomy for achalasia: A systematic review and meta-analysis[J]. Medicine (Baltimore), 2016, 95(10): e3001. DOI:10.1097/MD.0000000000003001 |
| [13] |
ZHANG Y, WANG H J, CHEN X D, et al. Per-oral endoscopic myotomy versus laparoscopic heller myotomy for achalasia: A meta-analysis of nonrandomized comparative studies[J]. Medicine (Baltimore), 2016, 95(6): e2736. DOI:10.1097/MD.0000000000002736 |
| [14] |
SCHLOTTMANN F, PATTIM G. Laparoscopic heller myotomy versus per oral endoscopic myotomy: evidence-based approach to the treatment of esophageal achalasia[J]. Am Surg, 2018, 84(4): 496-500. |
| [15] |
REPICI A, FUCCIO L, MASELLI R, et al. GERD after per-oral endoscopic myotomy as compared with Heller's myotomy with fundoplication: a systematic review with meta-analysis[J]. Gastrointest Endosc, 2018, 87(4): 934-943. DOI:10.1016/j.gie.2017.10.022 |
| [16] |
SANAKAM R, THOTA P N, PARIKH M P, et al. Peroral endoscopic myotomy leads to higher rates of abnormal esophageal acid exposure than laparoscopic Heller myotomy in achalasia[J]. Surg Endosc, 2019, 33(7): 2284-2292. DOI:10.1007/s00464-018-6522-4 |
| [17] |
贺德志, 王娟, 韩艳妙, 等. 环形肌切开和全层肌切开治疗贲门失弛缓症长期随访研究[J]. 中华消化内镜杂志, 2018, 35(5): 327-331. HE D Z, WANG J, HAN Y M, et al. Long-term efficacy of peroral endoscopic circular myotomy and full-thickness myotomy on treatment of achalasia of cardia[J]. Chin J Dig Endosc, 2018, 35(5): 327-331. DOI:10.3760/cma.j.issn.1007-5232.2018.05.006 |
| [18] |
KHASHABM A. The use of peroral endoscopic myotomy for the management of achalasia[J]. Gastroenterol Hepatol (N Y), 2018, 14(6): 387-389. |
| [19] |
KRISTENSEN H Ø, KIRKEGÅRD J, KJÆR D W, et al. Long-term outcome of peroral endoscopic myotomy for esophageal achalasia in patients with previous Heller myotomy[J]. Surg Endosc, 2017, 31(6): 2596-2601. DOI:10.1007/s00464-016-5267-1 |



