产科出血目前仍然是全世界范围内影响剖宫产发病率和死亡率的主要原因[1]。剖宫产大出血可能导致子宫切除、产妇死亡等不良结局[2]。输血是针对剖宫产大出血的有效急救措施;研究表明,发达国家剖宫产输血率为1.1%~7.8%,发展中国家最高达12.2%以上[3-4]。2015年“二胎政策”放开[5],我国再次剖宫产产妇逐年增加;ROUSE等[6]报道剖宫产输血率随剖宫产次数的增加而增加,表明再次剖宫产输血风险明显增加。已知剖宫产术中出血的危险因素包括产前贫血、宫缩乏力等[7],但对输血进行准确预测十分困难。麻醉和产科医师对术中输血的预判主要根据临床经验,尚缺乏可参考的临床证据,因此有必要提前预测产妇输血概率。
机器学习(machine learning,ML)是一门人工智能学科,利用数据训练模型,用模型进行预测,目前已广泛应用于医学领域[8-9]。其可通过对临床中的大量数据进行分析、计算和预测,帮助麻醉医师做出客观的预测和判断[10-11]。与传统统计学方法相比,机器学习模型可为患者提供更准确的预测,具有更好的预测性能[12]。因此本研究拟以再次剖宫产产妇作为研究对象,通过分析比较人工神经网络(artificial neural network,ANN)、极端梯度提升(extreme gradient boosting,XGB)和逻辑回归(logistic regression,LR)三种机器学习算法对再次剖宫产术中输血进行分析和预测,探索术中输血预测的新思路,帮助麻醉和产科医师术中提前识别需要输血的产妇,及时采取输血等干预措施。
1 对象与方法 1.1 对象本研究通过陆军军医大学第二附属医院伦理委员会批准(伦理审批号:2018-043-01)。通过医院电子病案医疗系统,总共纳入2015年10月至2017年10月于我院产科行再次剖宫产的产妇2 525例,记录产妇的年龄、入院时间、诊断等各项病例资料。纳入标准为:年龄20~45岁,病历资料齐全。排除标准为:孕龄 < 28周,严重凝血功能障碍、术前抗凝治疗以及合并出血性疾病。
1.2 纳入变量和结局基于文献检索和临床经验[13-14],研究纳入了患者信息、并发症、超声结果、检验结果、麻醉及术中因素等36个临床指标,详见表 1。研究的主要结局是输血,包括剖宫产术中红细胞等血制品的输注。目前剖宫产术中输血标准并不完全统一,基于指南和参考文献[15],我院剖宫产输血的指针为:产妇术中出血超过1 000 mL,持续出血合并心率加快、血压下降等生命体征改变需应用血管活性药物维持以及血红蛋白低于60 g/L等情况。
| 类型 | 指标 | |
| 患者信息 | 年龄、BMI、剖宫产次数、妊娠次数、孕周、距上次剖宫产时间、流产史 | |
| 并发症 | 子宫肌瘤、肝功能异常、肾功能异常、甲亢或甲减、妊娠期糖尿病、妊娠期高血压、子痫、胎盘早剥、胎膜早破、先兆子宫破裂 | |
| 超声结果 | 胎儿脐带绕颈、子宫前壁下段厚度、羊水指数、前置胎盘、术前胎心 | |
| 检验结果 | Hb、PLT、APTT、PT、TT、FIB | |
| 麻醉和术中因素 | 麻醉方式、ASA分级、手术时间、胎盘粘连、胎盘植入、盆腹腔粘连、新生儿体质量、宫缩乏力 | |
| BMI:体质指数;Hb:血红蛋白;PLT:血小板;PT:凝血酶原时间;APTT:活化部分凝血活酶时间;TT:凝血酶时间;FIB:血浆纤维蛋白原;ASA:美国麻醉医师协会 | ||
1.3 机器学习
本研究采用机器学习方法,利用监督学习从大量已标记剖宫产数据中进行学习,建立和训练出一个能够反映预测变量和输血结局之间相互关系的模型。首先将所有2 525个样本打乱后划分为两部分,前面75%为训练集,用于训练和优化机器学习模型,后面25%作为测试集,用于测试模型的最终表现。首先使用KFold方法将训练集数据划分为5份,分配到5个独立的文件夹中;其次挑选线性回归、线性判别、最近邻、决策树、朴素贝叶斯、支持向量机、Ada提升、随机森林、极端树、梯度提升决策树等11种机器学习算法,在每个Fold中依次进行训练和评估,最后使用机器学习框架scikit-learn中的cross_val_score方法进行交叉验证,观察不同算法的综合表现。最后根据算法表现,挑选了Logistic回归、XGB和ANN3个最终模型。机器学习的一个重要挑战是挑选合适的特征变量。以XGB算法为例,首先我们依据简单的线性相关性来评价所有36个特征,从中挑选出得分靠前的20个作为XGB算法的备选特征。然后,利用XGB模块提供的“feature_importances”和“plot_importance”方法来精选特征―前者用于描述各个特征的重要性评分(0~100),后者用于绘制评分靠前的重要特征图。最后,按重要性由高到低顺序排列这些特征,依次测试多个特征组合的表现,从而挑选出更少但更重要的特征。
3种机器学习算法实现均采用Python (版本号3.7.0)。Logistic回归模型的建立和训练使用Python软件包中的Scikit-learn(版本号0.20.1)。首先在训练集采用多因素Logistic回归分析,用重复5折交叉验证处理数据,得到输血最佳预测模型后用测试集最终评价模型的实际效果。
XGB模型同样使用Python机器学习软件包中的Scikit-learn进行训练和预测验证。在XGB的构建过程中,主要采用以决策树为基函数的提升方法。经过反复的多次训练、组合,得到一个最终模型。
ANN模型主要采用Keras(版本号2.2.4)和Tensorflow(版本号1.13.1)框架构建。人工神经网络的参数和超参数选择是一个难点,考虑到总体样本数量偏少,我们选择了简单的浅层BP模型,以简化模型、减轻过拟合现象。经多次尝试,初始模型选择adam优化器并设置Dropout=0.2进行训练的效果较好,最后应用训练好的BP模型对未经训练的样本进行预测,与真实值进行比较。实际ANN模型的输入层节点数根据实际纳入指标数确定(8个),输出层节点数为1(输出值为1表示输血,0表示未输血),隐含层数目(1层)和隐含层节点数(16个)根据多次迭代的结果择优确定[16]。
1.4 统计学分析计量资料采用x±s、M(P25,P75)表示,计数资料采用频数(百分比)表示。对输血组和非输血组的各项指标比较,连续型变量采用独立t检验或Mann-Whitney U检验,分类变量采用χ2检验或Fisher检验。
3种模型(或算法)的表现主要采用精确度、召回率、加权F1(综合了精确度和召回率的评价指标)和ROC曲线下面积(area under the receiver operating characteristic curve,AUROC)4个指标来衡量。
2 结果 2.1 研究对象一般特征本研究的有效样本对象共2 525例,其中332例(13.1%)进行了术中输血。输血组的术中出血量高于非输血组[(1 093.7±624.1) mL vs (306.5±127.0) mL; P < 0.001]。输血组产妇的手术时间和住院时间均长于非输血组[(117.2±50.5) min vs (76.5±21.0) min;(5.5±3.4) d vs (3.2±1.5) d; P < 0.001]。两组产妇比较差异有统计学意义的指标如表 2所示,包括孕周、剖宫产次数、妊娠次数、流产史、子宫前壁下段厚度、产前血红蛋白、血小板、活化部分凝血活酶时间、血浆纤维蛋白原、前置胎盘、胎盘粘连、胎盘植入、胎膜早破、盆腹腔粘连、宫缩乏力、胎儿体质量、麻醉方式、ASA分级等(P < 0.05)。
| 组别 | n | 年龄/岁 | BMI/kg·m-2 | 孕周/周 | 剖宫产次数 | 妊娠次数/次 | 流产史 | 妊娠合并子宫肌瘤 | 甲亢/甲减 | 距上次剖宫产时间/年 | 子宫前壁下段厚度/mm | 妊娠期糖尿病 | 妊娠期高血压 | 子痫 | 产前 Hb/g·dL-1 |
PLT/109·L-1 | PT/s | FIB/g·L-1 | APTT/s | TT/s | 肝功能异常 | 肾功能异常 | 胎盘植入 | 胎盘早剥 | 胎膜早破 | 盆腹腔粘连 | 前置胎盘 | 胎盘粘连 | 先兆子宫破裂 | 胎儿脐带绕颈 | 宫缩乏力 | 羊水指数/mm | 胎儿体质量/kg | 术中失血量/mL | 麻醉方式 | ASA分级 | 手术时间/min | 住院时间/d | |||||||
| 1 | 2 | ≥3 | 腰麻 | 硬膜外 | 腰硬联合 | 全麻 | Ⅰ-Ⅱ | Ⅲ-Ⅳ | |||||||||||||||||||||||||||||||||||||
| 非输血组 | 2 193 | 31.8±4.1 | 27.8±3.6 | 38.1±1.5 | 2 046(93.3) | 139(6.3) | 8(0.4) | 3.6±1.3 | 1 609(73.3) | 85(3.9) | 83(3.8) | 6.5±3.4 | 1.3±0.5 | 348(17.5) | 89(4.1) | 50(2.3) | 11.8±1.2 | 174.8±56.5 | 10.3±0.9 | 4.2±0.8 | 26.0±3.6 | 17.1±2.9 | 166(7.6) | 11(0.5) | 32(1.5) | 9(0.4) | 256(11.7) | 481(21.9) | 53(2.4) | 131(6.0) | 139(6.3) | 327(14.9) | 100(4.5) | 116.8±37.6 | 3.3±0.5 | 306.5±127.0 | 1894(86.4) | 70(3.2) | 137(6.2) | 91(4.1) | 2040(93.0) | 153(7.0) | 76.5±21.0 | 3.2±1.5 | |
| 输血组 | 332 | 31.7±5.0 | 27.4±4.1 | 36.2±2.1 | 292(88.0) | 40(12.0) | 0(0) | 4.0±1.4 | 283(85.2) | 9(2.7) | 9(2.7) | 6.7±3.7 | 1.6±0.7 | 50(15.1) | 9(2.7) | 8(2.4) | 10.6±1.5 | 184.8±66.5 | 10.4±0.7 | 4.1±0.9 | 27.0±4.4 | 17.0±2.4 | 30(9.0) | 1(0.3) | 98(29.5) | 1(0.3) | 18(5.4) | 129(38.9) | 245(73.8) | 108(32.5) | 25(7.5) | 52(15.7) | 92(27.7) | 120.3±39.0 | 2.9±0.5 | 1 093.7±624.1 | 256(77.1) | 3(0.9) | 29(8.7) | 44(13.3) | 109(32.8) | 223(67.2) | 117.2±50.5 | 5.5±3.4 | |
| P | 0.899 | 0.122 | < 0.001 | 0.001 | < 0.001 | < 0.001 | 0.337 | 0.374 | 0.432 | < 0.001 | 0.814 | 0.271 | 0.822 | < 0.001 | 0.009 | 0.127 | 0.025 | < 0.001 | 0.711 | 0.279 | > 0.999 | < 0.001 | > 0.999 | 0.001 | < 0.001 | < 0.001 | < 0.001 | 0.339 | 0.575 | < 0.001 | 0.165 | < 0.001 | < 0.001 | < 0.001 | < 0.001 | < 0.001 | < 0.001 | ||||||||
| BMI:体质指数;Hb:血红蛋白;PLT:血小板;PT:凝血酶原时间;APTT:活化部分凝血活酶时间;TT:凝血酶时间;FIB:血浆纤维蛋白原;ASA:美国麻醉医师协会 | |||||||||||||||||||||||||||||||||||||||||||||
2.2 机器学习结果
Logistic回归结果显示,术前Hb≤9.9 g/dL、PLT < 100/109·L-1、前置胎盘、胎盘粘连、宫缩乏力、ASAⅢ-Ⅳ和手术时间>100 min的产妇发生术中输血的风险更高,见表 3。
| 变量 | OR(95% CI) | P |
| 产前brHb/g·dL-1 | ||
| ≥11作参考组 | ||
| 10-10.9 | 1.878(0.924-3.820) | 0.082 |
| ≤9.9 | 16.831(9.035-31.354) | < 0.001 |
| PLT/109·L-1 | ||
| ≥100作参考组 | ||
| < 100 | 2.846(1.255-6.455) | 0.012 |
| 前置胎盘 | 18.346(8.280-40.648) | < 0.001 |
| 胎盘粘连 | 3.104(1.579-6.102) | 0.001 |
| 宫缩乏力 | 5.564(2.817-10.987) | < 0.001 |
| ASA分级 | ||
| Ⅰ~Ⅱ作参考组 | ||
| Ⅲ~Ⅳ | 4.999(2.580-9.683) | < 0.001 |
| 手术时间/min | ||
| ≤60作参考组 | ||
| 61~100 | 1.971(0.867-4.484) | 0.106 |
| > 100 | 5.515(2.145-14.178) | < 0.001 |
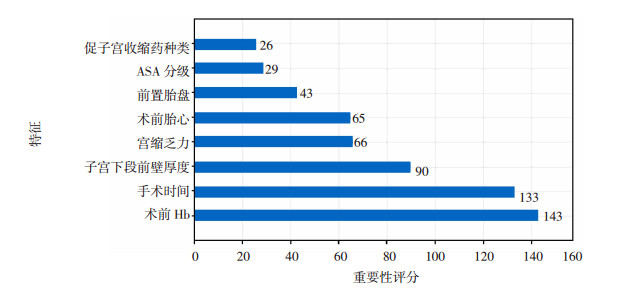
XGB预测模型最后得到8个最重要的特征,按照重要程度从高到低排序为:术前Hb、手术时间、子宫下段前壁厚度、宫缩乏力、术前胎心、前置胎盘、ASA分级、促子宫收缩药,评分越高的变量对模型的影响越大,结果如图 1所示。8个特征之间的相关性(包括与研究目标输血的相关性)如图 2所示,与输血相关性较大的指标包括:前置胎盘、ASA分级、手术时间、宫缩乏力和术前Hb,前置胎盘、ASA分级、手术时间、宫缩乏力与输血呈正相关,Hb与输血呈负相关。
|
| XGB预测模型的8个最重要的特征评分,评分越高的变量对模型的影响越大。对于一个训练好的XGB模型,可以利用get_fscore函数来获取其特征重要性F-score得分,亦可利用plot_importance函数将特征按重要性由高到低排列,同样以F-score得分来呈现。 图 1 XGB预测模型8个主要特征评分 |

|
| 相关性热图用于呈现不同因素之间的相关性大小(pearson相关系数)。横坐标和纵坐标对应交叉的格子内的数值为两个指标的相关性大小值,相关性的绝对值大小范围为0~1,值越大表示相关性越大;正值表示正相关,负值表示负相关。右侧的颜色渐变长条图指示不同的颜色代表不同的值。target为预测目标,即是否输血。比如左下角的-0.31表示术前Hb这一因素与是否输血之间的相关系数为-0.31(负相关)。 图 2 各指标之间的相关性热图(heat map) |
最后以人工神经网络模型为例,利用测试集中最后100个数据,绘制真实值和预测值散点图,蓝色小圈代表真实值,红色小点代表预测值,得到结果如图 3,获得较好预测效果。机器学习模型没有固定的方程,每个观察对象都对应1个不同的方程,将患者的变量特征输入模型后,即可为每个患者输出个体化的术中输血风险值。

|
| target为预测目标,即输血,1为输血,0为未输血。测试集中最后100个数据,绘制的真实值和预测值散点图,蓝色小圈代表真实值,红色小点代表预测值。可见实际输血14例,未输血86例,正确预测输血12例,未输血86例,仅2例预测错误。↑:示预测错误的2例示意 图 3 人工神经网络模型预测散点图 |
2.3 3种机器学习算法表现的评价
Logistic回归、XGB和ANN 3种机器学习算法的表现主要采用加权的F1、精确度、召回率和AUROC这4个指标来衡量。在全部样本上,采用将样本划分到5个Fold的方法来进行训练和交叉验证,并将交叉验证的指标求平均值然后比较其评价指标大小。Logistic回归的AUROC为0.960,略高于XGB的0.959和ANN的0.956。XGB的精确度为0.873,略高于Logistic回归的0.872和ANN的0.841。ANN的召回率为0.781,高于Logistic回归的0.760和XGB的0.759。XGB和ANN的F1均为0.950,高于Logistic回归的0.948(表 4)。
| 数据 | n | 模型 | F1 | 精确度 | 召回率 | AUROC |
| 全部样本 | 2 525 | Logistic回归 | 0.948 | 0.872 | 0.760 | 0.960 |
| XGB | 0.950 | 0.873 | 0.759 | 0.959 | ||
| ANN | 0.950 | 0.841 | 0.781 | 0.956 | ||
| 训练样本 | 1 893 | Logistic回归 | 0.951 | 0.952 | 0.954 | 0.868 |
| XGB | 0.966 | 0.967 | 0.964 | 0.904 | ||
| ANN | 0.960 | 0.961 | 0.961 | 0.882 | ||
| 测试样本 | 632 | Logistic回归 | 0.953 | 0.954 | 0.951 | 0.878 |
| XGB | 0.958 | 0.959 | 0.958 | 0.886 | ||
| ANN | 0.953 | 0.957 | 0.954 | 0.884 |
为了进一步比较3种机器学习方法的预测能力,再将全部样本随机划分为两部分:前75%训练集,后25%为测试集。然后,在训练集上再次训练3种模型,这时,模型并未接触到任何测试集中的样本。待模型训练结束后,再用训练出的模型在测试集上进行预测,并将真实输血状况与预测值进行比对,并查看其F1、精确度、召回率和AUROC 4个指标。分别就训练样本和测试样本来看,XGB的AUROC为0.904和0.886,高于Logistic回归的0.868和0.878,以及ANN的0.882和0.884;同时XGB的F1、精确度、召回率3个指标也均略高于Logistic回归和ANN。因此,就本次结果来看,XGB算法的表现略优于Logistic回归和ANN(表 4)。
3 讨论本研究回顾性分析了再次剖宫产产妇术中输血情况,采用机器学习算法对术中输血进行了预测研究,经过优化选择并比较了Logistic回归、XGB和ANN三种算法,为再次剖宫产产妇术中输血的风险评估和预测提供了新思路。既往关于剖宫产输血的预测研究大多笼统纳入了所有剖宫产人群,很少有专门区分初次剖宫产与再次剖宫产的研究。本研究中再次剖宫产术中输血的发生率为13.1%,远高于文献报道的1.1%~7.8%的剖宫产总体输血率[17]。另外,不同于一般剖宫产产妇,再次剖宫产产妇中输血产妇合并前置胎盘的比例高达73.8%,可见术前并发症多、手术难度增大、手术时间延长等可能是再次剖宫产术中输血率增加的原因。因此这些结果表明有必要探寻专门用于预测再次剖宫产术中输血的策略。
既往关于剖宫产围术期输血的预测研究大多采用传统的Logistic回归方法进行危险因素分析,很少专门对输血进行预测,由于传统方法存在数据处理工作量大、人工操作复杂等原因,其纳入的临床指标通常比较局限,很少纳入血液学指标如凝血4项及术前超声结果等各项计量资料,预测的灵敏度、特异性约在70%~80%之间,AUROC也不高(大多0.8~0.9)。本研究采用3种机器学习算法,纳入了30多个临床指标,通过对训练样本和测试样本的数据分析和预测验证,其F1、精确度、召回率均可达到90%以上,AUROC也接近0.9左右,较传统Logistic回归模型的预测效果大幅度提高。3种算法构建的预测模型最终都纳入产前血红蛋白、前置胎盘、宫缩乏力、ASA分级和手术时间这5个变量,这充分证明以上5个因素是再次剖宫产术中输血的重要预测因素,这与既往同类研究结果相吻合[13]。除了以上5个因素,研究还筛选出子宫下段前壁厚度、术前胎心和促子宫收缩药物等因素。GIZZO等[18]提出,当子宫下段前壁较薄处厚度 < 1.5 mm时,子宫破裂的风险明显增高,这可能与输血风险增加相关。促子宫收缩药物的应用是产科医师根据产妇情况采取的治疗措施,也可能影响输血情况。关于术前胎心,目前暂无研究讨论其与输血的关系。这3个因素在既往研究中少有提到,可能是潜在影响再次剖宫产术中输血的风险因素,需进一步的研究予以完善。
另外,本研究比较了Logistic回归、XGB和ANN 3种机器学习算法构建预测模型的各项评价指标。在全部样本上,3种算法的AUROC均可达0.95左右,其F1、精确度、召回率均表现较好且差异很小,说明3种模型在剖宫产术中输血的预测中均具有较大潜力。但就预测效果来看,XGB的4个指标(尤其是AUROC)均高于Logistic回归和ANN。因此就本研究结果来看,XGB算法的预测效果优于Logistic回归和ANN。而此前关于剖宫产输血预测的研究大多采用传统的Logistic回归分析方法,尽管Logistic回归容易理解并实现,且广泛应用于临床疾病的危险因素研究,但也有一些缺点,比如容易欠拟合,分类精度不高,预测效果容易受缺失数据影响等。从本研究结果可以发现相比传统统计学方法,基于机器学习XGB的预测模型可更好地用于再次剖宫产产妇术中输血预测。
XGB是当前比较流行的集成学习算法,其最大的特点在于它能够自动利用CPU的多线程进行并行,不容易过拟合,同时在算法上加以改进提高了精度。它本身不是一个单独的机器学习算法,而是通过构建并结合多个机器学习器来完成学习任务。即通过训练若干个个体学习器,结合成一个强学习器,以达到博采众长的目的。集成学习可以用于分类问题集成,回归问题集成,特征选取集成等,可以说所有的机器学习领域都可以看到集成学习的身影[19]。
本研究存在一定的局限性:首先,这是一项回顾性临床研究,预测结果需要进一步在前瞻性研究中验证。其次,本院作为该地区的危重产妇转诊治疗中心,纳入的产妇病情更加复杂,可能存在选择偏倚,需进一步多中心研究来完善相关结果。最后,本研究中可能还存在一些未纳入的影响因素,如产科医师和麻醉医师的临床经验等,未纳入的潜在因素也可能对结果有一定影响。
综上所述,本研究采用3种机器学习算法对较大样本的剖宫产临床数据进行处理分析和结果预测,发现再次剖宫产术中输血的5个重要预测变量为:术前Hb、手术时间、宫缩乏力、前置胎盘、ASA分级。同时将3种算法进行比较,发现Logistic回归、XGB和ANN这3种机器学习算法均可用于剖宫产术中输血的预测,其中XGB的预测效果比Logistic回归和ANN更准确。
| [1] |
SAAD A, COSTANTINE M M. Obstetric hemorrhage: recent advances[J]. Clin Obstet Gynecol, 2014, 57(4): 791-796. DOI:10.1097/GRF.0000000000000062 |
| [2] |
PEARSON G A, MACKENZIE I Z. Blood loss and blood transfusion at Caesarean section: a prospective observational study covering 30years[J]. Eur J Obstet Gynecol Reprod Biol, 2014, 181: 72-77. DOI:10.1016/j.ejogrb.2014.06.025 |
| [3] |
CHUA S C, JOUNG S J, AZIZ R. Incidence and risk factors predicting blood transfusion in Caesarean section[J]. Aust N Z J Obstet Gynaecol, 2009, 49(5): 490-493. DOI:10.1111/j.1479-828X.2009.01042.x |
| [4] |
GOUNDAN A, KALRA J K, RAVEENDRAN A, et al. Descriptive study of blood transfusion practices in women undergoing cesarean delivery[J]. J Obstet Gynaecol Res, 2011, 37(10): 1277-1282. DOI:10.1111/j.1447-0756.2010.01511.x |
| [5] |
曾义, 李杰, 段光友, 等. 再次剖宫产产后出血危险因素分析: 2442例产妇的回顾性研究[J]. 第三军医大学学报, 2019, 41(3): 265-269. ZENG Y, LI J, DUAN G Y, et al. Risk factors for postpartum hemorrhage in repeat cesarean delivery: a retrospective study of 2 442 women[J]. J Third Mil Med Univ, 2019, 41(3): 265-269. DOI:10.16016/j.1000-5404.201809015 |
| [6] |
ROUSE D J, MACPHERSON C, LANDON M, et al. Blood transfusion and cesareandelivery[J]. Obstet Gynecol, 2006, 108(4): 891-897. DOI:10.1097/01.AOG.0000236547.35234.8c |
| [7] |
SPIEGELMAN J, MOURAD M, MELKA S, et al. Risk factors for blood transfusion in patients undergoing high-order Cesarean delivery[J]. Transfusion, 2017, 57(11): 2752-2757. DOI:10.1111/trf.14274 |
| [8] |
KOUROU K, EXARCHOS T P, EXARCHOS K P, et al. Machine learning applications in cancer prognosis and prediction[J]. Comput Struct Biotechnol J, 2015, 13: 8-17. DOI:10.1016/j.csbj.2014.11.005 |
| [9] |
ZACHARAKI E I, KANAS V G, DAVATZIKOS C. Investigating machine learning techniques for MRI-based classification of brainneoplasms[J]. Int J Comput Assist Radiol Surg, 2011, 6(6): 821-828. DOI:10.1007/s11548-011-0559-3 |
| [10] |
KENDALE S, KULKARNI P, ROSENBERG A D, et al. Supervised machine-learning predictive analytics for prediction ofpostinduction hypotension[J]. Anesthesiology, 2018, 129(4): 675-688. DOI:10.1097/ALN.0000000000002374 |
| [11] |
LEE C K, HOFER I, GABEL E, et al. Development and validation of a deep neural network model for prediction of postoperative in-hospitalmortality[J]. Anesthesiology, 2018, 129(4): 649-662. DOI:10.1097/ALN.0000000000002186 |
| [12] |
LECUN Y, BENGIO Y, HINTON G. Deeplearning[J]. Nature, 2015, 521(7553): 436-444. DOI:10.1038/nature14539 |
| [13] |
BAO Y R, XU C L, QU X X, et al. Risk factors for transfusion in cesarean section deliveries at a tertiary hospital[J]. Transfusion, 2016, 56(8): 2062-2068. DOI:10.1111/trf.13671 |
| [14] |
BUTWICK A J, RAMACHANDRAN B, HEGDE P, et al. Risk factors for severe postpartum hemorrhage after cesarean delivery: case-controlstudies[J]. Anesth Analg, 2017, 125(2): 523-532. DOI:10.1213/ANE.0000000000001962 |
| [15] |
PEARSON G A, MACKENZIE I Z. Blood loss and blood transfusion at Caesarean section: a prospective observational study covering 30years[J]. Eur J Obstet Gynecol Reprod Biol, 2014, 181: 72-77. DOI:10.1016/j.ejogrb.2014.06.025 |
| [16] |
曹文哲, 应俊, 张亚慧, 等. 基于机器学习算法的前列腺癌诊断模型研究[J]. 中国医疗设备, 2016, 31(4): 30-35. CAO W Z, YING J, ZHANG Y H, et al. Diagnostic model research of prostate cancer based on machine learning algorithm[J]. China Med Devices, 2016, 31(4): 30-35. DOI:10.3969/j.issn.1674-1633.2016.04.006 |
| [17] |
GOUNDAN A, KALRA J K, RAVEENDRAN A, et al. Descriptive study of blood transfusion practices in women undergoing cesarean delivery[J]. J Obstet Gynaecol Res, 2011, 37(10): 1277-1282. DOI:10.1111/j.1447-0756.2010.01511.x |
| [18] |
GIZZO S, ZAMBON A, SACCARDI C, et al. Effective anatomical and functional status of the lower uterine segment at term: estimating the risk of uterine dehiscence byultrasound[J]. Fertil Steril, 2013, 99(2): 496-501. DOI:10.1016/j.fertnstert.2012.10.019 |
| [19] |
SHERIDAN R P, WANG W M, LIAW A, et al. Extreme gradient boosting as a method for quantitative structure-activity relationships[J]. J Chem Inf Model, 2016, 56(12): 2353-2360. DOI:10.1021/acs.jcim.6b00591 |



