原发性醛固酮增多症(primary aldosteronism,PA)是以血浆高醛固酮水平和低肾素水平为主要特征,有高血压伴(或不伴)低血钾的临床综合征。据报道超过10%的高血压患者为原发性醛固酮增多症[1], VAIDYA等[2]随访发现原醛患者较原发性高血压(essential hypertension, EH)患者的心血管事件(包括房颤、心肌梗死、心源性卒中及左室增大等)风险明显增高。2016年美国PA诊治指南[3]推荐血浆醛固酮浓度/血浆肾素活性比值(ratio of aldosterone/plasma rennin activity, ARR)的筛查是判断PA的第一步,给出以EH人群作为对照组的筛查切点, 并提出可能需要联合ARR和血浆醛固酮浓度(plasma aldosterone concentration,PAC)的指标,但没有明确其敏感性、特异性和诊断价值。目前血浆醛固酮与肾素水平的检测主要有化学发光法(chemilumininescent immunoassay,CLIA)和放射免疫法(radioimmunoassay,RIA)。有关两种方法的优劣比较时有报道,但结论不一,在相关指南上也未介绍两种方法的差异。基于上述,本研究选取PA患者60例,EH患者82例及健康受试者114例, 应用CLIA和RIA对同一受试对象分别测量PAC和直接肾素浓度(direct renin concentration,DRC)/血浆肾素活性(plasma renin activity,PRA),比较其对PA的筛查价值,并分析其筛查PA的最佳联合指标及诊断切点。
1 资料与方法 1.1 研究对象本研究为横断面研究,选取2018年1-10月在陆军特色医学中心高血压内分泌科就诊的60例确诊PA患者(PA组)的临床资料,其中单侧腺瘤或结节34例、双侧腺瘤或结节4例、单侧肾上腺增粗8例、双侧肾上腺增粗6例、影像学无异常8例。原醛的纳入条件(①~②为必备条件):①有高血压和/或低血钾的临床表现;②满足一项确诊试验阳性;如肾素受抑制,醛固酮>20 ng/L (200 pg/mL),可不行确诊试验[4];③影像学提示单侧/双侧肾上腺增生或腺瘤,或术后病理证实;④分侧肾上腺静脉取血术(adrenal vein sampling,AVS)结果提示存在优势分泌(48例)或双侧高分泌(12例)。纳入基线资料匹配的EH患者82例(EH组),排除继发性高血压(肾实质损害、肾动脉狭窄、原发性醛固酮增多症、库欣综合征、主动脉缩窄、阻塞性睡眠呼吸暂停低通气综合征等)及存在严重心肾功能衰竭的患者。同期招募健康受试者114例作为对照组,在试验前需要所有健康受试者同意并签署知情同意书,入选标准:①与PA组在年龄、性别、身高、体质量、体质量指数等基线资料匹配;②平静状态下于不同时间点规范测量3次血压,血压均<140/90 mmHg;③除外肝肾功能不全、心脑血管疾病、内分泌疾病、大血管病变等;④除外1个月内有特殊用药史(包括降压药、非甾体类抗炎药、甘草制剂及外源性激素等);⑤排除处于月经期、孕期女性。
1.2 方法所有受试者在采集血液标本之前需要先纠正低钾血症(使血钾>3.5 mmol/L);正常饮食状态;检查前停用利尿剂、醛固酮受体拮抗剂2~4周,停用β阻滞剂、可乐定、非甾体类抗炎药、二氢吡啶类钙阻滞剂、血管紧张素转化酶抑制剂和血管紧张素受体拮抗剂2周;本研究在试验日上午7:00至10:00之间,空腹采集血液标本,要求受试者站立2 h后静坐15 min,收集于EDTA抗凝采血管,检测PRA用4 ℃冰箱冷藏试管采集标本,立即送往实验室进行离心,所有检测均在标本采集当天完成[5]。
1.3 检测原理RIA应用西安核仪器厂放射免疫计数仪,及北京北方生物技术研究所提供的试剂盒,PRA检测批内变异<10%,批间变异<15%;PAC检测批内变异<10%,批间变异<15%。检测PAC和PRA,并由此浓度值计算ARR。测定原理为:测量单位时间内由血管紧张素原转化为血管紧张素Ⅰ(angiotensin Ⅰ,AngⅠ)的速率可以反映PRA,将采集的血液标本分成两份,其中一份在37 ℃温育一段时间后与兔抗-AngⅠ抗体反应,另一份则在4 ℃直接与抗体反应作为对照,计算单位时间AngⅠ的产生速率[ng/(dL·h)]。RIA检测PAC依据均相竞争原理,利用放射碘标记法检测样本中醛固酮含量(ng/dL)[6]。
CLIA应用意大利索灵公司全自动化学免疫分析仪计数仪,及意大利DIASORIN,LIAISON醛固酮测定及肾素测定试剂盒,DRC检测批内变异<2.58%~4.87%,批间变异<7.01%~13.03%;PAC检测批内变异<1.8%~4.2%,批间变异<5.6%~10.5%。检测PAC利用绵羊单克隆抗体竞争性捕获醛固酮分子反映血浆醛固酮浓度(pg/mL),而DRC则是通过特异性鼠单克隆抗体和异鲁米诺抗体结合物测得[7]。
1.4 确诊试验本研究选取临床常用的两种确诊试验:①生理盐水输注试验:试验前受试者在安静状态下卧床休息1 h,随后4 h内匀速静滴2 L 0.9%生理盐水, 试验在早上8:00-9:00开始,整个过程需监测血压和心率变化,在输注前及输注后分别采血测血浆肾素、醛固酮及血钾。生理盐水试验负荷后血醛固酮>10 ng/dL,原醛诊断明确,< ng/dL排除PA[8]。②卡托普利抑制试验:坐位或站位1 h后口服50 mg卡托普利, 服药前及服用后1、2 h测定血浆肾素、醛固酮, 试验期间患者需始终保持同一体位,正常人卡托普利抑制试验后血醛固酮浓度下降超过30%, 而原醛患者血醛固酮不受抑制[9]。生理盐水输注试验对血压无严格要求,但如有高血压急症或亚急症,充血性心力衰竭的情况优先采用卡托普利抑制试验。
1.5 统计学方法应用SPSS 20.0软件和Graphpad prism 5软件进行统计分析。正态分布的计量资料以x±s表示,组间比较采用单因素方差分析;偏态资料分布以M(P25~P75)表示,组间比较采用非参数检验。变量的相关性比较用Pearson相关性分析。采用ROC曲线分析,当曲线下面积(area under the cure,AUC)大于0.5时相关指标被认为有诊断价值。
2 结果 2.1 临床及生化结果比较3组人群的性别、年龄、体质量指数、血肌酐值无统计学差异。对比对照组,PA组和EH组的收缩压、舒张压明显较高(P < 0.001),而PA组血钾明显低于对照组和EH组(P < 0.001,表 1)。
| 组别 | n | 男/女(例) | 年龄/岁 | BMI/kg·m-2 | 收缩压/mmHg | 舒张压/mmHg | 血钾/mol·L-1 | 血肌酐/mol·L-1 |
| 对照组 | 114 | 44/70 | 46±12 | 24.4±3.2 | 115±14 | 79±9 | 4.1±0.3 | 68.9±13.1 |
| 原发性醛固酮增多症组 | 60 | 32/28 | 50±11 | 24.4±3.1 | 145±20a | 88±11a | 3.5±0.5a | 70.0±19.4 |
| 原发性高血压组 | 82 | 41/41 | 50±11 | 24.9±3.4 | 150±24a | 92±17a | 4.0±0.4b | 66.6±17.6 |
| a:P < 0.001,与对照组比较;b:P < 0.001,与原发性醛固酮增多症组比较 | ||||||||
2.2 两种方法检测指标比较
CLIA中PA患者的PAC显著高于对照组(P < 0.001);EH组与对照组的PAC也有统计学差异(P < 0.001)。PA组DRC水平处于抑制状态,明显低于对照组和EH组(P < 0.001)。RIA测得PAC在3组间无统计学差异(P=0.764)。PA组的PRA显著低于对照组和EH组(P < 0.001,表 2)。
| 组别 | n | 血浆醛固酮浓度(化学发光法)/pg·mL-1 | 血浆直接肾素浓度/μIU·mL-1 | 血浆醛固酮浓度/血浆直接肾素浓度[(pg· mL-1)/(μIU·mL-1)] | 血浆醛固酮浓度(放射免疫法) /ng·dL-1 | 血浆肾素活性/ ng·mL-1·h-1 | 血浆醛固酮浓度/血浆肾素活性[(ng·dL-1)/(mg·mL-1·h-1)] |
| 对照组 | 114 | 80.20(60.58~108.50) | 16.22(6.61~29.80) | 6(3~11) | 19(16~21) | 2.16(0.95~3.35) | 7.5(5~20) |
| 原发性醛固酮增多症组 | 60 | 167(110.30~326.00)a | 2.86(0.76~6.09)a | 64(25~198)a | 19(13~24) | 0.51(0.10~0.95)a | 45(17~175)a |
| 原发性高血压组 | 82 | 123(99.75~148.30)ab | 20.8(9.46~35.90)b | 7(3~13)b | 17.5(15~21) | 2.15(0.92~4.01)b | 7(4~22)b |
| a:P < 0.001, 与对照组比较;b:P < 0.01,与原发性醛固酮症增多症组比较 | |||||||
2.3 两种方法的相关性
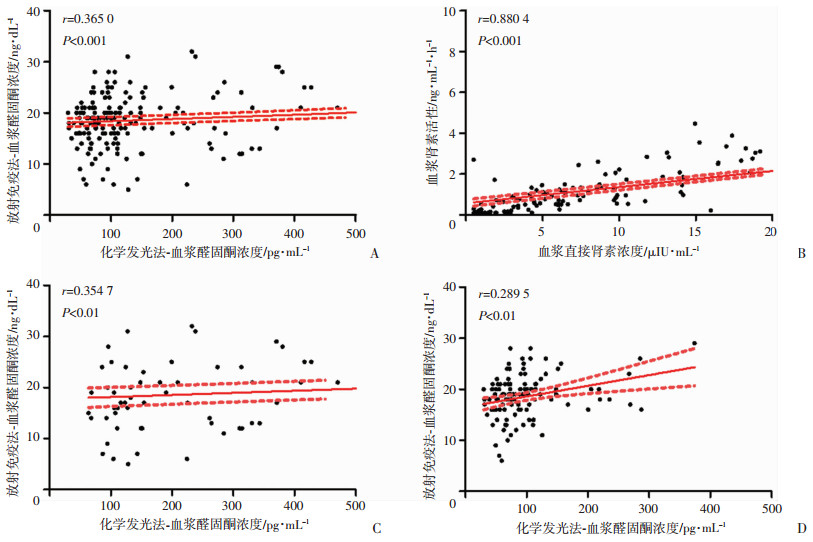
以对照组为对照分析两种方法的相关性,DRC与PRA具有很好的相关性(P < 0.01,r=0.880 4),两种方法检测的PAC也显著相关,但相关度偏低(r=0.365,P < 0.001)。两组间比较提示,PA组两种方法检测醛固酮浓度的相关性要优于对照组[(r=0.354 7,P=0.005) vs (r=0.289 5,P=0.002),图 1]。
|
| A:两种方法测量醛固酮浓度;B:血浆肾素浓度和血浆肾素活性;C:原发性醛固酮增多症组内两种方法测量醛固酮浓度;D:对照组内两种方法测量醛固酮浓度 图 1 化学发光法和放射免疫法的相关性分析 |
2.4 筛查原发性醛固酮增多症的指标联合和诊断切点
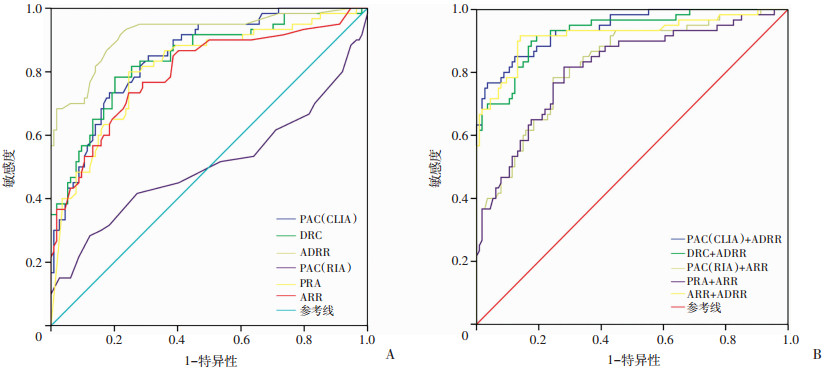
以PAC、DRC/PRA、ADRR、ARR及两两联合指标为检验变量,定义对照组状态变量为0,PA组为1,完成ROC曲线制作。切点值取曲线最左上方的点,此时敏感性和特异性之和最大,ADRR和ARR的切点值分别为12(pg· mL-1)/(μIU·mL-1)、20(ng·dL-1)/(ng·mL-1·h-1)。比较ROC曲线下面积,ADRR、ADRR联合DRC、ADRR联合PAC(CLIA)、ADRR联合ARR的AUC最大(P < 0.01), 分别为0.920、0.928、0.939、0.920,敏感性分别为91.53%、89.83%、76.27%和91.38%,特异性分别为78.07%、83.33%、96.49%和86.24%,约登指数分别为0.696、0.732、0.728和0.776。在诊断价值最优的前提下,筛查原发性醛固酮增多症的单一ADRR指标敏感性最高,ADRR联合PAC(CLIA)的特异性最高(表 3、图 2)。
| 项目 | 曲线下面积 | P | 95%CI | 敏感性 | 特异性 | 约登指数 | 切点值 |
| ADRR | 0.920 | < 0.001 | 0.869-0.956 | 91.53 | 78.07 | 0.696 | 12 |
| PAC(CLIA) | 0.848 | < 0.001 | 0.786-0.898 | 73.33 | 81.58 | 0.545 | 115 |
| DRC | 0.840 | < 0.001 | 0.777-0.891 | 78.33 | 79.82 | 0.582 | 6.11 |
| ARR | 0.798 | < 0.001 | 0.731-0.855 | 73.33 | 75.44 | 0.487 | 20 |
| PAC(RIA) | 0.505 | 0.930 | 0.428-0.581 | 28.33 | 87.72 | 0.161 | 23 |
| PRA | 0.811 | < 0.001 | 0.745-0.866 | 80.00 | 75.44 | 0.554 | 0.96 |
| PAC+ADRR (CLIA) | 0.939 | < 0.001 | 0.892-0.970 | 76.27 | 96.49 | 0.728 | 0.43 |
| DRC+ADRR | 0.928 | < 0.001 | 0.879-0.962 | 89.83 | 83.33 | 0.732 | 0.17 |
| PAC+ARR(RIA) | 0.822 | < 0.001 | 0.755-0.877 | 86.21 | 66.97 | 0.532 | 0.22 |
| PRA+ARR | 0.812 | < 0.001 | 0.744-0.868 | 77.59 | 74.31 | 0.519 | 0.31 |
| ARR+ADRR | 0.920 | < 0.001 | 0.868-0.956 | 91.38 | 86.24 | 0.776 | 0.19 |
| PAC:血浆醛固酮浓度;DRC:直接肾素浓度;PRA:血浆肾素活性;ARR:血浆醛固酮/肾素活性比值;ADRR:血浆醛固酮/直接肾素浓度比值;CLIA:化学放光法;RIA:放射免疫法 | |||||||
|
| A:单一诊断指标;B:联合诊断指标 图 2 单一指标与联合指标筛查原发性醛固酮增多症的ROC曲线图 |
3 讨论
美国原发性醛固酮增多症诊治指南推荐筛查试验是PA诊断流程的第一步, 目前检测相关指标的方法主要有RIA和CLIA。RIA较为成熟,但操作繁琐耗时,肾素和醛固酮需要分开测量,且稳定性和重复性不如CLIA;CLIA具有方便、快捷等优势,但不如RIA普及。
诸多国外研究如GLINICKI等[10]证实ADRR与ARR的相关性较好,两种检测技术可以相互替代,国内一些单位[11-12]进一步验证了该结论,而本研究得出两种方法检测醛固酮水平的相关性欠佳。因ARR的切点值与梁霞等[13]的报道是相符合的,可以排除实验条件和技术问题导致的误差,结论相悖的主要原因是不同厂家提供的RIA试剂盒检测PAC的准确性存在差异。国内提供RIA试剂盒的厂家有限,其质量也逊于进口试剂盒,基于成本限制、进口审批及CLIA尚未普及等因素,目前国内大部分医院仍在应用RIA, 试剂盒提供方以北京北方生物技术研究所为主,我们认为在严格控制检测方法情况下,其结果对临床诊治仍有参考意义。
根据厂家提供的试剂盒参考值资料,CLIA测量醛固酮值的参考范围大于RIA,分别为30~392 ng/dL,65~296 ng/dL,提示CLIA灵敏度更佳。RIA测量PAC的检测范围在63~2 000 ng/dL,而CLIA为30~1 000 ng/dL,波动幅度大于参考范围,因此PA组中醛固酮相关性较优于对照组。
国内外指南建议原醛的ARR筛查切点在20~40(ng·dL-1)/(ng·mL-1·h-1)之间。2008年美国原醛症指南建议的ADRR切点值为37(pg·mL-1)/(μIU·mL-1),ARR切点值为30(ng·dL-1)/(ng·mL-1·h-1), 而本研究的ADRR切点值为12(pg·mL-1)/(μIU·mL-1),ARR切点值为20(ng·dL-1)/(ng·mL-1·h-1)。分析可能的影响因素如下:①年龄:MA等[14]根据年龄分层建立不同的ADRR筛查切点值,年龄≥60岁时ADRR以37(pg·mL-1)/(μIU·mL-1)敏感性与特异性最佳,而年龄<60岁的人群ADRR为20(pg·mL-1)/ (μIU·mL-1)敏感性、特异性最佳。本研究PA组的平均年龄为50岁,ADRR<20(pg·mL-1)/(μIU·mL-1)更合理。②亚临床原发性醛固酮增多症:NANBA等[15]研究表明在部分高醛固酮水平的EH患者的肾上腺组织中已存在高表达醛固酮合成酶(CYP11B2)的异常细胞集(aldosterone-producing cell clusters,APCCs),有可能是PA早期的病理生理改变, 这部分人群可能是隐匿性原发性醛固酮增多症或原发性醛固酮增多症亚临床期。目前关于PA筛查切点的研究多以EH作为阴性对照组,有可能导致切点值偏高,在实际临床工作中若参照指南给出的筛查切点,可以发现这部分患者往往具有典型的临床表现,一些醛固酮水平不高、低钾血症不明显的患者容易被漏诊或误诊。③其他:人群的种族差异、检测仪器等因素对结果的判断影响也较大。因此,建立各地区的筛查标准对原醛的诊断甚为重要。此外,单一的筛查指标敏感性较高,特异性欠佳,为提高筛查诊断效率,指南提出筛查结果的判断可能需要联合ARR和PAC。王芳等[16]也提出ADRR联合ARR可提高筛查指标的诊断价值。本研究通过ROC曲线图分析显示在各项联合指标中,ADRR联合PAC(CLIA)的特异性和诊断价值最佳。
本研究的创新点:①纳入健康人群为对照,以EH对照有可能纳入部分PA症状不典型或亚临床期人群从而导致切点值偏高;②考虑了年龄因素对切点值的影响,结论更符合疾病人群特征,基于PA好发于中老年人群(40~50岁),ADRR切点值为20~30(pg·mL-1)/(μIU·mL-1),而本研究人群的平均年龄 < 50岁,得出ADRR切点值为12 (pg·mL-1)/(μIU·mL-1); ③国外PA指南已提出可能需要联合ARR和PAC的指标,但缺乏相关临床研究,本研究得出在诊断价值最优的前提下,联合ADRR和PAC(CLIA)可以显著提高诊断特异性,进一步证实了指南的建议。本研究的不足之处:限于PA人群样本量,没有进一步区分特发性醛固酮增多症和肾上腺腺瘤的切点值,此外目前关于特发性醛固酮增多症的定义观点不一,临床指南推荐的PA分型主要基于影像学结论,但随着AVS技术的发展,PA的分型必将需要联合影像学和AVS结果综合判断[17]。
综上所述,化学发光法的诊断准确性和敏感性优于放射免疫法,优先推荐以ADRR指标进行原发性醛固酮增多症的筛查,必要时可以联合化学发光法测得的PAC进一步提高特异性。
| [1] |
MONTICONE S, BURRELLO J, TIZZANI D, et al. Prevalence and clinical manifestations of primary aldosteronism encountered in primary care practice[J]. J Am Coll Cardiol, 2017, 69(14): 1811-1820. DOI:10.1016/j.jacc.2017.01.052 |
| [2] |
VAIDYA A, MULATERO P, BAUDRAND R, et al. The expanding spectrum of primary aldosteronism: implications for diagnosis, pathogenesis, and treatment[J]. Endocr Rev, 2018, 39(6): 1057-1088. DOI:10.1210/er.2018-00139 |
| [3] |
FUNDER J W, CAREY R M, MANTERO F, et al. The management of primary aldosteronism: case detection, diagnosis, and treatment: an endocrine society clinical practice guideline[J]. J Clin Endocrinol Metab, 2016, 101(5): 1889-1916. DOI:10.1210/jc.2015-4061 |
| [4] |
NANBA K, TAMANAHA T, NAKAO K, et al. Confirmatory testing in primary aldosteronism[J]. J Clin Endocrinol Metab, 2012, 97(5): 1688-1694. DOI:10.1210/jc.2011-2504 |
| [5] |
BURRELLO J, MONTICONE S, BUFFOLO F, et al. Diagnostic accuracy of aldosterone and renin measurement by chemiluminescent immunoassay and radioimmunoassay in primary aldosteronism[J]. J Hypertens, 2016, 34(5): 920-927. DOI:10.1097/HJH.0000000000000880 |
| [6] |
SEALEY J E, GORDON R D, MANTERO F. Plasma renin and aldosterone measurements in low renin hypertensive states[J]. Trends Endocrinol Metab, 2005, 16(3): 86-91. DOI:10.1016/j.tem.2005.02.006 |
| [7] |
ROSSI G P, CEOLOTTO G, ROSSITTO G, et al. Prospective validation of an automated chemiluminescence-based assay of renin and aldosterone for the work-up of arterial hypertension[J]. Clin Chem Lab Med, 2016, 54(9): 1441-1450. DOI:10.1515/cclm-2015-1094 |
| [8] |
AHMED A H, COWLEY D, WOLLEY M, et al. Seated saline suppression testing for the diagnosis of primary aldosteronism: a preliminary study[J]. J Clin Endocrinol Metab, 2014, 99(8): 2745-2753. DOI:10.1210/jc.2014-1153 |
| [9] |
SONG Y, YANG S M, HE W W, et al. Confirmatory tests for the diagnosis of primary aldosteronism: A prospective diagnostic accuracy study[J]. Hypertension, 2018, 71(1): 118-124. DOI:10.1161/HYPERTENSIONAHA.117.10197 |
| [10] |
GLINICKI P, JESKE W, BEDNAREK-PAPIERSKA L, et al. The ratios of aldosterone / plasma renin activity (ARR) versus aldosterone / direct renin concentration (ADRR)[J]. J Renin Angiotensin Aldosterone Syst, 2015, 16(4): 1298-1305. DOI:10.1177/1470320313519487 |
| [11] |
孙明芳, 杨珊, 何小群, 等. 基于血浆醛固酮/肾素浓度比的联合策略在原发性醛固酮增多症中的筛查价值[J]. 军事医学, 2015, 39(4): 279-283. SUN M F, YANG S, HE X Q, et al. Value of combination strategy based on plasma aldosterone / renin concentration ratio in screening of primary aldosteronism[J]. Mil Med Sci, 2015, 39(4): 279-283. DOI:10.7644/j.issn.1674-9960.2015.04.011 |
| [12] |
赖凤华, 曹筱佩, 林慧美, 等. 两种血浆肾素、醛固酮检测方法对原发性醛固酮增多症筛查效率的评价[J]. 中华高血压杂志, 2015, 23(2): 150-153. LAI F H, CAO X P, LIN H M, et al. Comparison of plasma renin and aldosterone measured by radioimmunoassay and chemiluminescence immunoassay in screening primary aldosteronism[J]. Chin J Hypertens, 2015, 23(2): 150-153. DOI:10.16439/j.cnki.1673-7245.2015.02.020 |
| [13] |
梁霞, 王小静, 余文珮, 等. 原发性醛固酮增多症诊断切点的研究及临床应用[J]. 第三军医大学学报, 2015, 37(11): 1146-1149. LIANG X, WANG X J, YU W P, et al. Determination of optimal cut-off point for primary aldosteronism and its diagnostic value in clinical practice[J]. J Third Mil Med Univ, 2015, 37(11): 1146-1149. DOI:10.16016/j.1000-5404.201501193 |
| [14] |
MA L Q, SONG Y, MEI M, et al. Age-related cutoffs of plasma aldosterone/renin concentration for primary aldosteronism screening[J]. Int J Endocrinol, 2018, 2018: 8647026. DOI:10.1155/2018/8647026 |
| [15] |
NANBA K, VAIDYA A, WILLIAMS G H, et al. Age-related autonomous aldosteronism[J]. Circulation, 2017, 136(4): 347-355. DOI:10.1161/CIRCULATIONAHA.117.028201 |
| [16] |
王芳, 马文君, 丛洪瀛, 等. 化学发光法测定血浆醛固酮和肾素浓度的参考区间及筛查原发性醛固酮增多症的价值[J]. 中国分子心脏病学杂志, 2017, 17(1): 1970-1973. WANG F, MA W J, CONG H Y, et al. The reference interval of plasma aldosterone and renin concentration detected by chemiluminescence immunoassay and the performance evaluation in screening primary aldosteronism[J]. Mol Cardiol China, 2017, 17(1): 1970-1973. DOI:10.16563/j.cnki.1671-6272.2017.02.007 |
| [17] |
LENDERS J W M, EISENHOFER G, REINCKE M. Subtyping of patients with primary aldosteronism: an update[J]. Horm Et Metab, 2017, 49(12): 922-928. DOI:10.1055/s-0043-122602 |



