主动脉穿透性溃疡是指动脉内膜和弹力纤维发生破裂,破裂可直至动脉中膜的病理状态。主动脉穿透性溃疡可以继续进展为主动脉壁间血肿或主动脉夹层,亦可形成主动脉假性动脉瘤或直接发生破裂。据文献报道,有症状的主动脉穿透性溃疡发生破裂的风险甚至高于主动脉夹层的破裂风险,其破裂率可达38%[1]。胸主动脉穿透性溃疡发生率高于腹主动脉[2]。自血管腔内治疗首次被应用于胸主动脉穿透性溃疡的治疗以来[3],其相对传统开放手术而言,并发症发生率和死亡率均明显下降[4-6]。由于主动脉穿透性溃疡的发病率相对较低,目前对于主动脉穿透性溃疡的治疗建议是基于发病率更高的主动脉夹层推断而来,其治疗存在一定争议[7]。本研究旨在通过回顾胸主动脉腔内隔绝术在胸主动脉穿透性溃疡的应用,分析其安全性和有效性,对其适应证的选择、手术设计提供理论依据。
1 资料与方法 1.1 临床资料收集我科2018年10月至2019年5月收治的胸主动脉穿透性溃疡患者的临床和随访资料。纳入标准:①影像学检查结果提示胸主动脉穿透性溃疡的患者,包括主动脉弓穿透性溃疡、胸降主动脉穿透性溃疡;②术前有全主动脉CTA影像学资料;③排除手术禁忌证后在我科行血管腔内治疗。排除标准:①升主动脉及腹主动脉穿透性溃疡的患者;②单纯主动脉壁间血肿患者;③患者主动脉穿透性溃疡并发其他主动脉疾病(如主动脉瘤),符合其他主动脉疾病诊断标准的患者;④拒绝行相关腔内治疗的患者。所有入组患者或患者指定的代理家属术前均签署手术知情同意书。
1.2 术前准备及术前评估所有患者入院后均严格控制血压和心率,以口服药物为主(如硝苯地平、美托洛尔、卡托普利等)。若口服药物血压控制欠佳,则增加静脉降压药物(如乌拉地尔)。若患者存在胸痛或腹痛,排除其他原因所致的疼痛后,必要时给予止痛药(如帕瑞昔布等)。所有患者入院后均完善全主动脉CTA检查,并进行三维重建。在三维重建影像中使用正交平面图像(orthogonal images)进行测量主动脉解剖学参数[8],所有患者均测量主动脉管壁外径。
1.3 手术方法 1.3.1 主动脉弓穿透性溃疡患者在DSA下采取平卧位,局部麻醉后使用改良Seldinger穿刺法穿刺右侧股动脉,置入8F导管鞘,在导丝引导下引入造影导管至穿透性溃疡近心端,对于主动脉弓穿透性溃疡患者需明确弓上三分支位置,采取左前斜45°造影。造影明确在胸主动脉腔内隔绝术中需重建左锁骨下动脉的患者,局部麻醉左侧肘内侧后使用改良Seldinger穿刺法穿刺左侧肱动脉,置入8F导管鞘或10F导管鞘,使用烟囱技术或开窗技术重建左锁骨下动脉。
1.3.2 胸降主动脉穿透性溃疡穿刺方法同1.3.1。穿透性溃疡患者结合术前影像学检查结果,采取最佳暴露角度调整DSA机头角度后造影。造影明确病变部位及重要分支动脉开口位置。结合术前测量结果选择合适的主动脉腔内移植物,腔内移植物近端锚定区定位于主动脉穿透性溃疡近心端2 cm处。对于病变较短者,可选择短段覆膜主动脉腔内移植物进行治疗,对于病变较长者,使用胸主动脉腔内移植物进行治疗。
1.3.3 主动脉腔内移植物选择结合术前测量结果选择合适的主动脉腔内移植物,腔内移植物近端锚定区定位于主动脉穿透性溃疡近心端2 cm处,完全遮蔽主动脉穿透性溃疡并向远端至少覆盖2 cm,若主动脉穿透性溃疡两端斑块较多,腔内移植物锚定区距离斑块2 cm。主动脉腔内移植物放大率选择5%~10%。
1.4 随访随访方案为,手术后第1、3、6个月和每年进行CTA检查和三维重建。评价主动脉穿透性溃疡隔绝情况,主动脉穿透性溃疡血栓化情况,以及主动脉腔内移植物锚定区主动脉管径变化。对于行左锁骨下动脉烟囱支架植入的患者,评价其双上肢血压情况。对有不良反应症状(胸痛、腹痛)或体征的患者需进行急诊CTA检查。所有随访工作均由血管外科医师完成。
2 结果2018年10月至2019年5月共有12例患者诊断(含影像学诊断)中包含主动脉溃疡,其中7例患者诊断为胸主动脉穿透性溃疡并行手术治疗。有1例诊断为腹主动脉溃疡伴壁间血肿,另有3例为诊断为腹主动脉瘤伴动脉穿透性溃疡行血管腔内治疗,1例患者拒绝手术治疗,均排除出本研究。共7例患者纳入本研究。
纳入研究的7名患者的一般情况见表 1。2例(28.6%)患者表现为胸痛,另5例患者无明显疼痛,由其他疾病行检查发现主动脉穿透性溃疡。患者术前影像学测量的解剖学参数及手术情况见表 2。病变位于主动脉弓3例,位于胸降主动脉4例。主动脉穿透性溃疡深度为(6.00±2.02) mm,宽度为(12.07±5.26) mm,长度为(14.71±9.05) mm。最大溃疡处主动脉直径(30.28±4.27) mm,主动脉近端锚定区直径(31.14±4.26) mm。主动脉腔内移植物直径(33.57±3.64) mm,主动脉腔内移植物长度(172.00±45.31) mm。主动脉腔内移植物放大率为(8.22±4.07)%。手术时间为(90.00±32.53) min。其中3例进行左锁骨下动脉烟囱支架植入。
| 临床资料 | 数据 |
| 男性/例数 | 6(85.7) |
| 年龄/岁 | 70.29±7.54 |
| 症状/例数 | 2(28.6) |
| 高血压病程/年 | 13.71±7.67 |
| 高血压分级/例数 | |
| 高血压1级 | 0 |
| 高血压2级 | 2(28.6) |
| 高血压3级 | 5(71.4) |
| 冠心病/例数 | 4(57.1) |
| 2型糖尿病/例数 | 2(28.6) |
| 吸烟/例数 | 6(85.7) |
| 吸烟指数/年支 | 721.42±599.90 |
| 术前住院天数/d | 2.71±2.21 |
| 术后住院天数/d | 3.57±0.78 |
| 临床资料 | 数据 |
| 病变部位例数/例数 | |
| 主动脉弓 | 3(42.9) |
| 降主动脉 | 4(57.1) |
| 溃疡个数/个 | 2.00±1.15 |
| 最大溃疡深度/mm | 6.00±2.02 |
| 最大溃疡宽度/mm | 12.07±5.26 |
| 最大溃疡长度/mm | 14.71±9.05 |
| 最大溃疡处主动脉直径/mm | 30.28±4.27 |
| 主动脉近端锚定区直径/mm | 31.14±4.26 |
| 主动脉腔内移植物直径/mm | 33.57±3.64 |
| 近端放大率/% | 8.22±4.07 |
| 主动脉腔内移植物长度/mm | 172.00±45.31 |
| 分支支架例数/例数(%) | 3(42.9) |
| 手术时间/min | 90.00±32.53 |
截止时间2019年6月,随访1~7个月。1例患者无影像学随访结果,电话随访患者一般情况良好,无胸痛等特殊不适。另6例患者随访CTA提示主动脉穿透性溃疡均隔绝良好,溃疡局部均完全血栓化,无各型内漏发生。近端锚定区主动脉直径为(33.33±2.80) mm (n=6)。3例进行左锁骨下动脉烟囱支架植入的患者中,1例出现左锁骨下烟囱支架内血栓形成,但患者无明显左上肢缺血、左锁骨下动脉盗血等症状,左上肢较右上肢收缩压约低40 mmHg,舒张压约低25 mmHg,予以继续随访观察。另2例左锁骨下烟囱支架通畅,患者双上肢血压无明显差异。在住院及随访期间,无截瘫、脑梗等并发症出现。随访期间无移植物近远端夹层等主动脉腔内移植物相关并发症发生,见图 1。
|
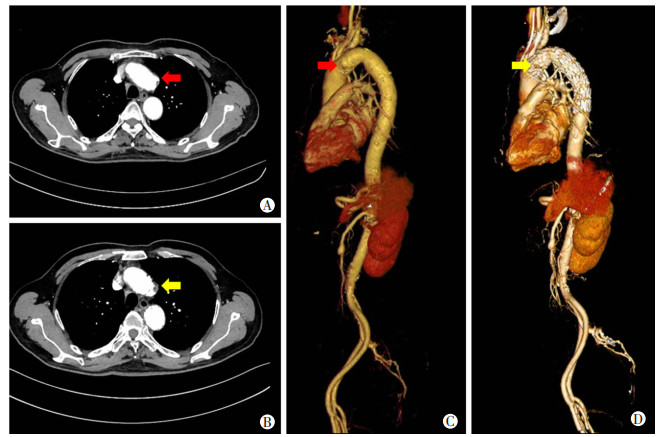
| A:主动脉弓溃疡术前CTA横断面,红色箭头示主动脉弓溃疡;B:主动脉弓溃疡腔内隔绝术术后CTA横断面,黄色箭头示主动脉弓溃疡已血栓化;C:主动脉弓溃疡术前全主动脉CTA三维重建,红色箭头示主动脉弓溃疡;D:主动脉弓溃疡术后全主动脉CTA三维重建,黄色箭头示主动脉弓溃疡已血栓化。 图 1 胸主动脉腔内隔绝术治疗胸主动脉穿透性溃疡手术前后影像学表现 |
3 讨论
主动脉穿透性溃疡、主动脉壁间血肿以及主动脉夹层并称为急性主动脉综合征(acute aortic syndrome, AAS),其主要特征表现为主动脉管壁不同程度的破裂[9-10]。有研究认为这三种疾病可以作为孤立的疾病发生,亦可作为疾病的不同阶段而相互关联[11],但亦有研究认为这三者有截然不同的发病过程和自然规律,将三者完全归为一类容易引起误解[12-13]。
主动脉穿透性溃疡发生是由动脉粥样硬化斑块的侵蚀和主动脉壁的炎症所引起[14-15],发生率约占急性主动脉综合征的2%~7%[16-17],但随着影像学技术的进步普及,其发现率逐渐升高。许多主动脉穿透性溃疡患者由于其他疾病进行增强CT检查而被筛选出来,在本研究中,共有5例患者是由于其他疾病进行检查而发现主动脉穿透性溃疡,而其中1例患者因肝脏占位需在完成胸主动脉腔内隔绝术后行外科手术切除肝脏病变。对于这类患者,积极治疗主动脉溃疡,有助于避免其外科手术围手术期严重不良事件的发生。
主动脉穿透性溃疡可进展为假性动脉瘤或发生破裂[18-19],抑或是进一步导致血液进入主动脉管壁而造成主动脉壁间血肿[20-22],而主动脉壁间血肿的患者中有近半数会继续进展为主动脉夹层或发生破裂[18, 23]。还有研究指出主动脉穿透性溃疡患者发生下肢动脉血栓栓塞发生率增加[24],但尚不能明确造成栓塞的栓子是否来源于主动脉穿透性溃疡[25]。
由于主动脉穿透性溃疡由于常常发生在钙化严重的粥样硬化的主动脉之上,发生主动脉穿透性溃疡的动脉硬化往往严重于主动脉夹层或主动脉壁间血肿的患者[26]。有学者提出主动脉的钙化和瘢痕会限制了血管管壁继续撕裂,在一定程度上可以使溃疡保持局限性[13]。我们认为正是由于主动脉粥样硬化形成的钙化和瘢痕导致主动脉管壁失去正常的力学性能和完整性,更容易导致溃疡的进一步发展。所以对于伴严重的主动脉钙化或是多发主动脉穿透性溃疡的患者,更应积极采取治疗措施。
与主动脉夹层好发于升主动脉不同的是,主动脉穿透性溃疡和主动脉壁间血肿均好发于降主动脉[2, 20, 27]。主动脉穿透性溃疡发生于升主动脉较为罕见。NATHAN等[2]分析了315例主动脉穿透性溃疡患者资料,其中溃疡位于在胸降主动脉占62%,溃疡位于在腹主动脉占31%,溃疡位于主动脉弓占7%[2],发生在胸主动脉的主动脉穿透性溃疡22.8%有症状,而发生在腹主动脉的主动脉穿透性溃疡6.7%有症状。而腹主动脉溃疡发生于肾动脉水平以下更为常见[25]。
由于主动脉穿透性溃疡病变往往局限,仅累及主动脉管壁的一小部分,且往往发生在高龄及并发症较多的患者中,因此,只有患者条件允许,血管腔内治疗是这类患者的第一线治疗[11]。而血管腔内治疗技术目前已广泛应用于降主动脉和腹主动脉疾病,为避免主动脉穿透性溃疡造成更严重的并发症,可在掌握好指征的情况下将血管腔内治疗技术应用在主动脉穿透性溃疡的治疗中。在2017年欧洲血管外科学会胸主动脉疾病管理指南中也建议复杂的B型主动脉穿透性溃疡或壁间血肿应考虑血管内修复[28]。由于血管腔内技术的进步,在指南中对于胸主动脉穿透性溃疡已无开放手术的推荐,在近年来的临床实践中亦无开放手术治疗主动脉穿透性溃疡的报道。
最初将血管腔内治疗应用于主动脉穿透性溃疡的结果均较为理想,手术成功率可达92%~100%[5, 29-30]。目前对于血管腔内治疗的主动脉穿透性溃疡患者的回顾性研究中,单中心病最大病例数为72例,在该研究中住院期间死亡率为4%,内漏发生率为6.7%,1年、5年以及10年的生存率分别为93%、72%以及60%[31]。在一项Meta分析中发现,310名进行血管腔内治疗的主动脉穿透性溃疡患者的手术成功率为98.3%,30 d死亡率为4.8%,1年生存率为91.1%,各型内漏是血管腔内治疗应用于主动脉穿透性溃疡后较为多见的并发症,其发生率可达8%[32]。在本研究中,手术成功率100%,30 d内无1例死亡,在随访阶段未发现各型内漏的出现,这些数据所展现的进步与对于疾病的认识和支架构型的改进密切相关,但由于随访时间较短,仍需在随访期间严密观察患者有无内漏等情况发生。
D’ANNOVILLE等[32]认为对于主动脉穿透性溃疡的手术指征为:持续或再发的症状,溃疡处主动脉直径>55 mm或每年增大超过10 mm,合并其他主动脉疾病等。GANAHA等[18]认为对于无症状主动脉穿透性溃疡可根据其形态学参数决定是否进行早期干预,若溃疡直径>0.2 mm或其颈部>0.1 mm,代表溃疡有更高的进展风险,即使无症状也建议可以早期干预。我们认为,对于主动脉穿透性溃疡的手术指征绝不能单纯照搬主动脉瘤或主动脉夹层的手术指征,溃疡的形态学参数可作为参考,但对于手术指征更应结合患者的一般情况、主动脉穿透性溃疡的部位(如左锁骨下动脉水平溃疡更易受血流冲击影响)、溃疡的形态学参数、患者基础疾病(高血压等)以及其他需要干预(如手术、内镜检查等)的疾病多方面因素进行整体把控。
对于需要进行腔内治疗的主动脉穿透性溃疡患者,术中主动脉腔内移植物的选择应结合患者病情充分考虑。对于主动脉腔内移植物长度的选择,我们认为腔内移植物锚定区应距离主动脉穿透性溃疡至少2 cm,若主动脉穿透性溃疡两端斑块较多,腔内移植物锚定区应距离斑块至少2 cm,不应将腔内移植物锚定于斑块上。腔内移植物长度应以覆盖病变为目的,应避免选择过长的腔内移植物,从而降低截瘫的发生风险。若锚定区需遮蔽如左锁骨下动脉等分支动脉,应根据患者情况综合考量,采取平行支架技术或开窗技术重建分支动脉。
对于腔内移植物放大率的选择方面,由于主动脉穿透性溃疡患者主动脉硬化程度较为严重,放大率的选择不宜选择过大,以免过大的放大率引起主动脉夹层等并发症,我们的经验是以5%~10%为宜,而对于选择烟囱技术重建分支动脉的患者,为避免内漏发生,放大率可略微偏大,但不宜超过20%。但特别需要注意的是,由于患者主动脉硬化严重,在进行术前解剖学参数测量的过程中需结合拟选用的主动脉腔内移植物选择测量基准,避免主动脉内、外径基准选择错误造成放大率选择的严重误差[33]。结合术后随访结果,该范围内的放大率未引起主动脉夹层等移植物相关并发症。
血管腔内治疗技术以其时间短、创伤小以及术后恢复快等特点,已成为包括腹主动脉瘤、Stanford B型主动脉夹层在内的主动脉疾病的主要治疗手段。本组主动脉穿透性溃疡患者,年龄较大、全身疾病较多,血管腔内治疗技术是这些患者最佳的治疗方式。这些患者短期疗效令人满意,但由于入组例数较少,且随访时间偏短,还需要进一步验证血管腔内治疗对于主动脉穿透性溃疡的远期安全性和有效性。
| [1] |
TITTLE S L, LYNCH R J, COLE P E, et al. Midterm follow-up of penetrating ulcer and intramural hematoma of the aorta[J]. J Thorac Cardiovasc Surg, 2002, 123(6): 1051-1059. DOI:10.1067/mtc.2002.121681 |
| [2] |
NATHAN D P, BOONN W, LAI E, et al. Presentation, complications, and natural history of penetrating atherosclerotic ulcer disease[J]. J Vasc Surg, 2012, 55(1): 10-15. DOI:10.1016/j.jvs.2011.08.005 |
| [3] |
MURGO S, DUSSAUSSOIS L, GOLZARIAN J, et al. Penetrating atherosclerotic ulcer of the descending thoracic aorta: treatment by endovascular stent-graft[J]. Cardiovasc Intervent Radiol, 1998, 21(6): 454-458. DOI:10.1007/s002709900303 |
| [4] |
PIFFARETTI G, TOZZI M, LOMAZZI C, et al. Penetrating ulcers of the thoracic aorta: results from a single-centre experience[J]. Am J Surg, 2007, 193(4): 443-447. DOI:10.1016/j.amjsurg.2006.08.073 |
| [5] |
DEMERS P, MILLER D C, MITCHELL R S, et al. Stent-graft repair of penetrating atherosclerotic ulcers in the descending thoracic aorta: mid-term results[J]. Ann Thorac Surg, 2004, 77(1): 81-86. DOI:10.1016/s0003-4975(03)00816-6 |
| [6] |
BOTTA L, BUTTAZZI K, RUSSO V, et al. Endovascular repair for penetrating atherosclerotic ulcers of the descending thoracic aorta: early and mid-term results[J]. Ann Thorac Surg, 2008, 85(3): 987-992. DOI:10.1016/j.athoracsur.2007.10.079 |
| [7] |
LANSMAN S L, SAUNDERS P C, MALEKAN R, et al. Acute aortic syndrome[J]. J Thorac Cardiovasc Surg, 2010, 140(6 Suppl): S92-S97; discussion S142-S146. DOI: 10.1016/j.jtcvs.2010.07.062.
|
| [8] |
FILLINGER M F, GREENBERG R K, MCKINSEY J F, et al. Reporting standards for thoracic endovascular aortic repair (TEVAR)[J]. J Vasc Surg, 2010, 52(4): 1022-1033, 1033.e15. DOI:10.1016/j.jvs.2010.07.008 |
| [9] |
NIENABER C A, POWELL J T. Management of acute aortic syndromes[J]. Eur Heart J, 2012, 33(1): 26-35. DOI:10.1093/eurheartj/ehr186 |
| [10] |
AKIN I, KISCHE S, INCE H, et al. Penetrating aortic ulcer, intramural hematoma, acute aortic syndrome: when to do what[J]. J Cardiovasc Surg (Torino), 2012, 53(1 Suppl 1): 83-90. |
| [11] |
ODERICH G S, KÄRKKÄINEN J M, REED N R, et al. Penetrating aortic ulcer and intramural hematoma[J]. Cardiovasc Intervent Radiol, 2019, 42(3): 321-334. DOI:10.1007/s00270-018-2114-x |
| [12] |
VILACOSTA I. Acute aortic syndrome[J]. Heart, 2001, 85(4): 365-368. DOI:10.1136/heart.85.4.365 |
| [13] |
SUNDT T M. Intramural hematoma and penetrating atherosclerotic ulcer of the aorta[J]. Ann Thorac Surg, 2007, 83(2): S835-S841; discussion S846-850. DOI: 10.1016/j.athoracsur.2006.11.019.
|
| [14] |
VILACOSTA I, ARAGONCILLO P, CAÑADAS V, et al. Acute aortic syndrome: a new look at an old conundrum[J]. Heart, 2009, 95(14): 1130-1139. DOI:10.1136/hrt.2008.153650 |
| [15] |
STANSON A W, KAZMIER F J, HOLLIER L H, et al. Penetrating atherosclerotic ulcers of the thoracic aorta: natural history andclinicopathologic correlations[J]. Ann Vasc Surg, 1986, 1(1): 15-23. DOI:10.1016/S0890-5096(06)60697-3 |
| [16] |
VILACOSTA I, SAN ROMÁN J A, ARAGONCILLO P, et al. Penetrating atherosclerotic aortic ulcer: documentation bytransesophageal echocardiography[J]. J Am Coll Cardiol, 1998, 32(1): 83-89. DOI:10.1016/s0735-1097(98)00194-6 |
| [17] |
EGGEBRECHT H, PLICHT B, KAHLERT P, et al. Intramural hematoma and penetrating ulcers: indications to endovascular treatment[J]. Eur J Vasc Endovasc Surg, 2009, 38(6): 659-665. DOI:10.1016/j.ejvs.2009.09.001 |
| [18] |
GANAHA F, MILLER D C, SUGIMOTO K, et al. Prognosis of aortic intramural hematoma with and without penetrating atherosclerotic ulcer: a clinical and radiological analysis[J]. Circulation, 2002, 106(3): 342-348. DOI:10.1161/01.cir.0000022164.26075.5a |
| [19] |
HARRIS J A, BIS K G, GLOVER J L, et al. Penetrating atherosclerotic ulcers of the aorta[J]. J Vasc Surg, 1994, 19(1): 90-98; discussion 98-99. DOI: 10.1016/s0741-5214(94)70124-5.
|
| [20] |
EVANGELISTA A, MUKHERJEE D, MEHTA R H, et al. Acute intramural hematoma of the aorta: a mystery in evolution[J]. Circulation, 2005, 111(8): 1063-1070. DOI:10.1161/01.CIR.0000156444.26393.80 |
| [21] |
NIENABER C A, RICHARTZ B M, REHDERS T, et al. Aortic intramuralhaematoma: natural history and predictive factors for complications[J]. Heart, 2004, 90(4): 372-374. DOI:10.1136/hrt.2003.027615 |
| [22] |
SOYAMA A, KONO T, MATSUOKA T, et al. A case of penetrating atherosclerotic ulcer treated with thoracic endovascular aortic repair[J]. Circulation, 2015, 132(24): 2352-2353. DOI:10.1161/CIRCULATIONAHA.115.018784 |
| [23] |
VON KODOLITSCH Y, CSÖSZ S K, KOSCHYK D H, et al. Intramural hematoma of the aorta: predictors of progression to dissection and rupture[J]. Circulation, 2003, 107(8): 1158-1163. DOI:10.1161/01.cir.0000052628.77047.ea |
| [24] |
PIFFARETTI G, TOZZI M, LOMAZZI C, et al. Endovascular repair of abdominalinfrarenal penetrating aortic ulcers: a prospective observational study[J]. Int J Surg, 2007, 5(3): 172-175. DOI:10.1016/j.ijsu.2006.06.004 |
| [25] |
FLOHR T R, HAGSPIEL K D, JAIN A, et al. The history of incidentally discovered penetrating aortic ulcers of the abdominal aorta[J]. Ann Vasc Surg, 2016, 31: 8-17. DOI:10.1016/j.avsg.2015.08.028 |
| [26] |
GIFFORD S M, DUNCAN AA, GREITEN L E, et al. The natural history and outcomes for thoracic and abdominal penetrating aortic ulcers[J]. J Vasc Surg, 2016, 63(5): 1182-1188. DOI:10.1016/j.jvs.2015.11.050 |
| [27] |
TOLENAAR J L, HARRIS K M, UPCHURCH G RJr, et al. The differences and similarities between intramural hematoma of the descending aorta and acute type B dissection[J]. J Vasc Surg, 2013, 58(6): 1498-1504. DOI:10.1016/j.jvs.2013.05.099 |
| [28] |
RIAMBAU V, BÖCKLER D, BRUNKWALL J, et al. Editor's choice-Management of descending thoracic aorta diseases: Clinical practice guidelines of the European Society for Vascular Surgery (ESVS)[J]. Eur J Vasc Endovasc Surg, 2017, 53(1): 4-52. DOI:10.1016/j.ejvs.2016.06.005 |
| [29] |
EGGEBRECHT H, HEROLD U, SCHMERMUND A, et al. Endovascular stent-graft treatment of penetrating aortic ulcer: results over a Median follow-up of 27 months[J]. Am Heart J, 2006, 151(2): 530-536. DOI:10.1016/j.ahj.2005.05.020 |
| [30] |
BRINSTER D R, WHEATLEY G H 3rd, WILLIAMS J, et al. Are penetrating aortic ulcers best treated using an endovascular approach?[J]. Ann Thorac Surg, 2006, 82(5): 1688-1691. DOI:10.1016/j.athoracsur.2006.05.043 |
| [31] |
CZERNY M, FUNOVICS M, SODECK G, et al. Results after thoracic endovascular aortic repair in penetrating atherosclerotic ulcers[J]. Ann Thorac Surg, 2011, 92(2): 562-566; discussion 566-567. DOI: 10.1016/j.athoracsur.2011.02.087.
|
| [32] |
D'ANNOVILLE T, OZDEMIR B A, ALRIC P, et al. Thoracic endovascular aortic repair for penetrating aortic ulcer: literature review[J]. Ann Thorac Surg, 2016, 101(6): 2272-2278. DOI:10.1016/j.athoracsur.2015.12.036 |
| [33] |
张荣杰, 刘军军, 冯家烜, 等. 主动脉夹层腔内修复术前动脉管径测量的现状与展望[J]. 中华普通外科杂志, 2017(6): 543-545. ZHANG R J, LIU J J, FENG J X, et al. Current status and prospects of preoperative arterial diameter measurement in aortic dissection[J]. Chin J Gen Surg, 2017(6): 543-545. DOI:10.3760/cma.j.issn.1007-631X.2017.06.031 |



