2. 710075 西安,西安高新医院神经内科;
3. 710061 西安,陕西省分子心脏病学重点实验室;
4. 710061 西安,环境与疾病相关教育部重点实验室
2. Department of Neurology, Xi'an Gaoxin Hospital, Xi'an, Shaanxi Province, 710075;
3. Key Laboratory of Molecular Cardiology, Xi'an, Shaanxi Province, 710061;
4. Key Laboratory of Environment and Genes Related to Diseases of Ministry of Education, Xi'an Jiaotong University, Xi'an, Shaanxi Province, 710061, China
动脉粥样硬化(atherosclerosis,AS)是一种发生于动脉壁、病因未明的慢性炎症性疾病,也是冠心病的主要病理基础和血管性死亡的主要原因。冠心病患者的体内长期存在着不同程度的慢性炎症状态,超敏C反应蛋白(high sensitive C-reactive protein,hsCRP)作为炎症标志物之一,不仅能够代表AS炎症状态,也可以直接通过增加单核细胞向AS斑块募集、诱导内皮功能障碍以及增加血管内皮纤溶酶原激活剂-1和其他黏附分子表达等途径促进AS的发生和发展[1-2];冠心病患者hsCRP水平的升高往往代表着心肌缺血和损伤的加重,升高越明显,损伤越重,并且hsCRP对急性冠脉综合征患者的短期死亡和主要心血管事件也有预测价值[3]。但对于那些hsCRP水平正常即体内炎症状态较低的患者,又有哪些因素影响着其冠状动脉病变(coronary artery disease, CAD)的严重程度目前仍未见相关报道。
同型半胱氨酸(homocysteine,Hcy)是蛋氨酸和半胱氨酸代谢过程中的一种含硫中间产物。流行病学研究发现血Hcy升高是动脉粥样硬化的重要危险因素[4],也与男性冠脉钙化和急性心肌梗死显著相关[5-6],低Hcy则是心肌梗死患者的自发性再灌注的独立预测因子[6];但遗憾的是目前关于血清Hcy浓度与CAD严重性的相关报道多数都是几十到几百例的小样本研究[7-9],尤其是在炎症状态正常的患者中Hcy浓度与CAD的关系更未见研究报道。本研究在hsCRP正常的冠心病患者中,对血清Hcy水平与CAD患病率和严重程度的关系进行了大样本的观察和分析,以期为此类患者的临床诊疗提供新的建议。
1 资料与方法 1.1 研究对象本研究纳入了2017年4月至2019年4月期间在西安交通大学第一附属医院心内科接受了冠状动脉造影的患者,根据JUPITER和CANTOS研究[10-11]将hsCRP≤2.0 mg/L定义为炎症水平正常;因此排除标准为:hsCRP>2.0 mg/L或未检测hsCRP的患者、家族性高Hcy血症、恶性肿瘤、严重的肝肾功能障碍、各种自身免疫性疾病、寄生虫感染、处于急性感染状态者、严重的心力衰竭或休克、风湿性心脏病和心脏瓣膜病等可能会引起干扰的相关疾病,最终共4 097例患者纳入本研究。本研究经过西安交通大学伦理委员会批准(XJTUIAF2019LSK143),并获得了所有参与者的书面知情同意书。
1.2 研究方法 1.2.1 病史采集和生化指标检测纳入研究的病例均仔细询问病史,收集并记录其性别、年龄、吸烟史、高血压病史、糖尿病病史和冠心病家族史等基本资料。入选病例入院第2天清晨的空腹静脉血吸入K2EDTA-标准抗凝管(BD Biosciences,USA)中,并于30 min内检测血脂各组分含量,以及Hcy、肌酐、尿酸、hsCRP等冠心病相关的炎性指标,指标均在本院检验科进行检测。
1.2.2 分组方法按照血清HCY浓度的三分位数将所有患者分为高Hcy组(>19.40 μmol/L, HHcy)、中Hcy组(>13.90~19.40 μmol/L, MHcy)和低Hcy组(≤13.90 μmol/L, LHcy);根据冠状动脉造影结果,至少一支主要血管狭窄程度>50%者定义为CAD组,其余定义为No-CAD组;然后根据诊断将CAD患者分为4个亚组:稳定型心绞痛(SA)、不稳定型心绞痛(UA)、非ST段抬高性心梗(NSTEMI)和急性ST段抬高性心梗(STEMI)。
1.2.3 冠状动脉病变严重程度评估本研究使用Gensini评分[12]系统对冠状动脉的狭窄程度进行量化评估,每处病变的分值=狭窄程度的评分×病变部位的系数,每位患者的总分是所有分支分数的总和。病变部位系数为:右冠RCA病变1分,左主干LM病变5分,左前降支LAD近段和回旋支LCX近段病变2.5分,LAD中段1.5分,LAD远段、第1对角支D1、钝缘支OM、LCX远段和后降支PD病变均为1分,第2对角支和左室后支病变0.5分;狭窄程度评分为:1%~25%狭窄记1分,26%~50%狭窄记2分,51%~75%狭窄记4分,76%~90%狭窄记8分,91%~99%狭窄记16分,100%狭窄记32分。
1.3 统计学分析使用SPSS 20.0统计分析软件对数据进行分析;连续变量以x±s表示,分类变量用计数和相应的百分比表示。连续变量均使用Shapiro-Wilk分析检验数据的正态性,如果符合正态分布则使用单因素方差分析组间差异,如果不符合正态分布则使用Kruskal-Wallis H检验分析组间差异;分类变量的组间差异采用χ2检验;Spearman相关分析检验双变量之间的相关性;在校正基线混杂因素后,使用多因素Logistic回归分析评估Hcy与CAD患病率、严重程度以及与不同冠心病亚型的关系;双侧检验,检验水准α =0.05。
2 结果 2.1 基线资料比较如表 1所示,与低Hcy组相比,高Hcy组的男性(P < 0.001)和有吸烟史者的比例较高(P < 0.001)、CAD的患病率更高(P < 0.001)、心功能更差(EF更低而LVEDD更高,P < 0.001),而糖尿病的患病比例较低(P < 0.001)。3组之间高血压和家族史的比例则未见明显差异。
| 组别 | n | CAD [例(%)] |
男性 [例(%)] |
高血压 [例(%)] |
糖尿病 [例(%)] |
吸烟 [例(%)] |
家族史 [例(%)] |
年龄 (x±s)/岁 |
射血分数 (%,x±s) |
左室舒张末期内径(x±s)/mm |
| 低Hcy组 | 1 372 | 996(72.6) | 715(52.1) | 789(57.5) | 489(35.6) | 489(35.6) | 241(17.6) | 60.58±9.65 | 65.02±8.97 | 49.17±4.37 |
| 中Hcy组 | 1 374 | 1 061(77.2) | 961(69.9) | 858(62.4) | 387(28.2) | 683(49.7) | 253(18.4) | 61.39±9.87 | 62.91±9.88 | 50.38±4.91 |
| 高Hcy组 | 1 351 | 1 130(83.6) | 1 111(82.2) | 793(58.7) | 264(19.5) | 778(57.6) | 256(18.9) | 60.54±10.66 | 61.01±10.78 | 51.43±5.58 |
| P值 | <0.001 | <0.001 | 0.023 | <0.001 | <0.001 | 0.642 | 0.036 | <0.001 | <0.001 |
2.2 临床生化指标的比较
高Hcy组的apoA1和HDL-C水平均比低Hcy组显著降低(P < 0.001),血糖和HbA1c的水平也明显更低(P < 0.001);与低Hcy组相比,高Hcy组的肌酐和尿酸水平显著较高(P < 0.001),代表体内炎症状态的hsCRP和WBC含量也显著较高(P < 0.001)。见表 2。
| 组别 | n | 总胆固醇/ mmol·L-1 |
低密度脂蛋白/ mmol·L-1 |
高密度脂蛋白/ mmol·L-1 |
甘油三酯/ mmol·L-1 |
葡萄糖/ mmol·L-1 |
白细胞/ 109·L-1 |
糖化血红蛋白 (%) |
血肌酐/ mmol·L-1 |
血尿酸/ mmol·L-1 |
超敏C反应蛋白 /mg·L-1 |
载脂蛋白A1/ 109·L-1 |
| 低Hcy组 | 1 372 | 3.75±0.96 | 2.12±0.80 | 1.03±0.25 | 1.52±1.09 | 6.68±3.00 | 6.63±2.25 | 6.11±1.64 | 58.86±15.61 | 298.44±76.92 | 0.74±0.49 | 1.16±0.19 |
| 中Hcy组 | 1 374 | 3.76±0.95 | 2.15±0.79 | 0.99±0.24 | 1.53±0.96 | 6.39±2.78 | 6.82±2.18 | 5.93±1.57 | 64.42±16.55 | 319.39±79.18 | 0.77±0.49 | 1.13±0.19 |
| 高Hcy组 | 1 351 | 3.67±0.94 | 2.12±0.81 | 0.95±0.22 | 1.49±0.92 | 6.02±2.33 | 7.07±2.68 | 5.68±1.15 | 70.65±41.36 | 325.41±84.62 | 0.81±0.50 | 1.09±0.18 |
| P值 | 0.013 | 0.391 | <0.001 | 0.459 | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 |
2.3 Hcy水平与CAD病变类型和病变严重程度的关系
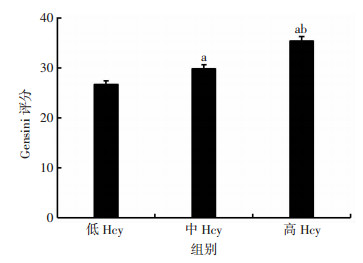
如表 3所示,高Hcy组有更高比例的三支病变(P=0.004)和心肌梗死(NSTEMI,P=0.002;STEMI,P < 0.001),更低比例的noCAD(P < 0.001);代表冠脉病变严重程度的Gensini评分在高Hcy组也显著增高(P < 0.001,图 1);双变量Spearman相关分析结果显示Gensini评分与血清Hcy水平呈显著正相关(r=0.122,P < 0.001)。
| 组别 | n | 单支病变 | 双支病变 | 三支病变 | 非CAD | 稳定型心绞痛 | 不稳定型心绞痛 | 非ST段抬高性心梗 | ST段抬高性心梗 |
| 低Hcy组 | 1 372 | 307(22.4) | 304(22.2) | 398(29.0) | 376(27.4) | 77(5.6) | 758(55.2) | 35(2.6) | 126(9.2) |
| 中Hcy组 | 1 374 | 313(22.8) | 335(24.4) | 425(30.9) | 313(22.8) | 82(6.0) | 775(56.4) | 54(3.9) | 150(10.9) |
| 高Hcy组 | 1 351 | 325(24.1) | 342(25.3) | 470(34.8) | 221(16.4) | 85(6.3) | 770(57.0) | 70(5.2) | 205(15.2) |
| P值 | 0.555 | 0.139 | 0.004 | <0.001 | 0.755 | 0.646 | 0.002 | <0.001 |
|
| a:P < 0.05,与低Hcy组比较;b:P < 0.05,与中Hcy组比较 图 1 Gensini评分在血清Hcy浓度三分位数组间的差异(x±SE) |
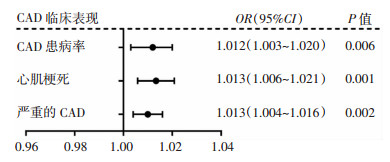
将Gensini评分三分位数的最高分位数(>34分)定义为严重CAD,然后对血清Hcy水平与CAD的发病、类型和严重程度进行多因素Logistic回归分析,结果显示即使在调整性别、年龄、高血压史、吸烟史、糖尿病史、白细胞、总胆固醇、高密度胆固醇、肌酐、尿酸、HbA1c、apoA1和hsCRP等所有的基线差异后,血清Hcy水平仍然与CAD的患病率、心肌梗死和更严重的CAD病变显著正相关(图 2)。
|
| 图 2 血清Hcy与CAD患病率、类型和严重程度的关系 |
3 讨论
冠心病是目前常见的心血管疾病之一[13],许多研究都证实冠心病患者的体内存在着持续的慢性炎症状态。作为经典的炎症标志物之一,hsCRP水平升高对急性冠脉综合征患者的主要心血管事件和病变严重程度均有诊断和预测价值[4, 6],并且也代表冠心病患者存在复发性心血管事件的风险,hsCRP升高提示患者预后不良,降低则提示患者预后良好[14]。JUPITER研究[10]证实甚至在一些“看似正常者”体内也存在着长期的hsCRP升高状态。对于冠心病患者中哪些指标可以作为其病变严重程度的独立预测因素目前已有许多研究,血Hcy浓度升高就是其中之一。但对于体内炎症状态正常的患者,又有哪些因素能够预测冠脉病变的严重性?是否血Hcy升高也与此类患者的冠脉病变严重程度显著相关,目前仍未见相关研究报道。
本研究的重要意义在于我们在血清hsCRP水平正常者中对Hcy浓度与CAD的患病率、类型和严重程度进行了大样本的分析和对比,研究结果显示高Hcy组患者的CAD患病率更高,三支病变和心肌梗死的比例更高,Gensini评分也更高;即使在调整了所有基线差异后,血清Hcy水平仍然与CAD的发病、心肌梗死和严重的CAD病变显著正相关;并且本研究还发现高Hcy组的患者心功能更差。提示我们对于这些体内炎症水平正常的冠心病患者,血Hcy浓度的监测可能有助于对其进行早期干预和改善结局。
YU等[15]的一项包括19 085例参与者的大型流行病学研究发现非饮酒的中国老年人中血浆Hcy浓度与T2DM患病风险负相关[15-16],本研究也同样发现高Hcy组的患者糖尿病发病率更低,并且血糖和HbA1c水平也显著降低,与YU等的研究结果基本一致,但这种负相关的潜在机制仍然需要基础研究进一步确认。此外,作为HDL-c中的主要载脂蛋白,apoA1和HDL-c因参与胆固醇的逆向转运而被认为是冠心病的保护性因子,有研究表明Hcy可通过影响HDL-c的合成相关基因等多种途径降低其水平[17];本研究也发现与低Hcy组相比,apoA1和HDL-c在高Hcy组显著降低,提示它们在高Hcy状态下保护作用减弱,与既往研究结果一致。
本研究也存在一定的局限性,首先虽然样本量较大,但未能获得所纳入患者的随访资料,因此无法判断血清hsCRP水平正常者中Hcy浓度是否也对冠心病患者的长期预后有影响;其次本研究纳入的患者均来自于西北地区的单中心,研究结果是否也适用于其他地区的人群也需要进一步研究确定。
总之,本研究发现在体内炎症水平正常的冠心病患者中,血清Hcy浓度是CAD患病率和严重程度的独立预测因子,加强对此类患者的积极监测和早期干预,可能有助于改善患者的预后和结局。
| [1] |
LIBBY P. Mechanisms of acute coronary syndromes and their implications for therapy[J]. N Engl J Med, 2013, 368(21): 2004-2013. DOI:10.1056/NEJMra1216063 |
| [2] |
KAMATH D Y, XAVIER D, SIGAMANI A, et al. High sensitivity C-reactive protein(hsCRP) & cardiovascular disease: An Indian perspective[J]. Indian J Med Res, 2015, 142(3): 261-268. DOI:10.4103/0971-5916.166582 |
| [3] |
孙宇轩, 李莉. 高敏C反应蛋白与冠状动脉性心脏病的关系[J]. 中华高血压杂志, 2017, 25(7): 680-684. SUN Y X, LI L. Relationship between high-sensitivity C-reactive protein and coronary heart disease[J]. Chin J Hypertens, 2017, 25(7): 680-684. DOI:10.16439/j.cnki.1673-7245.2017.07.023 |
| [4] |
MCCULLY K S. Homocysteine metabolism, atherosclerosis, and diseases of aging[J]. Compr Physiol, 2015, 6(1): 471-505. DOI:10.1002/cphy.c150021 |
| [5] |
KIM B J, KIM B S, KANG J H. Plasma homocysteine and coronary artery calcification in Korean men[J]. Eur J Prev Cardiol, 2015, 22(4): 478-485. DOI:10.1177/2047487314522136 |
| [6] |
MA Y, PENG D L, LIU C G, et al. Serum high concentrations of homocysteine and low levels of folic acid and vitamin B12 are significantly correlated with the categories of coronary artery diseases[J]. BMC Cardiovasc Disord, 2017, 17(1): 37. DOI:10.1186/s12872-017-0475-8 |
| [7] |
薛莉, 陈树兰, 贾绍斌, 等. 同型半胱氨酸与冠心病的相关性及其机制探讨[J]. 中华心血管病杂志, 2002, 30(9): 520-524. XUE L, CHEN S L, JIA S B, et al. The correlation between plasma homocysteine and coronary heart disease and the study on its pathogenesis[J]. Chin J Cardiol, 2002, 30(9): 520-524. DOI:10.3760/j:issn:0253-3758.2002.09.003 |
| [8] |
张志世, 王凌燕. 同型半胱氨酸与冠心病[J]. 中国循环杂志, 2016, 31(4): 405-407. ZHANG Z S, WANG L Y. Homocysteine and coronary heart disease[J]. Chin Circ J, 2016, 31(4): 405-407. DOI:10.3969/j.issn.1000-3614.2016.04.022 |
| [9] |
刘祥红, 师志云, 刘会玲, 等. 不同类型冠心病患者血清同型半胱氨酸水平变化研究[J]. 中国全科医学, 2019, 22(8): 920-924. LIU X H, SHI Z Y, LIU H L, et al. Correlation between homocysteine and different types of coronary heart disease[J]. Chin Gen Pract, 2019, 22(8): 920-924. |
| [10] |
RIDKER P M, DANIELSON E, FONSECA F A, et al. Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein[J]. N Engl J Med, 2008, 359(21): 2195-2207. DOI:10.1056/NEJMoa0807646 |
| [11] |
RIDKER P M, HOWARD C P, WALTER V, et al. Effects of interleukin-1β inhibition with canakinumab on hemoglobin A1c, lipids, C-reactive protein, interleukin-6, and fibrinogen: a phase Ⅱb randomized, placebo-controlled trial[J]. Circulation, 2012, 126(23): 2739-2748. DOI:10.1161/CIRCULATIONAHA.112.122556 |
| [12] |
GENSINI G G. A more meaningful scoring system for determining the severity of coronary heart disease[J]. Am J Cardiol, 1983, 51(3): 606. DOI:10.1016/s0002-9149(83)80105-2 |
| [13] |
HERRINGTON W, LACEY B, SHERLIKER P, et al. Epidemiology of atherosclerosis and the potential to reduce the global burden of atherothrombotic disease[J]. Circ Res, 2016, 118(4): 535-546. DOI:10.1161/CIRCRESAHA.115.307611 |
| [14] |
BOGATY P, POIRIER P, SIMARD S, et al. Biological profiles in subjects with recurrent acute coronary events compared with subjects with long-standing stable angina[J]. Circulation, 2001, 103(25): 3062-3068. DOI:10.1161/01.cir.103.25.3062 |
| [15] |
YU C, WANG J, WANG F, et al. Inverse association between plasma homocysteine concentrations and type 2 diabetes mellitus among a middle-aged and elderly Chinese population[J]. Nutr Metab Cardiovasc Dis, 2018, 28(3): 278-284. DOI:10.1016/j.numecd.2017.11.009 |
| [16] |
KARK J D, SELHUB J, BOSTOM A, et al. Plasma homocysteine and all-cause mortality in diabetes[J]. Lancet, 1999, 353(9168): 1936-1937. DOI:10.1016/s0140-6736(98)05381-1 |
| [17] |
高胜利, 李莉, 翟晓娟, 等. 心血管疾病中同型半胱氨酸与高密度脂蛋白胆固醇的关系[J]. 中华高血压杂志, 2015, 23(6): 522-525. GAO S L, LI L, ZHAI X J, et al. Relationship between homocysteine and high density lipoprotein cholesterol in cardiovascular diseases[J]. Chin J Hypertens, 2015, 23(6): 522-525. DOI:10.16439/j.cnki.1673-7245.2015.06.013 |



