遗传性视网膜变性(inherited retinal degeneration, IRD)是一组进行性感光细胞及色素上皮功能丧失,具有遗传特性的视网膜变性疾病,通常幼年时不易发现,青壮年时期出现明显视觉障碍,临床表现夜盲、视力下降、视野缩窄和视网膜电图异常[1-2]。最常见的遗传性视网膜变性为原发性视网膜色素变性(retinitis pigmentosa, RP),目前发现70多个致病基因与RP相关,被认为是世界性致盲眼病,其发病机制不清,尚缺乏有效的治疗方法[3-7]。与此相反,临床发现一组与遗传不相关,而具有与原发病因相伴或因原发病后继发改变如炎症、外伤、视网膜脉络膜阻塞、肿瘤等所导致的部分类似原发性视网膜色素变性的一组视网膜变性疾病,称继发性视网膜变性(secondary retinal degeneration,SRD)或假性视网膜色素变性(pseudo retinitis pigmentosa, PRP)[8-16]。PRP患者的眼底改变易与单侧视网膜色素变性混淆,后者眼底表现和ERG显示单眼视网膜色素变性特征无其他原因解释,具有RP眼底和病史特征,另眼眼底和ERG、视功能正常;随访5年以上无改变[17-19]。然而目前有文献报道1例初诊为单侧视网膜色素变性患者随访30年后发现最初正常眼逐渐显示出RP样退化的表现,颠覆了以往对单侧性视网膜色素变性的认识[20]。所以对原发性RP和PRP精准诊断,尤其对单侧视网膜色素变性的诊断和鉴别诊断十分重要。PRP患者在明确病因基础上积极治疗原发病,可有效减少误诊并能阻止病情进展,维持和提高患者的有效视功能,改善视觉质量和生活质量。本研究观察26例PRP患者的原发病因和临床特征,对诊断和鉴别诊断以及治疗继发视网膜变性类疾病有一定指导意义。
1 资料与方法 1.1 临床资料收集2014年12月至2018年10月在陆军军医大学第一附属医院眼科就诊的26例PRP患者,经过全面的眼科检查,包括最佳矫正视力(best corrected visual acuity,BCVA)(采用小数记录)、眼底彩色照相(color fundus photography,CFP)、视野(visual field,VF)和全视野闪光视网膜电图(full field flash electroretinogram,FERG),排除单侧性视网膜色素变性。单侧性视网膜色素变性诊断标准:单眼视力下降,视野缩窄,患眼眼底伴或不伴骨细胞样色素沉积,单侧视野和ERG改变无其他原因解释,有或无家族史,另眼眼底和ERG、视功能正常,随访5年以上无病变进展。采集26例PRP患者基本信息、病史及临床症状,在眼科临床数据库中筛查RP患者1330例,选取与PRP患者年龄相匹配的RP患者30例。RP患者中有或无家族史,有夜盲病史,无视网膜视神经病变、眼内炎症病史以及内眼手术史。双眼眼底色素紊乱,多伴有广泛骨细胞样色素沉积、视盘蜡黄、血管变细、视野缺损、FERG降低或熄灭,且有完整临床资料记录和眼科检查,包括BCVA、眼底彩色照相、眼底荧光血管造影、视野、FERG,与PRP患者进行两组之间病程、BCVA、眼底变化、FERG比较分析。
1.2 评价指标对PRP患者临床特征的主要评价指标包括原发病因、病程、BCVA、视野、FERG各波振幅和潜伏时间改变、眼底改变。
1.3 统计学分析采用SPSS 23.0统计软件进行分析。计量资料以x±s表示,采用t检验行差异性分析,检验水准α=0.05。
2 结果 2.1 一般情况PRP患者26例30眼,其中男性12例,女性14例,年龄26~56岁,单眼患病22例(84.6%),双眼患病4例(15.4%)。病程6个月至5年,BCVA从无光感~1.2,主诉包括视力下降,视物变形,视物遮挡感,所有患者能清楚说出视觉异常的时间点,但无1例患者主诉夜盲病史。在眼科临床数据库中选取年龄相匹配的RP患者30例60眼,其中男性13例,女性17例,年龄26~55岁,平均43岁,平均矫正视力0.3,病程15~45年。26例PRP原发病因:葡萄膜炎11例14眼(46.67%),视网膜脱离10例11眼(36.67%),外伤性视网膜病变4例4眼(13.33%),脉络膜骨瘤1例1眼(3.33%)。首诊时PRP患者基本资料见表 1。RP和PRP患者病程、BCVA比较差异有统计学意义(P<0.05),PRP患者健眼和患眼BCVA比较差异有统计学意义(P<0.05,表 2)。
| 诊断 | 性别/例 | 年龄/岁 | 眼只 | 最佳矫正视力 | |
| 女性 | 男性 | ||||
| 视网膜脱离 | 6 | 4 | 41.64±14.89 | 11 | 0.05±0.04a |
| 葡萄膜炎 | 8 | 3 | 45.82±12.92 | 14 | 0.44±0.49 |
| 外伤性视网膜病变 | 0 | 4 | 39.00±7.53 | 4 | 0.03±0.04a |
| 其他 | 0 | 1 | 39 | 1 | 0.7 |
| a: P<0.01,与葡萄膜炎患者比较 | |||||
| 组别 | n | 眼只 | 年龄/岁 | 病程/年 | 夜盲/例 | 遗传史/例 | 最佳矫正视力 |
| RP | 30 | 60 | 43.33±17.31 | 26.80±12.40a | 30 | 28 | 0.31±0.21a |
| PRP患眼 | 26 | 30 | 43.19±12.90 | 11.40±5.40 | 0 | 0 | 0.22±0.38 |
| PRP健眼 | 22 | 22 | 43.19±12.90 | 0 | 0 | 0 | 1.20±0.20a |
| a: P<0.05,与PRP患眼比较 | |||||||
2.2 PRP眼底特征
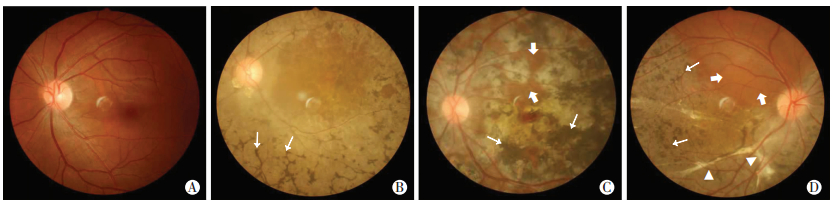
PRP患者表现为双眼不对称22例22眼。眼底色素改变异常表现为色素斑块粗大、形状不规则、污秽、杂乱,缺少骨细胞样色素分布特征,而在异常色素分布的间隙可见正常色泽的视网膜;血管形态大致正常,血管形态异常眼表现为迂曲变形、管径增粗或变细,部分血管可见白鞘形成;视盘色泽和大小正常,异常眼表现为视盘颜色变淡,苍白甚至萎缩;部分眼底表现为视网膜下灰白色增殖条带。而RP患者眼底表现为视网膜晦暗,色素紊乱,后极部和中周部视网膜可见骨细胞样色素沉积,血管纤细,视盘蜡黄,中晚期患者因视网膜色素上皮细胞萎缩,可显示硬化的脉络膜血管(图 1)。
|
A:左眼正常眼底;B:原发性视网膜色素变性患者左眼眼底视盘蜡黄,血管细,视网膜晦暗,色素紊乱,中周部视网膜可见典型骨细胞样色素沉积(↑);C:左眼脉络膜炎后患者眼底左眼视盘色淡红,边界清,视网膜血管未见异常,后极部色素斑块(白箭头所示)粗大,不规则,间杂正常色泽的视网膜( );D:右眼视网膜脱离后患者眼底除右眼黄斑上方可见正常色素和血管分布的视网膜( );D:右眼视网膜脱离后患者眼底除右眼黄斑上方可见正常色素和血管分布的视网膜( )外,下方、颞侧、颞上和鼻下方视网膜色泽晦暗,较多斑块状色素沉积(↑),视网膜下灰白色增殖条带(▲),视盘色淡红,边界稍模糊
图 1
正常人,RP和PRP患者眼底彩色图像比较 )外,下方、颞侧、颞上和鼻下方视网膜色泽晦暗,较多斑块状色素沉积(↑),视网膜下灰白色增殖条带(▲),视盘色淡红,边界稍模糊
图 1
正常人,RP和PRP患者眼底彩色图像比较
|
2.3 PRP视野和FERG特征
视野改变:RP患者双眼管状视野,对称。继发于葡萄膜炎的患者双眼视野不对称,患眼视敏度弥漫降低,或弥漫性视野缺损,与眼底病变范围一致。双眼患病者病变程度不同,视野改变不一致(图 2)。双眼患病的PRP患者FERG各波幅值同步降低,包括暗视视杆反应、最大混合反应和明视反应,但降低程度显著轻于同等眼底色素改变的RP患者。RP患者双眼FERG各波降低幅度显著,表现为视杆反应,Ops和视锥反应显著降低,这种降低程度与病程相关,早期患者可能仅仅表现为视锥反应或视杆反应降低,随着病程进展视锥、视杆反应、Ops逐步降低甚至熄灭;单眼患病的PRP患者首先表现为双眼FERG各波幅值和潜伏时间显著不对称,其次表现为患眼的FERG视杆、视锥反应和Ops同步降低,但降低的幅度显著低于RP患者。PRP患眼的眼底形态变化似乎很严重,然而FERG改变并不十分严重(图 3)。

|
| A:正常对照双眼视野正常;A1、A2分别是正常人右眼和左眼眼底彩色图像,A3、A4分别是正常人右眼和左眼视野图;B:RP患者双眼管状视野;B1、B2分别是RP患者右眼和左眼眼底彩色图像,B3、B4分别是RP患者右眼和左眼视野图;C:葡萄膜炎患者患眼(右眼)视敏度弥漫性降低,对侧眼视野正常;C1、C2分别是葡萄膜炎患者患眼和对侧眼眼底彩色图像,C3、C4分别是葡萄膜炎患者患眼和对侧眼视野图;D:视网膜脱离复位后患眼(右眼)视野弥漫性缺损,对侧眼(左眼)视野大致正常;D1、D2分别是视网膜脱离术后患者患眼和健眼眼底彩色图像,D3、D4分别是视网膜脱离术后患眼和对侧眼视野图 图 2 RP、PRP和正常人不同视野改变 |

|
| Normal:正常对照;RP:视网膜色素变性患者;UV:葡萄膜炎患者;RD:视网膜脱离术后患者;红色左眼,蓝色为右眼;正常人双眼眼底形态正常,FERG功能反应正常,双眼对称;RP患者双眼底色素紊乱,视盘蜡黄,血管细,FERG各项反应消失,双眼对称;右眼葡萄膜炎患者患眼眼底异常改变,患眼的FERG显示视锥和视杆反应同步降低,正常眼眼底未见异常,FERG正常,双眼不对称改变;右眼视网膜脱离术后患者患眼眼底病变区视网膜色泽异常,色素紊乱,视盘色淡,右眼FERG反应极重度降低,左眼眼底和FERG正常,双眼不对称 图 3 正常对照、RP和PRP患者FERG改变 |
3 讨论
PRP临床并不少见,常常被误诊为原发性视网膜色素变性。目前原发性视网膜色素变性尚无有效治疗方法,将PRP误诊为RP会造成PRP患者失去治疗机会,延误病情[22]。因此,临床上PRP的诊断和鉴别诊断非常重要。
文献报道脉络膜炎、肿瘤(或癌)相关视网膜病变和梅毒性视网膜病变可表现为PRP眼底改变[10-16]。所有这些报道均为个案报道,除去这些原发病因报道外,目前尚未见PRP与RP临床对比研究。本研究中PRP病因主要是葡萄膜炎、视网膜脱离、外伤性视网膜病变。这些PRP患者与RP患者的眼底改变重叠,单眼发病或双眼先后发病,特殊的眼底色素改变需要临床医师仔细分析,仔细检查,明确诊断,减少误诊、漏诊。炎症引起的PRP,正确的干预可以防止眼底形态和功能进一步损害。以肿瘤首发的PRP,如果能及时正确识别,早期干预,不仅稳定患者视功能,还可以改善患者预后。继发于视网膜脱离和外伤性视网膜病变的PRP患者视功能损害非常严重,及时有效的治疗,可以挽救患者视功能,提高患者生存质量。
本研究发现PRP在发病年龄、病史、病变发展过程、主诉、家族史和BCVA与RP完全不同。PRP发病年龄与原发病几乎同步或稍后,病程相对较短,无家族遗传史和夜盲病史,患眼视力下降急剧,患者可以清楚地说出患眼视力下降的时间区间或时间点,特别在单眼发病的患者中,因致病原因视功能变化差异较大,在本研究中外伤和视网膜脱离患者继发的PRP其视功能损害十分显著。而RP患者具有以下临床特征:发病年龄较小,双眼对称发病,病程长,病变进展缓慢,通常有遗传家族史,绝大多数患者有夜盲,对晚发型RP患者早期不易发现,患者出现症状或有警觉时,已进入中晚期,时间长达数十年,平均BCVA逐年降低,直至光感或无光感。
眼底形态改变是区分RP和PRP的关键:RP双眼对称,视盘蜡黄,血管纤细,视网膜异常表现典型骨细胞样色素沉积,分布具有规律性,大部分呈周边向中心发展型,伴随着黄斑区和后极部色素紊乱,RPE改变。PRP眼底改变不对称(除双眼外),眼底色素斑块粗大、形状不规则、污秽、杂乱,并且主要分布在原发病变区,特别注意病变未累及区域视网膜无色素异常,非病变区的视网膜色泽安全正常,眼底血管大致正常,如果原发病灶累及血管会导致部分血管出现迂曲变形、变细或白鞘。视盘形态和色泽基本正常,病变累及视盘后出现视盘充血、出血、水肿和萎缩苍白,而不是蜡黄改变。
RP和PRP患者FERG具有特征性改变:RP患者FERG表现呈多种多样,一般遵循视杆反应首先降低,后出现视锥反应降低,而视杆、视锥反应同步降低少见。以黄斑变性或视锥细胞变性为主的患者可首发视锥反应降低,对于单眼或双眼不对称的病例,除具备以上的临床特征外,基因检测也可以提供精准诊断。双眼患病的PRP患者FERG各波幅值同步降低,但降低程度显著轻于同等眼底色素的RP患者;单眼患病的PRP患者表现为双眼FERG各波潜伏时间和振幅显著不对称。RP患者双眼眼底改变和视功能变化是同步的,随着RPE萎缩和脉络膜毛细血管萎缩,最终导致RP患者FERG呈熄灭形或无法记录波形。本研究发现所有PRP患眼的眼底形态改变程度与FERG所反映的功能降低程度均不具有一致性,外伤和视网膜脱离所致的PRP患者视网膜病损不甚严重,但BCVA和FERG各波振幅明显降低但仍好于RP患者的FERG改变,葡萄膜炎患者表现为视网膜病损显著,视网膜色素污浊、灰暗,但FERG仍保留较好的波形改变,可能与葡萄膜炎累及部位是脉络膜,对感光细胞的损害较轻有关,故FERG结果较RP患者尚好。PRP患者FERG结果反映的视网膜感光细胞功能降低程度与眼底改变不一致,提示PRP患者继发的视网膜变性会残留部分功能正常的感光细胞,表明这种PRP是局限性的而不是弥漫性的和完全的损害。FERG反映的是视网膜内外层视网膜的整体功能,PRP患者眼底显示视网膜受损部位之外可存留正常的视网膜,因此PRP患者的FERG各波降低程度明显轻于RP患者,这个可能是慢性视网膜变性和急性短期受损后视网膜变性的主要原因,其机制有待进一步研究。
PRP病因复杂多样,除具有双眼不对称性外,根据临床典型的病史特征、病程、眼底改变、视野和FERG均有助于诊断和鉴别诊断其他类型视网膜变性,其中眼底改变、FERG是PRP与RP鉴别诊断的主要指标。根据不同的原发病因积极治疗PRP,为患者维持有效视功能争取时机,改善预后。
| [1] |
HAFLER B P. Clinical progress in inherited retinal degenerations: gene therapy clinical trials and advances in genetic sequencing[J]. Retina (Philadelphia, Pa), 2017, 37(3): 417-423. DOI:10.1097/IAE.0000000000001341 |
| [2] |
GUPTA P R, HUCKFELDT R M. Gene therapy for inherited retinal degenerations: initial successes and future challenges[J]. J Neural Eng, 2017, 14(5): 051002. DOI:10.1088/1741-2552/aa7a27 |
| [3] |
VERBAKEL S K, VAN HUET R A C, BOON C J F, et al. Non-syndromic retinitis pigmentosa[J]. Prog Retin Eye Res, 2018, 66: 157-186. DOI:10.1016/j.preteyeres.2018.03.005 |
| [4] |
ZOBOR D, ZRENNER E. Retinitis pigmentosa - a review. Pathogenesis, guidelines for diagnostics and perspectives[J]. Ophthalmologe, 2012, 109(5): 501-514;quiz 515. DOI: 10.1007/s00347-012-2555-6.
|
| [5] |
RIVOLTA C, SHARON D, DEANGELIS M M, et al. Retinitis pigmentosa and allied diseases: numerous diseases, genes, and inheritance patterns[J]. Hum Mol Genet, 2002, 11(10): 1219-1227. DOI:10.1093/hmg/11.10.1219 |
| [6] |
SEN P, BHARGAVA A, GEORGE R, et al. Prevalence of retinitis pigmentosa in South Indian population aged above 40 years[J]. Ophthalmic Epidemiol, 2008, 15(4): 279-281. DOI:10.1080/09286580802105814 |
| [7] |
FERRARI S, DI IORIO E, BARBARO V, et al. Retinitis pigmentosa: genes and disease mechanisms[J]. Curr Genomics, 2011, 12(4): 238-249. DOI:10.2174/138920211795860107 |
| [8] |
SALES M J, SAADI R, ROYER G, et al. Pseudoretinitis pigmentosa caused by congenital rubella (apropos of a case)[J]. Bull Soc Ophtalmol Fr, 1989, 89(1): 185-187. |
| [9] |
BENSON M D, MACDONALD I M. Bilateral uveitis and Usher syndrome: a case report[J]. J Med Case Rep, 2015, 9: 60. DOI:10.1186/s13256-015-0534-7 |
| [10] |
CARBONI G, FORMA G, BOND A D, et al. Bilateral paraneoplastic optic neuropathy and unilateral retinal compromise in association with prostate cancer: a differential diagnostic challenge in a patient with unexplained visual loss[J]. Doc Ophthalmol, 2012, 125(1): 63-70. DOI:10.1007/s10633-012-9327-0 |
| [11] |
TEMKAR S, MUKHIJA R, VENKATESH P, et al. Pseudo retinitis pigmentosa in a case of missed intraocular foreign body[J]. BMJ Case Rep, 2017, 2017: bcr-2017-220385. DOI:10.1136/bcr-2017-220385 |
| [12] |
VELA J I, MARCANTONIO I, DÍAZ-CASCAJOSA J, et al. Progression of retinal pigmentation mimicking unilateral retinitis pigmentosa after bilateral pars planitis: a case report[J]. BMC Ophthalmol, 2018, 18(1): 242. DOI:10.1186/s12886-018-0814-2 |
| [13] |
WILLERMAIN F, GREINER K, FORRESTER J V. Atypical end-stage birdshot retinochoroidopathy[J]. Ocul Immunol Inflamm, 2003, 11(4): 305-307. DOI:10.1076/ocii.11.4.305.18271 |
| [14] |
SEVGI D D, DAVOUDI S, COMANDER J, et al. Retinal pigmentary changes in chronic uveitis mimicking retinitis pigmentosa[J]. Albrecht Von Graefes Arch Fur Klinische Und Exp Ophthalmol, 2017, 255(9): 1801-1810. DOI:10.1007/s00417-017-3689-7 |
| [15] |
CHEBIL A, EL MATRI L. Retinitis pigmentosa associated with Coats-like fundus[J]. J Fr Ophtalmol, 2016, 39(2): 235-236. DOI:10.1016/j.jfo.2015.09.007 |
| [16] |
TURAN-VURAL E, TORUN-ACAR B, TÜKENMEZ N, et al. Usher syndrome associated with Fuchs' heterochromic uveitis: a case report[J]. Clin Ophthalmol, 2011, 5: 557-559. DOI:10.2147/OPTH.S19525 |
| [17] |
AOKI S, INOUE T, KUSAKABE M, et al. Unilateral pigmented paravenous retinochoroidal atrophy with retinitis pigmentosa in the contralateral eye: A case report[J]. Am J Ophthalmol Case Rep, 2017, 8: 14-17. DOI:10.1016/j.ajoc.2017.08.003 |
| [18] |
POTSIDIS E, BERSON E L, SANDBERG M A. Disease course of patients with unilateral pigmentary retinopathy[J]. Invest Ophthalmol Vis Sci, 2011, 52(12): 9244-9249. DOI:10.1167/iovs.11-7892 |
| [19] |
WELLER J M, MICHELSON G, JUENEMANN A G. Unilateral retinitis pigmentosa: 30 years follow-up[J]. BMJ Case Rep, 2014, 2014: bcr2013202236. DOI:10.1136/bcr-2013-202236 |
| [20] |
MIZOBUCHI K, KATAGIRI S, HAYASHI T, et al. Clinical findings of end-stage retinitis pigmentosa with a homozygous PDE6A variant (p.R653X)[J]. Am J Ophthalmol Case Rep, 2019, 13: 110-115. DOI:10.1016/j.ajoc.2018.12.019 |
| [21] |
GAUVIN M, CHAKOR H, KOENEKOOP R K, et al. Erratum to: Witnessing the first sign of retinitis pigmentosa onset in the allegedly normal eye of a case of unilateral RP: a 30-year follow-up[J]. Doc Ophthalmol, 2016, 132(3): 231. DOI:10.1007/s10633-016-9542-1 |
| [22] |
STROUGO Z, BADOUX A, DUCHANEL D. Psycho-affective problems associated with retinitis pigmentosa[J]. J Fr Ophtalmol, 1997, 20(2): 111-116. |



