临床上,经胸骨正中切口术后形成胸骨切口感染(sternal wound infections, SWI)的发生率可高达3%~5%[1]。根据病情严重情况可分为浅表胸骨切口感染(superficial sternal wound infection, SSWI)及深部胸骨切口感染(deep sternal wound infection, DSWI)。SSWI感染范围包括皮肤、皮下组织、和(或)胸大肌筋膜,死亡率为0.5%~4.4%[2]。DSWI是皮下组织下方的组织或空间的感染,可包含肋软骨炎、胸骨骨髓炎、纵隔炎等,死亡率高达7%~47%[3]。SWI延长了患者的住院时间,增加了患者治疗费用,给患者带来巨大痛苦。目前,国内对SWI的认识还不深刻,治疗方法不统一,很多患者延误了最佳治疗时机。我科于2017年3月到2019年3月收治SWI病人35例,其中SSWI 27例、DSWI 8例。采用整形外科多样化修复重建方法(清创术、负压封闭引流术、皮片移植术、肌瓣转移术)治疗,取得了较好的效果。
1 资料与方法 1.1 一般资料本组病例男性8例,女性27例。年龄范围为17~71岁,中位年龄50岁。病源分布为农村21例,城市14例。身体质量指数(body mass index,BMI)范围为18.8~38.7(kg/m2),其中超重及肥胖(BMI≥24)为20例。患者经胸骨正中切口术后形成切口感染至再次入院就诊时间范围为7~1 460 d,其中超过30 d的病例数为25。患者均可见不同严重程度的创面或窦道,大小范围为0.5 cm×1.0 cm~12.0 cm×3.0 cm,其中创面或窦道位于胸骨下段16例,胸骨上段14例,累及全胸骨5例。入院后行伤口分泌物培养:金黄色葡萄球菌3例,鲍曼不动杆菌1例、粘质沙雷菌1例、杰氏棒杆菌1例、木糖氧化产碱杆菌1例,其余阴性。本研究得到陆军军医大学第二附属医院伦理委员会批准(审批号:2019-研第037-01)。病例详细信息见表 1。
| 项目 | SWI(n=35) | SSWI(n=27) | DSWI(n=8) |
| 年龄(中位年龄) | 17~71(50) | 17~69(49) | 52~71(63) |
| 女性[例(%)] | 27(72.9) | 21(77.7) | 6(75.0) |
| BMI>24 kg/m2[例(%)] | 20(54.1) | 17(63.0) | 3(37.5) |
| 来源农村[例(%)] | 21(56.7) | 16(59.2) | 5(62.5) |
| 合并基础疾病[例(%)] | |||
| 高血压 | 6(17.1) | 4(14.8) | 2(25.0) |
| 糖尿病 | 7(20.0) | 3(11.1) | 4(50.0) |
| 心功能不全 | 3(8.6) | 2(7.4) | 1(12.5) |
| 原发心脏疾病[例(%)] | |||
| 风湿性心脏病 | 26(70.2) | 19(70.3) | 7(87.5) |
| 先天性心脏病 | 3(8.6) | 3(11.1) | 0(0.0) |
| 主动脉夹层 | 3(8.6) | 3(11.1) | 0(0.0) |
| 冠心病 | 2(5.7) | 1(3.7) | 1(12.5) |
1.2 治疗方法
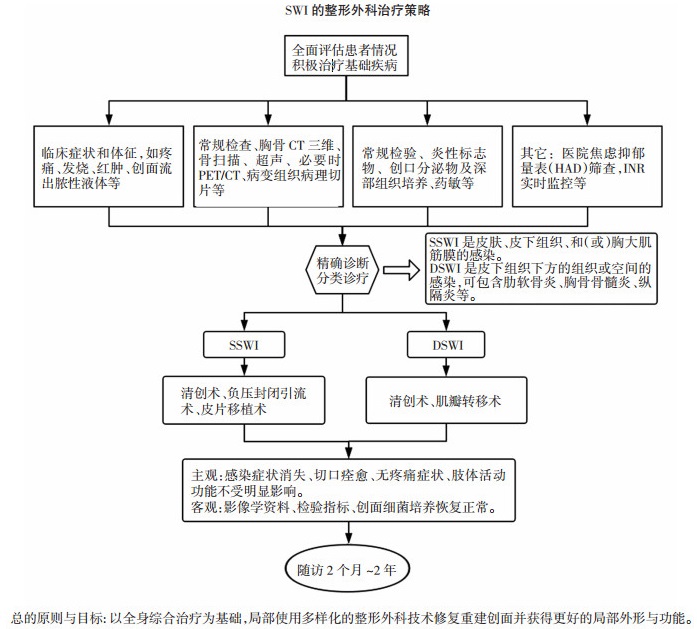
入院后全面评估患者的基本情况,完善必要检查,如胸骨CT及三维重建、全身静态骨扫描,感染区浅表软组织超声等;积极治疗基础疾病;根据创口分泌物培养及药敏试验选择敏感抗生素抗感染;经医院焦虑抑郁量表(hospital anxiety and depression scale,HADS)评估后,对具有焦虑抑郁情绪的患者进行积极的专科干预。人工瓣膜置换术后瓣膜及附近易发生血液聚集、凝固,形成血栓,影响瓣膜功能,严重者将危及生命。在治疗创面感染的同时,做好患者的抗凝和抗血小板治疗不仅有益患者预后,同时对手术时机选择也具有重要的指导意义。患者服用华法林期间,其人工瓣膜置换后凝血酶原时间维持在健康人的1.5~2.5倍,凝血酶原时间的国际化标准比值(international normalized ratio, INR)控制在1.8~3.0,其中行主动脉瓣置换术的患者控制在1.8~2.2,行人工二尖瓣置换术的患者控制在2.0~2.5,行人工三尖瓣置换术的患者控制在2.5~ 3.0。结合临床实践,我们制定了SWI的整形外科治疗策略(图 1)。
|
| 图 1 SWI的整形外科治疗策略 |
1.2.1 浅表胸骨切口感染(SSWI)的治疗
SSWI只涉及表浅的组织感染,主要采用负压封闭引流术。充分保护正常组织的前提下清除创面所有可见坏死组织(皮肤、肌肉等),并使用生理盐水充分清洗,遵循从创面中心向周围、从污染最少清洗到污染最严重的顺序,尽量减少消毒剂直接接触创面。清创后根据创面的大小选择合适的敷料,适当修整使其与创面充分贴合,根据病情选择中心负压或便携式负压装置。创面环境清洁干燥时,可选择间断负压模式促进创面的血液循环,压力范围为-60~-80 mmHg;创面脓性分泌物较多时,可选择持续负压及时排除分泌物,压力范围为-80~-120 mmHg;5~10 d更换负压材料,根据引流液的性质、量及创面情况决定是否继续使用。负压封闭引流术备好创基可直接缝合,若创面较大无法直接缝合,则使用皮片移植术覆盖创面。
1.2.2 深部胸骨切口感染(DSWI)的治疗对于感染严重、病灶累积层次较深的DSWI患者,主要方法为肌瓣转移术。以胸大肌肌瓣转移术为例,常规全身麻醉,沿胸骨正中原手术切口扩大切除瘢痕,去除感染组织及异物,彻底清除病灶,包括感染的胸骨及肋软骨、固定胸骨的钢丝、缝线、骨蜡等。使用大量的生理盐水、过氧化氢溶液冲洗创面,并更换手术器械及相关物品。彻底清创后,沿切口一侧胸大肌肌膜浅层游离皮下组织,根据创面缺损范围离断所需胸大肌,翻转胸大肌并于其深面游离形成肌瓣。在此过程中注意保护胸骨旁1.5 cm处的肌瓣营养血管蒂,并将肌瓣填塞至缺损区。肌瓣供区需准确止血,并放置引流管。关闭创面时,可用10号线将肌瓣固定并在对侧皮缘外侧打结,结下衬垫纱布减张,并置引流管于肌瓣下方,术后拆线可减少缝线残留,降低感染风险。4号线缝合皮肤切口,弹力绷带或胸带适当的加压包扎。术后3~5 d引流量 < 15 mL/24 h时,可拔出引流管。
2 结果 2.1 疗效分析27例SSWI患者平均更换负压封闭引流装置3次,其中22例切口直接缝合后Ⅰ期愈合,3例经皮片移植覆盖后愈合,2例未治愈出院,在院治疗时间范围为5~126 d,平均治疗时间57 d,治愈率92.6%。8例DSWI患者均采用了不同类型的肌瓣转移术,其中7例出院时切口Ⅰ期愈合,供区肢体活动不受明显影响,1例切缘皮肤部分坏死,积极处理后痂下愈合,在院治疗时间范围为10~96 d,平均治疗时间32 d,治愈率100%。所有患者随访2月至2年病情未复发。
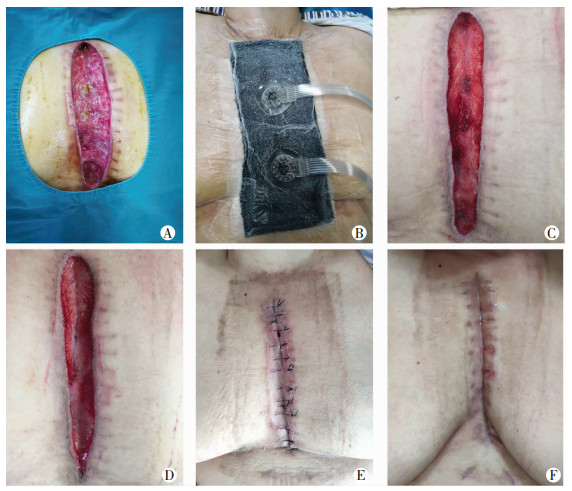
2.2 典型病例分析患者1,女性,48岁,因风湿性心脏病二尖瓣狭窄于心外科行人工二、三尖瓣植入术后胸骨切口感染20 d收入我科。患者胸骨正中可见纵行约20 cm×3 cm创面,深约1 cm,创面中上段可见两根外露钢丝,创面累及皮肤及皮下组织。创面分泌物培养为金黄色葡萄球菌。入院完善检查后诊断为SSWI,予以创面清创术联合负压封闭引流术,更换两次负压后创面缩小、肉芽组织新鲜,遂4号线缝合残余创面,适当加压包扎。术后创面Ⅰ期愈合出院,随访3个月,病情无复发,见图 2。
|
| A:人工二尖瓣植入术后20 d;B:负压封闭引流术;C;第一次负压封闭引流术后;D:第二次负压封闭引流术后;E:直接缝合术后;F:出院创面Ⅰ期愈合 图 2 清创术联合负压封闭引流术治疗SSWI及随访 |

|
| A:人工二尖瓣植入术后1月余;B:胸骨CT三维重建;C:彻底清创后创面;D:感染组织(胸骨、肋软骨、软组织)及异物(缝线、钢丝);E:游离完毕的右侧胸大肌肌瓣;F:术后即刻;G:术后1月 图 3 胸大肌肌瓣转移术治疗DSWI及随访 |
患者2,女性,57岁,因风湿性心脏病二尖瓣狭窄于心外科行人工二尖瓣植入术,术后胸骨切口感染1月余收入我科。糖尿病病史4年,胸骨下端可见约4 cm×2 cm创面,深度约2 cm,挤压可见白色黏稠液流出,创缘周围红肿,触痛明显。创面分泌物培养阴性。入院完善检查后诊断为DSWI,遂行胸大肌肌瓣转移术。常规全身麻醉后,沿原切口切除瘢痕及创面组织,咬除病变胸骨,去除钢丝、缝线等异物。术区可见白色黏稠液沿肋间隙流出,双侧第5、6、7、肋软骨呈虫蚀样改变甚至消失,遂沿肋弓做“人”字形切口,清除感染的肋软骨至正常。使用大量的生理盐水、过氧化氢溶液彻底冲洗创面,沿切口游离右侧胸大肌肌瓣,翻转填塞于缺损处。置负压吸引管于肌瓣供区和肌瓣深面,10号线固定肌瓣填塞缺损,对侧皮缘外侧打结并用纱布衬垫于结下减张。4号线缝合切口,适当加压包扎。术后切口Ⅰ期愈合,随访3个月,病情未复发。
3 讨论虽然近期国内外文献讨论了SWI的流行病学、危险因素、诊断以及手术和抗菌管理,但胸骨切口感染的诊疗却没有统一的指南[4]。复杂的病情需要由心胸外科、整形外科、重症医学科、临床微生物室等多学科团队的参与诊疗[5]。传统的SWI治疗方法是反复清创和定期换药。这种方法效率低,住院时间长,费用负担大,往往不利于创面愈合。综合国内外的临床研究进展,本研究团队通过危险因素的规避、客观检查指标的引导、个性化序贯性的整形外科修复重建方案的建立,以及术后定期的随访分析,建立完善的诊疗体系,减少患者住院时间,提高患者的治愈率。
临床回顾性分析发现,SWI的患者相关危险因素主要包括年龄、肥胖、胰岛素依赖性糖尿病、吸烟、慢性阻塞性肺病、外周血管疾病;术中危险因素是急诊手术、使用双侧胸廓内动脉、大量出血、大量使用骨蜡等;围手术期危险因素是机械通气时间延长、使用主动脉内球囊反搏、再次开胸手术等[6]。对SWI的诊断与分类认同较多的是将SSWI定义为只涉及皮肤、皮下组织、和(或)胸大肌筋膜的感染,无骨质感染。DSWI定义为以下任意一条表现:(1)从纵隔组织或胸腔液体培养分离到病原微生物;(2)术中发现纵隔炎的存在;(3)存在胸痛,胸骨松动或裂开,发热(超过38 ℃),纵隔引出脓性分泌物并在血培养中找到病原微生物,或纵隔区域组织中找到病原体[7-8]。SWI病程漫长,尤其是DSWI治疗难度大,花费多,很多患者延误最佳治疗时机,如果在急性期不加以充分治疗,严重时将可能导致患者死亡。故早期诊断并制定合理的诊疗计划显得非常重要。临床诊断主要通过临床症状和体征,大多数SWI患者通常在心脏手术后30 d内出现,症状通常包括低烧、炎症标志物水平升高、切口红肿、流出脓性液体等[8]。辅助检查包括计算机断层扫描及胸骨三维重建、磁共振成像、正电子发射断层扫描、超声、创口分泌物培养等[4, 9]。在治疗方面,自临床上开始使用不同的皮瓣修复胸骨切口感染以来,胸骨切口感染的治疗方法也在逐步改进[10]。国内刘吉福等[11]使用胸大肌瓣翻转、伤口内无异物存留技术成形治疗胸骨切口深部感染取得了良好的效果。总的治疗原则包括感染灶的清创,充分引流和使用肌瓣、肌皮瓣等组织修复,药敏指导下的抗生素治疗等[7]。我们认为在明确SWI诊断后,应尽早清创,彻底清除创面及创缘失活的软组织、骨组织、分泌物、暴露的缝线或钢丝等。早期的彻底清创,是治疗的关键,同时早期清创并充分引流也是预防SSWI进一步发展为DSWI的主要原则。
SWI实质是复杂的难治性创面,我科作为全院的“创面修复中心”,承担着创面的修复重建工作。针对SWI,整形外科常用修复重建技术主要包括清创术、负压封闭引流术、皮片移植术、肌瓣转移术等。负压封闭引流技术是使用特殊医用敷料覆盖或填充创面,生物半透膜封闭后使用引流管连接负压源,通过负压吸引治疗创面。负压封闭引流技术可以持续性的改善创面的微循环情况,减轻组织水肿,促进创基的肉芽生长,排除创面产生的感染代谢产物,为下一步手术修复创面提供良好的创基准备[12]。同时负压封闭引流术操作简单,安全易行,危重症患者可优先考虑。皮片移植术主要用于不能直接缝合的浅表创面,其作用可靠、创伤小、花费少,必要时可重复进行,临床治疗效果良好。肌瓣具有良好的血液供应和抗感染能力,适用于治疗深部感染或软组织缺损[13]。DSWI由于感染病灶深,大多数患者彻底清创后都会留下很大的创面与组织缺损,用于重建创面最常见的是胸大肌肌瓣。根据清创后缺损的位置可以选择不同的修复方案,胸大肌肌瓣修复胸骨上段,腹直肌肌瓣修复下段,两者联合可以修复整段胸骨甚至更大面积的缺损[10]。必要时使用钛板稳定胸骨,重建胸壁,同时使用有效的抗生素对症支持[14]。
虽然针对SWI的诊疗,整形外科治疗策略取得了良好的效果,但本研究为回顾性研究,故需要进一步的多中心、大数据的前瞻性临床研究制定临床规范,以确定SWI的最佳诊疗措施。在临床工作中,更需要多科室的联合协作,有效避免SWI危险因素,从源头上遏制疾病的发生发展,并建立起完善规范的SWI诊疗体系。
| [1] |
TEWARIE L, CHERNIGOV N, GOETZENICH A, et al. The effect of ultrasound-assisted debridement combined with vacuum pump therapy in deep sternal wound infections[J]. Ann Thorac Cardiovasc Surg, 2018, 24(3): 139-146. DOI:10.5761/atcs.oa.17-00244 |
| [2] |
CHAN M, YUSUF E, GIULIERI S, et al. A retrospective study of deep sternal wound infections: clinical and microbiological characteristics, treatment, and risk factors for complications[J]. Diagn Microbiol Infect Dis, 2016, 84(3): 261-265. DOI:10.1016/j.diagmicrobio.2015.11.011 |
| [3] |
KOTNIS-GASKA A, MAZUR P, OLECHOWSKA-JARZAB A, et al. Sternal wound infections following cardiac surgery and their management: a single-centre study from the years 2016-2017[J]. Pol J Cardio Thorac Surg, 2018, 15(2): 79-85. DOI:10.5114/kitp.2018.76472 |
| [4] |
COTOGNI P, BARBERO C, RINALDI M. Deep sternal wound infection after cardiac surgery: Evidences and controversies[J]. World JCrit Care Med, 2015, 4(4): 265-273. DOI:10.5492/wjccm.v4.i4.265 |
| [5] |
YUSUF E, CHAN M, RENZ N, et al. Current perspectives on diagnosis and management of sternal wound infections[J]. Infect Drug Resist, 2018, 11: 961-968. DOI:10.2147/IDR.S130172 |
| [6] |
MESZAROS K, FUEHRER U, GROGG S, et al. Risk factors for sternal wound infection after open heart operations vary according to type of operation[J]. Ann Thorac Surg, 2016, 101(4): 1418-1425. DOI:10.1016/j.athoracsur.2015.09.010 |
| [7] |
LAZAR H L, SALM T V, ENGELMAN R, et al. Prevention and management of sternal wound infections[J]. J Thorac Cardiovasc Surg, 2016, 152(4): 962-972. DOI:10.1016/j.jtcvs.2016.01.060 |
| [8] |
ABU-OMAR Y, KOCHER G J, BOSCO P, et al. European association for cardio-thoracic surgery expert consensus statement on the prevention and management of mediastinitis[J]. Eur J Cardiothorac Surg, 2017, 51(1): 10-29. DOI:10.1093/ejcts/ezw326 |
| [9] |
GLAUDEMANS A W, QUINTERO A M, SIGNORE A. PET/MRI in infectious and inflammatory diseases: will it be a useful improvement?[J]. Eur J Nucl Med Mol Imaging, 2012, 39(5): 745-749. DOI:10.1007/s00259-012-2060-9 |
| [10] |
KAMEL G N, JACOBSON J, RIZZO A M, et al. Analysis of immediate versus delayed sternal reconstruction with pectoralis major advancement versus turnover muscle flaps[J]. J Reconstr Microsurg, 2019. DOI:10.1055/s-0039-1688760 |
| [11] |
刘吉福, 高永顺, 李宝成, 等. 肌瓣成形新技术治疗胸骨切口深部感染23例[J]. 中国胸心血管外科临床杂志, 2018, 25(4): 321-324. LIU J F, GAO Y S, LI B C, et al. New technique of pectoral muscle flap reconstruction for 23 patients with deep sternal wound infections[J]. Chin J Clin Thorac Cardiovasc Surg, 2018, 25(4): 321-324. |
| [12] |
KIM P J, ATTINGER C E, STEINBERG J S, et al. Negative-pressure wound therapy with instillation: international consensus guidelines[J]. Plast Reconstr Surg, 2013, 132(6): 1569-1579. DOI:10.1097/PRS.0b013e3182a80586 |
| [13] |
SHI Y D, QI F Z, ZHANG Y. Treatment of sternal wound infections after open-heart surgery[J]. Asian J Surg, 2014, 37(1): 24-29. DOI:10.1016/j.asjsur.2013.07.006 |
| [14] |
LIMA SÁNCHEZ J, SÁNCHEZ MEDINA M T, GARCÍA DUQUE O, et al. Chronic sternoclavicular osteomyelitis: Salvage surgery with internal mammary artery perforator flap[J]. Cir Esp, 2015, 93(2): 129-131. DOI:10.1016/j.ciresp.2013.01.020 |



