长期处于社会压力影响下的人群会产生兴趣缺失、焦虑等行为学的改变[1-2]。社交挫败动物模型(social defeat model)是模拟人类在正常交往中遇到挫折和孤立无助的情景,让攻击性CD-1小鼠对C57小鼠进行短暂的攻击,并让C57小鼠长期处于攻击性CD-1小鼠的威胁和恐惧当中,给C57小鼠造成一种类似于人类的心理压力[3]。小鼠重复地暴露在社交失败的压力下就会引起明显的以兴趣缺乏、焦虑和社交回避行为为特点的抑郁样表现[4-7]。该抑郁模型在发病诱因上充分模拟人类精神和心理疾病病因,得出与人类相似的行为学表现,所以与人类疾病具有较高的一致性,对于研究人类精神和心理疾病是一个比较理想的动物模型。但该模型在建模过程中只是要求C57小鼠每天被筛选过的攻击鼠攻击5~10 min, 并未有应激量的量化和评价方法, 明确划分不同的应激量有助于探讨不同应激量对小鼠抑郁样行为的影响,因此,本文在进行建模时通过控制攻击时间、逃避空间以及直接比较被攻击强度与抑郁样行为相关性3种方式控制或观察应激量,最后比较何种方法可以更有效地区分不同应激量对抑郁样行为的影响,为之后关于应激量和不同抑郁程度的研究提供可以借鉴的方法。
不同的应激量可能会对抑郁样行为产生不同的影响,但奖赏可以缓冲应激造成的损害,降低小鼠抑郁样行为的发生。有研究表明每天喝糖水或接受性伴侣2周后进行束缚应激的小鼠,促肾上腺皮质激素、皮质酮的分泌和心率都会显著降低[8],同时还可以降低应激引起的下丘脑-垂体-肾上腺素轴(HPA轴)反应[9]。在另一项实验中,在2周内给予奖赏食物的斑马鱼与对照组相比,它们生理应激反应和焦虑样行为更低[10],但在进行慢性社交挫败建模过程中给予奖赏对抑郁样行为的作用尚不清楚,且奖赏在不同应激量下发挥的作用也需探明。因此在确定了社交挫败模型中定义应激量的方法后,在建模时将给予雌性C57小鼠陪伴作为奖赏,明确奖赏对抑郁样行为的影响并比较奖赏在不同应激量下的作用,为通过奖赏来预防和治疗抑郁提供新的思路。
1 材料与方法 1.1 材料 1.1.1 动物从陆军军医大学大坪医院动物中心订购6~8周清洁级(SPF级)雄性C57BL/6J小鼠和3~6月龄CD-1小鼠,按照实验动物饲养和管理要求,为实验动物提供恒温、恒湿的条件,温度维持在22~26 ℃,湿度为(50 ± 5)%;为其提供干燥清洁的木屑垫料并定期更换,保证充足的食物和饮用水,每天给予12 h的日光灯照明(7:00-19:00)。
1.1.2 主要试剂与仪器行为跟踪分析系统购自美国ANY-maze公司,社会交互、强迫游泳设备购自瑞沃德公司。蔗糖购自Sigma公司,酒精购自四川科伦药业股份有限公司。
1.2 建立慢性社交挫败抑郁模型建模正式开始前3 d筛选攻击鼠,将C57小鼠放入攻击鼠CD-1的笼子里,观察180 s内CD-1小鼠对C57的攻击情况,连续3 d发起攻击且每天攻击潜伏期少于30 s的CD-1小鼠为合格的攻击鼠,用于正式建模。建模持续21 d,每天将C57小鼠放入CD-1小鼠的隔间里,CD-1小鼠通常会攻击C57小鼠(表现为追逐、理毛和撕咬,即生理应激),5~10 min后将C57小鼠放入CD-1小鼠的邻近隔间,让其在每天剩余的时间可以看到和嗅到CD-1小鼠(即心理应激)。为了避免C57小鼠对攻击者适应,每天都将C57小鼠暴露于1个新的攻击者隔间,直到建模结束。建模过程中每天测量C57小鼠的体质量,观察其状态[11]。
由于该模型在建模过程中只是要求C57小鼠每天被筛选过的攻击鼠攻击5~10 min,并未有应激量的量化和评价方法,为探讨在社交挫败建模时如何确定应激量的大小,分别通过以下3种方式建模:直接比较被攻击强度与抑郁样行为的相关性(n=8);控制攻击时间,大应激量组每天被攻击10 min(n=6),小应激量组每天被攻击5 min(n=6), 对照组没有被攻击(n=6);控制逃避空间,大应激量组每天在294 mm×190 mm×125 mm的小笼子中被攻击(n=6),小应激量组每天在475 mm×350 mm×200 mm的大笼子中被攻击(n=6),对照组没有被攻击(n=6),为明确奖赏在不同应激量下的作用,在确定划分应激量大小的方法后,将雄性C57BL/6J小鼠随机分为小应激量奖赏组、小应激量无奖赏组、大应激量奖赏组、大应激量无奖赏组和对照组,每组8只。奖赏组和无奖赏组均在不同应激量下进行社交挫败建模,对照组没有被攻击,给予奖赏组每只雄性C57BL/6J小鼠1只雌性9~12周龄C57BL/6J小鼠陪伴24 h作为奖赏[8],比较在不同应激量下有无奖赏对抑郁样行为的影响。
1.3 行为学检测 1.3.1 社会交互测试分两个阶段完成,每个阶段2.5 min。第一个阶段在社会交互区放入空笼子,第二个阶段将攻击性较强的CD-1小鼠放到社会交互区中的笼子里,记录C57小鼠在社会交互区、角落区停留的时间和运动轨迹。分别计算社会交互区和角落区的社会交互指数,即第二阶段在社会交互区或角落区停留的时间与第一阶段停留时间的比值。
1.3.2 糖水偏好测试用于评估抑郁样行为中的快感缺乏水平,建模结束后,给C57提供2个装有自来水的瓶子喝水,让其适应双瓶24 h,24 h后将其中1个自来水瓶子换成装有1%糖水的瓶子,每天调换2个水瓶位置1次,并测量其质量,防止位置偏好带来的误差。糖水消耗量在总液体消耗量中所占的比例,作为衡量糖水偏好的指标。
1.3.3 强迫游泳测试最后一次糖水偏好测试完毕后即可进行强迫游泳测试,强迫游泳被用于检验抑郁样行为中的绝望行为。测试时,将C57小鼠放入透明柱形桶内(高50 cm,直径11 cm),桶内水位高17 cm [水温(25±1)℃],测试下1只小鼠前要换水。用摄像机录下6 min测试,计算后4 min内小鼠在水中静止不动的时间以及开始静止不动的潜伏期,静止定义为漂浮或为了保持头部抬出水面而小幅度划水。
1.4 统计学分析采用SPSS 22.0统计软件,计量资料以 ±s表示,两组间比较采用t检验,多组比较使用单因素方差分析,事后检验采用Dennett’s检验比较两组之间的差异。P < 0.05视为差异有统计学意义。
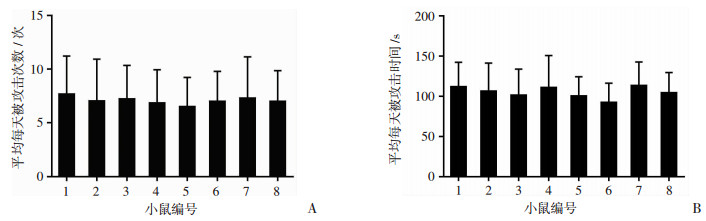
2 结果 2.1 比较被攻击强度与抑郁样行为的相关性采用直接建模的方法,建模完成后比较被攻击强度与抑郁样行为的相关性。结果发现:每只小鼠平均每天被攻击的次数和时间差异无统计学意义,无法区分开不同的应激量(图 1)。表明该方法无法很好地区分开不同应激量, 使用该方法探讨不同应激量对抑郁样行为的影响具有一定的局限性。
|
| 图 1 小鼠平均每天被攻击的次数(A)和时间(B) |
2.2 控制攻击时间确定不同应激量对小鼠抑郁样行为的影响
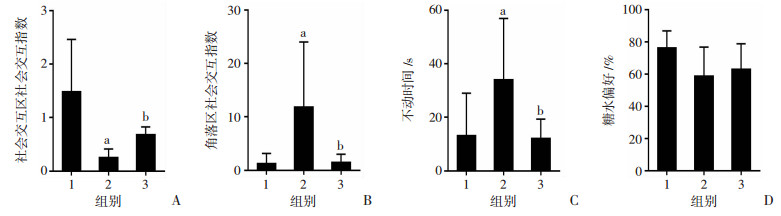
采用控制每天被攻击的时间来确定应激量,结果发现:小应激量组、大应激量组及对照组在社会交互区的社会交互指数(P=0.333)、角落区的社会交互指数(P=0.372)、强迫游泳不动时间(P=0.209)和糖水偏好(P=0.205)方面差异均无统计学意义(图 2)。表明该方法无法很好地区分不同应激量, 不适宜用于比较不同应激量对抑郁样行为的影响。

|
| 1:对照组;2:大应激量组;3:小应激量组A:社会交互区的社会交互指数; B:角落区的社会交互指数; C:强迫游泳不动时间; D:糖水偏好 图 2 控制攻击时间对不同应激量组小鼠抑郁样行为的影响 |
2.3 控制逃避空间确定不同应激量对小鼠抑郁样行为的影响
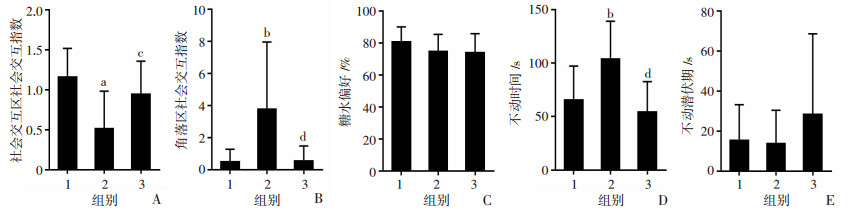
采用控制逃避空间的方法以确定应激量,结果发现:大应激量组在社会交互区的社会交互指数显著低于小应激量组和对照组(P < 0.05),而在角落区的社会交互指数显著高于小应激量组和对照组(P < 0.01);大应激量组强迫游泳的不动时间显著高于小应激量组和对照组(P < 0.05);糖水偏好各组间差异无统计学意义(P=0.190,图 3)。表明通过控制逃避空间确定应激量可以很好地比较不同应激量对抑郁样行为的影响。
|
| 1:对照组;2:大应激量组;3:小应激量组;a: P < 0.05,与对照组比较; b: P < 0.05,与大应激量组比较A:社会交互区的社会交互指数;B:角落区的社会交互指数;C:强迫游泳不动时间;D:糖水偏好 图 3 控制逃避空间对不同应激量组小鼠抑郁样行为的影响 |
2.4 奖赏对不同应激量造成的小鼠抑郁样行为的改善作用
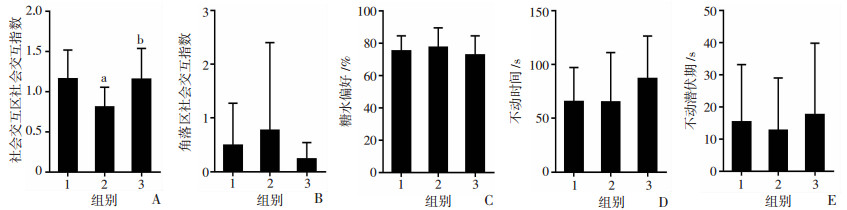
采用控制逃避空间定义应激量的大小,并在建模过程中将给予9~12周龄雌性C57小鼠陪伴作为奖赏。结果发现:在大应激量下,与对照组相比,无奖赏组社会交互区的社会交互指数显著降低(P < 0.001)、角落区的社会交互指数(P < 0.05)和强迫游泳不动时间(P < 0.05)显著增高,奖赏组社会交互区社会交互指数(P < 0.01)显著高于无奖赏组、角落区社会交互指数(P < 0.05)和强迫游泳不动时间(P < 0.05)则显著低于无奖赏组。糖水偏好和强迫游泳不动潜伏期各组间差异不明显。提示在大应激量下,奖赏可以显著降低小鼠抑郁样行为(图 4)。
|
| 1:对照组;2:无奖赏组;3:奖赏组;a: P < 0.01,b: P < 0.05,与对照组比较; c: P < 0.01,d: P < 0.05,与无奖赏组比较; A:社会交互区的社会交互指数B:角落区的社会交互指数C:糖水偏好;D:强迫游泳不动时间E:强迫游泳不动潜伏期 图 4 奖赏对大应激量下小鼠抑郁样行为的影响 |
在小应激量下,只有在社会交互区的社会交互指数方面,无奖赏组显著低于对照组(P < 0.05),且奖赏组显著高于无奖赏组(P < 0.05),其他行为学指标各组间差异无统计学意义。提示在小应激量下,奖赏降低了小鼠的社会回避行为(图 5)。
|
| 1:对照组;2:无奖赏组;3:奖赏组; a: P < 0.05,与对照组相比; b: P < 0.05,与无奖赏组相比; A:社会交互区的社会交互指数B:角落区的社会交互指数; C:糖水偏好;D:强迫游泳不动时间; E:强迫游泳不动潜伏期 图 5 奖赏对小应激量下小鼠抑郁样行为的影响 |
2.5 奖赏对大应激量下小鼠抑郁样行为的改善作用更为明显
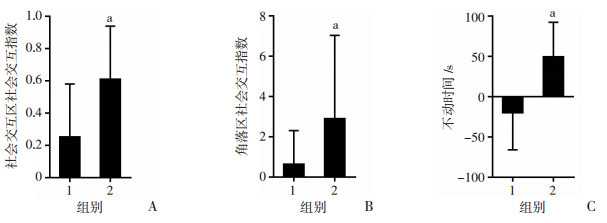
比较在不同应激量下奖赏组与无奖赏组之间各行为学指标的差值,结果发现:在社会交互区的社会交互指数(t=2.360, P=0.036)、角落区的社会交互指数(t=2.111, P=0.048)以及强迫游泳的不动时间(t=3.376, P=0.003)方面,奖赏组在大应激量下与无奖赏组的差值更大,对应激造成的抑郁样行为的恢复作用更明显(图 6)。
|
|
1:小应激量组;2:大应激量组;a: P < 0.05, 与小应激量组比较 A:奖赏组与无奖赏组在社会交互区的社会交互指数差值; B:奖赏组与无奖赏组在角落区的社会交互指数差值; C:奖赏组与无奖赏组强迫游泳不动时间的差值 图 6 奖赏在不同应激量下对小鼠抑郁样行为的影响 |
3 讨论
虽然社交挫败模型作为一种成熟的抑郁动物模型,已被广泛应用于抑郁、焦虑等精神障碍疾病病理研究中,但通过怎样的方式定义应激量还未有系统的研究。本研究参照GOLDEN等[11]介绍的方法建立模型,并在建模过程中通过3种方式确定应激量的大小,比较何种方式更能够合理地区分开大小应激量,且易于控制,干扰因素最小,可行性强。结果发现第一种方法即根据被攻击次数和时间定义应激量理论上是最理想的方法,但在实际操作中由于CD-1小鼠均是经过筛选的攻击鼠,所以平均每天被攻击的次数和时间非常接近,无法区分开不同应激量。第二种方法控制每天被攻击的时间定义应激量,发现每天被攻击5 min和10 min对抑郁样行为的影响差异不明显,这可能是由于在建模时,攻击鼠都是最开始的几分钟攻击性最强,后面在适应了小鼠的闯入或小鼠表现出投降不动的行为后则攻击性减弱,所以用控制攻击时间的方法也无法很好地区分不同的应激量。第三种方法,控制逃避空间来定义应激量对小鼠的社会交互指数和强迫游泳的不动时间均产生显著影响,可能是由于在小笼子中,小鼠的逃避空间更小,更容易被CD-1小鼠攻击到,而在大笼子中,小鼠更容易从CD-1小鼠的攻击中逃脱。因此,在之后进行有关应激量的研究时,可以采用控制逃避空间的方法来定义应激量。
应激是抑郁发生和发展的重要危险因素,但不同应激量对小鼠抑郁样行为的影响还有待探讨。在一项关于转基因小鼠的研究中讨论了应激量对抑郁样行为的影响,结果发现不同应激量会对转基因小鼠造成不同程度的抑郁样行为,但野生型(WT)小鼠并未出现该现象[12]。在本研究中,通过合理的定义应激量,发现在野生型小鼠中,大应激量比小应激量造成的抑郁样行为更明显,尤其是社会回避行为。这提示要关注不同应激量对心理健康的影响,且在人类的日常生活中,对应激量的评价更加复杂,有研究根据对1 755名受访者的访谈表明,慢性应激(被定义为持续压力超过12个月)比急性应激更能预测抑郁症状[13]。这提示在日常的生活中,不仅要关注那些比较强烈的急性应激,更应该关注那些虽然微小但持续时间很长的小应激,这些应激很容易被忽视,但却会对我们的心理健康造成持续严重的危害。在临床抑郁症的诊断和治疗中,也应该考虑慢性应激的重要影响。
已有研究表明奖赏对应激造成的损伤具有缓冲作用,在人类中,奖赏的经历可以减少个体由童年创伤和近期压力生活事件引起的情绪障碍[14],短暂暴露在奖赏刺激下(例如色情图像)会减缓随后的皮质醇反应,并提高在压力下解决问题的能力[15]。在动物实验研究中也证实奖赏可以减少小鼠的应激反应和抑郁样行为。已有研究使用慢性社交挫败应激模型探讨奖赏与应激耐受性和抑郁样行为之间的关系,但主要是利用该模型探讨社交挫败模型对乙醇奖赏[16-17]或药物奖赏的影响[18];在社交挫败模型过程中给予奖赏,观察奖赏对抑郁样行为的影响的研究还鲜见报道。本研究在不同应激量的范式下,在社交挫败应激过程中给予奖赏,发现无论是在何种应激量下,奖赏都在一定程度上降低了抑郁样行为,尤其是社会回避行为。
为探讨奖赏在不同应激量下的作用,本研究在不同应激量下建模时,给予雌性鼠陪伴作为奖赏,发现奖赏在大应激量下发挥的作用更大,对抑郁样行为的改善作用更明显。但在临床抑郁症的治疗过程中,抑郁程度越严重的患者对抗抑郁药的反应越差[19],似乎本研究的结果与临床现象并不一致,分析其原因发现这或许是由于本研究中小应激量本身造成的抑郁样行为较轻,奖赏发挥作用的空间较小,而大应激量虽然造成的抑郁样行为较重,但奖赏依然可以改善其造成的抑郁样行为,这提示在临床中抑郁严重程度与对抗抑郁药的反应可能并不只是简单的负相关。奖赏在临床上对抑郁程度较重患者的作用,可以作为今后进一步研究的课题。
综上所述,本研究通过比较三种定义应激量方法的建模效果,确定了在社交挫败模型中区分应激量大小的有效方法,并通过科学的定义应激量阐明了不同应激量对抑郁样行为的影响,以及奖赏在不同应激量下发挥的作用。为之后探索不同应激量的影响提供依据,同时,关于奖赏和应激量的关系的研究结果也为抑郁症的预防和治疗提供新的思路。但本研究尚缺乏行为学表现的神经生物机制研究,未来可进一步进行奖赏影响不同应激量下抑郁样行为的机制研究,以探明奖赏和应激对抑郁的共同作用机制。
| [1] |
BRAIN P F. Mammalian behavior and the adrenal cortex. A review[J]. Behav Biol, 1972, 7(4): 453-477. |
| [2] |
FUCHS E, FLVGGE G. Social stress in tree shrews: effects on physiology, brain function, and behavior of subordinate individuals[J]. Pharmacol Biochem Behav, 2002, 73(1): 247-258. DOI:10.1016/s0091-3057(02)00795-5 |
| [3] |
TOYODA A. Social defeat models in animal science: What we have learned from rodent models[J]. Nihon Chikusan Gakkaiho, 2017, 88(7): 944-952. DOI:10.1111/asj.12809 |
| [4] |
RYGULA R, ABUMARIA N, FLVGGE G, et al. Anhedonia and motivational deficits in rats: impact of chronic social stress[J]. Behav Brain Res, 2005, 162(1): 127-134. DOI:10.1016/j.bbr.2005.03.009 |
| [5] |
RYGULA R, ABUMARIA N, DOMENICI E, et al. Effects of fluoxetine on behavioral deficits evoked by chronic social stress in rats[J]. Behav Brain Res, 2006, 174(1): 188-192. DOI:10.1016/j.bbr.2006.07.017 |
| [6] |
KUDRYAVTSEVA NN, BAKSHTANOVSKAYA I V, KORYAKINA L A. Social model of depression in mice of C57BL/6J strain[J]. Pharmacol Biochem Behav, 1991, 38(2): 315-320. DOI:10.1016/0091-3057(91)90284-9 |
| [7] |
BERTON O. Essential role of BDNF in the mesolimbic dopamine pathway in social defeat stress[J]. Science, 2006, 311(5762): 864-868. DOI:10.1126/science.1120972 |
| [8] |
ULRICH-LAI Y M, CHRISTIANSEN A M, OSTRANDER M M, et al. Pleasurable behaviors reduce stress via brain reward pathways[J]. Proc Natl Acad Sci U S A, 2010, 107(47): 20529-20534. DOI:10.1073/pnas.1007740107 |
| [9] |
ULRICH-LAI Y M, OSTRANDER M M, THOMAS I M, et al. Daily limited access to sweetened drink attenuates hypothalamic-pituitary-adrenocortical axis stress responses[J]. Endocrinology, 2007, 148(4): 1823-1834. DOI:10.1210/en.2006-1241 |
| [10] |
MANUEL R, ZETHOF J, FLIK G, et al. Providing a food reward reduces inhibitory avoidance learning in zebrafish[J]. Behav Processes, 2015, 120: 69-72. DOI:10.1016/j.beproc.2015.08.013 |
| [11] |
GOLDEN S A, COVINGTON H E 3rd, BERTON O, et al. A standardized protocol for repeated social defeat stress in mice[J]. Nat Protoc, 2011, 6(8): 1183-1191. DOI:10.1038/nprot.2011.361 |
| [12] |
BARTOLOMUCCI A, CAROLA V, PASCUCCI T, et al. Increased vulnerability to psychosocial stress in heterozygous serotonin transporter knockout mice[J]. Dis Model Mech, 2010, 3(7/8): 459-470. DOI:10.1242/dmm.004614 |
| [13] |
MCGONAGLE K A, KESSLER R C. Chronic stress, acute stress, and depressive symptoms[J]. Am J CommunityPsychol, 1990, 18(5): 681-706. |
| [14] |
GESCHWIND N, PEETERS F, JACOBS N, et al. Meeting risk with resilience: high daily life reward experience preserves mental health[J]. Acta Psychiatr Scand, 2010, 122(2): 129-138. DOI:10.1111/j.1600-0447.2009.01525.x |
| [15] |
CRESWELL J D, DUTCHER J M, KLEIN W M, et al. Self-affirmation improves problem-solving under stress[J]. PLoS One, 2013, 8(5): e62593. DOI:10.1371/journal.pone.0062593 |
| [16] |
MACEDO G C, MORITA G M, DOMINGUES L P, et al. Consequences of continuous social defeat stress on anxiety- and depressive-like behaviors and ethanol reward in mice[J]. Horm Behav, 2018, 97: 154-161. DOI:10.1016/j.yhbeh.2017.10.007 |
| [17] |
KARLSSON C, SCHANK J R, REHMAN F, et al. Proinflammatory signaling regulates voluntary alcohol intake and stress-induced consumption after exposure to social defeat stress in mice[J]. Addict Biol, 2017, 22(5): 1279-1288. DOI:10.1111/adb.12416 |
| [18] |
MONTAGUD-ROMERO S, AGUILAR M A, MALDONADO C, et al. Acute social defeat stress increases the conditioned rewarding effects of cocaine in adult but not in adolescent mice[J]. Pharmacol Biochem Behav, 2015, 135: 1-12. DOI:10.1016/j.pbb.2015.05.008 |
| [19] |
DER-AVAKIAN A, MAZEI-ROBISON M S, KESBY J P, et al. Enduring deficits in brain reward function after chronic social defeat in rats: susceptibility, resilience, and antidepressant response[J]. Biol Psychiatry, 2014, 76(7): 542-549. DOI:10.1016/j.biopsych.2014.01.013 |



