近年来,随着功能影像技术的发展,工作记忆成了神经和心理学研究的热点。工作记忆包括临时的大脑存储和执行复杂的认知任务所必需的信息的集合[1]。它由多个组成过程或阶段组成,例如编码、维护和检索给定的信息等[2]。目前,神经心理学和临床上广泛采用数字工作记忆任务评价认知功能,其中使用最为广泛的是正序和倒序数字广度任务。现已有较多研究报道[3-5],多个脑区参与了工作记忆活动,并且起着重要的作用,最尤为突出的是前额叶皮层。
近红外光谱技术(functional near-infrared spectroscopy,fNIRS)是近年来快速发展起来的一项非侵入光学测量方法。在700~900 nm的近红外光谱范围内,生物组织具有高散射、低吸收的特性,它能够对大脑皮层的脑活动进行实时检测,已经被广泛用于研究认知活动时额叶到颞叶的皮层活动[6-8]。本研究探讨数字记忆脑皮层活动特点,已有的相关脑成像研究发现数字信息的编码、维护和检索的过程中主要激活脑区在前额叶区域,fNIRS正好可以满足本研究的需要[9-11]。另外,与功能性磁共振成像(functional magnetic resonance imaging,fMRI)相比,fNIRS具有使用方便、价格便宜和噪音小的特点,被试可以在一个安静、舒适环境下,在更接近自然、真实的状态下进行脑认知活动。
本研究利用fNIRS技术,对23位受试者的数字正序、倒序记忆以及静息状态下血氧饱和度进行数据采集,分析、处理数字记忆三个阶段(信息编码、信息维护、信息检索)的脑激活及大脑皮层含氧血红蛋白(HbO2)浓度时程变化曲线,探讨数字工作记忆不同阶段的脑神经机制,为深入研究大脑的认知活动机制提供参考数据。
1 资料与方法 1.1 研究对象本研究选取本校在校师生23例,男性10例,女性13例,年龄20~24(22.48±1.24)岁,大学本科学历。被试均为健康右利手,无神经及精神疾病史。试验前均告知被试试验内容和流程,对本研究知情并签署了知情同意书。该研究方案于2016年经第三军医大学医学伦理委员会批准通过。
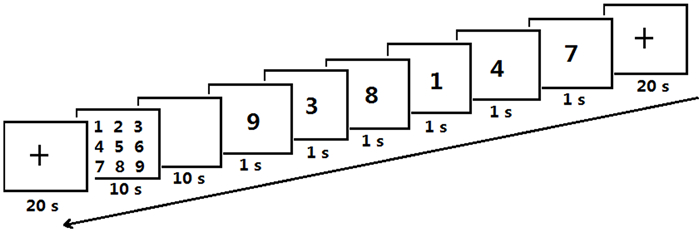
1.2 试验任务采用组块(block)设计,刺激序列编写、刺激呈现、运行并实时记录由Eprime软件完成(图 1)。被试需要分别完成数字正序、倒序记忆两种任务,每种任务6个组块。组块之前是休息期(20 s),显示屏中央显示黑色十字,提示被试做好准备,1个block即将开始;屏幕上随机连续出现6个0~9的数字,每个数字显示1 s,中间没有间隔;数字出现完毕后有10 s的屏幕空白,提示被试整理记忆;然后屏幕出现一系列数字,被试通过单击屏幕上的数字按钮排序(正序/倒序),要求10 s之内完成此任务。记忆任务分为3个阶段:编码期、维持期和检索期,共26 s,数字编码期(第1~6秒)是字母刺激时间;维持期(第7~16秒)是被试静坐回忆时期;检索期(第17~26秒)是被试回忆数字且排序。每名被试在正式试验前要求培训至少30 min以上,确保正确率达到95%以上。
|
| 编码阶段:数字随机以1 s为间隔依次呈现;维持阶段:空白屏幕10 s;检索阶段:10 s内完成屏幕数字排序 图 1 数字记忆试验范式 |
1.3 数据采集
通过NIRScout系统(Medical Technologies, LLC.美国)进行近红外数据采集,近红外探头包括7个光源和8个探测器(图 2),左右共有20个探测通道,源探间距为3 cm,采样频率为3.71 Hz。根据国际10-20系统中F7、F8、FP1和FP2的电极位点将探头置于被试左右两侧前额叶(prefrontal cortex,PFC)。三维数字化定位仪(PATRIOT, Polhemus, Colchester, Vermont, USA)进行通道的三维坐标定位,通过NIRS_SPM软件(http//www.fil.ion.ucl.ac.uk/spm/)空间配准,产生通道的分布及MNI坐标如表 1和图 3所示。

|
| 红色实心圆球S:光源;绿色实心圆球D:探测器; 光源和探测器之间紫色的连线:光学探测通道; L:大脑左侧;R:大脑右侧;数字表示国际10-20系统头皮脑电图电极位置 图 2 双侧大脑PFC光源探测器布局 |
| 通道 | 布罗德曼分区 | 解剖区 | MNT坐标 | 覆盖概率 | ||
| CH01 | 45 | 三角肌区域 | -44 | 43 | 31 | 59% |
| CH02 | 9 | 背外侧前额叶皮质 | -28 | 43 | 46 | 99% |
| CH03 | 46 | 背外侧前额叶皮质 | -48 | 49 | 8 | 66% |
| CH04 | 10 | 额极区 | -35 | 65 | -4 | 51% |
| CH05 | 9 | 背外侧前额叶皮质 | -22 | 53 | 40 | 79% |
| CH06 | 10 | 额极区 | -26 | 68 | 11 | 93% |
| CH07 | 10 | 额极区 | -12 | 66 | 28 | 87% |
| CH08 | 9 | 背外侧前额叶皮质 | -10 | 43 | 55 | 53% |
| CH09 | 9 | 背外侧前额叶皮质 | 2 | 53 | 43 | 100% |
| CH10 | 8 | 背外侧前额叶皮质 | 12 | 42 | 56 | 56% |
| CH11 | 10 | 额极区 | -11 | 73 | -2 | 58% |
| CH12 | 10 | 额极区 | 4 | 70 | 15 | 100% |
| CH13 | 10 | 额极区 | 17 | 73 | -1 | 59% |
| CH14 | 10 | 额极区 | 17 | 65 | 29 | 81% |
| CH15 | 9 | 背外侧前额叶皮质 | 27 | 51 | 42 | 89% |
| CH16 | 10 | 额极区 | 31 | 67 | 13 | 95% |
| CH17 | 9 | 背外侧前额叶皮质 | 31 | 40 | 49 | 89% |
| CH18 | 45 | 三角肌区域 | 47 | 39 | 35 | 60% |
| CH19 | 10 | 额极区 | 38 | 65 | 1 | 59% |
| CH20 | 46 | 背外侧前额叶皮质 | 50 | 49 | 15 | 57% |

|
| 数字表示近红外NIRScout系统通道 图 3 双侧大脑PFC通道定位 |
1.4 试验数据分析
为了去除原始数据中含有生理、仪器等噪声,采用NIRS LAB软件对原始数据进行预处理。所有记录的fNIRS信号先进行截止频率为0.2 Hz的低通滤波去除以1 Hz为中心的心脏搏动信号,然后进行截止频率为0.01 Hz的高通滤波去除慢漂移,再应用修正的比尔-朗伯(吸收)定律将每个通道2个波长的光强信号转换为血液动力学参数,选用通道的平均值作为基线,计算所有通道的血液动力学参数,然后通过广义线性模型(general linear model,GLM)建模,方波脉冲函数与典型的血流动力学响应函数(HRF)进行卷积处理,分别计算被试在记忆的不同阶段,编码期、维持期、检索期的激活响应,最后对所有被试5个组块正序、倒序记忆任务编码期、维持期、检索期中激活均显著的通道的HbO2相对浓度变化曲线进行平均,获取每个任务不同的编码阶段的HbO2血液动力学变化的时间特性。
1.5 统计学分析采用SPSS 22.0统计软件,对每个被试的数字记忆正序、倒序、任务的正确率和反应时间进行配对样本t检验,选取正序、倒序记忆任务编码期、维持期、检索期中激活均显著的通道,提取所有被试每个阶段激活通道的beta值,分别进行单样本t检验,检验水准:α=0.05。
2 结果 2.1 行为学结果23例健康青年人按键判断, 正序反应时间(reaction time,RT)为(8.40±0.99)s,正确率(accuracy, ACC)为(98.2±2.5)%;倒序RT为(8.90±0.78)s,正确率ACC为(95.2±2.5)%。数字记忆正序、倒序任务的正确率和反应时配对样本t检验(t=0.402, P=0.696),差异无统计学意义。
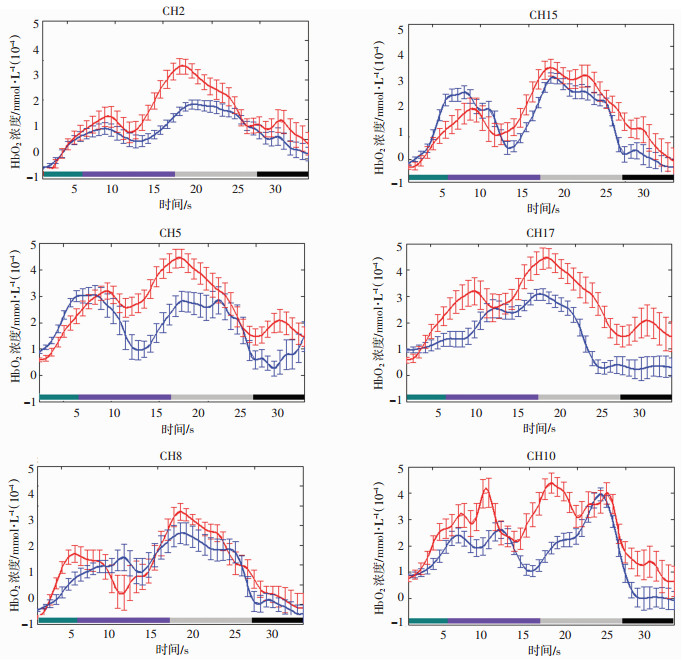
2.2 血液动力学HbO2变化的时间特性由于背外侧前额叶(dorsolateral prefrontal cortex, DLPFC)为数字记忆的关键脑区,因此重点研究DLPFC通道的HbO2平均相对含量。选取正序、倒序都显著激活的DLPFC通道(CH17、15、10、2、5、8),叠加所有被试通道的6个组块,平均时程曲线如图 4所示,图中蓝线为数字正序的HbO2时程曲线,红线为数字倒序的HbO2时程曲线。从图中可以看出,前面6 s为刺激呈现,数字记忆的编码期,呈明显的上升趋势,在大约8 s处到达峰值,接着10 s记忆维持期,曲线呈明显的回落趋势,随后的10 s为数字记忆检索期,HbO2再度呈现上升阶段,20 s处到达峰值,且比上一峰值高,任务休息期,曲线慢慢回落到基线状态。在编码和检索阶段,倒序记忆任务诱发的HbO2浓度的变化比正序记忆具有更高的峰值。
|
| 图中蓝线为数字正序的HbO2时程曲线;红线为数字倒序的HbO2时程曲线;绿色实线表示数字编码期;紫色实线表示数字维持期;灰色实线表示数字检索期;黑色实线表示休息 图 4 数字正序、倒序双侧大脑DLPFC的光学探测通道HbO2相对含量变化曲线 |
2.3 数字正序、倒序记忆大脑的激活模式
数字正序、倒序任务执行时,各个通道beta的单样本t检验大脑激活如图 5所示。数字正序任务编码、检索期显著激活的区域主要位于左侧的DLPFC(BAs 9和46)、额极区(BA10)、眼窝前额皮质(BA11);倒序任务在编码、检索阶段激活显著的区域为双侧的DLPFC(BAs 9和46)、额极区(BA10)、眼窝前额皮质(BA11);维持期脑区激活均明显下降。由于DLFC为工作记忆的关键脑区,对正序、倒序都显著激活的DLPFC通道进行了单样本t检验,正序任务的编码期、检索期左DLPFC激活明显,倒序任务编码期、检索期双侧DLPFC激活明显,但两个任务的维持期DCPFC激活均显著下降(P < 0.05, 表 2)。

|
| 红色点表示光源,黄色点表示探测器,右侧颜色条显示单样本t检验各通道t值大小,t值越大表明大脑激活越强 图 5 数字正、倒序记忆时大脑激活图 |
| 通道 | |||||||||||||||||
| 正序 | 倒序 | ||||||||||||||||
| 编码期 | 维持期 | 检索期 | 编码期 | 维持期 | 检索期 | ||||||||||||
| T | P | T | P | T | P | T | P | T | P | T | P | ||||||
| CH 2 | 3.515 | 0.032 | 2.808 | 0.031 | 3.842 | 0.038 | 2.832 | 0.042 | 2.421 | 0.043 | 3.217 | 0.039 | |||||
| CH 5 | 2.857 | 0.044 | 1.943 | 0.048 | 3.242 | 0.031 | 3.157 | 0.031 | 2.649 | 0.032 | 3.538 | 0.036 | |||||
| CH 8 | 2.457 | 0.027 | 2.043 | 0.049 | 2.942 | 0.037 | 3.263 | 0.028 | 2.871 | 0.039 | 3.701 | 0.037 | |||||
| CH 10 | 2.262 | 0.049 | 2.005 | 0.050 | 2.842 | 0.041 | 2.831 | 0.043 | 2.703 | 0.049 | 3.142 | 0.040 | |||||
| CH 15 | 2.108 | 0.048 | 1.805 | 0.050 | 2.434 | 0.039 | 2.751 | 0.049 | 1.943 | 0.038 | 3.281 | 0.039 | |||||
| CH 17 | 2.064 | 0.047 | 1.951 | 0.047 | 2.104 | 0.038 | 2.964 | 0.047 | 2.275 | 0.043 | 3.291 | 0.042 | |||||
考虑男女对数字的敏感性可能会影响结果,将被试按照性别分为男性和女性两组,采用SPSS软件对两组任务的数字编码期、维持期、检索期的通道HbO2相对浓度做了双样本统计检验,不同性别间差异无统计学意义(t=3.45,P=0.67)。
3 讨论本研究利用任务态的近红外脑成像技术,通过考察被试在工作记忆的信息编码,信息维护、信息检索三个阶段中双侧DLPFC的HbO2的变化及激活模式,研究了工作记忆时的DLPFC的神经响应,揭示工作记忆时DLPFC的神经机制。
本研究血流动力学结果显示,记忆任务诱发DLPFC(BAs9, 10)HbO2集中增加。被试在数字正序、倒序记忆任务中HbO2均有显著变化。任务诱发的HbO2时间历程清晰地显示了编码和检索阶段对应的两个峰值,这与之前使用类似刺激方案的fMRI报道一致[12]。在信息编码期,前额叶的神经电反应增多,需要血氧供给,因此曲线逐渐上升。根据血流动力学响应的延迟效应,在8 s左右达到峰值,符合预期设想结果,工作记忆与静息状态下的对比,即工作记忆由于前额叶的神经电反应增多,需要血氧供给,导致曲线上升,而静息时相反[13-15]。
信息检索一直是记忆研究的核心和焦点,本研究显示健康被试在数字正序、倒序记忆检索阶段均有显著的峰值。根据fMRI研究报告显示记忆的检索阶段,由于存在数字串排序、检索等多个认知活动,因为血氧响应明显高于编码、保持期,因此这一时期的HbO2浓度为整个记忆时期的最高值。JAHANI等[16]采用fNIRS研究健康成年人在面孔名称配对联想学习任务下的记忆编码和检索过程中前额叶、顶叶和颞叶皮层脑活动,其结果表明编码新的面孔名称与重复的面孔名称相对比,左DLPFC显著激活。另外,认知任务的复杂性与DLPFC的激活呈显著相关性。编码新面孔中神经活动的更多参与可能是因为需要更多的认知资源,比如注意力的参与或语义处理。事实上,与简单任务相比,更难的任务需要更多的大脑活动和更广泛的大脑区域的参与。本研究正序/倒序任务在检索期血氧响应均明显高于编码期、维持期,这可能因为数字检索任务相对比较复杂,涉及回忆、排序更多的认知活动,从而引发了更强的HbO2浓度变化。
本研究结果显示数字正序任务的编码期、检索期显著激活了双侧的DLPFC、额极区、眼窝前额皮质,其中左侧DLPFC激活更强,这一结果与之前的神经影像学研究结果相符。前额叶皮层(PFC)对工作记忆的干预包括两个主要组成部分:短期记忆和执行过程。虽然短期记忆是一个维持有限数量的信息活跃的过程,但是执行过程与信息管理相关,并且满足于存储信息。神经生理学研究表明,位于DLPFC皮层的神经元在信息的编码和检索过程中具有重要作用。MCCARTHY等[17]的研究结果显示右侧额中回在空间记忆任务中的激活强烈,而左侧额中回在非空间工作记忆任务中激活强烈。文献[18-19]也证实了空间工作记忆的优势半球为右半球,激活主要为右侧额叶;而非空间工作记忆时优势半球为左半球,激活最明显的为左侧额叶。本研究结果证实了左侧DLPFC在工作记忆信息编码、检索过程中的重要作用,说明近红外光谱成像技术可以较为准确地测量大脑皮层区域的HbO2浓度变化,从而推测大脑皮层的神经活动,为临床医学诊断及研究提供了一种很有前景的技术手段。
工作记忆是一个复杂的信息加工系统,除了具体的脑区分工之外,还需要更多的脑区协调完成任务。神经影像学研究发现前额叶的腹侧和背侧区域主要负责对工作记忆物体的颜色、距离、方向等进行存储和调节[20]。记忆负载较低时,脑区分工较为明确,当负载较高时,自动趋向更多的脑网络协调完成。WIJEAKUMAR等[21]在fNIRS和fMRI的研究结果均显示,随着工作记忆负荷的增加,左侧额顶叶的激活增强;MCKENDRICK等[22]采用fNIRS发现在执行加工过程中,注意力和体力劳动的负荷会导致工作记忆性能下降,双侧额叶前部皮质失活。这些研究结果表明额叶的激活与工作记忆密切相关。本研究结果发现相对于正序记忆,倒序任务激活了更多的脑区,双侧的DLPFC、额极区、眼窝前额皮质均有显著激活,进一步证实了随着负载提高,除了左侧DLPFC激活增强外,右侧DLPFC的激活也显著提高。可能由于倒序记忆任务需要数字逆转,涉及更多的复杂神经、生理认知活动,需要调控更多的信息[3, 5],因此倒序的编码、检索期双侧的DLPFC、额极区、眼窝前额皮质均有显著激活。
综上所述,数字正序记忆的编码、检索过程由以左侧半球为优势的脑区共同参与完成,其中左侧DLPFC可能是信息编码、检索提取的重要脑区。数字倒序记忆的编码、检索过程由双侧脑区共同参与完成,除DLPFC之外,额极区、眼窝前额皮质都参与了信息编码、检索过程,这些脑区的广泛激活可能与负载的增加有关,说明在数字信息的加工、处理和存储中需要更多的脑区协调完成。
临床上卒中患者、阿尔茨海默病、精神疾病患者等都有不同程度的记忆减退,如果能及时干预治疗,可减弱或停止渐进性认知衰退。本研究采用fNIRS探讨了健康被试工作记忆前额叶HbO2的相对变化,提供了一种新的技术手段研究大脑记忆功能。未来的工作将应用fNIRS捕捉卒中患者、阿尔茨海默病、精神疾病患者等早期的大脑活动变化,有助于发现早期记忆损伤并及时干预治疗。
| [1] |
张世娟, 卢洁, 王晓怡, 等. 正常老年人数字记忆功能的磁共振成像[J]. 中国老年学杂志, 2011, 31(3): 384-386. ZHANG S J, LU J, WANG X Y, et al. Functional MRI study of digital working memory in the healthy old people[J]. Chin J Gerontol, 2011, 31(3): 384-386. DOI:10.3969/j.issn.1005-9202.2011.03.007 |
| [2] |
吴永明, 柏林, 张增强, 等. 正常人长时数字记忆信息提取的神经基础的功能磁共振研究[J]. 生理学报, 2011, 63(4): 319-324. WU Y M, BAI L, ZHANG Z Q, et al. A study on the neuronal mechanism of retrieval of long-term digital memory in human by functional magnetic resonance imaging[J]. Acta Physiol Sin, 2011, 63(4): 319-324. DOI:10.13294/j.aps.2011.04.006 |
| [3] |
OGAWA Y, KOTANI K, JIMBO Y. Relationship between working memory performance and neural activation measured using near-infrared spectroscopy[J]. Brain Behav, 2014, 4(4): 544-551. DOI:10.1002/brb3.238 |
| [4] |
SHEN J, ZHANG G, YAO L, et al. Real-time fMRI training-induced changes in regional connectivity mediating verbal working memory behavioral performance[J]. Neuroscience, 2015, 289: 144-152. DOI:10.1016/j.neuroscience.2014.12.071 |
| [5] |
WIJEAKUMAR S, HUPPERT T J, MAGNOTTA V A, et al. Validating an image-based fNIRS approach with fMRI and a working memory task[J]. Neuroimage, 2017, 147: 204-218. DOI:10.1016/j.neuroimage.2016.12.007 |
| [6] |
BASSO MORO S, CUTINI S, URSINI M L, et al. Prefrontal cortex activation during story encoding/retrieval: a multi-channel functional near-infrared spectroscopy study[J]. Front Hum Neurosci, 2013, 7: 925. DOI:10.3389/fnhum.2013.00925 |
| [7] |
张静娜, 王莉, 张晔, 等. 基于功能近红外光谱技术的镜像运动脑激活特征的初步研究[J]. 第三军医大学学报, 2018, 40(18): 1682-1687. ZHANG J N, WANG L, ZHANG Y, et al. Brain activation characteristics during mirror movements in healthy subjects: findings by functional near-infrared spectroscopy[J]. J Third Mil Med Univ, 2018, 40(18): 1682-1687. DOI:10.16016/j.1000-5404.201804010 |
| [8] |
FERRARI M, QUARESIMA V. A brief review on the history of human functional near-infrared spectroscopy (fNIRS) development and fields of application[J]. Neuroimage, 2012, 63(2): 921-935. DOI:10.1016/j.neuroimage.2012.03.049 |
| [9] |
WIJEAKUMAR S, HUPPERT T J, MAGNOTTA V A, et al. Validating an image-based fNIRS approach with fMRI and a working memory task[J]. Neuroimage, 2017, 147: 204-218. DOI:10.1016/j.neuroimage.2016.12.007 |
| [10] |
TIAN F H, YENNU A, SMITH-OSBORNE A, et al. Prefrontal responses to digit span memory phases in patients with post-traumatic stress disorder (PTSD): a functional near infrared spectroscopy study[J]. Neuroimage Clin, 2014, 4: 808-819. DOI:10.1016/j.nicl.2014.05.005 |
| [11] |
BOTDORF M, RIGGINS T. When less is more: Thinner fronto-parietal cortices are associated with better forward digit span performance during early childhood[J]. Neuropsychologia, 2018, 121: 11-18. DOI:10.1016/j.neuropsychologia.2018.10.020 |
| [12] |
SIDHU M K, STRETTON J, WINSTON G P, et al. A functional magnetic resonance imaging study mapping the episodic memory encoding network in temporal lobe epilepsy[J]. Brain, 2013, 136(Pt 6): 1868-1888. DOI:10.1093/brain/awt099 |
| [13] |
KHARITONOVA M, WINTER W, SHERIDAN M A. As working memory grows: A developmental account of neural bases of working memory capacity in 5- to 8-year old children and adults[J]. J Cogn Neurosci, 2015, 27(9): 1775-1788. DOI:10.1162/jocn_a_00824 |
| [14] |
SCHAEFFER J D, YENNU A S, GANDY K C, et al. An fNIRS investigation of associative recognition in the prefrontal cortex with a rapid event-related design[J]. J Neurosci Methods, 2014, 235: 308-315. DOI:10.1016/j.jneumeth.2014.07.011 |
| [15] |
BOAS D A, ELWELL C E, FERRARI M, et al. Twenty years of functional near-infrared spectroscopy: introduction for the special issue[J]. Neuroimage, 2014, 85(Pt 1): 1-5. DOI:10.1016/j.neuroimage.2013.11.033 |
| [16] |
JAHANI S, FANTANA A L, HARPER D, et al. fNIRS can robustly measure brain activity during memory encoding and retrieval in healthy subjects[J]. Sci Rep, 2017, 7(1): 9533. DOI:10.1038/s41598-017-09868-w |
| [17] |
MCCARTHY G, PUCE A, CONSTABLE R T, et al. Activation of human prefrontal cortex during spatial and nonspatial working memory tasks measured by functional MRI[J]. Cereb Cortex, 1996, 6(4): 600-611. DOI:10.1093/cercor/6.4.600 |
| [18] |
D'ESPOSITO M, AGUIRRE G K, ZARAHN E, et al. Functional MRI studies of spatial and nonspatial working memory[J]. Brain Res Cogn Brain Res, 1998, 7(1): 1-13. DOI:10.1016/S0926-6410(98)00004-4 |
| [19] |
LUNDSTROM B N, INGVAR M, PETERSSON K M. The role of precuneus and left inferior frontal cortex during source memory episodic retrieval[J]. Neuroimage, 2005, 27(4): 824-834. DOI:10.1016/j.neuroimage.2005.05.008 |
| [20] |
SALA J B, RÄMÄ P, COURTNEY S M. Functional topography of a distributed neural system for spatial and nonspatial information maintenance in working memory[J]. Neuropsychologia, 2003, 41(3): 341-356. DOI:10.1016/S0028-3932(02)00166-5 |
| [21] |
WIJEAKUMAR S, HUPPERT T J, MAGNOTTA V A, et al. Validating an image-based fNIRS approach with fMRI and a working memory task[J]. Neuroimage, 2017, 147: 204-218. DOI:10.1016/j.neuroimage.2016.12.007 |
| [22] |
MCKENDRICK R, MEHTA R, AYAZ H, et al. Prefrontal hemodynamics of physical activity and environmental complexity during cognitive work[J]. Hum Factors, 2017, 59(1): 147-162. DOI:10.1177/0018720816675053 |



