2. 400010 重庆,重庆医科大学附属第二医院妇产科;
3. 400016重庆,重庆医科大学临床检验诊断学教育部重点实验室;
4. 330029 南昌,江西省肿瘤医院:重症医学科
2. Department of Obstetrics and Gynecology, the Second Affiliated Hospital of Chongqing Medical University, Chongqing, 400010;
3. Key Laboratory of Laboratory Medical Diagnostics of Ministry of Education, Chongqing Medical University, Chongqing, 400016, China;
4. Department of Critical Care Medicine, Jiangxi Cancer Hospital, Nanchang, Jiangxi Province, 330029
肿瘤相关成纤维细胞(cancer-associated fibroblasts,CAFs)是乳腺癌组织中主要的成分之一[1],在促进肿瘤细胞生长、侵袭、转移及多种临床药物耐受中发挥重要作用[2]。G蛋白偶联雌激素受体(G protein-coupled estrogen receptor,GPER)是近年被鉴定出的第3种独立作用的雌激素受体,从分子构象上而言属于G蛋白偶联受体(G protein-coupled receptor,GPCRs)超家族成员。但与传统GPCRs细胞膜表达定位不同的是,GPER在肿瘤细胞内的表达分布呈现“复杂性”:它被发现可定位于细胞内多个部位,如细胞膜、内质网、核糖体与高尔基体,甚至细胞核中[3-5]。提示在不同的细胞类型与生理条件下,细胞内GPER可能呈现不同的表达定位特点,甚至可能在细胞内各亚细胞器之间相互穿梭。同时,研究团队在前期证实GPER介导CAFs中芳香化酶基因CYP19A1与糖酵解基因PDK4高转录活性,可能是促进肿瘤组织中局部雌激素水平增加与酸性微环境的关键因素,从而在乳腺癌细胞增殖、转移及药物耐受中扮演始动作用[6-7]。GPER或是介导CAFs与肿瘤细胞之间“交叉对话”进而促进乳腺癌进展的重要媒介。
研究显示,成纤维细胞生长因子2(fibroblast growth factors 2,FGF2)的过表达与肿瘤发生、发展密切相关。它不仅参与肿瘤血管新生,还间接调控肿瘤细胞的生长及侵袭转移能力[8-10]。然而,乳腺癌微环境CAFs中GPER介导的生长因子调节作用研究甚少,其与FGF2的调控机制及下游生物学作用更是研究“盲点”。考虑到肿瘤细胞与CAFs是密不可分的整体,且既往相关GPER研究多集中在CAFs本身(即单独培养)。因此,本研究拟进一步利用17-β雌二醇(E2)、FGF2中和抗体等小分子化合物首次探讨共培养条件下乳腺癌微环境CAFs中GPER活化对FGF2的表达调控机制及其旁分泌对肿瘤细胞侵袭的影响。
1 材料与方法 1.1 材料MCF-7与MDA-MB-468细胞系购自中科院上海细胞库,研究团队前期已构建体外稳定培养的永生化CAFs细胞株[2, 6-7]。高糖DMEM培养基、南美胎牛血清购自Gibco公司。E2购自Sigma公司,PKA特异性抑制剂H-89、AKT抑制剂Wortmannin(WM)、BCA蛋白浓度测定试剂盒购自杭州碧云天公司。p-ERK抗体、t-ERK抗体、p-AKT抗体、t-AKT抗体、p-PKA及β-actin抗体购自美国Bioworld公司,GPER抗体购自Abcam公司,FGF2中和抗体购自Millipore公司。DAPI与FITC标记山羊抗兔IgG抗体购自北京中杉金桥公司,FGF2 ELISA试剂盒购自Rapidbio公司,总RNA提取试剂盒、逆转录试剂盒购自TaKaRa公司,荧光定量PCR试剂盒购自BioTeKe公司,Transwell小室购自Corning公司,基质胶购自R&D公司,二氧化碳培养箱购自Thermo scientific公司,多功能酶标仪购自Sunrise公司,MiniOpticon实时PCR仪和稳压DNA电泳仪购自Bio-Rad公司。
1.2 方法 1.2.1 细胞培养MCF-7、MDA-MB-468及CAFs细胞均培养于10%胎牛血清的高糖DMEM培养基中,37 ℃、5% CO2培养箱内生长,隔日换液,待细胞生长至90%左右时用0.25%胰酶消化离心后传代。
1.2.2 乳腺肿瘤细胞条件培养基的获取乳腺癌MCF-7与MDA-MB-468细胞生长于10% FBS的高糖DMEM培养基,待细胞生长至70%~80%,将培养液更换为1% FBS的培养基继续培养30 h后,将培养基收集后离心,其上清液即为肿瘤细胞条件培养基(conditioned medium,CM)[7]。
1.2.3 CAFs与乳腺癌细胞共培养模型根据实验需求选取以下方式:①收集肿瘤细胞CM处理CAFs细胞36 h;②Transwell小室法共培养24 h,CAFs细胞种于上室,肿瘤细胞种于下室,细胞比例为3 :1。分别得到CAFs+MCF-7与CAFs+MDA-MB-468共培养细胞模型[7]。
1.2.4 GPER核输出信号(NES)序列突变依托上海吉码制药技术有限公司对GPER NES序列:YFINLAVADLILV的核心区域LIL进行突变,得到突变型YFINLAVADAAAV的质粒,课题组已在前期研究中用脂质体2000转染等方法获得稳定筛选的GPER NES序列突变型细胞株CAFs(M)[7]。
1.2.5 细胞免疫荧光检测CAFs细胞中GPER表达定位取单独培养及共培养条件下对数期生长的野生型CAFs与突变型CAFs(M)细胞胰酶消化离心重悬后以2×105/mL接种于底部放有小玻片的24孔板中,置于细胞孵箱中培养,待细胞生长状态及密度合适后,取出24孔板用PBS洗3次,加入4%多聚甲醛200 μL固定20 min,PBS洗3次,10%山羊血清37 ℃封闭30 min,加入GPER抗体(1 :100稀释)30~40 μL,4 ℃孵育过夜,PBS洗3次,暗室中加入FITC荧光二抗(1 :200),37 ℃ 60 min,PBS洗3次,加入DAPI(1 :10)染核5 min,PBS洗3次,每次5 min,封片后,倒置荧光显微镜下拍照。
1.2.6 荧光定量PCR检测CAFs细胞中FGF2 mRNA表达量CAFs细胞单独培养或取不同的共培养细胞模型,待CAFs细胞生长至70%~80%后,更换无血清培养基饥饿24 h。加入100 nmol/L E2处理CAFs细胞12 h,各组调整DMSO至一致,最后分别得到对照组(ctrl)、E2处理组(E2),处理相应时间后立即终止药物处理,用TRIzol试剂提取各组CAFs细胞中总RNA,逆转录为cDNA。逆转录及PCR反应均按照TaKaRa试剂盒及荧光定量PCR试剂盒说明进行操作。FGF2上游引物序列为5′-AGCCAGGTAACGGTTAGCAC-3′,下游引物序列为5′-GGAGAAGAGCGACCCTCAC-3′; 以β-actin为内参照,上游引物序列为5′-AGCGAGCATCCCCC-AAAGTT-3′,下游引物序列为5′-GGGCACGAAGGCTCATCATT-3′。实验重复3次。
1.2.7 ELISA法检测CAFs细胞上清中FGF2的分泌量实验分组同1.2.6,待CAFs细胞生长至80%~90%后,更换无血清培养基饥饿24 h。分别加入100 nmol/L E2联合10 μmol/L WM、1 μmol/L H-89处理CAFs细胞24 h,各组调整DMSO至一致,最后分别得到对照组、E2处理组、E2+WM处理组、E2+H-89处理组、WM处理组与H-89处理组,处理相应时间后立即终止药物处理,收集细胞上清液,保存于-80 ℃冰箱,按ELISA试剂盒操作说明书检测各组样本中FGF2的含量。实验重复3次。
1.2.8 Western blot法检测CAFs细胞中p-ERK、p-AKT及p-PKA蛋白表达实验分组同1.2.6。CAFs细胞生长至60%~70%,无血清DMEM培养基饥饿细胞12 h,用MCF-7与MDA-MB-468细胞条件培养基处理细胞36 h后,对照组用无血清培养基处理相同时间,依照实验分组加入100 nmol/L E2处理30 min,各组调整DMSO至一致,处理相应时间后立即终止,PBS洗3次,最后将细胞移入EP管中。收集细胞、细胞总蛋白提取、测蛋白浓度、制胶、上样(100 μg)、电泳、转膜(ERK、AKT、PKA蛋白转膜时间分别为18 min、26 min、18 min)、封闭、一抗孵育(稀释比例均为1 :1 000)、二抗(山羊抗兔IgG,1 :1 000)孵育、ECL化学发光成像,Quantity one软件进行灰度值测定。实验重复3次。
1.2.9 Transwell法检测乳腺癌细胞侵袭能力预冷的无血清DMEM培养基以1 :6体积稀释液态基质胶,将稀释后的基质胶40 μL加入24孔板中的Trans-well小室的上室中,放于37 ℃孵育6 h。吸净基质胶表面的液体,加入70 μL无血清DMEM培养基,37 ℃孵育30 min。CAFs细胞种于下室,肿瘤细胞种于上室,细胞比例为1 :3。细胞贴壁后,分别于下室中加入100 nmol/L E2联合上室中加入2 μg/mL FGF2中和抗体于37 ℃、5% CO2条件下培养24 h,各组调整DMSO至一致,最后分别得到对照组(ctrl)、E2处理组(E2)、E2+FGF2中和抗体处理组、FGF2中和抗体处理组,处理相应时间后立即终止药物处理,用棉签抹掉上室基质胶上的细胞,PBS洗3遍,将小室置于4%多聚甲醛中固定10 min,0.1%结晶紫染液染色10 min后,PBS洗3遍,用棉签吸干水分,显微镜下随机挑选5个视野,计数侵袭到下室的细胞数,计算每个视野的相对平均侵袭细胞数。实验重复3次。
1.3 统计学分析采用SPSS 19.0统计软件,数据用x±s表示,多组间比较采用重复测量方差分析,两两比较采用q检验,P < 0.05为差异有统计学意义。
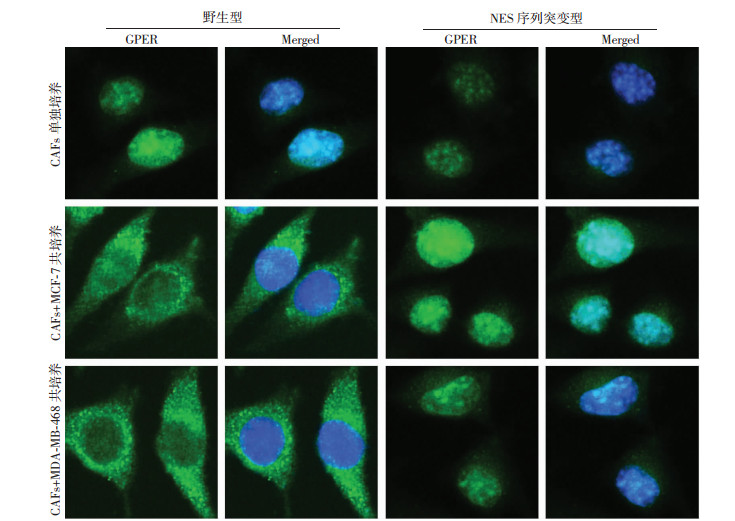
2 结果 2.1 不同亚型乳腺癌细胞均可诱导CAFs中GPER发生细胞质转位细胞免疫荧光实验表明:CAFs单独培养条件下,GPER主要表达于细胞核,而与ER+乳腺癌MCF-7及ER-乳腺癌MDA-MB-468细胞共培养后,CAFs中GPER的表达定位由细胞核转位入细胞质中;GPER NES序列突变后,上述两种亚型的乳腺癌细胞均不能使CAFs(M)中GPER发生核质转位(图 1)。
|
| 单独培养条件下GPER定位于CAFs的细胞核,而共培养条件下则定位于CAFs的细胞质;绿色荧光代表目的蛋白GPER;蓝色荧光代表细胞核;Merged为两者融合图像 图 1 细胞免疫荧光检测不同培养条件下CAFs细胞中GPER的表达定位情况(×400) |
2.2 共培养条件下,E2活化细胞质GPER促进CAFs细胞表达与分泌FGF2
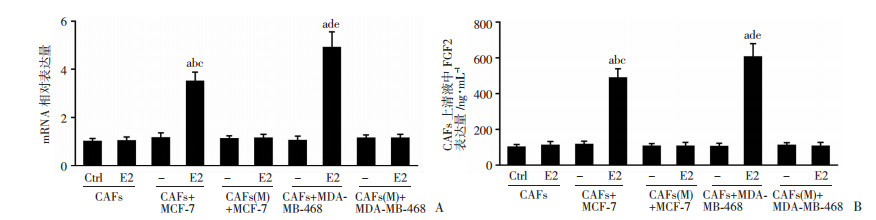
荧光定量PCR数据显示,共培养条件下,E2可明显上调CAFs细胞内FGF2 mRNA表达水平,显著高于对照组(P < 0.05,图 2A)。ELISA结果进一步提示,E2显著促进共培养模型CAFs细胞上清液中FGF2的分泌量(P < 0.05,图 2B)。而单独培养条件下,则未观察到上述现象。此外,共培养模型CAFs中GPER NES序列突变后,可显著抑制E2诱导的CAFs细胞内FGF2 mRNA表达量及上清液中的分泌量(P < 0.05,图 2A、B)。
|
| A:共培养条件下,GPER NES序列突变阻断CAFs细胞中E2诱导的FGF2 mRNA表达;B:共培养条件下,GPER NES序列突变阻断CAFs细胞上清液中E2诱导的FGF2分泌量;a:P < 0.05,与CAFs+E2组比较;b:P < 0.05,与CAFs+MCF-7组比较;c:P < 0.05,与CAFs(M)+MCF-7+E2组比较;d:P < 0.05,与CAFs+MDA-MB-468组比较;e:P < 0.05,与CAFs(M)+MDA-MB-468+E2组比较 图 2 荧光定量PCR及ELISA法检测E2对乳腺癌CAFs中FGF2表达的影响 |
2.3 E2活化CAFs细胞中GPER/AKT与GPER/PKA信号通路
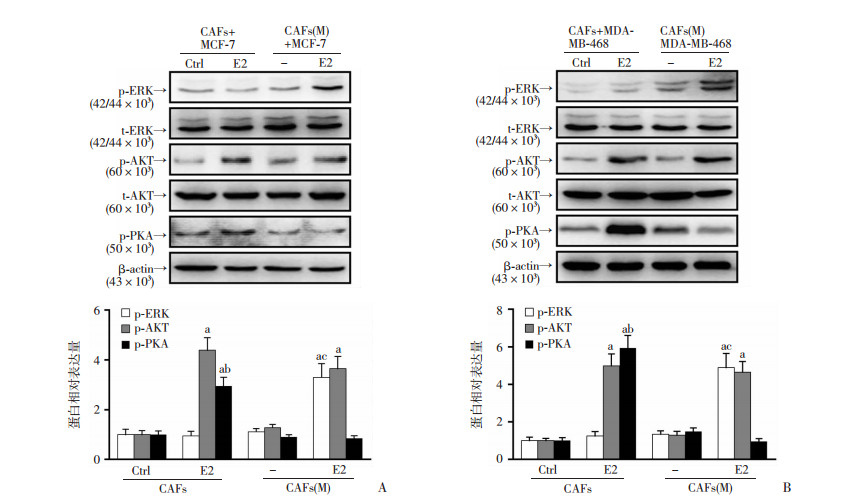
GPER活化后信号通路下游主要涉及3条快速非基因组信号:分别为ERK、AKT以及PKA通路。本实验筛选了CAFs细胞中上述通路活化情况,Western blot结果显示:共培养条件下,E2显著促进CAFs细胞中p-AKT与p-PKA的蛋白表达量,在两种亚型的乳腺癌细胞分组中均可得到验证(P < 0.05,图 3A、B)。有趣的是,突变CAFs细胞中GPER NES序列后,PKA信号被显著抑制,ERK信号却得到活化(图 3A、B)。以上数据说明,雌激素可通过GPER/AKT与GPER/PKA信号通路激活共培养模型CAFs细胞中的快速非基因组信号。
|
| A、B:分别为MCF-7和MDA+MB-468细胞中GPER/AKT与GPER/PKA信号通路蛋白表达及半定量分析;a:P < 0.05,与Ctrl组比较;b:P < 0.05,与CAFs(M)+E2组比较;c:P < 0.05,与CAFs(M)组比较 图 3 Western blot检测药物处理后共培养模型CAFs中快速非基因组信号活化情况 |
2.4 E2活化CAFs细胞中GPER/PKA信号促进FGF2表达
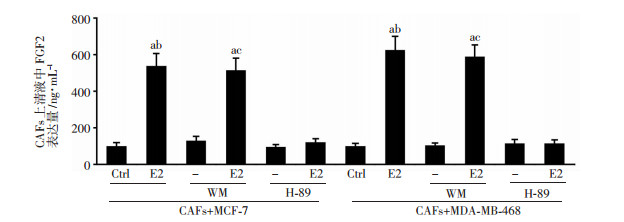
ELISA法检测结果进一步显示,PKA特异性抑制剂(H-89)可明显阻断共培养模型CAFs中E2诱导的FGF2外分泌量(P < 0.05),AKT特异性抑制剂(WM)则不能(图 4)。以上数据提示,雌激素促进乳腺癌CAFs中细胞质GPER依赖性的FGF2表达,其机制与GPER/PKA信号活化相关。
|
| E2活化共培养模型CAFs细胞中GPER/PKA信号促进FGF2表达;a:P < 0.05,与对应Ctrl组比较;b:P < 0.05,与对应E2+H-89组比较;c:P < 0.05,与对应WM组比较 图 4 ELISA法检测药物处理后共培养模型CAFs中FGF2的表达 |
2.5 E2通过诱导CAFs细胞旁分泌FGF2促进乳腺癌细胞侵袭
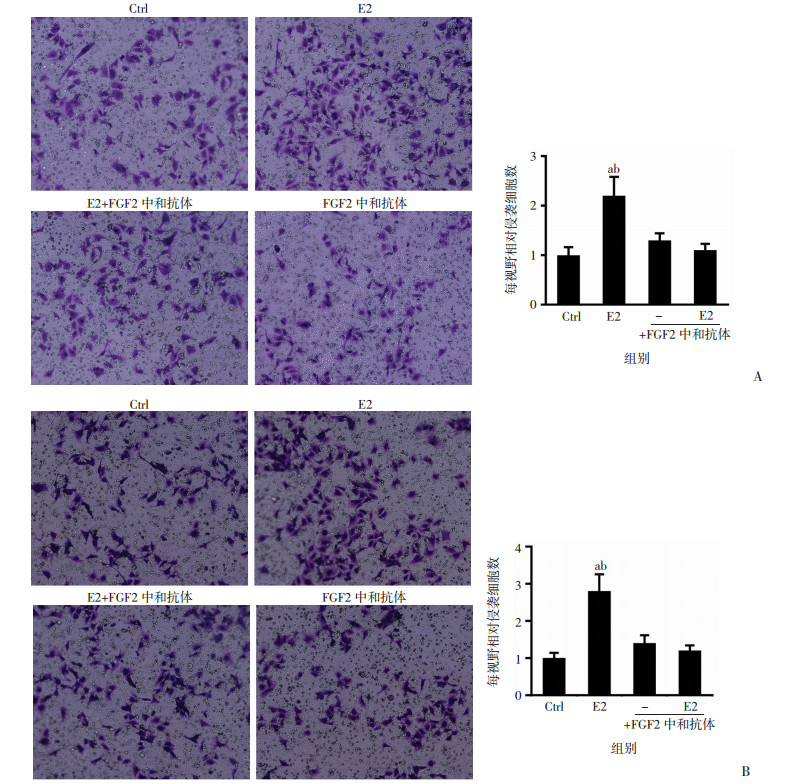
Transwell小室实验结果显示:E2作用于共培养模型中CAFs后可明显提高乳腺癌细胞的侵袭能力(图 5A、B),应用FGF2中和抗体显著阻断以上效应(P < 0.05)。表明雌激素活化CAFs中细胞质GPER依赖性的下游PKA信号旁分泌FGF2进而促进乳腺癌细胞侵袭。
|
|
a:P < 0.05,与Ctrl组比较;b:P < 0.05,与E2+FGF2中和抗体组比较 A:CAFs与ER+乳腺癌MCF-7细胞共培养;B:CAFs与ER-乳腺癌MDA-MB-468细胞共培养 图 5 Transwell小室法检测药物处理后共培养模型乳腺癌细胞侵袭能力的变化(×200) |
3 讨论
肿瘤的发生、发展不仅仅是肿瘤实质细胞本身的单独作用,同时其微环境成分也作为肿瘤的核心特征被广泛接受[11]。研究团队前期体外实验数据显示CAFs单独培养条件下GPER主要表达于细胞核中,而这与免疫组化实验所观察到GPER主要表达于肿瘤间质成纤维细胞(tumor stromal fibroblasts,TSFs)细胞质的结果不相符合[7]。事实上,生理条件下CAFs可能受到肿瘤组织中多种成分的影响,仅仅单独研究CAFs中GPER的生物学功能可能是不妥的,乳腺癌细胞与CAFs之间的“交叉对话”应考虑在内,这更加符合实体肿瘤真实的“内部环境”。本研究在不同亚型的乳腺癌(ER+型MCF-7与ER-型MDA-MB-468)细胞中均证实了GPER的核质转位现象,提示CAFs中GPER的核质转位可能是乳腺肿瘤的普遍特点之一,其在肿瘤进展及药物耐受中或发挥关键性作用,可能是潜在的治疗靶点。
近年来,GPER所介导的肿瘤旁分泌效应越来越受到关注。CIRILLO等[12]报道CAFs中GPER可介导乳腺组织局部雌激素异常升高促进ER+乳腺癌快速生长。此外,在ER-乳腺癌SKBR-3细胞中GPER还可介导血管生长因子(VEGF)大量分泌,促进内皮细胞形成新生血管网[13]。同样,我们在前期研究中也证实GPER创造乳酸微环境引起乳腺癌细胞能量代谢重塑,从而导致肿瘤细胞的临床多药耐受[7]。本研究进一步明确了乳腺癌微环境GPER与成纤维细胞因子家族成员FGF2的潜在调控关系:共培养条件下E2活化CAFs中细胞质GPER促进FGF2的表达及外分泌,突变GPER的NES序列后可阻断上述效应。同时,CAFs单独培养条件下未观察到上述现象,进一步提示共培养下微环境GPER细胞质定位的独特生物学作用。
本研究还发现,共培养条件下(即GPER表达于CAFs细胞质),E2激活CAFs细胞中AKT与PKA信号通路。这与早先的研究结果部分相符:即雌激素活化GPER致使G蛋白中Gβγ亚基与Gα亚基分离,其中Gβγ亚基刺激酪氨酸激酶Src进而活化细胞表面基质金属蛋白酶信号,使细胞释放肝素结合性表皮生长因子,进一步反式激活细胞表面表皮生长因子受体及其下游ERK与AKT信号通路;Gα亚基则可特异性活化环磷腺苷进而激活其下游的PKA信号通路[1, 3, 5-6]。随后,我们通过突变GPER NES序列阻断其出核后(即GPER表达于CAFs细胞核),E2却激活CAFs细胞中AKT与ERK信号通路,提示不同生理状态下,CAFs中GPER介导的下游信号通路可能发生改变,细胞中或存在细胞核GPER依赖性的ERK信号与细胞质GPER依赖性的PKA信号活化为主导的“优势信号”等多种作用模式。通过查阅相关文献,FILARDO等[14]研究发现乳腺癌MCF-7细胞内GPER/PKA信号通路的活化可使ERK信号通路失活,这在一定程度上也支持了GPER/ERK与GPER/PKA信号之间可能存在“内部相互拮抗”效应,出现“此消彼长”的有趣现象,但其具体机制还有待进一步研究。
本研究进一步发现:共培养条件下,E2活化CAFs细胞中GPER/PKA信号参与FGF2的表达调控。分别用AKT特异性抑制剂WM以及PKA特异性抑制剂H-89预处理CAFs细胞后,包含H-89的处理组中细胞上清液内FGF2的分泌量显著下调,提示E2所活化的PKA信号通路调控细胞中FGF2的表达。这与TREMBLAY等[15]研究结果类似:他们在卵巢颗粒细胞瘤中筛选了PKA信号通路下游的转录靶基因,FGF2正是其下游靶点之一。然而,在含有WM的处理组中,本研究并未发现其可逆转E2诱导的FGF2变化,说明雌激素/GPER/AKT信号通路虽然在CAFs细胞中得到显著活化,但是并不参与FGF2的调控。结合现有的研究表明,FGF2的过量表达及其下游信号的异常活化参与肿瘤恶性临床进展[16-17]。巧合的是,这与本研究Transwell小室实验中获得的数据相吻合:E2作用于共培养模型中CAFs后可明显提高乳腺癌细胞的侵袭能力,应用FGF2中和抗体显著阻断以上效应。因此,我们推测乳腺癌CAFs中雌激素/GPER/PKA/FGF2通路可能在肿瘤恶性进展中扮演着重要作用,由GPER所介导的FGF2外分泌或是部分乳腺癌患者预后较差的原因之一,但是这还需要更多的体内外实验来进一步验证以上信号通路所发挥的具体生物学作用。
| [1] |
LAPPANO R, MAGGIOLINI M. GPER is involved in the functional liaison between breast tumor cells and cancer-associated fibroblasts (CAFs)[J]. J Steroid Biochem Mol Biol, 2018, 176: 49-56. DOI:10.1016/j.jsbmb.2017.02.019 |
| [2] |
SUN K X, TANG S F, HOU Y X, et al. Oxidized ATM-mediated glycolysis enhancement in breast cancer-associated fibroblasts contributes to tumor invasion through lactate as metabolic coupling[J]. EBio Medicine, 2019, 41: 370-383. DOI:10.1016/j.ebiom.2019.02.025 |
| [3] |
YU T H, LIU M R, LUO H J, et al. GPER mediates enhanced cell viability and motility via non-genomic signaling induced by 17β-estradiol in triple-negative breast cancer cells[J]. J Steroid Biochem Mol Biol, 2014, 143: 392-403. DOI:10.1016/j.jsbmb.2014.05.003 |
| [4] |
YIN H, ZHU Q, LIU M R, et al. GPER promotes Tamo-xifen-resistance in ER+ breast cancer cells by reduced Bim proteins through MAPK/Erk-TRIM2 signaling axis[J]. Int J Oncol, 2017, 51(4): 1191-1198. DOI:10.3892/ijo.2017.4117 |
| [5] |
HSU L H, CHU N M, LIN Y F, et al. G-protein coupled estrogen receptor in breast cancer[J]. IJMS, 2019, 20(2): 306. DOI:10.3390/ijms20020306 |
| [6] |
LUO H J, LIU M R, LUO S J, et al. Dynamic monitoring of GPER-mediated estrogenic effects in breast cancer associated fibroblasts: An alternative role of estrogen in mammary carcinoma development[J]. Steroids, 2016, 112: 1-11. DOI:10.1016/j.steroids.2016.03.013 |
| [7] |
YU T, YANG G, HOU Y, et al. Cytoplasmic GPER trans-location in cancer-associated fibroblasts mediates cAMP/PKA/CREB/glycolytic axis to confer tumor cells with multidrug resistance[J]. Oncogene, 2017, 36(15): 2131-2145. DOI:10.1038/onc.2016.370 |
| [8] |
AKL M R, NAGPAL P, AYOUB N M, et al. Molecular and clinical significance of fibroblast growth factor 2 (FGF2/bFGF) in malignancies of solid and hematological cancers for personalized therapies[J]. Oncotarget, 2016, 7(28): 44735-44762. DOI:10.18632/oncotarget.8203 |
| [9] |
TRAER E, JAVIDI-SHARIFI N, AGARWAL A, et al. Ponatinib overcomes FGF2-mediated resistance in CML patients without kinase domain mutations[J]. Blood, 2014, 123(10): 1516-1524. DOI:10.1182/blood-2013-07-518381 |
| [10] |
SEO J H, YU J H, SUH H, et al. Fibroblast growth factor-2 induced by enriched environment enhances angiogenesis and motor function in chronic hypoxic-ischemic brain injury[J]. PLoS ONE, 2013, 8(9): e74405. DOI:10.1371/journal.pone.0074405 |
| [11] |
QIAO A X, GU F, GUO X J, et al. Breast cancer-associated fibroblasts: their roles in tumor initiation, progression and clinical applications[J]. Front Med, 2016, 10(1): 33-40. DOI:10.1007/s11684-016-0431-5 |
| [12] |
CIRILLO F, PELLEGRINO M, MALIVINDI R, et al. GPER is involved in the regulation of the estrogen-metabolizing CYP1B1 enzyme in breast cancer[J]. Oncotarget, 2017, 8(63): 106608-106624. DOI:10.18632/oncotarget.22541 |
| [13] |
DE FRANCESCO E M, SIMS A H, MAGGIOLINI M, et al. GPER mediates the angiocrine actions induced by IGF1 through the HIF-1α/VEGF pathway in the breast tumor microenvironment[J]. Breast Cancer Res, 2017, 19(1): 129. DOI:10.1186/s13058-017-0923-5 |
| [14] |
FILARDO E J, QUINN J A, FRACKELTON A R Jr, et al. Estrogen action via the G protein-coupled receptor, GPR30: stimulation of adenylyl cyclase and cAMP-mediated attenuation of the epidermal growth factor receptor-to-MAPK signaling axis[J]. Mol Endocrinol, 2002, 16(1): 70-84. DOI:10.1210/mend.16.1.0758 |
| [15] |
TREMBLAY P G, SIRARD M A. Transcriptomic analysis of gene cascades involved in protein kinase A and C signaling in the KGN line of human ovarian granulosa tumor cells[J]. Biol Reprod, 2017, 96(4): 855-865. DOI:10.1093/biolre/iox024 |
| [16] |
GIULIANELLI S, RIGGIO M, GUILLARDOY T, et al. FGF2 induces breast cancer growth through ligand-independent activation and recruitment of ERα and PRBΔ4 isoform to MYC regulatory sequences[J]. Int J Cancer, 2019, ijc.32252. DOI:10.1002/ijc.32252 |
| [17] |
MIURA K, OBA T, HAMANAKA K, et al. FGF2-FGFR1 pathway activation together with thymidylate synthase upregulation is induced in pemetrexed-resistant lung cancer cells[J]. Oncotarget, 2019, 10(11): 1171-1192. DOI:10.18632/oncotarget.26622 |



