先天性肛门直肠畸形(anorectal malformations, ARMs)是儿童最常见的消化道畸形,发病率在新生儿为(2~5)/10 000,病理类型从简单的肛门狭窄、直肠会阴瘘到复杂的直肠膀胱瘘、泄殖腔畸形[1]。其中先天性肛门闭锁伴直肠舟状窝瘘(anorectal malformation with vestibular fistula, ARMVF)是女性ARMs患儿中最常见的类型,在女性ARMs中的发生率约为30%, 占ARMs患儿的10%~30%[2]。传统观点认为直肠会阴瘘、直肠舟状窝瘘等位置较低的病理类型术后预后更好。但长期随访结果表明:低位ARMs术后发生便秘的比例达到42%~70%,严重影响患儿的生活质量,其中ARMVF的便秘发生率最高,不低于61.4%[3-4]。本研究对我院2015年1月至2017年12月收治的51例ARMVF患儿临床资料及术后肛门功能随访进行统计分析,探究其术后便秘发生的可能原因,以期指导临床治疗。
1 资料与方法 1.1 临床资料收集2015年1月至2017年12月于我院行肛门成形术的ARMVF患儿临床资料51例。40例行分期手术(结肠造瘘-后矢状入路经骶会阴肛门成形术-结肠造瘘关闭术),11例行一期手术(后矢状入路经骶会阴肛门成形术)。肛门成形术时取直肠盲端标本,测量并记录患儿盲端位置及瘘口大小,采集直肠周围肌群图片。本组患儿手术年龄3.8~18.0(7.87±3.64)个月。分期手术者在关瘘时取结肠肠壁作为自身对照。本研究通过重庆医科大学附属儿童医院伦理委员会审查[(2019)年伦审(研)第(122)号]。
1.2 方法 1.2.1 术后肛门功能评估由同一名医师在完成手术治疗后6个月至3年对该组患儿进行电话随访,采用Rintala评分量表[5](>3岁)及修正评分量表(≤3岁)进行肛门功能评价。评价标准:①Rintala评分:总分0~20分,正常(≥17分),良好(13~16分),良(9~12分),差(≤8分)。②修正Rintala评分:总分0~17分,正常(≥15分),良好(10~14分),良(6~9分),差(≤5分)。便秘判断[6-7],具有以下症状中2种及以上者:排便次数 < 3次/周;大便干硬成团块状;排便费力;腹部“起包”;需要泻药协助排便。
1.2.2 标本制备标本经4%多聚甲醛溶液固定,脱水,石蜡包埋后行冠状连续切片,切片厚度4 μm,漂片后捞片于防脱载玻片备用。
1.2.3 HE及免疫组织化学染色HE染色:每例标本切片行常规HE染色,于光学显微镜下进行神经肌肉结构观察。免疫组织化学染色:采用中杉金桥PV-9000二步法,S-100兔抗人抗体、Calretinin(CR)兔抗人抗体均购于福州迈新生物技术开发公司。
1.2.4 肛门直肠周围肌群发育评估51例患儿均由同一名高级职称医师行后矢状入路经骶会阴肛门成形术,术中采集直肠周围肌群图片,术后采用盲法由同一位高年资专科医师主观评价直肠周围肌肉发育情况。
1.2.5 骶尾部MRI本组病例术前均行骶尾部MRI(GE Signapopeller HD 1.5T Echospeed型),评价脊柱、脊髓发育。
1.3 统计学分析采用SPSS 24.0统计软件,计量资料以x±s表示,组间比较采用独立样本t检验;计数资料采用χ2检验或Fisher确切概率检验。P < 0.05表示差异具有统计学意义。
2 结果 2.1 排便功能随访获访48例,失访3例。手术并发症包括1例切口感染和1例直肠黏膜脱垂,均对症处理后治愈。根据Rintala评分标准,肛门功能分类见表 1。12例(25.0%)便秘合并粪污,无大便失禁者。经Fisher确切概率检验,肛门功能评分非便秘组得分高于便秘组(P=0.014)。
2.2 手术方式
便秘组15例(占总病例数31.3%)行分期手术,5例(10.4%)行一期手术;非便秘组22例(45.8%)行分期手术,6例(12.5%)行一期手术,经连续性校正χ2检验,手术方式在两组患儿间差异无统计学意义(χ2=0.003,P>0.05)。
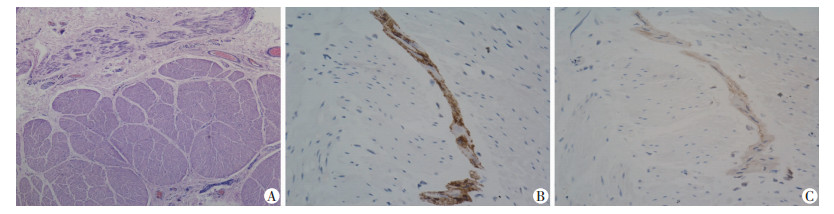
2.3 直肠盲端肠神经肌肉发育 2.3.1 HE染色标本均有不同程度的肠肌层发育异常,表现为肌层肥厚,大量结缔组织将肌束分割,排列紊乱(图 1A)。
|
| A:HE染色观察直肠末端肌层肥厚,排列紊乱(×40);B~C:免疫组织化学染色观察(二步法×400);B:S-100阳性;C:CR阳性 图 1 ARMVF患儿直肠盲端肠神经肌肉发育情况 |
2.3.2 免疫组织化学染色
结果采用定性判断,镜下观察免疫染色阳性的细胞呈棕黄色或黄褐色(图 1B、C)。S-100(+)、CR(+)记为有肠神经节细胞;S-100(+)、CR(-)记为无肠神经节细胞;再根据HE染色结合该患儿年龄,进一步分为肠神经节细胞发育正常或发育差[8]。经Fisher确切概率检验,肠神经节细胞发育异常程度组间差异具有统计学意义(P=0.025,表 2)。
2.4 肛门直肠周围肌群发育
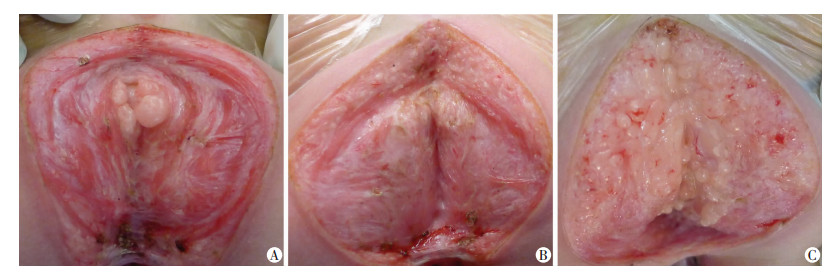
直肠周围肌群发育判断:肌肉走形规则清楚,分布清晰,肌纤维粗大且纹理清楚者评为优;直肠周围肌群走形紊乱,分布不清,肌纤维细小模糊不清且为大量脂肪组织所代替者评为差;介于二者之间视为良[9](图 2)。本组所有病例肛门直肠周围肌群发育优10例(10/51,19.6%),良26例(26/51,51.0%)、差15例(15/51,29.4%),随访到患儿中肛周肌群发育情况见表 3,经χ2检验,非便秘组肛周肌群发育优于便秘组(P=0.044)。
|
| A:肛周肌群发育优;B:肛周肌群发育良;C:肛周肌群发育差 图 2 ARMVF患儿肛门直肠周围肌群发育情况 |
2.5 瘘管大小及直肠盲端位置
经两独立样本t检验,瘘口大小及直肠盲端位置在两组间差异均无统计学意义(表 4)。
| 组别 | n | 瘘口大小 | 直肠盲端距肛隐窝距离 |
| 便秘组 | 20 | 5.20±1.28 | 9.75±1.97 |
| 非便秘组 | 28 | 5.25±1.99 | 9.64±1.89 |
| P值 | 0.150 | 0.837 |
2.6 骶尾部MRI
本组患儿骶尾部异常者共15例(29.4%),随访患儿中有13例。便秘组中11例(22.9%)正常,9例(18.8%)异常;非便秘组中24例(50.0%)正常,4例(8.3%)异常。经χ2检验,非便秘组骶尾部异常率低于便秘组(χ2=5.573,P=0.010)。
3 讨论ARMVF作为女性患儿中最常见的ARMs病理类型,被归类为“低位”,通常其术后排便功能被认为有更好的预后。但PEA等[10]和RINTALA等[5]对低位ARMs术后肛门功能进行随访,发现近半数的患儿存在不同程度的便秘。越来越多国内外研究表明ARMs患者肠神经系统发育异常可能是其术后便秘发生的重要因素[3, 11-12]。但排便作为一种复杂的生理活动,是多组织、多器官协同的结果,受饮食、心理、排便习惯等多方面影响。Rintala量表评分结果显示本研究随访到的患儿只有5例(10.4%)评分为良(便秘组4例,非便秘组1例),可判定为排便功能障碍。另16例虽未达到量表所给定的排便障碍标准,却存在反复便秘的情况。便秘组中17例便秘症状可通过饮食调整和排便功能训练缓解,余3例需长期使用助泻剂(开塞露等)辅助排便。提示医务人员在随访ARMs患儿肛门功能过程中,不能仅根据总体得分来评判患儿的排便功能异常与否,需关注各项症状的情况,有针对性地制订个体化术后肛门功能训练指导方案。
有研究对分期及一期手术的ARMVF进行术后排便功能评估发现,接受不同手术方式患儿在大便失禁、污粪及便秘方面差异无统计学意义[13-14]。本研究随访到的患儿37例行分期手术,11例行一期手术,术后便秘发生差异亦无统计学意义。故该病理类型的手术方式可结合患儿具体病情、术者经验及父母的意愿选择。
与LOMBARDI等[3]报道的ARMVF直肠盲端肠神经节细胞均发育异常稍不同,本研究通过组织学观察发现随访到的患儿肠神经节细胞发育正常者1例,余47例(97.8%)患儿均表现为直肠盲端肠神经节细胞发育不良或未见肠神经节细胞,且所有标本肠肌层有不同程度发育异常,可能与粪便潴留致直肠盲端继发性肥厚扩张有关。直肠盲端肠神经元及肌层发育异常致肠道不能进行正常舒缩活动,可能与术后便秘、粪污等并发症的发生相关。因此,直肠盲端肠神经节细胞发育不仅对术后肛门功能具有预测指导意义,也提示在术中不宜过多保留直肠盲端。
同样,肛周肌群及骶尾部骨骼神经作为排便反射中重要组成部分,其发育不良可致肛周肌群的感觉异常,引起排便障碍[15-16]。本研究发现部分ARMVF肛周肌群发育缺陷,肌肉走行紊乱,甚至为大量脂肪组织代替;非便秘组肛周肌群发育优于便秘组。对随访到的患儿骶尾部MRI情况进行统计,发现15例(29.4%)骶尾部异常,主要表现为脊髓栓系综合征、终丝脂肪变性、脊髓中央管扩张和骶尾椎形态异常等。与不合并骶尾部异常患儿相比,术后便秘发生差异具有统计学意义。提示无论何种病理类型,术前均应常规行骶尾部MRI检查,异常者除了及时纠正相关畸形外,在术后肛门功能训练中需引起更多关注并及时采取干预措施,避免便秘等并发症的发生。
本研究暂未观察到瘘口大小及直肠盲端距离在两组间的差异,其与便秘的关系有待于样本量扩大进一步探究。
本研究分析了ARMVF术后便秘的可能原因,同时也存在不足,一是肛门功能随访时患儿年龄偏小,不能很好评估其社会心理情况。有学者报道随着年龄的增长,ARMs患儿便秘情况会得到改善[17],因此患儿术后远期肛门功能及社会心理评价需要长期规律随访及样本量的扩大。二是术后肛门功能恢复涉及合并畸形、术后正规康复训练、系统长期肠道管理、家长依从性等方面,本研究仅对有限的因素进行了探讨,暂未对其他情况合并分析,具有一定局限性。但ARMVF术后高便秘率在肛门功能康复训练中不容忽视,因此对此类患儿不能仅依据病理类型评估预后,需结合直肠盲端肠神经肌肉、肛周肌群及骶尾部发育等情况综合预估,对可能出现的问题行前瞻性预防并及时处理,避免术后顽固性便秘的发生。
| [1] |
LEVITT M A, PEÑA A. Anorectal malformations[J]. Orphanet J Rare Dis, 2007, 2: 33. DOI:10.1186/1750-1172-2-33 |
| [2] |
MURPHY F, PURI P, HUTSON J M, et al. Incidence and frequency of different types, and classification of anorectal malformations[M]//HOLSCHNEIDER A M, HUTSON J M. Anorectal malformations in children. Berlin: Springer-Verlag Berlin Heidelberg, 2006: 163-184. DOI: 10.1007/978-3-540-31751-7_8.
|
| [3] |
LOMBARDI L, BRUDER E, CARAVAGGI F, et al. Abnormalities in "low" anorectal malformations (ARMs) and functional results resecting the distal 3 cm[J]. J Pediatr Surg, 2013, 48(6): 1294-1300. DOI:10.1016/j.jpedsurg.2013.03.026 |
| [4] |
LEVITT M A, KANT A, PEÑA A. The morbidity of constipation in patients with anorectal malformations[J]. J Pediatr Surg, 2010, 45(6): 1228-1233. DOI:10.1016/j.jpedsurg.2010.02.096 |
| [5] |
RINTALA R J, LINDAHL H G, RASANEN M. Do children with repaired low anorectal malformations have normal bowel function?[J]. J Pediatr Surg, 1997, 32(6): 823-826. DOI:10.1016/S0022-3468(97)90628-X |
| [6] |
王维林.关于儿童便秘诊治问题//第七届全国小儿肝胆、肛肠及新生儿外科学术研讨会论文集[C].青岛: 2011: 9-11. WANG W L. On the diagnosis and treatment of constipationin children//Proceedings of the 7th National Symposium on Pediatric Hepatobiliary, Anorectal and Neonatal Surgery[C]. Qingdao: 2011: 9-11. |
| [7] |
ROME FOUNDATION. Guidelines: rome Ⅲ diagnostic criteria for functional gastrointestinal disorders[J]. J Gastrointestin Liver Dis, 2006, 15(3): 307-312. |
| [8] |
GUINARD-SAMUEL V, BONNARD A, DE LAGAUSIE P, et al. Calretinin immunohistochemistry: a simple and efficient tool to diagnose Hirschsprung disease[J]. Mod Pathol, 2009, 22(10): 1379-1384. DOI:10.1038/modpathol.2009.110 |
| [9] |
HUSSAIN S M, STOKER J, LAMÉRIS J S. Anal sphincter complex: endoanal MR imaging of normal anatomy[J]. Radiology, 1995, 197(3): 671-677. DOI:10.1148/radiology.197.3.7480737 |
| [10] |
PEÑA A. Posterior sagittal anorectoplasty: Results in the management of 332 cases of anorectal, malformations[J]. Pediatr Surg Int, 1988(3): 94-104. DOI:10.1007/bf00182760 |
| [11] |
王龙, 孟祥宇, 史兴晔, 等. 先天性肛门直肠畸形肛门内括约肌肌间神经节细胞及神经丛的研究[J]. 中国医师杂志, 2008, 10(5): 607-609. WANG L, MENG X Y, SHI X Y, et al. Study on the ganglion cell and the number of nerve plexus in the internal sphincter of the internal anus sphincter of rats with congenital anorectal malformations(ARM)[J]. J Chin Physician, 2008, 10(5): 607-609. DOI:10.3760/cma.j.issn.1008-1372.2008.05.010 |
| [12] |
PANDEY A, PANDEY P, SINGH S P, et al. Histology with immunohistochemistry of the fistula region in female anorectal malformation: Can it be used for neo-anus reconstruction?[J]. J Paediatr Child Health, 2018, 54(2): 177-182. DOI:10.1111/jpc.13691 |
| [13] |
KARAKUS S C, USER I R, AKCAER V, et al. Posterior sagittal anorectoplasty in vestibular fistula: with or without colostomy[J]. Pediatr Surg Int, 2017, 33(7): 755-759. DOI:10.1007/s00383-017-4102-7 |
| [14] |
LAURITI G, DI RENZO D, LELLI CHIESA P, et al. One-stage repair of anorectal malformations in females with vestibular fistula: a systematic review and meta-analysis[J]. Pediatr Surg Int, 2019, 35(1): 77-85. DOI:10.1007/s00383-018-4378-2 |
| [15] |
贾慧敏, 王维林, 袁正伟, 等. 先天性肛门直肠畸形胎鼠腰骶髓副交感神经元发育异常的研究[J]. 中华小儿外科杂志, 2004, 25(3): 279-281. JIA H M, WANG W L, YUAN Z W, et al. Quantitative analysis of the rectal parasympathetic neurons in rats with anorectal malformation[J]. Chin J Pediatr Surg, 2004, 25(3): 279-281. DOI:10.3760/cma.j.issn.0253-3006.2004.03.024 |
| [16] |
YUAN Z W, LUI V C, TAM P K. Deficient motor innervation of the sphincter mechanism in fetal rats with anorectal malformation: a quantitative study by fluorogold retrograde tracing[J]. J Pediatr Surg, 2003, 38(9): 1383-1388. DOI:10.1016/S0022-3468(03)00401-9 |
| [17] |
WAKHLU A, KUREEL S N, TANDON R K, et al. Long-term results of anterior sagittal anorectoplasty for the treatment of vestibular fistula[J]. J Pediatr Surg, 2009, 44(10): 1913-1919. DOI:10.1016/j.jpedsurg.2009.02.072 |



