2. 心理学院行为医学教研室
2. Department of Behavioral Medicine, School of Psychology, Army Medical University (Third Military Medical University), Chongqing, 400038, China
我国为肝癌发病大国,全世界每年新发肝癌病例的一半左右在中国[1]。在我国的肿瘤排行榜上,肝癌的发病率和病死率均位居第2位[2]。根治性肝癌切除手术是降低死亡率、提高生存率的关键。但为了防止手术后肝功能衰竭,术前需评估切除后剩余(保留)的肝脏体积(future liver remnant,FLR)占标准肝脏体积(standard liver volume, SLV)的比例,对无肝硬化者,剩余肝体积应占到标准肝脏体积的30%以上,有肝硬化者,剩余肝体积应≥40%,才能施行肝癌切除手术[3]。由于我国以慢性乙肝患者为主的肝癌高危人群大多没有定期行肝癌筛查,很多患者在出现症状而就医时已属中晚期,肿瘤巨大,且常伴有肝炎后肝硬化,肝脏储备功能差,在需要行大范围肝切除的根治性手术时,常常因剩余肝体积不足而无法施行手术,致使我国的肝癌根治切除率小于30%。
近年来,一种全新的手术方式开始成为肝胆外科领域的热点,即联合肝脏离断和门静脉结扎的二步肝切除术(associating liver partition and portal vein ligation for staged hepatectomy,ALPPS)。该手术分两步(两期)进行,第一期手术将病侧肝脏离断及门静脉结扎,以刺激肝细胞增生,使健侧肝体积在短期(数日)内快速增加,以保证第二期手术(病肝切除术)后,健侧剩余肝足以代偿肝脏功能。该手术为剩余肝体积不足的肝癌患者提供了根治性切除的机会,被誉为肝胆外科革命性的突破[4]。但该手术风险较大,手术并发症发生率高,国外的资料报道其并发症率达27%~72.9%,死亡率高达9%~25%[5]。国内有个案或小样本的报道,探讨了适应证、手术方法、术中配合、预后等方面的内容,但关于ALPPS术后并发症的观察分析方面,缺少报道。
我科从2014年7月至2017年6月为26例中晚期肝癌患者成功实施了ALPPS手术,现将该组病人术后并发症的观察分析方面内容,报告如下。
1 资料与方法 1.1 一般资料2014年7月至2017年6月,笔者所在的陆军军医大学第一附属医院肝胆外科对26例剩余肝体积不足的中晚期原发性肝癌患者实施了ALPPS手术。男性21例,女性5例,中位数年龄44岁(33~66岁)。26例患者均合并肝炎后肝硬化,肝功能Child-Pugh分级均为A级。
1.2 术前预留/剩余肝体积评估方法患者术前均行相关血液学检测及影像学检查,以CT三维成像技术测定、以EDDA软件计算剩余肝脏体积占标准肝脏体积的比例,计算公式为:剩余肝体积占比=剩余肝体积/标准肝体积×100%[3]。第一期手术后每周行一次CT检查,评估预留肝体积增长的情况。本研究中26例患者一期手术前评估预留肝体积所占比例均小于40%(平均28.88%),一期手术后肝体积平均增生65.07%;两期手术间隔时间平均28.8 d(13~84 d)(表 1)。
| 序号 | 一期手术术前FLR/SLV(%) | 二期手术术前FLR/SLV(%) | 肝体积增长率(%) | 两期手术间隔(d) |
| 01 | 28 | 40 | 42.86 | 28 |
| 02 | 36 | 49 | 36.11 | 19 |
| 03 | 28 | 41 | 46.43 | 21 |
| 04 | 28 | 45 | 60.71 | 29 |
| 05 | 19 | 40 | 110.53 | 26 |
| 06 | 39 | 53 | 35.89 | 24 |
| 07 | 33 | 45 | 36.36 | 13 |
| 08 | 34 | 55 | 61.76 | 32 |
| 09 | 29 | 44 | 51.72 | 16 |
| 10 | 28 | 40 | 42.86 | 17 |
| 11 | 26 | 42 | 61.54 | 26 |
| 12 | 39 | 72 | 84.62 | 35 |
| 13 | 27 | 51 | 88.89 | 77 |
| 14 | 22 | 40 | 81.82 | 84 |
| 15 | 38 | 55 | 44.74 | 20 |
| 16 | 15 | 44 | 193.33 | 13 |
| 17 | 21 | 42 | 100 | 22 |
| 18 | 27 | 40 | 48.15 | 15 |
| 19 | 25 | 40 | 60 | 26 |
| 20 | 27 | 42 | 55.56 | 33 |
| 21 | 30 | 41 | 36.67 | 13 |
| 22 | 29 | 50 | 72.41 | 64 |
| 23 | 36 | 50 | 38.89 | 13 |
| 24 | 34 | 40 | 17.65 | 26 |
| 25 | 20 | 48 | 140 | 27 |
| 26 | 33 | 47 | 42.42 | 32 |
1.3 手术方法
一期手术在开腹或腹腔镜下沿镰状韧带或其右侧缘行原位肝实质离断(射频辅助方式为使用射频凝血器沿肝脏预切除线凝固肝组织),保留肝动脉血供,结扎患侧门静脉支。待保留侧肝脏剩余体积达到标准后根据患者整体的状态决定二期手术时机。二期手术在开腹或者腹腔镜下切除右肝动脉、右肝胆管、右门静脉、肝右及肝中静脉,切除患侧肝脏。26例患者一期手术的方式分别为:腹腔镜手术14例,开腹手术12例(其中射频消融术辅助6例);二期手术方式为:腹腔镜手术8例,开腹手术18例。
1.4 围手术期并发症的观察护理密切观察病情变化,观察记录并发症的发生、发展、处理及转归情况。使用Clavien-Dindo分级系统进行术后并发症分级,该分级系统将外科并发症分为Ⅰ~Ⅴ五级,其中≥Ⅲb级的为严重并发症,包括:并发症需再次手术处理(Ⅲb级)、并发症需重症监护治疗(Ⅳ级)、死亡(Ⅴ级)[6]。随时与主管医生沟通,并在出院时查阅完整的医疗记录及护理记录文书,请主管医生再次确认记录资料的准确性。
1.5 随访所有病人出院后前3个月每月随访1次,随后每3个月随访1次。
2 结果 2.1 患者手术及随访结局本组患者在14例病人出现并发症,其中Ⅱ级5例,Ⅲa级7例,Ⅳa级1例,Ⅴ级1例。并发症包括肝功能不全、胸腔积液、腹水、感染性等,除2例病人(7.7%)发生严重并发症外(1例因败血症转入重症监护室治疗后好转,另一例因术后肝功能衰竭死亡。),其余病人经保守治疗后好转。
本研究中1例患者在二期术后22 d死亡,余25例患者中位随访时间为28月(8~59个月)。1年、3年总体生存率分别为88%(22/25)、52%(13/25),1年、3年无瘤生存率分别为56%(14/25)、16%(4/25)(如图 1)。

|
| A:无瘤生存率; B:总体生存率 图 1 本组25例中晚期原发性肝癌患者生存曲线图 |
2.2 术后肝功能的变化情况及预后
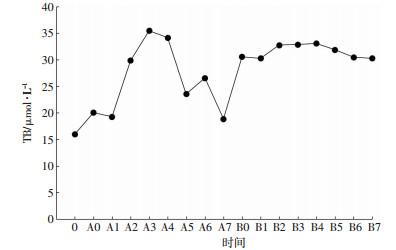
密切观察肝功能的变化情况及变化趋势,对于判断肝功能的恢复情况,以及有无肝功能衰竭至关重要。本研究中患者ALT及TB在一期术后迅速上升后很快恢复,在二期术后ALT及TB仅小幅度升高并逐渐恢复(如图 2-3)。本组26例中,25例病人术后肝功能均逐渐恢复至正常,1例病人在二期术后第5天出现“胆酶分离”现象,术后13天时出现昏迷,考虑肝性脑病,随后逐渐出现多器官功能衰竭,经治疗无效死亡。

|
| 0:手术前,A0:一期手术当日;B0:二期手术当日;A1~A7、B1~B7:一期、二期术后第1天~术后第7天 图 2 25例患者两次手术后谷丙转氨酶(ALT)变化趋势 |
|
| 0:手术前,A0:一期手术当日;B0:二期手术当日;A1~A7、B1~B7:一期、二期术后第1天~术后第7天 图 3 25例患者两次手术后总胆红素(TB)变化趋势 |
第一期手术后,术后第一周26例病人均出现了不同程度的低白蛋白症(血清白蛋白 < 35 g/L),需静脉输入人血白蛋白治疗,第二周随着自身肝脏合成功能的恢复,无须外源性白蛋白补充。第二次手术后,所有患者在术后第一周均接受了人血白蛋白治疗,至术后第二周,13例病人(50%)仍因低蛋白血症而需间断输入白蛋白。
2.3 胸腔积液的处理结果一期手术后,34.6%(9/26)的患者发生了胸腔积液。其中8例病人在术后3~7天、1例在术后第9天出现了不同程度的低中度发热、胸闷、气短、氧饱和度下降,超声检查证实右侧胸腔积液1例,左侧胸腔积液1例,双侧胸腔积液7例。除一例因积液量大于500 mL、行胸腔穿刺置管引流后好转,其余患者积液量较少,经保守治疗后积液逐渐吸收、好转。
二期手术后,12例病人(46.2%)发生了胸腔积液(右侧胸腔积液10例,双侧胸腔积液2例),其中2例发生在术后第3~7天,10例发生在术后8~12 d。除一例积液量少自行吸收之外,其余11例胸腔积液量较大(>500 mL),行胸腔穿刺抽液或置管引流后好转。
2.4 腹水的处理结果一期手术后,21例病人每日腹腔引流液均小于500 mL,于术后一周内拔出腹腔引流管,5例病人(19.2%)因每日腹腔引流液大于500 mL,经静脉输入白蛋白、利尿药物等处理后,腹水逐渐减少,于术后第二周拔管。二期手术后,14例病人(53.8%)在术后一周内每日腹腔引流液大于500 mL,经对症支持治疗后于术后第二周拔出腹腔引流管。
2.5 感染性并发症的观察及处理本组病例一期手术后发生感染性并发症4例(15.4%),其中3例为肺部感染、1例胆道感染;二期手术后发生感染性并发症7例(26.9%),其中肺部感染3例、腹腔感染2例、胆道感染1例、切口感染1例。均经抗感染药物治疗后好转。仅1例因败血症感染性休克转入重症监护室,经抗感染、对症支持等治疗后好转。本组病人未发生胆漏等与肝切除有关的并发症。
3 讨论我国的肝癌发病率及死亡率在肿瘤排行榜上高居第二位,根治性肝癌切除手术是降低死亡率、提高生存率的关键。对于传统方法无法切除的巨大肝癌、肝功能储备差的肝硬化肝癌等患者,联合肝脏离断和门静脉结扎的二步(二期)肝切除术(ALPPS)为其提供了根治性切除的机会。但该手术作为肝胆外科领域的最新术式,国内仅有零星报道,关于两期手术围手术期间的肝功能变化规律、并发症的观察及特点分析等,缺少报道。
对本组26例ALPPS术后肝功能指标的观察发现,两次手术后,谷丙转氨酶(ALT)的峰值均出现在术后第1~2天,一期术后ALT升高的幅度较二期术后更大、峰值更高。原因与第一次手术施行病肝分隔及门静脉结扎所致的病肝缺血缺氧、肝细胞损伤有关。从术后第3天开始,ALT持续下降,表明肝细胞损伤逐渐恢复(见图 1)。总胆红素在一期术后表现为快升快降的趋势,一期手术后,一方面患侧肝脏的肝细胞缺血缺氧致肝脏功能减弱,另一方面,结扎患侧肝脏(病肝)的门静脉分支后,可使对侧(健侧)肝脏的血流量增加,各种营养物质和细胞因子促使健侧肝组织快速增生,肝功能快速回升至代偿水平[7]。但第二次手术的大面积肝切除,肝实质的减少及手术创伤,使胆红素值在术后第1~5天均在较高水平,随后剩余肝的功能逐渐恢复至代偿水平,胆红素值逐渐下降(见图 3)。而在术后5天之后总胆红素仍进行性升高者,应高度警惕剩余肝功能失代偿及肝功能衰竭的发生。因此,ALPPS术后严密观察肝功能的变化趋势具有重要的临床意义。
本组资料显示并发症中胸腔积液最为常见,一期手术后其发生率为34.6%,多发生在术后第3~7天,但积液量较少,仅1例需行胸腔穿刺置管引流;二期手术后,12例(46.2%)发生胸腔积液,以右侧胸腔积液为主,多发生在术后第8~12天,积液量较大,其中11例行胸腔穿刺抽液或引流。国外的文献亦报道ALPPS术后胸腔积液为常见并发症(发生率为6.0%~47.1%)[5]。分析原因,一方面与手术操作刺激膈肌、损伤淋巴回流通路等原因有关,另一方面,由肝硬化及肝脏手术引起的低蛋白血症也可加重第三间隙的渗出,包括胸腔积液、腹腔积液等(本组病例中大多数病人亦出现了中等量的腹水)[5, 8]。本研究中对于有胸腔积液且取坐位时B超测定一侧胸腔内液性暗区最大深度≥5 cm的患者(估计积液量大于500 ml)采取胸腔穿刺引流处理[9]。因此,在一期手术后第1周、二期手术后第2周,应密切观察病人的体温及呼吸情况,出现低中度发热、胸闷、气短、氧饱和度下降等症状时,应考虑胸腔积液的可能性,及时行床旁超声检查协助诊断,根据积液量的多少制定治疗方案,做好胸腔穿刺及胸腔闭式引流等相关护理。
感染亦是ALPPS术后常见并发症[5]。本组病例两期手术后感染性并发症的发生率分别为15.4%、26.9%,其中肺部感染居第一位。分析原因,一方面,胸腔积液及胸腔穿刺置管等操作增加了肺部感染的机会,另一方面,也与术后胸水、腹水、手术创伤等原因使病人卧床时间增加、咳嗽咳痰乏力等因素有关[10]。因此,对ALPPS术的患者,术前应加强深呼吸锻炼、进行有效咳嗽咳痰的练习,制定活动计划,鼓励病人术后早期下床活动等,以减少肺部感染的发生。
此外,胆漏作为肝切除术后并发症之一,表现为腹痛、发热等症状,腹腔引流管引流出胆汁是判断术后胆漏的重要依据。胆漏可导致肝断面包裹性积液、胆汁性腹膜炎,严重者可继发腹腔感染和肝功能衰竭。本组患者未发生胆漏,结合文献分析,本组26例患者均为半肝切除,其中20例采用了腹腔镜解剖性肝切除及射频消融技术,解剖性肝切除断面管道结构较少,能有效降低胆漏及出血风险,而射频消融术独特的热封闭效应避免了肝脏创面的形成[3]。本研究虽未发现一例胆漏患者,胆漏仍为肝切除常见并发症,术后应严密观察,有助于医生及时了解患者情况并及时处理,避免出现严重后果。
本研究中25例术后正常出院的患者均获得随访,本研究中晚期肝癌患者在既往认为是没有手术切除机会的,在经过ALPPS术后,大部分病人均获得了较好的生存获益。本研究中围术期死亡率为4%(1/25),明显高于传统肝切除术。原因一方面可能与术前手术评估有关,在患者术前评估时,应充分考虑患者肝脏储备情况,除了ICG 15分钟滞留率和肝脏剩余体积/标准肝体积之外,还应考虑患者的肝硬化程度、心肺功能及有无合并证等情况。另一方面与本组病例数有限,其代表性不足。为了进一步分析ALPPS的优势,需要精心设计的多中心随机对照试验。
综上所述,ALPPS为传统方法无法手术切除的肝癌患者提供了根治性切除肝癌病灶的机会,使大部分的晚期肝癌患者获得较好的生存,但因术式新,手术复杂,密切观察围手术期并发症的发生情况,积极采取措施防范严重并发症发生,尽可能减少围术期死亡率具有重要临床意义。
| [1] |
WALY RAPHAEL S, ZHANG Y D, CHEN Y X. Hepatocellular carcinoma: focus on different aspects of management[J]. ISRN Oncol, 2012, 2012: 421673. DOI:10.5402/2012/421673 |
| [2] |
陈建国. 中国肝癌发病趋势和一级预防[J]. 临床肝胆病杂志, 2012, 28(4): 256-260. CHEN J G. Trends in the incidence of liver cancer and its primary prevention in China[J]. J Clin Hepatol, 2012, 28(4): 256-260. DOI:10.3969/j.issn.1001-5256.2012.04.006 |
| [3] |
王强, 闫军, 冯晓彬, 等. 射频辅助的ALPPS治疗合并肝硬化的原发性肝癌:我们的初步经验[J]. 中国普外基础与临床杂志, 2016, 23(1): 14-17. WANG Q, YAN J, FENG X B, et al. Radiofrequency-assisted ALPPS treatment the patients with cirrhosis-related primary hepatocellular carcinoma: An initial report[J]. Chin J Bases Clin Gen Surg, 2016, 23(1): 14-17. |
| [4] |
TORRES O J, MORAES-JUNIOR J M, LIMA E LIMA N C, et al. Associating liver partition and portal vein ligation for staged hepatectomy (ALPPS): A new approach in liver resections[J]. Arq Bras Cir Dig, 2012, 25(4): 290-292. DOI:10.1590/S0102-67202012000400015 |
| [5] |
SCHADDE E, ARDILES V, ROBLES-CAMPOS R, et al. Early survival and safety of ALPPS: first report of the International ALPPS Registry[J]. Ann Surg, 2014, 260(5): 829-836. DOI:10.1097/SLA.0000000000000947 |
| [6] |
DINDO D, DEMARTINES N, CLAVIEN P A. Classification of surgical complications[J]. Ann Surg, 2004, 240(2): 205-213. DOI:10.1097/01.sla.0000133083.54934.ae |
| [7] |
王春阳, 王小明. ALPPS的研究现状及应用前景[J]. 肝胆胰外科杂志, 2017, 29(1): 81-83, 88. WANG C Y, WANG X M. Research Status and Application Prospect of ALPPS[J]. J Hepatopancreatobiliary Surg, 2017, 29(1): 81-83, 88. DOI:10.11952/j.issn.1007-1954.2017.01.023 |
| [8] |
袁卫平, 谭新华, YUAN Wei-ping, 等. 原发性肝癌切除术后胸水成因的临床研究[J]. 中国癌症防治杂志, 2009, 1(2): 134-136. YUAN W P, TAN X H, YUAN W P, et al. Clinical research on cause of pleural fluid after hepatectomy[J]. Chin J Oncol Prevent Treat, 2009, 1(2): 134-136. DOI:10.3969/j.issn.1674-5671.2009.02.013 |
| [9] |
刘鹏飞, 徐雯, 刘凯, 等. 原发性肝癌术后胸腔积液的预防和处理[J]. 同济大学学报(医学版), 2017, 38(2): 95-97. LIU P F, XU W, LIU K, et al. Factors related to postoperative pleural effusion in patients with primary liver cancer[J]. J Tongji Univ (Med Sci), 2017, 38(2): 95-97. DOI:10.16118/j.1008-0392.2017.02.019 |
| [10] |
管向东, 唐朝霞. 腹部手术后肺部感染的处理[J]. 中国实用外科杂志, 2011, 31(9): 874-876. GUAN X D, TANG Z X. Treatment of pulmonary infection after abdominal surgery[J]. Chin J Prac Surg, 2011, 31(9): 874-876. |



