神经母细胞瘤(neuroblastoma,NB)是好发于儿童外周交感神经系统的高度恶性实体肿瘤,起病较隐匿,侵袭性高,易发生早期转移[1],占所有儿科癌症死亡人数的15%[2]。研究表明,NB的初始分期在很大程度上决定选择何种治疗方式是最合适的[3]。因此,明确诊断及有无转移并进行正确分期(分期标准:1993年Brodeur修改之后International Neuroblastoma Staging System, INSS)对患儿的治疗以及预后具有重要作用。
奥曲肽(octreotide)是生长抑素类似物,与肿瘤细胞表面表达的生长抑素受体(somatostatin receptor, SSTR)具有高亲和力,可特异性结合[4],在神经内分泌肿瘤的诊断和治疗中占据重要地位[5-6]。SSTR G蛋白具有7个跨膜结构域,5种亚型,其中SSTR2是NB细胞表面高度表达的SSTR,从而为生长抑素类似物在临床影像诊断的应用提供了分子靶向基础[7]。文献[8]显示99mTc标记的生长抑素类似物显像可获得较好的图像质量及较高的肿瘤检测灵敏度。因此,奥曲肽的应用有助于NB的诊断及治疗[9]。本研究分析本院行全身99mTc-奥曲肽显像(99mtechnetium-hydrazinonicotinyl-tyr 3-octreotide,99mTc-HTOC)检查的32例临床疑似NB患儿情况,探讨其在NB诊断及分期中的应用价值。
1 资料与方法 1.1 研究对象选择2016年3月至2018年3月在本院进行99mTc-HTOC显像的32例临床疑似NB、并至少接受了一项传统影像学检查的患儿;男性21例,女性11例,年龄3个月至8岁,其中≤4岁的31例,>4岁的1例。收集患儿的所有影像学资料、病理结果及临床病史。
纳入标准:①年龄≤14岁;②至少有一种传统影像学检查怀疑NB;③血细胞计数:Hb≥90 g/L,WBC≥2.0×1012/L,PLT≥100×109/L;④肝、肾功能:ALT≤40 U/L,AST≤40 U/L,胆红素 < 2.5 mg/dL, 肌酸酐 < 2 mg/dL;⑤全身奥曲肽显像检查前停止生长抑素相关治疗(短效药物停用≥48 h,长效药物停用≥4周)。排除标准:已切除肿瘤的患儿。
1.2 放射性药物的制备① 10 μg前体(HYNIC,上海吉尔医药有限公司)、20 mg共配体(Tricine,北京鼎国生物技术有限公司)、10 mg乙二胺乙二酸(EDDA,Fluka公司)、10 mg氯化亚锡(E.Merek.Germany)、50 μL的氢氧化钠(重庆川东化工有限公司)以及925~1 110 MBq的高锝酸钠(重庆原子高科股份有限公司),将其在无菌玻璃瓶内混匀;②将以上制备液放置在100 ℃沸水中水浴15 min后,放置常温备用;③利用滤膜对制备液进行纯化;④纯化后应用薄层扫描仪进行放化纯度检测;⑤所有操作必须遵守无菌操作原则,制备液放化纯度≥90%即可抽取370 MBq制备液进行注射;⑥药物均经过细菌培养、热源检测等安全性检测。
1.3 显像方法采用单光子发射型计算机断层显像仪(SPECT, GE Millenium VG),能峰140 keV,窗宽20%,全身采集模式:采集速度为15 cm/min,像素1 024×256,层厚4.42 mm;断层扫描模式:扫描速度30 s/帧,矩阵128× 128,每个探头旋转180°。在放射性药物注射后的第1、4小时分别进行全身扫描及断层扫描。应用HERMES (Hermes Medical Solutions AB, Sweden)软件系统进行SPECT图像和CT图像的异机融合成像分析。
1.4 图像分析奥曲肽图像均由两名主治医师共同阅片,意见不一致时再由一名主任医师参与阅片并最终达成一致。当任何奥曲肽非生理性摄取区出现放射性摄取浓聚、并明显比周围及对侧相应部位放射性摄取浓聚时,即为奥曲肽摄取阳性表达。
1.5 参考标准及统计学分析采用参考标准是组织病理学、传统影像学检查及临床随访结果相结合,传统影像学扫描部位均为肿瘤相应部位。由于技术及伦理的原因,未对所有的转移病灶进行组织病理学检查。采用SPSS19.0软件进行数据处理,计数资料以百分比表示,采用配对四格表卡方检验,P < 0.05表示差异有统计学意义。
2 结果 2.1 患儿症状特征及原发肿瘤部位本研究选取32例患儿,临床表现包括不明原因的发热、腹痛、腹胀、腹部包块、咳嗽及喘息等,大多数患儿都是以发现包块就诊。其中原发肿瘤部位在左侧腹膜后9例、右侧腹膜后9例、双侧腹膜后3例、左侧肾上腺1例、右侧肾上腺1例、腹部1例、纵隔7例、左侧颈部1例。
2.2 99mTc-HTOC显像与传统影像学对病灶的检出率32例患儿中有30例行超声检查,32例行CT检查,9例行MRI检查。组织病理学检查诊断为NB的30例患儿中,99mTc-HTOC显像对原发病灶检出29例,断层显像对病灶的显示优于全身平面显像(图 1、2),而传统影像学检查检出30例,两种方法对NB原发灶检出的阳性率差异无统计学意义(P>0.05);99mTc-HTOC显像对全身转移灶检出率100%(45/45处),而传统影像学检查检出率42.2%(19/45处),主要转移部位为骨、淋巴结及肝脏等(表 1);99mTc-HTOC显像对全身转移灶的检出具有明显的优势,特别是对全身骨转移病灶的检出。
|
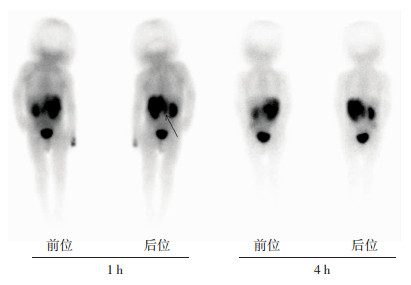
| 箭头示:左侧腹膜后包块奥曲肽阳性表达 图 1 左侧腹膜后分化差型NB 99mTc-HTOC前后位(第1、4小时)平面显像 (1岁男性) |
| 病灶 | 99mTc-HTOC | 传统影像学 |
| 原发病灶 | 29 | 30 |
| 转移病灶 | 45 | 19 |
| 骨 | 28 | 2 |
| 肝脏 | 3 | 3 |
| 淋巴结 | 11 | 10 |
| 其他 | 3 | 4 |
2.3 99mTc-HTOC诊断NB的灵敏度
32例患儿均经组织病理学检查明确诊断,其中27例患儿经手术切除获取标本,5例患儿经穿刺活检获取标本。组织病理学与99mTc-HTOC显像均诊断为NB的有29例,均未诊断为NB的有1例,99mTc-HTOC显像阳性病理阴性的有1例,99mTc-HTOC显像阴性病理阳性的有1例(表 2);两种方法诊断NB的阳性率差异无统计学意义(P=1)。99mTc-HTOC显像诊断NB的灵敏度96.7%(29/30例),特异度50.0%(1/2例),阳性预测值96.7%(29/30例),阴性预测值50%(1/2例),诊断符合率达93.8%(30/32例)。30例99mTc-HTOC阳性显像病例中,病理学确认29例为NB(图 3),1例为左侧腹膜后未成熟畸胎瘤Ⅱ级(图 4);2例99mTc-HTOC阴性显像病例中,病理学确认1例为右侧腹膜后NB,另1例为(肠周、大网膜)Burkitt淋巴瘤。
| 99mTc-HTOC | 组织病理学(例) | ||
| 阳性 | 阴性 | 合计 | |
| 阳性 | 29 | 1 | 30 |
| 阴性 | 1 | 1 | 2 |
| 合计 | 30 | 2 | 32 |
| 阳性代表诊断NB;阴性代表非NB | |||
|
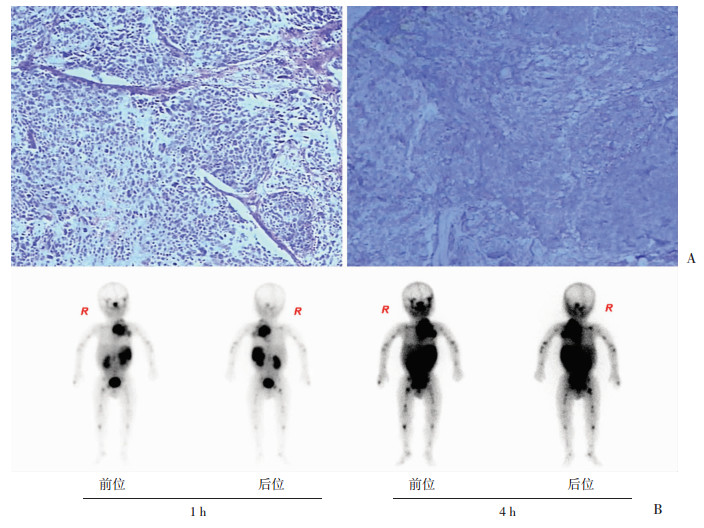
| A:病理学观察左:HE×100;右:免疫组化(S-P ×100) CgA(+)、ALK灶(+)、N-MYC弱(+)、Syn(+); B: 99mTc-HTOC图像左上纵隔肿块奥曲肽高表达及全身多处骨转移 图 3 左侧颈部淋巴结分化差型NB病理表现及99mTc-HTOC图像 (1岁男性患儿) |
|
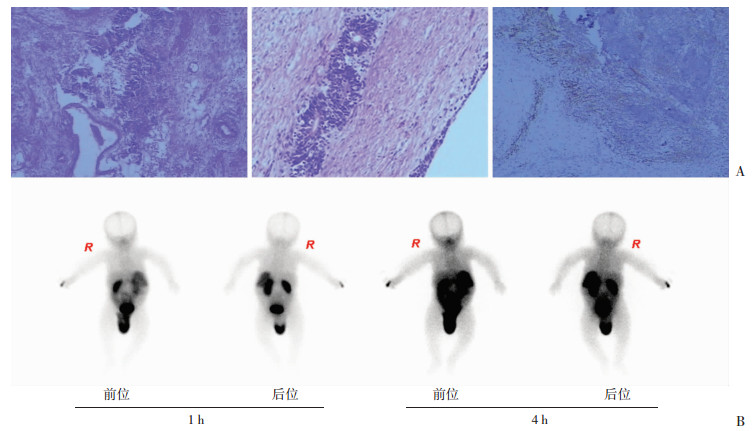
| A:病理学观察从左至右分别为:HE×40、HE×100及免疫组化(S-P ×100);免疫组化显示CgA灶(+),Syn神经胶质及原始神经管(+);B:99mTc-HTOC图像左侧腹膜后巨大团状不均匀的放射性摄取增高 图 4 左侧腹膜后未成熟畸胎瘤病理表现及99mTc-HTOC图像 (3个月男性患儿) |
2.4 肿瘤初始分期改变
在30例确诊为NB的患儿中,Ⅰ期2例,Ⅱ期2例,Ⅲ期8例,Ⅳ期13例,ⅣS期5例。因行99mTc-HTOC显像改变初始分期的有3例(10%),其中1例患儿行99mTc-HTOC显像后发现肝脏及左侧肾上腺区的转移,因而肿瘤初始分期从ⅡA期上升到Ⅳ期,其余2例患儿99mTc-HTOC显像均发现全身多处的骨转移灶,因而肿瘤初始分期从Ⅲ期上升到Ⅳ期。
3 讨论NB占儿童4岁以下所有肿瘤的15%,本组病例4岁以下患儿占96.9%(31/32例)。NB的临床症状缺乏特异性,易早期转移。因此,如果有一种靶向性的诊断方式,不仅能早期而准确的诊断NB并能正确分期,对NB的治疗以及预后都具有深远的影响。
目前NB的影像学检查方法有传统影像学检查方法(超声、CT、MRI)、全身骨显像(whole body bone scan, 99mTc-MDP)、123I-间碘代苄胍(MIBG)、正电子发射型计算机断层显像(positron emission tomography/computed tomography,18F-FDG PET/CT)以及生长抑素显像。传统影像学检查方法对原发病灶检出率高,但在定性以及全身转移灶检出方面较差。99mTc-MDP对明确有无骨转移具有很高的灵敏度,但缺乏特异性,因此对全身骨转移灶及原发灶的检出都低于99mTc-HTOC显像。MIBG是肾上腺素能神经元阻滞剂,能特异性的与肾上腺素受体结合,可被神经嵴来源的组织和肿瘤摄取和滞留;研究显示,123I-MIBG是功能显像的金标准,但其诊断阴性率仍可达15%[10]。18F-FDG PET/CT可以反映肿瘤细胞的增殖代谢情况,早期发现微小病灶及转移灶,近年来在儿童NB的诊断及分期中极为重要[11-12],但其受限于辐射剂量较高且价格昂贵。生长抑素显像是通过利用放射性核素标记生长抑素类似物与NB细胞表面表达的生长抑素受体结合从而达到显像目的,这构成了NB奥曲肽显像的分子成像基础[13]。生长抑素显像在诊断上较123I-MIBG、18F-FDG PET/CT有更好的准确性,这种蛋白质受体反映NB的增殖、分裂和复发转移[10]。因此,99mTc-HTOC对NB的原发灶及转移灶都具有高度特异性。
本研究显示,99mTc-HTOC显像对儿童NB的诊断有较好的灵敏度,但特异度较低仅50%,可能与本研究样本量相对较少有关。1例假阳性病例为3个月女患儿,超声和CT均示左侧腹膜后巨大囊实性混合肿块,99mTc-HTOC示左侧腹膜后巨大团状不均匀的放射性摄取增高,而病理学证实为左侧腹膜后未成熟畸胎瘤,可能的原因是99mTc-HTOC表现为巨大团状不均匀的放射性摄取增高不是典型的NB的显像表现,也可出现在奥曲肽低度表达的畸胎瘤中。1例假阴性病例为2岁女患儿,超声和CT均示腹膜后巨大占位,提示NB,99mTc-HTOC示腹膜后包块未见奥曲肽摄取,可能是由该病例肿瘤细胞表面表达的SSTR类型的差异造成的。因此,在诊断NB时应根据多种检查结果联合判断。
99mTc-HTOC显像在儿童NB全身转移病灶检出方面具有明显的优势,特别是对骨转移灶的检出;但对软组织转移灶的发现也有不足,可能是99mTc能量低,分辨率差,也可能因为软组织和骨组织病灶SSTR表达的差异性。常规的影像学检查由于检查部位比较局限并且缺乏特异性,对全身转移灶的检出率低。本组患儿因行99mTc-HTOC显像有3例改变了初始分期,因而及时行99mTc-HTOC显像对儿童NB是非常必要的,不仅有助于定性诊断,更助于准确分期,较好地指导选择治疗方案、提高判断预后准确性。99mTc具有优良的核物理性能和活泼的化学性质,应用99mTc标记奥曲肽方法简便易行,并且99mTc-HTOC具有辐射剂量低、价格便宜的特点,在实际临床工作中易于推行。
目前,对于高危组患儿治疗预后差,长期无瘤生存率不及50%[14]。高危组患儿在第4次及第8次化疗结束后均需要进行治疗评估[10]。可以选用99mTc-HTOC显像对患儿原发灶及转移灶进行评估,以便及时发现原发灶及转移灶是否对化疗药物敏感来决定是继续还是需要更改化疗方案。还可应用放射性核素标记奥曲肽具有被NB肿瘤细胞高摄取的特点[15],来对NB进行靶向治疗。比如,进一步研究应用放射性核素177Lu标记奥曲肽用于NB的靶向治疗。这种治疗方法被称为生长抑素受体介导的放射性核素治疗,疗效较好且无严重的不良反应,将是NB治疗研究发展的重要方向。
| [1] | MATSUSHITA K, UCHIDA K, SAIGUSA S, et al. Low NDRG1 mRNA expression predicts a poor prognosis in neuroblastoma patients[J]. Prediatr Surg Int, 2013, 29(4): 363–368. DOI:10.1007/s00383-012-3248-6 |
| [2] | SWIFT C C, EKLUND M J, KRAVEKA J M, et al. Updates in diagnosis, management, and treatment of neuroblastoma[J]. Radiographics, 2018, 38(2): 566–580. DOI:10.1148/rg.2018170132 |
| [3] | WHITTLE S B, SMITH V, DOHERTY E, et al. Overview and recent advances in the treatment of neuroblastoma[J]. Expert Rev Anticancer Ther, 2017, 17(4): 369–386. DOI:10.1080/14737140.2017.1285230 |
| [4] |
卢晓莉, 张俊, 王峰, 等. 68Ga-DOTA-NOC胰腺癌生长抑素受体靶向显像的实验研究[J].
中华核医学与分子影像杂志, 2013, 33(5): 372–376.
LU X L, ZHANG J, WANG F, et al. 68Ga-DOTA-NOC somatostatin receptor-targeting imaging in pancreatic carcinoma[J]. Chin J Nucl Med Mol Imaging, 2013, 33(5): 372–376. DOI:10.3760/cma.j.issn.2095-2848.2013.05.014 |
| [5] | TAÏEB D, GARRIGUE P, BARDIÈS M, et al. Application and dosimetric requirements for gallium-68-labeled somatostatin analogues in targeted radionuclide therapy for gastroenteropancreatic neuroendocrine tumors[J]. PET Clin, 2015, 10(4): 477–486. DOI:10.1016/j.cpet.2015.06.001 |
| [6] | NARAYANAN S, KUNZ P L. Role of somatostatin analogues in the treatment of neuroendocrine tumors[J]. Hematol Oncol Clin North Am, 2016, 30(1): 163–177. DOI:10.1016/j.hoc.2015.09.008 |
| [7] | PROVOST C, PRIGNON A, CAZES A, et al. 68Ga-DOTATOC and FDG PET imaging of preclinical neuroblastoma models[J]. Anticancer Res, 2016, 36(9): 4459–4466. DOI:10.21873/anticanres.10990 |
| [8] | MIKOLAJCZAK R, MAECKE H R. Radiopharmaceuticals for somatostatin receptor imaging[J]. Nucl Med Rev Cent East Eur, 2016, 19(2): 126–132. DOI:10.5603/NMR.2016.0024 |
| [9] | KONG G, HOFMAN M S, MURRAY W K, et al. Initial experience with gallium-68 DOTA-octreotate PET/CT and peptide receptor radionuclide therapy for pediatric patients with refractory metastatic neuroblastoma[J]. J Pediatr Hematol Oncol, 2016, 38(2): 87–96. DOI:10.1097/MPH.0000000000000411 |
| [10] | SIMON T, HERO B, SCHULTE J H, et al. 2017 GPOH guidelines for diagnosis and treatment of patients with neuroblastic tumors[J]. Klin Padiatr, 2017, 229(3): 147–167. DOI:10.1055/s-0043-103086 |
| [11] | DHULL V S, SHARMA P, PATEL C, et al. Diagnostic value of 18F-FDG PET/CT in paediatric neuroblastoma:comparison with 131I-MIBG scintigraphy[J]. Nucl Med Commun, 2015, 36(10): 1007–1013. DOI:10.1097/MNM.0000000000000347 |
| [12] |
王剑杰, 周鑫, 王骁, 等. 18F-FDG PET/CT儿童神经母细胞瘤诊断分期中的应用[J].
中国医学影像学杂志, 2014, 22(12): 936–940, 942.
WANG J J, ZHOU X, WANG X, et al. 18F-FDG PET/CT in the staging of pediatric neuroblastoma[J]. Chin J Med Imaging, 2014, 22(12): 936–940, 942. DOI:10.3969/j.issn.1005-5185.2014.12.016 |
| [13] | OLSEN I H, LANGER S W, FEDERSPIEL B H, et al. 68Ga-DOTATOC PET and gene expression profile in patients with neuroendocrine carcinomas:strong correlation between PET tracer uptake and gene expression of somatostatin receptor subtype 2[J]. Am J Nucl Med Mol Imaging, 2016, 6(1): 59–72. |
| [14] | PANDEY G K, KANDURI C. Long noncoding RNAs and neuroblastoma[J]. Oncotarget, 2015, 6(21): 18265–18275. DOI:10.18632/oncotarget.4251 |
| [15] | ALEXANDER N, VALI R, AHMADZADEHFAR H, et al. Review: the role of radiolabeled dota-conjugated peptides for imaging and treatment of childhood neuroblastoma[J]. Curr Radiopharm, 2018, 11(1): 14–21. DOI:10.2174/1874471011666171215093112 |




