2. 400042 重庆, 重庆医科大学附属第一医院超声消融治疗中心
2. Ultrasound Ablation Center, the First Affiliated Hospital of Chongqing Medical University, Chongqing, 400042, China
近年来, 高强度聚焦超声(high intensity focused ultrasound, HIFU)已经广泛应用于子宫肌瘤的治疗,并获得较为满意的效果[1-3],但由于超声波在声通道上传播的过程中会发生不同程度的反射、折射等物理特性及空化效应,会使声通道上的组织或周围组织发生副损伤,如子宫内膜损伤[4]、腹壁皮肤损伤[5]和盆底筋膜水肿[6]等。磁共振成像(MRI)可以显示HIFU术后未出现临床症状的腹壁、骶骨等信号异常[7-8]。子宫肌瘤超声消融治疗后受孕、分娩的妇女日益增多[9],超声消融子宫肌瘤后子宫肌层的完整性得以保留是其安全性的关键。然而HIFU消融子宫肌瘤时是否对子宫浆肌层造成损伤,仍是临床关注的热点问题。本研究通过观察子宫肌瘤超声消融后子宫浆肌层损伤的早期MRI影像学特征及损伤发生情况,探讨其安全性,为子宫肌瘤患者选择HIFU治疗提供依据。
1 资料与方法 1.1 一般资料选取2013-2017年在重庆医科大学附属第一医院妇科门诊诊断为子宫肌瘤而入院接受HIFU消融治疗的子宫肌瘤患者,其中术前、术后MRI资料完整者671例。搜集患者术前病史及MRI资料、HIFU治疗记录,进行随访。纳入标准:①年龄21~55(38.72±6.76)岁,近期无生育计划;②靶肌瘤数目为1个,最大径≥4 cm且≤10 cm。排除标准:术前有子宫肌瘤HIFU治疗史或肌瘤剔除史者。入选患者均签署知情同意书。本研究获重庆医科大学附属第一医院伦理委员会批准(2006-16号)。
1.2 HIFU治疗采用海扶刀©JC型聚焦超声肿瘤治疗系统(重庆海扶医疗科技股份有限公司)单次治疗,超声换能器中心组合包括超声显像探头,换能器频率0.8 MHz,物理学焦域1.5 mm×1.5 mm×10.0 mm,声功率0~400 W (可调), 显像超声频率3.5 MHz,循环脱气水耦合[7]。术前常规准备包括:肠道准备、备皮、导尿并留置导尿管。治疗时嘱患者俯卧,前腹壁与水槽内的脱气水充分接触,给予镇痛、镇静;术中根据患者耐受情况、靶区灰度变化并结合彩色多普勒超声和超声造影判断消融效果,适时终止治疗[5, 7]。
1.3 MRI检查采用GE HDxt 3.0T MRI扫描仪(Singa HD Excite, GE healthcare, 美国),8通道相控腹部线圈,对所有患者于消融前1周内及消融后3 d内行盆腔平扫加增强MRI检查。平扫采用T1加权FSE序列(TR 270 ms,TE 2.1 ms,层厚5 mm,层距1 mm);T2加权FRFSE序列(TR 3 400 ms,TE 110 ms,层厚5 mm,层距1.5 mm);增强扫描采用LAVA序列(TR 4.2 ms,TE 2.0 ms,层厚2.5 mm,层距0.5 mm)。增强对比剂采用钆双胺注射液(欧乃影0.5 mmol/mL,剂量15~20 mL),经肘静脉注射(注射流率2 mL/s),注射后即刻行矢状位和轴位动态增强扫描,观察至注射造影剂后120 s。
1.4 数据测量影像数据分析与测量由2名影像医师(分别有13年和10年执业经历)独立完成, 数据取均值, 有异议者与上级医师(25年执业经历)3人共同分析达成共识后确定。体积采用椭球体公式,V=0.523 3×横径×上下径×前后径;肌瘤体积消融率=无灌注区体积/肌瘤体积×100%;观察造影剂注射后120 s内始终无强化确定为损伤。子宫肌瘤所在肌壁的浆肌层无损伤表现为环状强化无灌注缺损, 有损伤表现为强化局部缺损。选择浆膜面环状强化缺损最大处,横向或纵向测量其最大长度以评价损伤范围。
1.5 统计学分析采用SPSS 22.0统计软件。计量资料以x ±s表示,计数资料以率表示。符合正态分布的计量资料采用独立样本t检验,反之则用Mann-Whitney U检验;计数资料比较采用χ2检验或Fisher精确概率。检验水准:α=0.05。
2 结果 2.1 一般资料比较符合入选标准的子宫肌瘤患者共400例,年龄21~55(38.72±6.76)岁;靶肌瘤400个,其中前壁肌瘤174个(43.50%)、后壁肌瘤93个(23.25%)、侧壁肌瘤105个(26.25%)、宫底肌瘤28个(7.00%);黏膜下肌瘤(FIGO Ⅱ型/Ⅲ型) 16个(4.00%)、肌壁间肌瘤(FIGO Ⅳ型/Ⅴ型) 261个(65.25%)、浆膜下肌瘤(FIGO Ⅵ型) 123个(30.75%)。
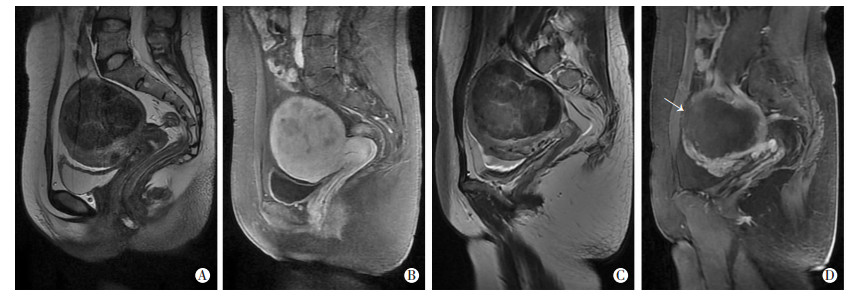
2.2 子宫肌瘤消融及浆肌层损伤情况400例患者中, 子宫浆肌层损伤者90例(22.50%), 体积消融率为(86.91±17.78)%,高于无损伤者[(80.93± 16.25)%,Z=-2.805,P=0.005]。子宫浆肌层损伤表现为:T2WI显示肌瘤病灶呈类圆形,边界清晰,周边肌层信号连续, 而动态增强序列见子宫浆肌层局部灌注缺损。90例子宫浆肌层灌注缺损范围为3.9~66.3(25.9±14.8)mm(图 1)。
|
| A:HIFU治疗前T2WI示子宫后壁肌层内见一类圆形病灶并凸向浆膜;B:增强T1WI示病灶强化略低于子宫肌壁;C:HIFU治疗后T2WI示类圆形病灶边界清晰,周边肌层信号连续;D:增强T1WI示病灶内无强化,箭头示子宫浆肌层环状强化见局部缺损(35.7 mm) 图 1 子宫肌瘤HIFU治疗前后早期MRI表现 |
2.3 不同位置子宫肌瘤浆肌层损伤情况
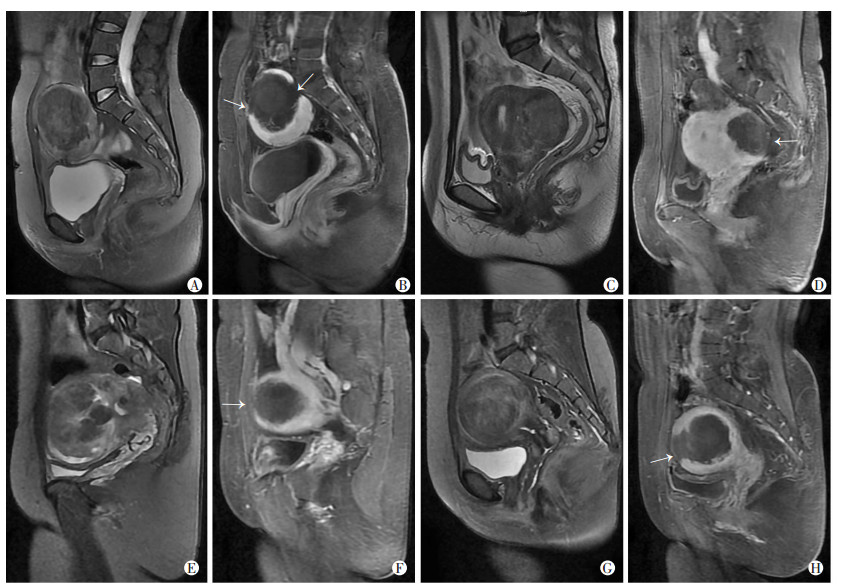
子宫宫底肌瘤和前壁肌瘤浆肌层损伤发生率相当,分别为28.57%(8/28)和28.16%(49/174);后壁肌瘤和侧壁肌瘤发生率接近,分别为13.98%(13/93)和19.05%(20/105)。前壁、侧壁及宫底肌瘤的子宫浆肌层损伤多发生于子宫肌瘤的腹侧, 即声通道的前场,也可发生于近骶骨的位置, 即声通道的后场;后壁肌瘤浆肌层损伤均发生于声通道的后场(图 2)。
|
| A:HIFU治疗前T2WI示子宫前壁肌瘤;B:HIFU治疗后增强T1WI示病灶内无强化,箭头示腹侧和近骶骨处均显示子宫浆肌层环状强化局部缺损(40.1、19.0 mm);C:HIFU治疗前T2WI示子宫后壁肌瘤;D:HIFU治疗后增强T1WI示病灶内无强化,箭头示子宫浆肌层环状强化见近骶尾骨处局部缺损(31.4 mm);E:HIFU治疗前T2WI示子宫宫底肌瘤;F:HIFU治疗后增强T1WI示病灶内无强化,箭头示子宫浆肌层环状强化见腹侧局部缺损(31.9 mm);G:HIFU治疗前T2WI示子宫侧壁肌瘤;H:HIFU治疗后增强T1WI示病灶内无强化,箭头示子宫浆肌层环状强化见腹侧局部缺损(18.7 mm) 图 2 HIFU治疗后不同位置的肌瘤子宫浆肌层损伤早期MRI表现 |
2.4 不同类型肌瘤浆肌层损伤情况
子宫黏膜下肌瘤16个,均无浆肌层损伤。浆膜下肌瘤浆肌层损伤发生率高于肌壁间肌瘤,分别为43.09% (53/123)和14.18%(37/261)(χ2=16.327,P < 0.001)。浆膜下肌瘤子宫浆肌层损伤范围高于肌壁间肌瘤[(26.8±15.5) vs (24.6±14.0)mm],但差异无统计学意义(t=-0.692,P=0.491)。
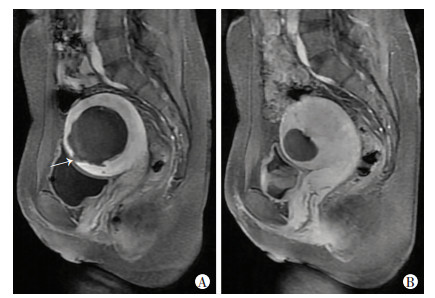
2.5 临床安全性及随访患者均未发生严重并发症。其中90例子宫浆肌层损伤患者均无阴道持续出血表现,也无血尿、血便等膀胱及肠道损伤表现。术后阴道血性分泌物3例(3.33%),略高于无损伤者(2.56%),差异无统计学意义(χ2=0.148,P=0.701);出现腹壁硬结1例(1.11%),略高于无损伤者(0.97%),差异无统计学意义(χ2= 0.014,P=0.904);术后随访1周均已恢复正常。90例子宫浆肌层损伤患者中,HIFU术后3、6个月分别有4例和2例患者行MRI检查,增强MRI均显示子宫浆肌层强化完整(图 3)。
|
| A:HIFU治疗后3 d内增强T1WI示病灶内无强化,箭头示子宫浆肌层环状强化见局部缺损(10.7 mm);B:HIFU治疗后3个月增强T1WI示病灶内无强化,周边肌层信号连续 图 3 HIFU治疗后随访子宫浆肌层MRI表现 |
3 讨论
HIFU消融治疗子宫肌瘤是将体外的超声波聚焦到肿瘤组织,焦点处瞬间升温达60~100 ℃致组织凝固性坏死,从而达到杀灭肿瘤的目的[10],已成为子宫肌瘤常用的治疗方法。多组病例报道显示:子宫肌瘤超声消融后,均未发生妊娠期子宫破裂等不良妊娠结局[9, 11]。但目前对于超声消融子宫肌瘤时是否造成子宫肌层的副损伤,仍缺乏足够的临床证据。MRI是基于激发后质子弛豫的多参数、多方位成像技术。增强T1WI可以提供局部组织的血供状态信息,T2WI对病变组织显示较为敏感,具有图像空间分辨率高的特点,这两种序列显像结合可用于子宫肌瘤超声效果结果的评价,具有独特的价值,因而利用其评估超声消融子宫肌瘤后子宫浆肌层是否发生损伤及浆肌层损伤的影像学特点,对超声消融技术用于有生育计划的子宫肌瘤患者具有重要意义。
本研究增强MRI评价结果显示:子宫肌瘤平均体积消融率超过80%,与同类技术多组病例报道结果基本一致[1, 12-13]。MRI影像分析发现:注射造影剂后120 s内,22.5%的患者子宫浆肌层局部未出现强化,定义为影像学所见的损伤。T2WI显示类圆形病灶边界清晰,周边肌层信号连续,而增强T1WI见子宫浆肌层局部灌注缺损,范围不等(3.9~66.3 mm),且子宫肌瘤体积消融率高,更易出现子宫浆肌层损伤。提示临床治疗时可控制消融范围,避免子宫浆肌层损伤的发生。本研究还通过比较HIFU消融后增强MRI图像发现:子宫浆肌层损伤可以发生于声通道的前场,也有发生于后场,与子宫肌瘤的不同位置有关;位于前壁、侧壁及宫底肌瘤的子宫浆肌层损伤多发生于子宫肌瘤的腹侧,即声通道的前场,表明在声波传播路径上有能量沉积,特别是近焦域位置。本研究所用的JC型聚焦超声肿瘤治疗系统,物理学焦域1.5 mm×1.5 mm × 10.0 mm,指声压在空间6 dB衰减的区域[14],在焦域外能量急骤下降,但由于声通道组织的声速及组织衰减系数差异,造成声通道前场的能量沉积。位于后壁的肌瘤紧邻骶尾骨或肌瘤受骶岬压迫,易发生子宫后壁浆肌层损伤(声通道后场),靶组织离骶骨距离近,超声波衰减少,致骶骨吸收能量的同时也反射超声能量,造成子宫浆肌层热损伤;肌瘤受骶岬压迫时,浆肌层缺血更易损伤。因此,在以后治疗后壁或临近骶尾骨的肌瘤时,除了需要关注骶尾骨的热沉积[8, 15],还应避免能量过多沉积导致浆肌层不可逆性损伤。
本研究发现浆膜下子宫肌瘤在超声消融时浆肌层灌注缺损发生率明显高于肌壁间肌瘤(P < 0.05),黏膜下肌瘤未发生浆肌层损伤,表明超声消融治疗不同类型的肌瘤发生浆肌层损伤的风险不同。这可能是因为浆膜下肌瘤(FIGO分型[16]:Ⅵ型)以压迫突向浆膜生长为特征,甚至部分区域仅有薄肌层或浆膜覆盖,而黏膜下肌瘤浆膜侧有较完整的浆肌层,超声消融时浆肌层可以保留完整。因此,在今后的临床治疗过程中,浆膜下子宫肌瘤HIFU消融时应严密观察监控超声显示的灰度增高区域,避免过度热损伤。
在临床安全性方面,本研究通过动态增强MRI重点观察了子宫浆肌层灌注缺损的患者近期并发症发生情况,未发现有患者出现发热、血尿、血便等感染及损伤症状,随访中也无并发症发现。尽管在3个月及6个月接受再次增强MRI检查的患者数量较少,但仍观察到子宫浆肌层恢复正常灌注,初步证实超声消融后出现的子宫浆肌层灌注缺损为可逆性改变。
本研究的局限性在于无法获得病理样本来证实增强MRI上的灌注缺损是否是凝固性坏死;子宫浆肌层损伤后修复过程也未获得病理学结果,因此需要进一步扩大术后近、远期增强MRI患者的数量和(或)取得相关病理样本,来研究浆肌层损伤是否具有可逆性。在HIFU治疗后剖宫产的患者中未发现盆腔粘连[13]。牟燕等[17]报道的HIFU治疗后接受盆腔手术的患者与无HIFU治疗史的患者盆腔粘连发生率差异无统计学意义。传统手术子宫浆膜层结构破坏后由纤维组织沉积封闭创口,易造成粘连。超声消融子宫肌瘤后,无论是否有浆肌层灌注缺损,浆膜结构仍保留完整,是否其修复主要为再生的间皮细胞迁延修复,也需要进一步深入研究。
本研究结果表明:超声消融子宫肌瘤后子宫浆肌层损伤具有可逆性,增强MRI显示的无灌注区并不能等同于组织发生凝固性坏死,也见于动脉短暂痉挛或动脉供血阻断[18],但在目前未获得病理证据的情况下,保持影像学上完整的强化边缘是确保临床安全性的关键。提示临床治疗时需要根据不同的治疗目的,控制消融范围,特别是对于有生育计划的子宫肌瘤患者应避免子宫浆肌层实质性损伤。
| [1] | CHEN J, LI Y, WANG Z, et al. Evaluation of high-intensity focused ultrasound ablation for uterine fibroids: an IDEAL prospective exploration study[J]. BJOG, 2018, 125(3): 354–364. DOI:10.1111/1471-0528.14689 |
| [2] |
陈文直, 唐良萏, 杨武威, 等. 超声消融治疗子宫肌瘤的安全性及有效性[J].
中华妇产科杂志, 2010, 45(12): 909–912.
CHEN W Z, TANG L D, YANG W W, et al. Study on the efficacy and safety of ultrasound ablation in treatment of uterine fibroids[J]. Chin J Obst Gynecol, 2010, 45(12): 909–912. DOI:10.3760/cma.j.issn.0529-567x.2010.12.007 |
| [3] |
朱丽, 陈文直, 陈锦云, 等. 子宫肌瘤超声消融与MRI信号特征关系的研究[J].
第三军医大学学报, 2009, 31(14): 1370–1373.
ZHU L, CHEN W Z, CHEN J Y, et al. MR image features of uterine fibroids after ultrasound ablation: report of 80 fibroids[J]. J Third Mil Med Univ, 2009, 31(14): 1370–1373. DOI:10.3321/j.issn:1000-5404.2009.14.012 |
| [4] |
汤顾航, 周杨洋, 王健, 等. 高强度聚焦超声治疗子宫黏膜下肌瘤[J].
中国介入影像与治疗学, 2014, 11(5): 294–297.
TANG G H, ZHOU Y Y, WANG J, et al. High-intensity focused ultrasound in treatment of submucosal fibroid[J]. Chin J Interv Imaging Ther, 2014, 11(5): 294–297. DOI:10.13929/j.1672-8475.2014.05.010 |
| [5] | YIN N, HU L, XIAO Z B, et al. Factors influencing thermal injury to skin and abdominal wall structures in HIFU ablation of uterine fibroids[J]. Int J Hyperthermia, 2018, 34(8): 1298–1303. DOI:10.1080/02656736.2018.1433880 |
| [6] |
张学花, 翟昭华, 董国礼, 等. MRI评价子宫肌瘤高强度聚焦超声消融术后盆底筋膜改变[J].
中国医学影像技术, 2017, 33(10): 1540–1544.
ZHANG X H, ZHAI Z H, DONG G L, et al. MRI evaluating changes of pelvic fascia after high intensity focused ultrasound ablation of uterine fibroids[J]. Chin J Med Imaging Technol, 2017, 33(10): 1540–1544. DOI:10.13929/j.1003-3289.201703126 |
| [7] |
尹娜, 王玲, 胡亮, 等. HIFU治疗超声衰减宽度 < 10 mm声通道腹壁瘢痕子宫肌瘤患者的有效性及安全性[J].
中国介入影像与治疗学, 2018, 15(4): 221–225.
YIN N, WANG L, HU L, et al. Efficacy and safety of HIFU ablation for uterine fibroids in patients with abdominal surgical scars in acoustic pathway causing acoustic attenuation width < 10 mm[J]. Chin J Interv Imaging Ther, 2018, 15(4): 221–225. DOI:10.13929/j.1672-8475.201708039 |
| [8] |
崔运能, 田橄, 陈向东, 等. 高强度聚焦超声治疗子宫肌瘤及子宫腺肌瘤术后早期并发症的MR表现[J].
临床放射学杂志, 2018, 37(3): 461–465.
CUI Y N, TIAN G, CHEN X D, et al. MR features of complications after high intensity focused ultrasound treatment in uterine fibroids and adenomyomas[J]. J Clin Radiol, 2018, 37(3): 461–465. DOI:10.13437/j.cnki.jcr.2018.03.025 |
| [9] |
王玲, 胡亮, 刘畅, 等. 267例无生育史的子宫肌瘤患者经高强度聚焦超声消融治疗术后妊娠结局分析[J].
第三军医大学学报, 2018, 40(20): 1865–1869.
WANG L, HU L, LIU C, et al. Analysis of pregnancy outcomes in 267 nulliparous women after high-intensity focused ultrasound ablation of uterine fibroids[J]. J Third Mil Med Univ, 2018, 40(20): 1865–1869. DOI:10.16016/j.1000-5404.201803109 |
| [10] |
何佳. 子宫黏膜下肌瘤高强度聚焦超声治疗[J].
中国实用妇科与产科杂志, 2016, 32(2): 145–148.
HE J. High intensity focused ultrasound(HIFU) for submucosal fibroids[J]. Chin J Pract Gynecol Obstet, 2016, 32(2): 145–148. |
| [11] |
李俊书, 陈文直, 胡亮, 等. 不孕症患者子宫肌瘤HIFU消融术后妊娠相关影响因素分析[J].
中国超声医学杂志, 2016, 32(11): 1018–1022.
LI J S, CHEN W Z, HU L, et al. Analyze relevant influence factors on reproductive outcomes after HIFU ablation treatment for infertile women with uterine fibroids[J]. Chin J Ultrasound Med, 2016, 32(11): 1018–1022. |
| [12] | WANG W, WANG Y, WANG T, et al. Safety and efficacy of US-guided high-intensity focused ultrasound for treatment of submucosal fibroids[J]. Eur Radiol, 2012, 22(11): 2553–2558. DOI:10.1007/s00330-012-2517-z |
| [13] | QIN J, CHEN J Y, ZHAO W P, et al. Outcome of unintended pregnancy after ultrasound-guided high-intensity focused ultrasound ablation of uterine fibroids[J]. Int J Gynaecol Obstet, 2012, 117(3): 273–277. DOI:10.1016/j.ijgo.2012.01.011 |
| [14] |
王智彪, 李发琪, 冯若. 治疗超声原理与应用[M]. 南京: 南京大学出版社, 2008: 197.
WANG Z B, LI F Q, FENG R. The principle and application of therapeutic ultrasound[M]. Nanjing: Nanjing University Press, 2008: 197. |
| [15] |
邓凤莲, 邹建中, 李锐, 等. 高强度聚焦超声治疗子宫肌瘤对骶骨影响因素探讨[J].
中国介入影像与治疗学, 2009, 6(5): 457–460.
DENG F L, ZOU J Z, LI R, et al. Impact factors of high intensity focused ultrasound treatment of uterine leiomyoma on the sacrum[J]. Chin J Interv Imaging Ther, 2009, 6(5): 457–460. DOI:10.13929/j.1672-8475.2009.05.021 |
| [16] |
子宫肌瘤的诊治中国专家共识专家组. 子宫肌瘤的诊治中国专家共识[J].
中华妇产科学杂志, 2017, 52(12): 793–800.
Chinese Expert Consensus Expert Group on the Diagnosis and Treatment of Uterine Fibroids. Chinese Expert consensus on diagnosis and treatment of uterine leiomyoma[J]. Chin J Obstet Gynecol, 2017, 52(12): 793–800. DOI:10.3760/cma.j.issn.0529-567x.2017.12.001 |
| [17] |
牟燕, 刘晓芳, 何佳. 高强度聚焦超声治疗子宫肌瘤和子宫腺肌病后盆腔黏连情况分析[J].
重庆医学, 2016, 45(10): 1339–1342.
MU Y, LIU X F, HE J. Analysis on pelvic adhesion situation patients after treatment of uterine fibroids and adenomyosis by high intensity focused ultrasound[J]. Chongqing Med, 2016, 45(10): 1339–1342. DOI:10.3969/j.issn.1671-8348.2016.10.013 |
| [18] | CHENG H L, HAIDER M A, DILL-MACKY M J, et al. MRI and contrast-enhanced ultrasound monitoring of prostate microwave focal thermal therapy: an in vivo canine study[J]. J Magn Reson Imaging, 2008, 28(1): 136–143. DOI:10.1002/jmri.21415 |



