自闭症谱系障碍(autism spectrum disorder, ASD)是一种较为严重的发育障碍性疾病,包括自闭症、阿斯伯格综合征、儿童期崩解障碍和未分类的广泛性发育障碍。ASD的特征表现为社交障碍,重复或限制的兴趣或行为[1]。大部分ASD患者不能独立生活,需要终身陪伴,给家庭和社会带来了巨大的负担。在过去的20年中,ASD患病率一直在上升。尽管存在种族、社会经济背景的差异,全世界大多数国家的患病率在1%左右。目前尚无针对ASD核心症状的有效药物。
ASD的确切病因尚不清楚,遗传和环境因素共同介导了其病理发生[2]。大量实验研究显示慢性神经炎症、兴奋性抑制神经递质失调、线粒体功能失调和氧化应激作为重要的途径参与到ASD的病理发生机制当中[3-5]。性激素异常调节参与ASD的病理发生,ASD患者具有明显的性别差异,即男孩发病明显多于女孩,其比例大约为4 :1[6]。脑的两性分化始于胚胎发育的中晚期及生后发育的早期,提示雌激素对脑发育的影响可能为ASD患者中产生性别差异的关键因素。在斑马鱼实验中证实雌激素能够抑制CNTNAP2突变引起的自闭症样行为[7],同时在小鼠中亦证实雌二醇可以改善Pvalb杂合小鼠的自闭症样行为[8]。雌激素通过雌激素受体α(estrogen receptor α, ERα)和β(ERβ)两型核受体和膜受体(G蛋白偶联受体30)发挥作用,其中ERβ广泛分布于中枢神经系统,并在脑发育中起重要作用[9-10]。最近的研究资料也显示,ERβ在大脑中表达下调与自闭症的病理发生有关[11],而上调ERβ往往能够改善自闭症样行为[12]。ly3201为ERβ的选择性激动剂,在体实验证实ly3201能够选择性激活内源性ERβ;生后早期ly3201处理能否用于自闭症样行为的治疗尚需进一步证实。
BTBR T+tf/J (BTBR)小鼠是一种近交系小鼠,能够模拟ASD的典型核心症状使其成为研究自闭症谱系障碍的理想实验动物模型。本实验采用雄性BTBR小鼠及C57BL/6J小鼠在生后2 d(P2)给予ly3201处理,在生后14 d(P14)采用荧光定量PCR结合免疫组化检测大脑皮层与海马内ERβ的表达,在成年检测自闭症相关的行为学变化,阐明新生期注射ly3201能否通过激活内源性ERβ水平改善BTBR小鼠的自闭症样行为。
1 材料与方法 1.1 材料 1.1.1 动物BTBRT+tf/J (BTBR)鼠购自南京大学模式生物研究中心,C57BL/6J(C57)小鼠购自陆军军医大学实验动物中心。孕鼠饲养于安静、清洁的动物房内,室温稳定于21~26 ℃。每日早、中、晚各观察孕鼠情况1次。小鼠出生当天记为P0, 并选取雄性小鼠进行实验。
1.1.2 药物ly3201由瑞典卡罗林斯卡学院生物科学与营养学系Jan-Ake Gustafsson教授惠赠。
1.1.3 实验试剂与药品无水乙醇购自成都市科龙化工试剂厂;RNA提取试剂盒购自北京康为世纪生物技术有限公司;mRNA反转录试剂盒、RT-PCR试剂盒购自日本TaKaRa生物公司。
1.1.4 仪器与设备行为跟踪分析系统(Ethovision 11.0)购自诺达思(北京)信息技术有限公司;三箱社交实验设备、交互社交实验设备、旷场实验设备、高架十字迷宫设备、明暗箱实验设备购自深圳市瑞沃德生命科技有限公司。CFX96荧光定量PCR仪购自美国Bio-Rad公司。
1.2 方法 1.2.1 药物处理利用随机数字表将小鼠分为4组(n=6):C57生理盐水组(C57SAL)、C57药物处理组(C57LY)、BTBR生理盐水组(BTBRSAL)和BTBR药物处理组(BTBRLY)。药物处理组在生后2 d(出生当天为P0)给予ly3201腹腔注射,注射剂量为1.6 mg/kg;生理盐水组腹腔注射等量生理盐水。
1.2.2 标本采集P14小鼠处死后,小心剥离脑组织,于冰上分离大脑整体的皮层和整体的海马,置于EP管中保存于-80 ℃超低温冰箱中,留mRNA提取。部分脑组织用新鲜的4%多聚甲醛固定13 h,经常规浸蜡、包埋方法制备蜡块,用于免疫组化检测。
1.2.3 免疫组化检测免疫组化的切片厚度均为5 μm。ERβ抗体由瑞典卡罗林斯卡学院生物科学与营养学系Jan-Ake Gustafsson教授惠赠,工作时1 :100稀释,过夜孵育。二抗为生物素标记的羊抗鸡抗体。镜下控制DAB显色时间,待显色合适后,水洗-脱水-透明-封片,进行观察分析。
1.2.4 RT-qPCR检测利用mRNA提取试剂盒提取小鼠脑组织mRNA;利用反转录试剂盒将mRNA反转录为cDNA存于-80 ℃;荧光定量RT-qPCR,ERβ上游引物序列:5′-ACACCTTGCCTGTAAACAGAGA-3′,下游引物序列5′-GCAGAAGTGAGCATCCCTCTT-3′,产物大小104 bp;选用GAPDH作内参,GAPDH上游引物序列: 5′-AGGTCGGTGTGAACGGATTTG-3′, 下游引物序列: 5′-TGTAGACCATGTAGTTGAGGTCA-3′,产物大小123 bp。利用PT-qPCR试剂盒配制PCR反应液。反应条件:95 ℃ 30 s,95 ℃ 5 s,60 ℃ 30 s,共同循环40次,4 ℃保存。反应结束后分析PT-qPCR溶解扩增曲线,记录Ct值。应用Ct值计算ERβ相对内参基因GAPDH的相对表达量,并进行组间统计分析。
1.2.5 行为学分析 1.2.5.1 三箱社交实验三箱社交实验装置为40 cm×60 cm×22 cm大小矩形碳酸酯箱。分为左中右三箱,之间由带有可活动门的墙体分隔。每只小鼠实验后用70%乙醇溶液清洁箱体后自然晾干5 min。实验开始前,将小鼠由中间箱放入箱体自由探索10 min。实验开始,小鼠和物体分别放在左右两个箱中,将实验小鼠中间箱放入并记录10 min。用Ethovision 11.0分析统计小鼠在每个箱中的停留、嗅探时间,并计算偏好系数:箱体时间偏好系数=(小鼠箱体时间-物体箱体时间)/(小鼠箱体时间+物体箱体时间);嗅探时间偏好系数=(小鼠嗅探时间-物体嗅探时间)/(小鼠嗅探时间+物体嗅探时间)。
1.2.5.2 理毛实验将每只小鼠单独放置到1个干净的标准鼠笼中,距鼠笼15 cm处用摄像机记录小鼠行为20 min。统计后10 min小鼠理毛(小鼠用嘴梳理头部、四肢、背部、会阴和尾部)时间。
1.2.5.3 交互社交实验将每只小鼠单独放置到1个20 cm×20 cm×17 cm大小矩形碳酸酯箱中,放入年龄匹配的发情C57雌鼠,视频记录5 min。统计实验小鼠对C57雌鼠身体各部分的嗅探时间:鼻对鼻、鼻对身体、鼻对会阴嗅探时间,并统计5 min内实验小鼠对箱体的探索时间。
1.2.5.4 埋珠实验在27 cm ×16.5 cm ×12.5 cm大小的箱体底部平铺5 cm厚的山杨木屑,将20颗黑色玻璃珠(直径15 mm)以4×5的排列方式放置于木屑上。将小鼠放入箱体30 min,记录埋珠(小鼠将玻璃珠埋入山杨木屑中)数量(玻璃珠埋入体积>50%)。
1.2.5.5 旷场实验实验装置为40 cm×40 cm×30 cm方形灰色树脂盒。实验开始将小鼠放置在装置中心,摄像记录30 min。用Ethovision 11.0软件分析统计小鼠总的运动路程和在中心区域(将装置底面以4×4方式划分为16小格,中间4格为中心区域)停留时间。
1.2.5.6 高架十字迷宫实验迷宫包括中间区域(6 cm×6 cm),两个开臂(30 cm×6 cm×15 cm), 两个闭臂(30 cm×6 cm×15 cm)。将小鼠面向开臂由中间区域放入,任其自由探索,视频记录10 min。Ethovision 11.0软件分析统计小鼠在开臂停留时间百分比(开臂时间/总时间×100%),高架穿梭次数(进出各臂次数总和)。
1.2.5.7 明暗箱实验明暗箱装置包括明箱(20 cm× 15 cm×25 cm)和暗箱(20 cm×15 cm×25 cm)。箱子间有一活动小门允许小鼠自由通过。将小鼠由明箱放入,摄像记录10 min。用Ethovision 11.0软件分析统计明箱中停留时间和两箱间穿梭次数。
1.3 统计学分析计量资料以x±s表示,采用SPSS 24.0统计软件进行分析。对于三箱社交实验中各处理组小鼠对不同箱体的探索时间、嗅探时间、箱体、嗅探时间偏好系数的分析,采用配对t检验;其余检测指标均采用单因素方差分析,检验水准α=0.05。
2 结果 2.1 新生期激活ERβ诱导幼鼠脑内ERβ表达升高免疫组化结果显示,ERβ在皮层、海马、下丘脑多个脑区均有较高水平的表达,而BTBR小鼠ERβ在脑内的表达显著降低,ly3201注射后则显著增加C57和BTBR小鼠内ERβ的表达。采用荧光定量PCR检测P14小鼠大脑皮层和海马中ERβ mRNA的表达,发现BTBR小鼠大脑皮层与海马内ERβ mRNA表达明显低于C57小鼠(P < 0.01)。ly3201注射后,C57小鼠和BTBR小鼠皮层与海马内ERβ mRNA的表达显著上调(P < 0.05,P < 0.01)。提示ly3201注射后,激活小鼠脑内ERβ,显著上调ERβ mRNA的表达。见图 1。

|
| A:免疫组化染色检测各组小鼠大脑皮层中ERβ表达(褐色为阳性细胞,SABC);B:荧光定量PCR检测小鼠皮层中ERβ mRNA的表达;C:荧光定量PCR检测小鼠海马中ERβ mRNA的表达;a:P < 0.05,b:P < 0.01,与C57SAL组比较;c:P < 0.01,与BTBRSAL组比较 图 1 ly3201处理后P14小鼠大脑中ERβ表达升高 |
2.2 新生期激活ERβ可改善成年BTBR小鼠的社交行为
三箱社交实验用于检测小鼠社交能力,正常小鼠在三箱社交实验中,在小鼠箱体中的时间应多于在物体箱体中的时间,对小鼠嗅探时间也应多于对物体的嗅探,其偏好系数应偏向于小鼠(结果为正值)。三箱社交检测结果显示:C57SAL组小鼠表现出正常的社交能力,即C57SAL组小鼠在小鼠箱体中的时间显著多于在物体箱体中停留的时间(P < 0.01),对小鼠嗅探时间多于对物体的嗅探时间(P < 0.01),箱体偏好系数(正值)与嗅探时间偏好系数(正值)偏向小鼠。BTBRSAL组小鼠表现出了明显的社交缺陷:在物体箱体中停留的时间显著多于在小鼠箱体中的时间(P < 0.01),对物体的嗅探时间显著多于对小鼠的嗅探时间(P < 0.05),箱体偏好系数(P < 0.01)与嗅探时间偏好系数(P < 0.01)为负值,偏向箱体。经ly3201处理后,BTBRLY组小鼠在小鼠箱体中的时间显著多于在物体箱体中停留的时间(P < 0.05),对小鼠嗅探时间多于对物体的嗅探时间(P < 0.05),箱体偏好系数(P < 0.01)与嗅探时间偏好系数(P < 0.01)大于BTBTLY组,偏向于小鼠,提示新生期ly3201处理能够有效改善成年BTBR小鼠的社交行为缺陷。同时实验结果也显示新生期ly3201处理不影响C57小鼠的社交能力。见图 2。

|
| A:三箱行为学热图 颜色越接近红色代表停留时间越长,越接近蓝色代表停留时间越短;B:小鼠在各个箱体中停留时间 a:P < 0.01,b:P < 0.05,与物体箱体比较;C:小鼠嗅探时间 a:P < 0.01,b:P < 0.05,与物体箱体比较;D:箱体停留时间偏好系数 a:P < 0.01,与C57SAL组比较;b:P < 0.01,与BTBRSAL组比较;E:嗅探时间偏好系数 a:P < 0.01,与C57SAL组比较;b:P < 0.01,与BTBRSAL组比较 图 2 新生期ly3201处理改善成年BTBR小鼠在三箱社交行为检测中的社交行为缺陷 Fig.2 |
2.3 新生期激活ERβ可改善成年交互社交行为,但不影响重复样行为
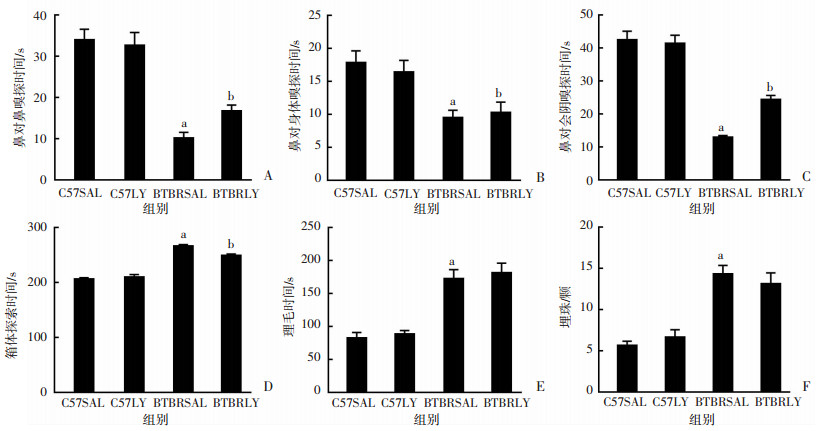
社会交互行为学实验是用于检测小鼠社交能力的另一种方法,正常小鼠对C57发情雌鼠各部位的嗅探时间都应有一个较高值,特别是在鼻对鼻、鼻对会阴嗅探时间,而对箱体的探索时间较少。结果显示:BTRBSAL组小鼠表现出明显的交互社交缺陷,鼻对鼻、鼻对身体、鼻对会阴的嗅探时间明显少于C57SAL组小鼠(P < 0.05),而对箱体的探索时间多于C57SAL组(P < 0.05)。新生期ly3201处理后,与BTBRSAL组比较,BTBRLY组小鼠明显增加了鼻对鼻、鼻对会阴嗅探时间(P < 0.05),减少了对箱体的探索时间(P < 0.05),表明ly3201在交互社交实验中改善了BTBR自闭症小鼠的交互社交能力。埋珠和理毛实验用于检测自闭症小鼠的重复样行为,正常小鼠理毛时间较短,埋珠数较少。与C57SAL组小鼠相比较,BTBRSAL组小鼠理毛时间增加、埋珠数量增多(P < 0.05),表现出重复样行为;而新生期ly3201处理没有影响BTBR小鼠的重复样行为。见图 3。
|
| a:P < 0.05,与C57SAL组比较;b:P < 0.05,与BTBRSAL组比较A:鼻对鼻嗅探时间;B:鼻对身体嗅探时间;C:鼻对会阴嗅探时间;D:鼻对箱体的探索时间;E:理毛时间;F:埋珠数 图 3 新生期ly3201处理特异性改善BTBR小鼠交互社交行为缺陷 |
2.4 新生期激活ERβ不影响成年BTBR小鼠运动能力和焦虑样行为
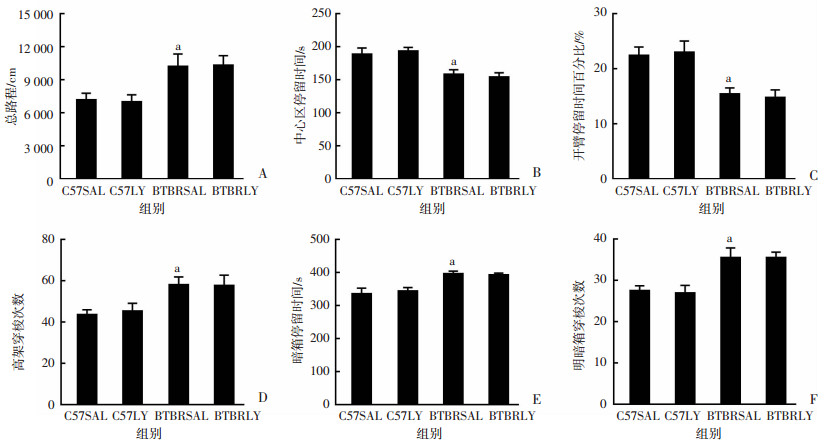
运动能力会对社交行为的检测产生影响,因此采用旷场实验检测小鼠的运动能力。实验结果显示:新生期ly3201处理不影响成年BTBR小鼠在旷场实验中运动总路程(图 4A)。中央时间反映小鼠的焦虑情况,在旷场实验中,小鼠待在中心区时间与焦虑呈负相关,结果显示BTBRSAL组小鼠在中心区时间明显低于C57SAL组(P < 0.05),而新生期ly3201处理对中央时间无显著影响(图 4B)。
|
| A:旷场实验总路程;B:旷场实验中心区停留时间;C:高架十字迷宫开臂停留时间百分比;D:高架十字迷宫穿梭次数;E:暗箱停留时间;F:明暗箱穿梭次数;a:P < 0.05,与C57SAL组比较 图 4 新生期ly3201处理不影响BTBR小鼠运动能力和焦虑样行为 |
高架十字迷宫与明暗箱实验亦被广泛用于检测啮齿类动物的焦虑水平。高架十字迷宫实验中,开臂停留时间百分比与焦虑呈负相关。实验结果显示:在高架十字迷宫实验中,BTBRLY组小鼠的焦虑样行为没有得到改变(图 4C、D)。明暗箱实验中,小鼠待在暗箱中的时间与焦虑程度呈正相关。实验结果显示ly3201未能减少BTBR在暗箱中停留时间(图 4E、F)。表明ly3201不影响BTBR小鼠的运动功能和焦虑行为,ly3201对BTBR小鼠的社交行为改善是一种特异性的作用。
3 讨论ASD患病率呈逐年增高的趋势。近年来,越来越多的儿童被诊断出患有此病,目前没有作用于ASD核心症状的有效药物, 探索ASD治疗的新靶点越来越受到关注。胎儿及婴幼儿期睾酮升高会增加觉醒相关的刺激大量传入杏仁体, 使得男孩较女孩对早期的应激更为敏感,引起焦虑和恐惧,产生社交逃避, 而女孩雌激素水平升高,则对早期应激反应产生保护效应。基于此,推测ASD中男孩较女孩患病率显著升高与体内性激素水平密切相关。雌激素通过激活内源性雌激素受体ERβ[13],在脑发育过程中通过影响神经元的发育、突触形成、环路发育等多个重要环节影响认知、学习和记忆过程。在尸检的ASD患者中已经证实ERβ、CYP19A1及共刺激分子其mRNA水平和蛋白水平在额中回均显著下调。动物实验证实衣霉素减少雄性小鼠前额叶ERβ的蛋白水平并通过激活氧化应激反应产生社交行为缺陷,ERβ特异性激动剂ERB-041进行预处理则抑制衣霉素引起的社交行为缺陷[14]。这些研究提示大脑中ERβ表达下调在ASD发病过程中起到了重要作用,而用ERβ激动剂治疗ASD可能是一个有希望的治疗方案。
BTBR小鼠广泛应用于ASD的研究,具有能够模拟临床自闭症样行为的典型特征,包括社交障碍和重复刻板行为。为检测新生期ERβ特异性激动剂ly3201处理的治疗效应,在小鼠成年后进行了自闭症相关行为学的检测。本实验发现新生期ly3201处理可以显著改善BTBR小鼠社交缺陷和交互社交缺陷,且不影响C57小鼠的社交行为。运动功能往往会影响社交能力;开场实验检测发现ly3201并不影响BTBR小鼠的运动能力,提示新生期ly3201处理对BTBR小鼠社交行为及交互社交行为的改善是非常特异的。理毛实验和埋珠实验用于检测啮齿类动物的重复刻板样行为,与文献[15]报道一致。BTBR小鼠具有典型的重复刻板行为,即理毛时间延长,埋珠数量增加;而新生期ly3201处理并不能改善BTBR小鼠具有的典型的重复刻板行为,提示新生期ly3201处理能够特异性选择性地改善BTBR小鼠的社交行为。
ASD为脑发育障碍性疾病,生后2周为脑发育的关键期。我们前期研究证实新生期为ERβ在海马、小脑及皮层高表达的关键期,并因此而影响生后脑的发育[16]。免疫组化结果显示生后2 d给予ly3201处理增加C57与BTBR小鼠脑内ERβ的表达,荧光定量PCR结果显示ly3201处理显著上调C57与BTBR小鼠海马与皮层内ERβ mRNA的表达。最新的研究显示出生前暴露炔诺酮引起杏仁体中ERβ的表达水平下调及自闭症样行为[11];而出生前与出生后采用白藜芦醇处理则激活杏仁体中ERβ的表达并进而改善自闭症样行为。由此可见在发育关键期激活ERβ可以有效改善自闭症行为[12];而其具体的细胞学机制有待进一步阐明。
综上所述,本实验证实了在新生期给予ERβ激动剂ly3201处理,能够特异性的改善BTBR小鼠社交缺陷,这可能是由于ly3201激活了皮层与海马内ERβ的表达,ERβ的选择性激动剂可能为一新的靶点用于ASD的治疗。
| [1] | CHEN J A, PEÑAGARIKANO O, BELGARD T G, et al. The emerging picture of autism spectrum disorder:genetics and pathology[J]. Annu Rev Pathol, 2015, 10: 111–144. DOI:10.1146/annurev-pathol-012414-040405 |
| [2] | GOINES P E, ASHWOOD P. Cytokine dysregulation in autism spectrum disorders (ASD):possible role of the environment[J]. Neurotoxicol Teratol, 2013, 36: 67–81. DOI:10.1016/j.ntt.2012.07.006 |
| [3] | VARGAS D L, NASCIMBENE C, KRISHNAN C, et al. Neuroglial activation and neuroinflammation in the brain of patients with autism[J]. Ann Neurol, 2005, 57(1): 67–81. DOI:10.1002/ana.20315 |
| [4] | MORGAN J T, CHANA G, PARDO C A, et al. Microglial activation and increased microglial density observed in the dorsolateral prefrontal cortex in autism[J]. Biol Psychiatry, 2010, 68(4): 368–376. DOI:10.1016/j.biopsych.2010.05.024 |
| [5] | YOUNG A M, CAMPBELL E, LYNCH S, et al. Aberrant NF-kappaB expression in autism spectrum condition:A mechanism for neuroinflammation[J]. Front Psychiatry, 2011, 2: 27. DOI:10.3389/fpsyt.2011.00027 |
| [6] | BERKEL S, ELTOKHI A, FR HLICH H, et al. Sex hormones regulate SHANK expression[J]. Front Mol Neurosci, 2018, 11: 337. DOI:10.3389/fnmol.2018.00337 |
| [7] | HOFFMAN E J, TURNER K J, FERNANDEZ J M, et al. Estrogens suppress a behavioral phenotype in zebrafish mutants of the autism risk gene, CNTNAP2[J]. Neuron, 2016, 89(4): 725–733. DOI:10.1016/j.neuron.2015.12.039 |
| [8] | FILICE F, LAUBER E, VÖRCKEL K J, et al. 17-β estradiol increases parvalbumin levels in Pvalb heterozygous mice and attenuates behavioral phenotypes with relevance to autism core symptoms[J]. Mol Autism, 2018, 9: 15. DOI:10.1186/s13229-018-0199-3 |
| [9] | KREZEL W, DUPONT S, KRUST A, et al. Increased anxiety and synaptic plasticity in estrogen receptor beta -deficient mice[J]. Proc Natl Acad Sci USA, 2001, 98(21): 12278–12282. DOI:10.1073/pnas.221451898 |
| [10] | FAN X T, WARNER M, GUSTAFSSON J A. Estrogen receptor beta expression in the embryonic brain regulates development of calretinin-immunoreactive GABAergic interneurons[J]. Proc Natl Acad Sci USA, 2006, 103(51): 19338–19343. DOI:10.1073/pnas.0609663103 |
| [11] | ZOU Y L, LU Q M, ZHENG D, et al. Prenatal levonorgestrel exposure induces autism-like behavior in offspring through ERβ suppression in the amygdala[J]. Mol Autism, 2017, 8: 46. DOI:10.1186/s13229-017-0159-3 |
| [12] | XIE W G, GE X H, LI L, et al. Resveratrol ameliorates prenatal progestin exposure-induced autism-like behavior through ERβ activation[J]. Mol Autism, 2018, 9: 43. DOI:10.1186/s13229-018-0225-5 |
| [13] | CRIDER A, THAKKAR R, AHMED A O, et al. Dysregulation of estrogen receptor beta (ERβ), aromatase (CYP19A1), and ER co-activators in the middle frontal gyrus of autism spectrum disorder subjects[J]. Mol Autism, 2014, 5(1): 46. DOI:10.1186/2040-2392-5-46 |
| [14] | CRIDER A, NELSON T, DAVIS T, et al. Estrogen receptor β agonist attenuates endoplasmic reticulum stress-induced changes in social behavior and brain connectivity in mice[J]. Mol Neurobiol, 2018, 55(9): 7606–7618. DOI:10.1007/s12035-018-0929-8 |
| [15] | AMODEO D A, RIVERA E, COOK E H JR, et al. 5HT2A receptor blockade in dorsomedial striatum reduces repetitive behaviors in BTBR mice[J]. Genes Brain Behav, 2017, 16(3): 342–351. DOI:10.1111/gbb.12343 |
| [16] | FAN X T, WARNER M, GUSTAFSSON J A. Estrogen receptor beta expression in the embryonic brain regulates development of calretinin-immunoreactive GABAergic interneurons[J]. Proc Natl Acad Sci USA, 2006, 103(51): 19338–19343. DOI:10.1073/pnas.0609663103 |



