肺癌是全球最常见的恶性肿瘤,其发病率及死亡率居恶性肿瘤首位,大约85%肺癌为非小细胞肺癌(non-small cell lung cancer,NSCLC),而30%~50%的NSCLC会发生脑转移[1-3]。晚期肺癌中位生存期仅1~3个月,表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitors, EGFR-TKIs)分子靶向治疗给晚期肺癌带来了11.3个月的无进展疾病生存期[4]。目前用于检测EGFR突变检测的方法主要包括:ARMS、二代测序(next generation sequencing,NGS)和ddPCR等。但其费用较高;另外,基因检测一般需要组织样本以保证其特异性和敏感性,部分患者病变部位特殊或一般情况稍差,导致标本获取不理想而致检测失败。对于该类愿意接受EGFR-TKI治疗的人群,需要一种新的方法评价EGFR突变,指导临床选择EGFR-TKI药物,延长患者生存期。因此,本研究通过分析116例NSCLC患者临床及MRI特征与EGFR基因突变状态,以探讨肺NSCLC患者临床脑转移MRI特征与EGFR突变(19外显子缺失突变和21外显子L858R错义突变)的关系。为一些无临床活检指征的患者,在抗肿瘤治疗前是否可行一线EGFR-TKI靶向治疗提供一定的临床证据;同时,精确指导临床选择EGFR-TKI药物,提高晚期肺癌生存质量,延长生存期。
1 资料与方法 1.1 临床资料收集本院2011年1月至2017年1月,经病理确诊为肺NSCLC的患者共116例,男性82例,女性34例。患者均于抗肿瘤治疗前行颅脑MRI增强检查提示颅脑转移。本研究获得本院伦理委员会批准[医研伦审(2017)第35号],所有患者书面知情同意豁免。
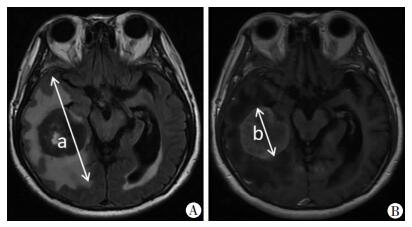
1.2 颅脑MRI扫描方法及MRI参数使用西门子公司1.5T或3.0T超导型磁共振扫描仪,头颅线圈。116例患者行颅脑T1WI(TR/TE 400/18 ms)、T2WI(TR/TE 4000/120 ms)及Flair(TR/TE 2000/20 ms)序列横断位平扫,而后给予静脉注射顺磁性造影剂钆喷酸葡胺(注射剂量0.2 mL/kg)后行横断位、矢状位和冠状位T1WI增强扫描;并收集脑转移瘤部位、数量、强化方式、转移瘤灶最大瘤周水肿直径(图 1A)、最大转移瘤灶最大径(图 1B)及瘤周水肿指数。瘤周水肿指数=(最大转移瘤灶瘤周水肿最大径-最大转移瘤灶直径)/最大转移瘤灶最大径[5]。
|
| A:Flair序列a:转移瘤灶最大瘤周水肿直径;B:MRI增强序列b:最大脑转移瘤最大径 图 1 MRI检测转移瘤(48岁,男性右下肺腺癌伴右侧颞叶转移瘤患者)相关指标 |
1.3 基因检测
患者均应用扩增阻滞突变系统(ARMS)方法检测了肺原发灶或者转移灶组织的EGFR基因突变状态。主要探讨EGFR基因外显子19和21的2种主要基因突变位点(del和L858R)。
1.4 统计学分析采用SPSS 20.0统计软件。不同基线特征间EGFR不同类型突变率采用χ2检验,必要时使用Fisher确切概率法。水肿直径、肿瘤直径和水肿指数在不同EGFR突变类型间比较采用Kruskal-Wallis检验,两两组间比较采用Bonferroni法作多重校正。单因素Logistic回归显示与EGFR 19缺失突变和L858R错义突变或EGFR 19缺失突变有相关性的因素(P < 0.1)纳入构建预测模型。单因素回归系数与对应协变量乘积之和作为判断EGFR 19缺失突变和L858R错义突变的预测模型(模型1)或EGFR 19缺失突变的预测模型(模型2)。利用R软件包“pROC”函数“roc.test”进行成对曲线下面积比较。P < 0.05定为有统计学意义。Origin 8.0用于作散点图。
2 结果 2.1 EGFR突变与患者临床特征关系116例NSCLC脑转移患者中,EGFR野生型66例,EGFR突变型50例(43.1%),其中EGFR 19缺失突变22例(19.0%),L858R突变共28例(24.1%)。男性82例,女性34例;年龄大于60岁49例,小于或等于60岁67例;有吸烟史54例,无吸烟史62例(表 1)。年龄与EGFR突变类型显著相关(P=0.025),与年龄>60岁患者相比,年龄<60岁患者有较高比例的19 Del突变(25.4% vs 10.2%, P=0.040),但有较少比例的L858R突变(16.4% vs 34.7%, P=0.025)。女性突变率多于男性(55.9% vs 37.8%),但差异无统计学意义(P=0.14)。EGFR19、21外显子突变状况与患者的性别、吸烟状态、原发灶位置及CEA值关系无统计学意义(P>0.05,表 2)。
| 临床特征 | 例数 | 百分比 |
| 性别 | ||
| 女 | 34 | 29.3% |
| 男 | 82 | 70.7% |
| 年龄 | ||
| ≤60岁 | 67 | 57.8% |
| >60岁 | 49 | 42.2% |
| 吸烟史 | ||
| 无 | 62 | 53.4% |
| 有 | 54 | 46.6% |
| 原发病灶位置 | ||
| 右肺 | 73 | 62.9% |
| 左肺 | 43 | 37.1% |
| EGFR突变 | ||
| 野生型 | 66 | 56.9% |
| 19缺失突变 | 22 | 19.0% |
| L858R突变 | 28 | 24.1% |
| 脑转移灶个数 | ||
| 单发 | 29 | 25.0% |
| 多发 | 87 | 75.0% |
| 脑转移灶位置 | ||
| 幕上 | 59 | 50.9% |
| 幕下 | 2 | 1.7% |
| 幕上和幕下 | 55 | 47.4% |
| 强化方式 | ||
| 非均匀 | 18 | 15.5% |
| 环状 | 32 | 27.6% |
| 结节样 | 36 | 31.0% |
| 混合型 | 30 | 25.9% |
| 临床特征 | 中位值(范围) | |
| 脑转移灶(n=201) | ||
| 水肿直径/cm | 2.69(0.00~11.68) | |
| 肿瘤最大径/cm | 1.39(0.20~7.13) | |
| 水肿指数 | 0.757(0.000~4.921) | |
| CEA/ng·mL-1 | 8.16(0.74~1.65) | |
| 基线特征 | 野生型 | 19缺失 | L858R |
| 性别 | |||
| 女 | 15(44.1) | 7(20.6) | 12(35.3) |
| 男 | 51(62.2) | 15(18.3) | 16(19.5) |
| 年龄 | |||
| ≤60岁 | 39(58.2) | 17(25.4)a | 11(16.4)a |
| >60岁 | 27(55.1) | 5(10.2) | 17(34.7) |
| 吸烟史 | |||
| 无 | 31(50.0) | 12(19.4) | 19(30.6) |
| 有 | 35(64.8) | 10(18.5) | 9(16.7) |
| 原发病灶位置 | |||
| 右肺 | 42(57.5) | 17(23.3) | 14(19.2) |
| 左肺 | 24(55.8) | 5(11.6) | 14(32.6) |
| CEA/ng·mL-1b | 7.52(0.74~1065) | 4.79(0.79~500) | 10.12(0.92~1059) |
| a:P < 0.05,与>60岁比较;b:数据形式为中位值(范围),其余数据形式为例(%) | |||
2.2 EGFR突变与脑转移灶MRI特征关系
分析EGFR突变与MRI特征,包括脑转移瘤部位、个数、强化方式、最大转移瘤灶最大径、最大转移瘤灶瘤周水肿直径及瘤周水肿指数的相关性。MRI检查脑转移瘤病灶共201个,其中单发病灶29例,多发病灶87例(172个脑转移灶)。统计分析结果显示(表 3、图 2),瘤周水肿直径和瘤周水肿指数与EGFR突变状态(野生型、19 DEL和L858R突变)具有显著相关性。多重校正后,野生型组瘤周水肿直径显著高于19缺失突变组(中位值: 2.87 vs 1.54, P=0.008);L858R突变组瘤周水肿直径亦显著高于19缺失突变组(中位值: 3.31 vs 1.54, P=0.034)。然而瘤周水肿指数仅在野生型组中显著高于19缺失突变组(中位值: 0.979 vs 0.413, P=0.012)。
| MRI影像特征 | 野生型 | 19 Del | L858R |
| 脑转移灶个数 | |||
| 单发 | 20(69.0) | 3(10.3) | 6(20.7) |
| 多发 | 46(52.9) | 19(21.8) | 22(25.3) |
| 脑转移灶位置a | |||
| 幕上 | 38(64.4) | 9(15.3) | 12(20.3) |
| 幕下 | 2(100) | 0(0.0) | 0(0.0) |
| 幕上和幕下 | 26(47.3) | 13(23.6) | 16(29.1) |
| 强化方式a | |||
| 不均匀 | 10(55.6) | 4(22.2) | 4(22.2) |
| 环状 | 21(65.6) | 5(15.6) | 6(18.8) |
| 结节样 | 22(61.1) | 7(19.4) | 7(19.4) |
| 混合型 | 13(43.3) | 6(20.0) | 11(36.7) |
| a:Fisher确切概率法 | |||

|
| A:水肿直径;B:肿瘤直径;C:水肿指数a:P < 0.05,EGFR19缺失突变与野生型比较;b:P < 0.05,EGFR 19缺失突变与EGFR L858R突变比较 图 2 颅脑转移灶MRI影像特征在不同EGFR突变的比较 |
2.3 脑转移灶MRI及临床特征对EGFR突变的评价
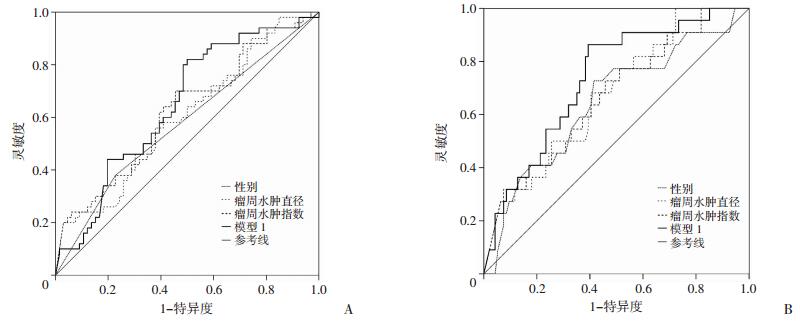
为了探讨肺NSCLC脑转移MRI对EGFR突变的检测能力,比较116例肺NSCLC脑转移患者MRI及临床特征与EGFR突变的相关性,单因素logistic回归分析显示,年龄、瘤周水肿直径及水肿指数与EGFR 19缺失突变和L858R突变有显著相关性,即水肿直径每增加1 cm和水肿指数越高,EGFR 19缺失突变和L858R突变发生率越低(OR=0.868, 95%CI: 0.753~1.000, P=0.050;OR=0.640, 95%CI: 0.421~0.974, P= 0.037)。模型1评分值越高,EGFR敏感突变发生率越高(OR=1.808, 95%CI: 1.151~2.839, P=0.010)。对于单独分析EGFR 19缺失突变有类似结果。但是对基线特征校正后,模型1和模型2都分别不是EGFR敏感突变或EGFR 19缺失突变的独立预测因素。ROC曲线分析模型1和模型2对EGFR L858R和19 DEL(图 3 A)以及19 DEL突变(图 3B)的预测效能(AUC)分别为0.648(95%CI: 0.470~0.683)和0.733 (95%CI: 0.625~0.842)。总之,MRI及临床特征对EGFR突变具有重要的预测能力。
|
| A:对19缺失和L858R突变的预测效能;B:对19缺失的预测效能 图 3 脑部病灶MRI特征与临床基线特征对EGFR突变的预测效能 |
3 讨论
EGFR-TKI(厄洛替尼和吉非替尼)在晚期NSCLC患者的治疗中取得了显著的效果,改善患者预后,延长患者生存期,对脑转移瘤的患者也具有一定控制作用[6]。本研究通过分析116例NSCLC患者临床特征及MRI影像(脑转移瘤个数、部位、强化方式、最大病灶最大径、最大病灶瘤周水肿直径及水肿指数)与EGFR基因突变状态(19外显子缺失突变和21外显子L858R点突变)之间的关系,发现年龄、瘤周水肿直径及水肿指数与EGFR 19缺失突变和L858R突变有显著相关性,并构建年龄+瘤周水肿直径+水肿指数的预测模型,ROC曲线分析显示,该模型对L858R,19 DEL突变的预测率(AUC)分别为64.8%和73.3%。因此,我们提出临床特征及MRI影像可很好的预测EGFR基因突变,对经济基础差、无临床活检指征的患者选用EGFR-TKI靶向治疗,提供重要的理论基础。
年龄+瘤周水肿直径+水肿指数预测模型对NSCLC患者EGFR突变的预测效能,不差于血清游离DNA突变富集PCR及测序分析的检测方法。年龄+瘤周水肿直径+水肿指数预测模型对EGFR突变L858R,19 DEL突变的预测率(AUC)分别为64.8%和73.3%,而血清EGFR突变富集PCR及测序分析的预测率仅为71.2%;而且该模型在80.9%特异性下有40.9%的灵敏度,而血清游离DNA检测的敏感性和特异性为35.6%和95.5%[7]。另外一项国内的研究显示,血清EGFR mRNA水平与组织之间的一致率仅为61.6%,而转移淋巴结与血清EGFR mRNA水平具有较高的一致率(76.4%)[8]。这些结果证实,通过分析NSCLC脑转移临床特征及MRI影像学特征,构建年龄+瘤周水肿直径+水肿指数EGFR突变的预测模型,可很好的预测EGFR基因突变,为经济基础差、无法进行穿刺活检的患者选用EGFR-TKI靶向治疗,提供重要的理论基础。
脑转移灶低水平的瘤周水肿可能是EGFR基因突变侵袭性的一种形式。既往研究报道NSCLC患者EGFR基因突变型较野生型发生脑转移概率高[9-10],EGFR信号途径的活化或EGFR突变可促进肿瘤生长和免疫逃逸[11-12],而不激活炎症反应。MRI具有良好的分辨力,可从各个方位清晰地显示脑组织的形态,并且实现功能成像,是肿瘤脑转移瘤首选的检查方法。EGFR基因突变型较野生型,肿瘤细胞增殖周期明显缩短,侵袭转移明显增加。而且EGFR野生型、EGFR 19外显子缺失突变和L858R突变肿瘤具有不同的生物学行为[13]。有报道显示EGFR突变的特性可能与NSCLC患者影像学相关。SHI等[14]发现:EGFR 19外显子缺失突变与胸部CT小病灶、胸膜凹陷征且无肺纤维化征象有关,而21外显子突变与边缘棘突征和非实性结节有关。LIU等[15]发现:小病灶、胸膜凹陷征、空泡征以及支气管血管束增粗与肺NSCLC EGFR突变具有显著相关性。有研究显示NSCLC EGFR突变组患者SUV值较低[16]。SEKINE等[17]探讨了脑转移NSCLC患者EGFR基因突变状态与颅脑转移灶影像的关系。总之,这些研究提供了从影像学方面判断EGFR突变的可能性。本研究通过MRI分析201个NSCLC患者脑转移灶发现,瘤周水肿直径和瘤周水肿指数在EGFR野生型和2种主要突变类型3组间差异有统计学意义(P < 0.05),野生型组瘤周水肿直径及瘤周水肿指数均显著高于19缺失突变组;19外显子缺失突变组中位脑转移灶个数较EGFR野生组及L858R突变组中位脑转移灶个数多,且19外显子突变组肿瘤中位大小较野生型及L858R组均小,与SEKINE等报道的结果类似。
年龄+瘤周水肿直径+水肿指数预测EGFR突变状态的模型,不增加患者经济负担、穿刺风险,而且具有较高预测精度,具有重要的临床意义。然而本研究还存在一定的缺陷:①本研究为单中心、小样本的回顾性研究,需要进一步扩大样本量,进行多中心研究证实肺NSCLC脑转移瘤MRI影像学特征与EGFR突变的相关性;②由于颅内转移灶表达较难获得,该研究假设NSCLC颅内转移灶和原发灶EGFR突变状态具有较高一致性;③该研究主要是为一些经济基础差、无临床活检指征的患者,在抗肿瘤治疗前,是否可行一线EGFR- TKI靶向治疗,提供一定的临床证据;而未纳入EGFR-TKI治疗中、后的MRI影像资料分析内容之中;需进一步纳入MRI动态影像资料进一步完善该研究,精确指导临床选择EGFR-TKI药物,提高晚期肺癌生存质量,延长生存期。
| [1] | GASPAR L E, CHANSKY K, ALBAIN K S, et al. Time from treatment to subsequent diagnosis of brain metastases in stage Ⅲ non-small-cell lung cancer: a retrospective review by the Southwest Oncology Group[J]. J Clin Oncol, 2005, 23(13): 2955–2961. DOI:10.1200/JCO.2005.08.026 |
| [2] | OLMEZ I, DONAHUE B R, BUTLER J S, et al. Clinical outcomes in extracranial tumor sites and unusual toxicities with concurrent whole brain radiation(WBRT) and Erlotinib treatment in patients with non-small cell lung cancer(NSCLC) with brain metastasis[J]. Lung Cancer, 2010, 70(2): 174–179. DOI:10.1016/j.lungcan.2010.01.018 |
| [3] | STARK A M, STÖHRING C, HEDDERICH J, et al. Surgical treatment for brain metastases: Prognostic factors and survival in 309 patients with regard to patient age[J]. J Clin Neurosci, 2011, 18(1): 34–38. DOI:10.1016/j.jocn.2010.03.046 |
| [4] | LA SALVIA A, ROSSI A, GALETTA D, et al. Intercalated chemotherapy and epidermal growth factor receptor inhibitors for patients with advanced non-small-cell lung cancer: a systematic review and meta-analysis[J]. Clin Lung Cancer, 2017, 18(1): 23–33. DOI:10.1016/j.cllc.2016.08.006 |
| [5] | 任广, 陈爽, 耿道颖. 脑肿瘤瘤周水肿MSCT灌注成像的定量研究[J]. 放射学实践, 2011, 26(5): 483–487. DOI:10.3969/j.issn.1000-0313.2011.05.003 |
| [6] | MAEMONDO M, INOUE A, KOBAYASHI K, et al. Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR[J]. N Engl J Med, 2010, 362(25): 2380–2388. DOI:10.1056/NEJMoa0909530 |
| [7] | ZHAO X, HAN R B, ZHAO J, et al. Comparison of epidermal growth factor receptor mutation statuses in tissue and plasma in stage Ⅰ-Ⅳ non-small cell lung cancer patients[J]. Respiration, 2013, 85(2): 119–125. DOI:10.1159/000338790 |
| [8] | ZHUO Y, GUO Q, SONG P, et al. Correlation study and significance of the EGFR expression in serum, lymph nodes and tumor tissue of NSCLC[J]. Thorac Cancer, 2014, 5(1): 31–37. DOI:10.1111/1759-7714.12048 |
| [9] | BUREL-VANDENBOS F, AMBROSETTI D, COUTTS M, et al. EGFR mutation status in brain metastases of non-small cell lung carcinoma[J]. J Neurooncol, 2013, 111(1): 1–10. DOI:10.1007/s11060-012-0990-5 |
| [10] | LI Q, DENG M, XI M, et al. Characteristics and treatment of brain metastases from esophageal squamous cell carcinoma[J]. J Cancer, 2018, 9(5): 901–905. DOI:10.7150/jca.21511 |
| [11] | LIM S O, LI C W, XIA W, et al. EGFR signaling enhances aerobic glycolysis in triple-negative breast cancer cells to promote tumor growth and immune escape[J]. Cancer Res, 2016, 76(5): 1284–1296. DOI:10.1158/0008-5472.CAN-15-2478 |
| [12] | CHEN N, FANG W, ZHAN J, et al. Upregulation of PD-L1 by EGFR activation mediates the immune escape in EGFR-driven NSCLC: implication for optional immune targeted therapy for nsclc patients with EGFR mutation[J]. J Thorac Oncol, 2015, 10(6): 910–923. DOI:10.1097/JTO.0000000000000500 |
| [13] | HSIAO S H, CHOU Y T, LIN S E, et al. Brain metastases in patients with non-small cell lung cancer: the role of mutated-EGFRs with an exon 19 deletion or L858R point mutation in cancer cell dissemination[J]. Oncotarget, 2017, 8(32): 53405–53418. DOI:10.18632/oncotarget.18509 |
| [14] | SHI Z, ZHENG X, SHI R, et al. Radiological and clinical features associated with epidermal growth factor receptor mutation status of exon 19 and 21 in lung adenocarcinoma[J]. Sci Rep, 2017, 7(1): 364. DOI:10.1038/s41598-017-00511-2 |
| [15] | LIU Y, KIM J, QU F, et al. CT Features associated with epidermal growth factor receptor mutation status in patients with lung adenocarcinoma[J]. Radiology, 2016, 280(1): 271–280. DOI:10.1148/radiol.2016151455 |
| [16] | CHO A, HUR J, MOON YW, et al. Correlation between EGFR gene mutation, cytologic tumor markers, 18F-FDG uptake in non-small cell lung cancer[J]. BMC Cancer, 2016, 16: 224. DOI:10.1186/s12885-016-2251-z |
| [17] | SEKINE A, KATO T, HAGIWARA E, et al. Metastatic brain tumors from non-small cell lung cancer with EGFR mutations: distinguishing influence of exon 19 deletion on radiographic features[J]. Lung Cancer, 2012, 77(1): 64–69. DOI:10.1016/j.lungcan.2011.12.017 |



