肝细胞癌(hepatocellular carcinoma, HCC),是全球最常见癌症之一,位居肿瘤死亡原因第3位[1],是一种具有高复发倾向的恶性肿瘤,根治性切除后的5年复发率高达70%以上[2]。目前复发性肝癌(recurrent HCC,RHCC)的治疗策略有经导管肝动脉化疗栓塞术(transcatheter arterial chemoembolization, TACE)、分子靶向治疗、免疫治疗等非根治性疗法和再次手术切除、射频消融、肝移植等根治性的治疗手段。但由于供体匮乏等原因的限制,只有少数复发性肝癌患者有望获得肝移植,绝大部分患者的治疗仍采取手术切除、射频消融术等方式。在手术切除治疗复发性肝癌上,开腹肝切除术存在术中出血量较大、术后并发症较多、住院时间较长等缺点,而腹腔镜肝切除在这些指标上都优于开腹手术,并且远期肿瘤学结果与开腹手术相当[3]。自2009年路易斯维尔宣言发表以来[4],随着世界上各大肝胆中心腹腔镜肝切除技术的进步,目前的腹腔镜肝切除已实现了无手术禁区。研究表明,腹腔镜肝切除术治疗复发性肝癌安全可行、疗效确切[5]。射频消融术是可以达到根治性治疗的另一主要手段,尤其在复发小肝癌的患者中,与开腹手术相比,可以达到相同的远期疗效,有着开腹手术无法比拟的微创、短住院时间、患者满意度高等优点[2, 6-7]。目前国内外在对比腹腔镜肝切除和射频消融治疗复发性肝癌疗效的研究中,尚少见前瞻性的随机对照研究(RCT)研究,针对复发性肝癌根治性治疗方式的选择仍缺乏基于更高级别循证医学证据的推荐。本研究采用前瞻性随机对照的方法,对比腹腔镜肝切除术与射频消融术治疗复发性肝癌的围手术期和远期肿瘤学结果,并对影响患者再次复发的因素。进行初步研究探讨,为复发性肝癌患者手术方式的选择提供更高级别的循证医学证据。
1 资料与方法 1.1 临床资料纳入2016年9月至2017年9月在陆军军医大学(第三军医大学)第一附属医院全军肝胆外科研究所的复发性肝癌患者80例(男性75例,女性5例),其中腹腔镜肝切除术(laparoscopic hepatectomy, LH)39例,射频消融术(radiofrequency ablation, RFA)41例,两组年龄分别为LH组:(50.0±10.0)岁; RFA组:(48.9± 11.3)岁, (P>0.05),中位年龄为LH组:51.0岁; RFA组:49.0岁,复发肿瘤大小,LH组:(21.0±6.8)mm;RFA组:(18.2±8.2)mm, (P>0.05),所有患者均严格按照入组标准并按随机原则,纳入本项研究中。
入组标准:①男女不限,年龄18~70岁;②术前病理诊断为复发性肝细胞癌,根治切除术后首次复发,既往行肝切除手术史,未进行其他相关外科手术、射频消融、经TACE处理,无确定性放化疗,未服用分子靶向药物、未行免疫治疗等抗癌处理;③复发肿瘤要求:复发肿瘤符合米兰标准(单个肿瘤直径不超过5 cm或较多发的肿瘤少于3个并且最大直径不超过3 cm)[8]。复发癌灶在超声下可视,未侵犯门静脉、肝动静脉及下腔静脉浸润,无淋巴结或肝外转移;④肿瘤无破裂或出血,不邻近肠管、胃、胆囊或膈肌,不邻近第一肝门或重要血管及胆管等。⑤Child-Pugh分级A级或者B级,ICG-R15<15%;⑥自愿参加研究,自愿接受两组中任何一组进行治疗,知情同意。
排除标准:①非肝脏复发性肿瘤,如结直肠转移癌,术后病理学检查为胆管细胞性或者混合细胞性肝癌; ②严重的上腹部粘连,不能耐受腹腔镜手术的CO2气腹;③中国香港、澳门特别行政区、中国台湾地区与国外,估计术后难以追踪、随访者。
1.2 方法通过对国内外相关文献的学习,腹腔镜肝切除术与射频消融术在治疗复发性肝癌上有相近的远期肿瘤学结果,此中期随访报告的随访终止时间为术后2年,本研究最终随访时间为3年,对比两组患者围术期相关指标,1、2年总生存率,无瘤生存率。所有患者住院期间及随访期间数据,均收集于本研究所。本研究已获得陆军军医大学第一附属医院伦理委员会批准[2017科研第(34)号],并在ClinicalTrails.gov注册,注册号为:NCT03313648。所有入组的患者均知情同意。
1.3 统计学分析汇总前期有关临床试验及国内外文献,以肝癌复发后腹腔镜肝切除术后3年生存率83%,组间6%的临床差异为预期目标,以80%的检验效能,检验水准:α=0.05,P<0.05差异有统计学意义。考虑10%的脱落率,采用NCSS PASS 11.0.7软件,按照差异性检验估算样本量为80。应用COX比例风险模型分析影响术后再次复发的危险因素,通过Kaplan-Meier法计算总生存率,无瘤生存率,组间用Log-Rank法进行比较。
1.4 随机化入组在决定患者入组后,我研究所1名专职人员通过计算机生成随机数字化表,并随机选取表中数字,打印出每个数字并放入信封,数字尾数为奇数则患者纳入LH组,数字尾数为偶数则纳入RFA组。在患者拟行手术的前1天,手术医师在盛有信封的容器中随机抽取。相应数字尾数的患者得到相应的手术治疗,整个随机化入组方案只有该专职人员有权知晓。
1.5 手术方法 1.5.1 腹腔镜肝切除术根据既往手术方式、肝脏储备功能情况、肿瘤部位、数目等选择解剖性或非解剖性切除。腹腔镜探查肝硬化严重程度,肿瘤有无破裂出血、膈肌有无侵犯、网膜、腹腔及盆腔脏器有无肿瘤侵犯及种植,肝十二指肠韧带有无肿大淋巴结。若肿瘤未复发于肝脏表面,则使用术中超声探查,确定肿瘤位置。需行解剖性肝切除时,先解剖出预切除肝段的Glisson蒂,行区域性入肝血流阻断。非解剖性切除时,在距肿瘤边缘2 cm划定预切除线以保证足够切缘。因本研究患者既往均行肝切除手术,腹腔内会有一定程度的粘连,遂需逐渐分离粘连,并充分暴露手术区域。以超声刀离断肝实质,Biclamp止血钳处理肝段面渗血。若术中出现腹腔镜下难以控制的大出血、因患者肝硬化程度较重,肝段面渗血无法处理或患者腹腔内粘连极为严重腹腔镜下无法完全分离粘连,则及时中转开腹,此时需计算中转开腹率。
1.5.2 射频消融术患者取仰卧位,彩色超声探查腹腔各脏器,重点查看肝脏、肝门部、门静脉、肝内外胆管有无肿瘤播散及侵犯。经左侧肘静脉注射六氟化硫造影剂(59 mg/5 mL),结合术前上腹部增强CT及脏器声学造影检查,确定肝内肿瘤位置、数量、血供、大小及位置,决定穿刺针数目、穿刺部位和深度于体表标记。根据探查结果决定患者体位,常规消毒铺巾后,2%利多卡因麻醉,于标记点在彩色超声引导下行经皮肝穿刺活检术,然后沿窦道将射频消融治疗针穿刺进入上述病变部位行射频消融术治疗。术后48 h复查脏器声学造影判断病灶是否消融完全。
1.5.3 随访以手术时间为时间0点,术后前3个月,每月随访1次,3个月后每3个月随访1次,共随访3年,本中期随访报告随访至第2年。每次随访检查血常规、肝功、甲胎蛋白(AFP)、HBV-DNA定量,脏器声学造影、腹部增强CT或肿瘤特异性磁共振。当怀疑肝外转移症状出现时,如:咳嗽、骨痛或身体其他部位异常肿胀等,则加行胸部CT及全身PET-CT。患者复查时,若在上述影像学检查中确诊有新发肿瘤,则判定为再次复发;若在2年随访期内患者死亡,则术后第1天至死亡日期为生存期。
2 结果2016年9月至2017年9月,拟参加本研究的80例患者中,随机分至LH组39例,RFA组41例,两组均无失访病例。
LH组有1例患者因术中肝硬化严重且出血较多而中转开腹,1例患者因术后1 d出现肝静脉出血而行再次开腹止血手术,RFA组所有患者均顺利完成手术,无严重并发症。LH组和RFA组患者在肿瘤特性、年龄、性别、术前肝功能分级、既往手术类型、复发肿瘤大小等指标上差异无统计学意义(P>0.05,表 1)。
| 组别 | 性别(男/女) | 年龄/岁 | 乙肝(是/否) | AFP/μg·L-1 | 肝硬化(是/否) | CHILD分级(A/B) | BCLC分级(0/A2/A3) |
| LH组 | 38/1 | 50.026±10.003 | 37/2 | 437.108±1221.208 | 37/2 | 38/1 | 18/17/4 |
| RFA组 | 37/4 | 48.878±11.308 | 37/4 | 1087.159±6272.428 | 39/2 | 39/2 | 24/9/8 |
| P值 | 0.360 | 0.633 | 0.676 | 0.527 | 1.000 | 1.000 | 1.000 |
| 组别 | ALT/IU·L-1 | AST/IU·L-1 | TBIL/μmol·L-1 | ALB/g·L-1 | PLT/109·L-1 | 复发肿瘤大小/mm | |
| LH组 | 50.354±87.217 | 36.733±29.046 | 15.536±6.275 | 43.131±5.297 | 131.051±52.857 | 20.974±6.834 | |
| RFA组 | 37.268±29.339 | 42.017±42.879 | 18.612±9.129 | 44.149±4.029 | 130.732±51.752 | 18.220±8.170 | |
| P值 | 0.366 | 0.523 | 0.084 | 0.335 | 0.987 | 0.107 | |
| 组别 | 复发肿瘤个数 (单发/多发) |
首次手术方式 (解剖/非解剖) |
首次手术肿瘤个数 (单发/多发) |
首次切除肿瘤大小/mm | 首次手术至复发时间/月 | 肿瘤分化程度 (高/中/低) |
|
| LH组 | 37/2 | 10/29 | 37/2 | 38.692±20.077 | 33.4±63.0 | 5/25/9 | |
| RFA组 | 39/2 | 17/24 | 38/3 | 54.585±27.111 | 21.9±27.5 | 5/30/6 | |
| P值 | 1.000 | 0.161 | 1.000 | 0.004 | 0.293 | 0.605 | |
两组患者手术时间LH组(193.4±74.4)min;RFA组[(15.6±5.9)min; P<0.05], 术中失血量LH组(287.9±269.6)mL, 住院时间LH组(15.1±4.5)d,RFA组[(6.0±2.8)d; P<0.05],两组患者围术期资料如表 2所示。
| 组别 | 手术时间/min | 术中出血/mL | 术中输血(是/否) | 术后进食时间/d | 术后下床活动时间/d | 住院时间/d |
| LH组 | 193.4±74.4 | 287.9±269.6 | 3/36 | 2.9±0.9 | 3.1±2.1 | 15.1±4.5 |
| RFA组 | 15.6±5.9 | 0/41 | 1±0 | 1±0 | 6.0±2.8 | |
| P值 | 0.000 | 0.111 | 0.000 | 0.000 | 0.000 |
2.1 并发症
两组患者均无术后切口感染、胆漏、围术期死亡及肝衰竭情况发生,LH组有1例腹腔出血,有2例出现术后出现发热,(1例为肝断面包裹性积液,1例为深静脉导管相关感染引起发热),7例术后出现腹水,2例出现反应性胸腔积液;RFA组有1例出现胸腔积液,1例出现术后发热,1例出现腹水,见表 3。
| 组别 | 腹腔出血 | 术后发热 | 肝断面积液 | 腹水 | 胸腔积液 |
| LH组 | 1 | 3 | 1 | 7 | 2 |
| RFA组 | 0 | 1 | 0 | 1 | 1 |
| P值 | 0.487 | 0.353 | 0.487 | 0.027 | 0.611 |
2.2 复发转移情况及生存率
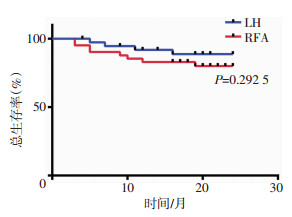
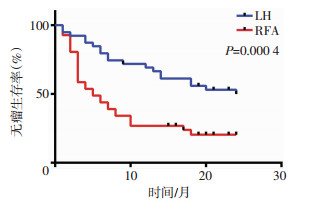
至此中期随访期内LH组再次复发转移19例,RFA组复发转移32例;两组1、2年无瘤生存率,LH组为69.2%、51.3%;RFA组为26.8%、22.0%;两组差异有统计学意义(P<0.05)。LH组5例出现转移,分别为右侧肾上腺转移、腹壁转移、腰椎转移、肺部转移、直肠转移,其中2例合并门静脉癌栓;RFA组5例出现转移,其中2例为肺部转移、1例膈肌转移、1例膈上淋巴结转移、1例腹膜转移。两组1、2年总体生存率分别为,LH组92.3%、89.7%;RFA组85.4%、80.5%。两组术后生存指标如表 4及图 1、2所示。
| 组别 | 总生存时间/月 | 无瘤生存时间/月 | 死亡(是/否) | 再次复发(是/否) |
| LH组 | 19.3±6.8 | 16.4±8.5 | 4/35 | 19/20 |
| RFA组 | 18.6±6.2 | 8.3±7.2 | 8/33 | 32/9 |
| P值 | 0.657 | 0.000 | 0.350 | 0.010 |
|
| 图 1 两组患者2年总生存时间曲线分析 |
|
| 图 2 两组患者无瘤生存时间曲线分析 |
2.3 影响再复发和复发后生存期的因素
将性别、年龄、AFP值、术前肝功、CHILD分级、是否感染HBV、复发肿瘤位置、大小、个数、首次手术肿瘤位置、大小、是否存在肝硬化、手术方式、术后病理分化程度等引入COX比例风险模型做影响2次复发的多因素分层分析,结果显示影响两组患者2次复发的独立危险因素为患者术前AFP水平及选择术式的不同,见表 5,本中期随访分析中,年龄、性别、复发肿瘤个数、肿瘤病理分化程度不是患者复发后的无瘤生存期的影响因素。
| B(回归系数) | SE(标准误) | Wald | df | P值 | Exp(B) | 95% Exp(B)置信区间 | ||
| 下限 | 上限 | |||||||
| AFP | 0.566 | 0.246 | 5.281 | 1 | 0.014 | 1.761 | 1.087 | 2.852 |
| 手术方式 | -2.533 | 0.535 | 22.407 | 1 | 0.000 | 0.079 | 0.028 | 0.227 |
3 讨论
肝细胞癌目前在世界范围内位居肿瘤相关死亡原因第3名[1],尽管目前对于肝细胞癌,手术切除仍是根治性治疗的金标准[9],部分小肝癌患者,根治性切除术后3年总体生存率可接近90%[3],但根治性切除后5年复发率高达70%[10],迄今为止仍没有有效方法防止术后复发。腹腔镜肝切除术在复发性肝癌治疗上的安全性、可行性和有效性,已被国内外研究广泛认同[11-13]。射频消融术在小肝癌,特别是≤3 cm癌结节的疗效已经被医学界广泛接受并被证明是可以与手术切除相当的治疗方式[14]。因肝癌患者术后会常规定期复诊,故复发性癌结节在发现时直径多在5 cm以内。中山大学1项多中心的研究表明,对于5 cm以下的复发性肝细胞癌行RFA治疗,3年生存率为48.6%,与手术切除44.5%比较,差异无统计学意义(P=0.79)[6]。以上研究表明,采用腹腔镜肝切除术和射频消融术这两种微创根治性手术方式治疗复发性肝癌,在选择性病例中,其远期肿瘤学结果与传统开腹手术相当。但目前还没有明确的研究证据支持哪种治疗方法更适合复发性肝癌的患者。
本研究通过RCT的方法来研究腹腔镜肝切除和射频消融术这两种根治性治疗复发性肝癌的手术方式在围术期指标、术后无瘤生存期、术后总生存期的差异,并且分析影响术后再次复发的危险因素。我们发现,围术期指标中,在手术时间、术中输血、术后进食时间、患者下床活动时间、住院时间上,射频消融术与腹腔镜肝切除术相比都有明显的优势,射频消融术术中几乎无失血,故失血量忽略不计。在总生存期的比较上,两种术式术后1、2年生存期差异无统计学意义;而在无瘤生存率的比较上,行腹腔镜肝切除患者的1、2年无瘤生存率要优于行射频消融术的患者。通过COX比例风险模型进行多因素分析影响患者术后无瘤生存时间的可能因素,结论得出手术方式及患者术前AFP水平是影响术后再次复发的危险因素。这表明AFP水平越高的患者,肿瘤往往恶性程度越高,术后的无瘤生存期越短。年龄、是否感染乙肝、复发肿瘤大小、复发肿瘤个数均不是治疗后再复发的危险因素。本研究得出结果腹腔镜肝切除术与射频消融术在治疗复发性肝癌患者的总生存期相当,GAVRIILIDIS等[15]的1项Meta分析提出射频消融与手术再切除在1、3、5年的总生存率及无瘤生存率差异无统计学意义,但1项针对中国的629例复发性肝癌患者的多中心前瞻性队列研究表明,手术切除的5年生存率优于射频消融术[16]。在无瘤生存期的比较上,手术切除有明显的优势[17-18]。本研究之所以得出总生存期上两组差异无统计学意义,可能与随访时间较短,病例数较少有关。所以我们认为,在复发性肝癌患者复发后根治性治疗手段的选择上,倾向于当患者年轻或手术耐受性较好、全身状况较好时,选择腹腔镜肝切除术,因其有更优的无瘤生存期,有可能得到更好的预后及肿瘤学结果;当患者年迈或全身情况较差、手术耐受性不佳时,可选择射频消融术,可以达到在根治性治疗的前提下,规避并发症,也可得到较好的肿瘤学结果。
日本学者认为初次肝切除时单发肿瘤,1年以上复发,复发肝癌没有门静脉浸润是预后较好的3个因素,满足这3个因素的患者5年生存率可达86%[19]。对于本研究复发后的肿瘤, 首次复发间期、复发肿瘤的个数、大小对复发性肝癌术后再次复发无显著性影响,原因可能是:①本研究多发肿瘤病例数较少;②首次复发间期均为20个月左右等有关。研究表明患者术前AFP不仅是影响初次手术后复发也是复发后治疗再复发的危险因素,高浓度AFP的肝癌一般恶性程度较高,同时复发肿瘤个数及复发后的Child-Pugh分级是影响复发术后总生存期的危险因素[6-7, 20]。本研究得出AFP是影响复发术后再次复发的危险因素的结果,与文献[7]报道一致,可能与AFP与肿瘤生物学行为有关。
因本研究系中期随访分析,存在病例数较少、单中心研究、随访时间较短等不足,有待多中心、大样本、长时间随访的研究进一步印证本研究所提出的结论。
| [1] | JEMAL A, BRAY F, CENTER M M, et al. Global cancer statistics[J]. CA Cancer J Clin, 2011, 61(2): 69–90. DOI:10.3322/caac.20107 |
| [2] | CHOI D, LIM H K, RHIM H, et al. Percutaneous radiofrequency ablation for recurrent hepatocellular carcinoma after hepatectomy: long-term results and prognostic factors[J]. Ann Surg Oncol, 2007, 14(8): 2319–2329. DOI:10.1245/s10434-006-9220-8 |
| [3] | CHAN A C, POON R T, CHOK K S, et al. Feasibility of laparoscopic re-resection for patients with recurrent hepatocellular carcinoma[J]. World J Surg, 2014, 38(5): 1141–1146. DOI:10.1007/s00268-013-2380-3 |
| [4] | BUELL J F, CHERQUI D, GELLER D A, et al. The international position on laparoscopic liver surgery: The Louisville Statement, 2008[J]. Ann Surg, 2009, 250(5): 825–830. DOI:10.1097/SLA.0b013e3181b3b2d8 |
| [5] | GOH B K, TEO J Y, CHAN C Y, et al. Review of 103 cases of laparoscopic repeat liver resection for recurrent hepatocellular carcinoma[J]. J Laparoendosc Adv Surg Tech A, 2016, 26(11): 876–881. DOI:10.1089/lap.2016.0281 |
| [6] | LIANG H H, CHEN M S, PENG Z W, et al. Percutaneous radiofrequency ablation versus repeat hepatectomy for recurrent hepatocellular carcinoma: a retrospective study[J]. Ann Surg Oncol, 2008, 15(12): 3484–3493. DOI:10.1245/s10434-008-0076-y |
| [7] | LU M D, YIN X Y, XIE X Y, et al. Percutaneous thermal ablation for recurrent hepatocellular carcinoma after hepatectomy[J]. Br J Surg, 2005, 92(11): 1393–1398. DOI:10.1002/bjs.5102 |
| [8] | MAZZAFERRO V, REGALIA E, DOCI R, et al. Liver transplantation for the treatment of small hepatocellular carcinomas in patients with cirrhosis[J]. N Engl J Med, 1996, 334(11): 693–699. DOI:10.1056/NEJM199603143341104 |
| [9] | ERRIDGE S, PUCHER P H, MARKAR S R, et al. Meta-analysis of determinants of survival following treatment of recurrent hepatocellular carcinoma[J]. Br J Surg, 2017, 104(11): 1433–1442. DOI:10.1002/bjs.10597 |
| [10] | BRUIX J, SHERMAN M, American Association for the Study of Liver Diseases. Management of hepatocellular carcinoma: an update[J]. Hepatology, 2011, 53(3): 1020–1022. DOI:10.1002/hep.24199 |
| [11] | BELLI G, CIOFFI L, FANTINI C, et al. Laparoscopic redo surgery for recurrent hepatocellular carcinoma in cirrhotic patients: feasibility, safety, and results[J]. Surg Endosc, 2009, 23(8): 1807–1811. DOI:10.1007/s00464-009-0344-3 |
| [12] | BELLI G, FANTINI C, D'AGOSTINO A, et al. Laparoscopic versus open liver resection for hepatocellular carcinoma in patients with histologically proven cirrhosis: short- and middle-term results[J]. Surg Endosc, 2007, 21(11): 2004–2011. DOI:10.1007/s00464-007-9503-6 |
| [13] | HU M, ZHAO G, XU D, et al. Laparoscopic repeat resection of recurrent hepatocellular carcinoma[J]. World J Surg, 2011, 35(3): 648–655. DOI:10.1007/s00268-010-0919-0 |
| [14] | FENG K, YAN J, LI X, et al. A randomized controlled trial of radiofrequency ablation and surgical resection in the treatment of small hepatocellular carcinoma[J]. J Hepatol, 2012, 57(4): 794–802. DOI:10.1016/j.jhep.2012.05.007 |
| [15] | GAVRIILIDIS P, ASKARI A, AZOULAY D. Survival following redo hepatectomy vs radiofrequency ablation for recurrent hepatocellular carcinoma: a systematic review and meta-analysis[J]. HPB (Oxford), 2017, 19(1): 3–9. DOI:10.1016/j.hpb.2016.10.003 |
| [16] | WANG K, LIU G, LI J, et al. Early intrahepatic recurrence of hepatocellular carcinoma after hepatectomy treated with re-hepatectomy, ablation or chemoembolization: a prospective cohort study[J]. Eur J Surg Oncol, 2015, 41(2): 236–242. DOI:10.1016/j.ejso.2014.11.002 |
| [17] | CHEN X, CHEN Y, LI Q, et al. Radiofrequency ablation versus surgical resection for intrahepatic hepatocellular carcinoma recurrence: a meta-analysis[J]. J Surg Res, 2015, 195(1): 166–174. DOI:10.1016/j.jss.2015.01.042 |
| [18] | THOMASSET S C, DENNISON A R, GARCEA G. Ablation for recurrent hepatocellular carcinoma: a systematic review of clinical efficacy and prognostic factors[J]. World J Surg, 2015, 39(5): 1150–1160. DOI:10.1007/s00268-015-2956-1 |
| [19] | ARII S, MONDEN K, NIWANO M, et al. Results of surgical treatment for recurrent hepatocellular carcinoma; comparison of outcome among patients with multicentric carcinogenesis, intrahepatic metastasis, and extrahepatic recurrence[J]. J Hepatobil Pancreat Surg, 1998, 5(1): 86–92. DOI:10.1007/pl00009956 |
| [20] | ZHANG X, LI C, WEN T, et al. Appropriate treatment strategies for intrahepatic recurrence after curative resection of hepatocellular carcinoma initially within the Milan criteria: according to the recurrence pattern[J]. Eur J Gastroenterol Hepatol, 2015, 27(8): 933–940. DOI:10.1097/MEG.0000000000000383 |



