我国肾癌发病率目前呈逐年上升趋势,占成人恶性肿瘤的2%~3%。近年来,随着健康意识的提高,有50%~60%的肾癌患者可被早期发现和治疗[1],大大提高了肾癌的治愈率和5年生存率。外科手术是肾癌最重要的治疗方式,1993年,WINFIELD等[2]报道了首例腹腔镜肾部分切除术治疗肾脏良性病变。随着手术理念和仪器设备的提升和进步,以机器人辅助腹腔镜手术为代表的肾肿瘤外科治疗已进入精准医学时代。自2004年美国Mayo医院GETTMAN等[3]首先报道机器人辅助下经腹腔入路肾部分切除术(robotic-assisted transperitoneal laparoscopic partial nephrectomy,RALPN)治疗肾肿瘤取得较好效果以来,随着手术机器人系统的逐渐完善和普及,机器人手术在操作精准度、稳定度以及视野的清晰度和层次感等方面展现出较好的优势,得到手术医师及患者的普遍推荐和认可[4-5]。按手术入路不同,机器人辅助下肾部分切除术可分为经腹腔(RALPN)和经后腹腔(robot-assisted retroperitoneal partial nephrectomy,RARPN)两种方式。由于机器人辅助腹腔镜手术对操作空间的要求较高,目前国外大部分报道仍以经腹腔入路为主[6]。但大部分肾脏手术经后腹腔入路更符合手术习惯,因而国内学者在多年经后腹腔入路腹腔镜手术的基础上,将后腹腔入路引入机器人手术,取得了较多的经验[7]。本研究回顾性分析本科2011年6月至2018年6月机器人辅助经后腹腔入路肾部分切除术共118例,对患者术前资料、手术时间、热缺血时间、出血量、术后引流管拔除时间、住院时间、术后并发症以及术后随访情况等进行分析,用以指导该术式适应证的选择及围手术期并发症的预防和处理。
1 资料与方法 1.1 临床资料收集本院2011年6月至2018年6月间收治的118名肾肿瘤患者,其中男性68例,女性50例,年龄为14~84(51.3±12.5)岁,体质量指数(BMI)为(24.6± 3.0)kg/m2; 肿瘤分期:T1a 78例,T1b 40例,肿瘤长径(3.5±1.4)cm,肿瘤R.E.N.A.L.评分[8]为(5.4±1.7)分。入选标准:①术前通过病史采集、辅助检查[血液指标、心电图、胸片、输尿管CT成像(computed tomography urography, CTU)+肾血管CT成像(computed tomography angiography, CTA)、发射型计算机断层扫描(emission computed tomography, ECT)[9]等]明确诊断和手术指征; ②若合并冠心病、高血压、糖尿病等疾病需进行专科治疗并评估无绝对手术禁忌; ③肿瘤分期为T1aN0M0~T1bN0M0。本研究经本院伦理委员会审批通过(KY201016)。
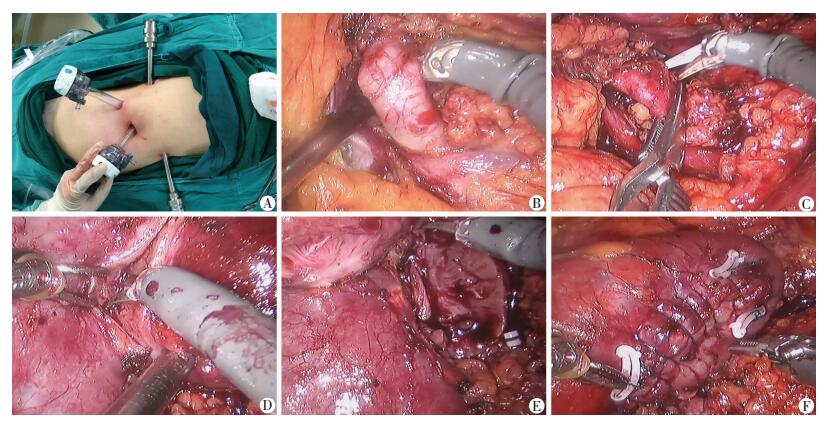
1.2 手术方法采用正侧折刀位。于腋中线髂嵴上方三横指(3~4 cm)处行横切口约2 cm为镜孔,血管钳分离并扩开腰背筋膜,手指推开周围脂肪组织,置入扩张器并充气扩张后腹腔空间,于肋缘与髂骨中点延长线与腋后线交点处切开8 mm纵行切口,手指引导下置入2臂套管,手指进一步推开腹膜,于2臂套管水平、腋前线外下方2 cm处切开8 mm纵行切口,手指引导下置入1臂套管(若腹膜推开困难,可直视下游离后置入),于1臂套管与镜头套管连线中点下方6~8 cm处手指引导下置入12 mm套管为辅助孔,两机器臂与镜头之间成角需大于90°(图 1A)。接CO2气腹,维持14 mmHg压力。使用30°镜,置入机器臂分离并切除腹膜后脂肪组织,用组织粉碎器(深圳好克医疗仪器有限公司)粉碎后负压吸出。沿腰大肌外侧缘上方约1 cm处纵行切开肾周筋膜。于肾门处分离出肾动脉(图 1B)。再行肾周粘连松解术,暴露肿瘤位置(必要时超声定位)。使用动脉阻断钳夹闭肾动脉(图 1C)。使用单极剪刀完整切除肿瘤(图 1D、E),2-0/3-0倒刺线连续分层缝合肾实质,缝线首尾使用Hem-o-lok夹(美国泰利福医疗器械公司)固定(图 1F)。松开动脉阻断钳,检查无活动性出血后,置入引流管,取出标本。固定引流管并逐层缝合切口。
|
| A:套管位置; B:分离肾动脉; C:阻断肾动脉; D:标记切缘; E:完整切除肿瘤; F:缝合肾脏 图 1 RARPN手术步骤 |
1.3 观测指标及随访 1.3.1 观测指标
包括年龄、BMI值、R.E.N.A.L.评分、肿瘤长径、手术时间、热缺血时间、术中出血量、术后引流管拔除时间、术后肠道排气时间、住院时间及术后住院期间并发症情况。
1.3.2 随访指标包括血常规、尿常规、肾功能、胸片、ECT及增强CT等检查项目。电话或门诊随访(常规术后1年内每3个月随访,术后1年以上每半年随访),截止时间2018年10月。
1.4 统计学分析采用SPSS 22.0统计软件。计量资料以x±s表示,组间比较用Student’s t检验。P < 0.05表示差异有统计学意义。
2 结果 2.1 治疗效果分析118例患者均成功完成手术。手术时间为(127.6± 34.5)min,热缺血时间为(19.8±5.1)min,出血量为(97.3±67.3)mL,术后引流管拔除时间为(2.7±0.6)d,术后肠道通气时间为(1.9±0.7)d,住院时间为(6.0±0.9)d。患者不同肿瘤分期(T1a和T1b)分析:T1a组手术时间、热缺血时间短于T1b组(P < 0.05);两组年龄、BMI值、手术时间、术中出血量、术后引流管拔除时间、肠道通气时间、住院时间等差异无统计学意义(表 1)。患者不同BMI(<24 kg/m2和≥24 kg/m2)分析:BMI<24 kg/m2组手术时间短于BMI≥24 kg/m2组(P < 0.05),两组年龄、肿瘤长径、R.E.N.A.L.评分、热缺血时间、术中出血量、术后引流管拔除时间、肠道通气时间、住院时间等差异无统计学意义(表 2)。术后并发症:1例在术后24 h后发生迟发性出血,予以卧床、抗炎、止血,必要时输血等对症支持治疗后痊愈。
| 分期 | n | 年龄/岁 | BMI/kg·m-2 | 手术时间/min | 热缺血时间/min | 出血量/mL | 术后引流管拔除时间/d | 术后肠道通气时间/d | 住院时间/d |
| T1a | 78 | 49.9±12.4 | 24.6±3.1 | 119.3±31.8 | 18.9±4.7 | 89.7±67.3 | 2.6±0.6 | 1.8±0.7 | 5.8±1.0 |
| T1b | 40 | 54.1±12.3 | 24.6±3.0 | 143.7±34.2 | 21.7±5.5 | 112.1±65.8 | 2.8±0.7 | 2.1±0.8 | 6.2±0.7 |
| P值 | 0.08 | 0.93 | <0.01 | <0.01 | 0.08 | 0.06 | 0.11 | 0.06 |
| BMI/kg·m-2 | n | 年龄/岁 | 肿瘤长径/cm | R.E.N.A.L.评分/分 | 手术时间/min | 热缺血时间/min | 出血量/mL | 术后引流管拔除时间/d | 术后肠道通气时间/d | 住院时间/d |
| <24 | 47 | 49.5±14.0 | 3.5±1.5 | 5.3±1.6 | 117.5±35.4 | 20.4±6.2 | 91.2±53.7 | 2.7±0.7 | 1.9±0.8 | 5.8±0.7 |
| ≥24 | 71 | 5.5±11.4 | 3.6±1.2 | 5.4±1.7 | 134.2±32.5 | 19.5±4.2 | 101.3±75.1 | 2.7±0.6 | 1.9±0.7 | 6.1±1.1 |
| P值 | 0.20 | 0.91 | 0.73 | <0.01 | 0.36 | 0.42 | 0.88 | 0.77 | 0.09 |
患者术后病理诊断肾透明细胞癌76例(64.4%),囊性肾癌3例(2.5%),嗜酸性肾细胞癌2例(1.6%),嫌色细胞癌7例(5.9%),血管平滑肌脂肪瘤30例(25.4%)。病理组织学检查显示切缘均为阴性。
2.2 随访随访3个月至5年,平均随访36个月。在随访期内每3~6个月复诊CTU等,117例未见复发、远处转移等征象,复查肾小球滤过率(glomerular filtration rate, GFR)较术前均无明显变化,1例随访第5年复发出现双肺转移瘤,给予靶向药物苹果酸舒尼替尼治疗。截至2018年10月,失访13例。
3 讨论达芬奇(Da Vinci)手术机器人是目前外科运用最广泛的手术机器人系统, 是外科微创技术新的里程碑。泌尿系统因其器官解剖位置较深,术野时常狭小,术中解剖分离和重建难度大,特别适合达芬奇手术机器人的应用。
机器人辅助肾部分切除术(robotic partial nephrectomy,RPN)目前主要有经腹腔和经后腹腔两种入路。经腹腔入路的优点主要在于腹腔内空间大,暴露更为清晰,对腹侧肿瘤的处理更直接,是机器人手术的传统入路。但腹腔内解剖相对复杂,尤其是对于背侧肿瘤,暴露相对困难,从而增加手术难度,同时,经腹腔手术对肠道等脏器有一定的干扰,增大了并发症的发生率[10-12]。为此,国内外学者尝试经后腹腔入路用于弥补和解决经腹腔入路的短板,在国内学者的探索下,经后腹腔入路术式已得到较大的改良和推广[13]。我科自2011年开展RPN以来,前期也以经腹腔入路为主,逐渐尝试并过渡至经后腹腔入路,通过实践发现:经后腹腔入路在手术操作、患者恢复等方面有一定的优势,故目前主要以经后腹腔入路操作为主。《欧洲泌尿外科指南》认为T1a期的肾肿瘤(长径≤4 cm)可行机器人手术治疗,但对于T1b期以上肾肿瘤(长径4~7 cm)未明确说明何种术式更优。我们在临床实践中将T1b期肾肿瘤一并纳入, 同时考虑到经后腹腔入路对于操作空间要求较高,患者体型可能影响手术操作,本研究根据不同的肿瘤分期(T1a和T1b)和BMI(<24 kg/m2和≥24 kg/m2)分别进行分析。结果表明:①T1a的肿瘤在手术时间、热缺血时间上较T1b的肿瘤有明显优势,原因为经后腹腔入路的操作空间为人工间隙,相对较小,当肿瘤较大时,后腹腔空间小导致操作受限的劣势得以凸显; ②BMI<24 kg/m2较BMI≥24 kg/m2的患者在手术时间上明显缩短,原因为BMI高的患者肾周脂肪囊可能较厚,分离去除需花费较多时间,在清除脂肪获得空间后,手术操作无特殊,因而其余指标无差异。在开展过程中我们的体会有:①经后腹腔入路相对于经腹腔入路在手术时间、热缺血时间、术后恢复上有一定优势[14]。国外研究表明热缺血时间每增加1 min都可能增加术后急性肾衰等肾功能损伤概率[15]。因此,减少肾脏热缺血时间尤为重要。上述优势原因为后腹腔入路解剖及毗邻相对简单,术中显露肾动脉较经腹腔入路更直接,且无需分离肾静脉,提高了手术的安全性,同时不受腹腔内既往病史的干扰,术后胃肠道恢复较快,禁食水时间短,术后引流管拔除时间早,缩短了平均住院时间,更符合快速康复外科手术的理念。对于右侧肾脏手术,还可以减少用于抬肝的辅助孔导致的创伤和耗材使用。②术前行CTU+CTA了解解剖位置,必要时行3D打印构建模型指导,术中也可行超声精确定位,对于复杂肿瘤如肾门处肿瘤尤其适用。③术中若出现损伤腹膜,可先游离破口周围组织,用Hem-o-lok夹闭破口,同时用气腹针排气。④对于肥胖(BMI>24 kg/m2)或肿瘤位于肾下极的患者仍会因较多脂肪遮挡而操作空间不足,所以我们在术中尽量更多地分离并离断脂肪,用组织粉碎器破碎后吸出,可获得较大的操作空间,增加操作便利。⑤对于靠腹侧等难暴露的肿瘤,充分游离肾周后,用数根纱条将肾腹侧垫高并调整,可以很好地暴露肿瘤。⑥经后腹腔入路中,T1a期肿瘤为良好的适应证; 对于T1b期肿瘤,虽然受后腹腔操作空间的局限,暴露难度增大,但此入路解剖较简单,熟练后也可弥补空间小带来的不足。我们的经验是机器人经后腹腔入路肾部分切除术需主刀10台作为学习曲线。
目前国内外肾肿瘤手术治疗相关报道中均提及在技术条件可行的情况下,机器人辅助腹腔镜肾部分切除术是一个重要的选择[16-18]。经过大量实际操作和长期的观察随访,我们认为经后腹腔入路机器人辅助肾部分切除术具有操作方便,肾动脉显露好,对腹腔脏器影响较小,术后康复快的特点。术者可依据患者具体情况和手术习惯进行选择,最大限度使患者受益。
| [1] | CHEN W, ZHENG R, BAADE P D, et al. Cancer statistics in China, 2015[J]. Ca Cancer J Clin, 2016, 66(2): 115–132. DOI:10.3322/caac.21338 |
| [2] | WINFIELD H N, DONOVAN J F, GODET A S, et al. Laparoscopic partial nephrectomy: initial case report for benign disease[J]. J Endourol, 1993, 7(6): 521–526. DOI:10.1089/end.1993.7.521 |
| [3] | GETTMAN M T, BLUTE M L, CHOW G K, et al. Robotic-assisted laparoscopic partial nephrectomy: technique and initial clinical experience with DaVinci robotic system[J]. Urology, 2004, 64(5): 914–918. DOI:10.1016/j.urology.2004.06.049 |
| [4] | PATTON M W, SALEVITZ D A, TYSON M D ND, et al. Robot-assisted partial nephrectomy for complex renal masses[J]. J Robot Surg, 2016, 10(1): 27–31. DOI:10.1007/s11701-015-0554-8 |
| [5] | CHOI J E, YOU J H, KIM D K, et al. Comparison of perioperative outcomes between robotic and laparoscopic partial nephrectomy: a systematic review and meta-analysis[J]. Eur Urol, 2015, 67(5): 891–901. DOI:10.1016/j.eururo.2014.12.028 |
| [6] | PAK J S, LEE J J, BILAL K, et al. Utilization trends and outcomes up to 3 months of open, laparoscopic, and robotic partial nephrectomy[J]. J Robot Surg, 2017, 11(2): 223–229. DOI:10.1007/s11701-016-0650-4 |
| [7] |
高宇, 张旭. 机器人肾部分切除术的应用现状和研究进展[J].
微创泌尿外科杂志, 2016, 5(1): 56–62.
GAO Y, ZHANG X. Current status and research progress of robotic partial nephrectomy[J]. J Minim Invas Urol, 2016, 5(1): 56–62. DOI:10.19558/j.cnki.10-1020/r.2016.01.016 |
| [8] | MIYAKE H, FURUKAWA J, HINATA N, et al. Significant impact of R.E.N.A.L. nephrometry score on changes in postoperative renal function early after robot-assisted partial nephrectomy[J]. Int J Clin Oncol, 2015, 20(3): 586–592. DOI:10.1007/s10147-014-0751-x |
| [9] | LUCIANI L G, CHIODINI S, DONNER D, et al. Early impact of robot-assisted partial nephrectomy on renal function as assessed by renal scintigraphy[J]. J Robot Surg, 2016, 10(2): 123–128. DOI:10.1007/s11701-016-0576-x |
| [10] | MIYAKE H, HINATA N, IMAI S, et al. Partial nephrectomy for hilar tumors: comparison of conventional open and robot-assisted approaches[J]. Int J Clin Oncol, 2015, 20(4): 808–813. DOI:10.1007/s10147-015-0783-x |
| [11] | GHANI K R, PORTER J, MENON M, et al. Robotic retroperitoneal partial nephrectomy: a step-by-stepguide[J]. BJU Int, 2014, 114(2): 311–313. DOI:10.1111/bju.12709 |
| [12] | GARISTO J, BERTOLO R, DAGENAIS J, et al. Robotic versus open partial nephrectomy for highly complex renal masses:comparisonof perioperative, functional, and oncological outcomes[J]. Urol Oncol, 2018, 36(10): 471.e1–471.e9. DOI:10.1016/j.urolonc.2018.06.012 |
| [13] |
李新涛, 张旭, 吕香君. 后腹腔入路机器人肾部分切除术:手术效果与技术现状[J].
微创泌尿外科杂志, 2016, 5(2): 124–128.
LI X T, ZHANG X, LYU X J. Robot-assisted retroperitoneal partial nephrectomy: summary on technical experience and operation efficacy[J]. J Minim Invas Urol, 2016, 5(2): 124–128. DOI:10.19558/j.cnki.10-1020/r.2016.02.018 |
| [14] |
吕香君, 张旭, 马鑫, 等. 经后腹腔入路机器人肾部分切除术手术经验和临床疗效总结(附单中心189例病例报道)[J].
微创泌尿外科杂志, 2016, 5(2): 65–68.
LYU X J, ZHANG X, MA X, et al. Clinical experience and efficacies of retroperitoneal robotic partial nephrectomy: a single center reports with 189 cases[J]. J Minim Invas Urol, 2016, 5(2): 65–68. DOI:10.19558/j.cnki.10-1020/r.2016.02.001 |
| [15] | THOMPSON R H, LANE B R, LOHSE C M, et al. Every minute counts when the renal hilum is clamped during partial nephrectomy[J]. Eur Urol, 2010, 58(3): 340–345. DOI:10.1016/j.eururo.2010.05.047 |
| [16] | MAURICE M J, KAOUK J H, RAMIREZ D, et al. Robotic partial nephrectomy for posterior tumors through a retroperitoneal approach offers decreased length of stay compared with the transperitoneal approach: a propensity-matched analysis[J]. J Endourol, 2017, 31(2): 158–162. DOI:10.1089/end.2016.0603 |
| [17] | SHIROKI R, FUKAMI N, FUKAYA K, et al. Robot-assisted partial nephrectomy: superiority over laparoscopic partial nephrectomy[J]. Int J Urol, 2016, 23(2): 122–131. DOI:10.1111/iju.13001 |
| [18] | LJUNGBERG B, BENSALAH K, CANFIELD S, et al. EAU guidelines on renal cell carcinoma: 2014 update[J]. Eur Urol, 2015, 67(5): 913–924. DOI:10.1016/j.eururo.2015.01.005 |



