2. 210000 南京,中国人民解放军第454医院胸外科
2. Department of Thoracic Surgery, No. 454 Hospital of PLA, Nanjing, Jiangsu Province, 210000, China
当今时代,战争冲突中大量爆炸性武器的使用,以及大规模使用简易爆炸装置(improvised explosive devices,IED)出现,使爆炸冲击伤的发生率大大增加。肺是冲击伤的重要致死性靶器官,受到冲击伤后极易发生急性肺损伤(acute lung injury,ALI),伤情变化快,常导致严重的后果,死亡率高[1]。大规模爆炸性武器的应用,常导致大量平民的爆炸伤,其中有很多伤亡者是儿童。至2006年伊拉克战争导致的死亡人数,超过了65万,其中儿童伤亡,占全部伤亡人数的15%以上[2]。
肺泡表面活性物质(pulmonary surfactant,PS)在维持肺功能中有着重要的作用,PS的质量变化是急性肺损伤的重要原因之一。PS由肺表面活性物质相关蛋白-A(SP-A)、B(SP-B)、C(SP-C)和D(SP-D)等组成,其中SP-B对于PS的功能和板层小体的形成都非常重要,其合成分泌不足或其发生变性失活时,会造成严重的呼吸功能障碍[3-4],尤其在新生儿会造成新生儿呼吸窘迫综合征(respiratory distress syndrome of newborn,NRDS)。
婴幼儿的肺等器官与成年肺在生物力学特点、损伤机制和伤后病理生理特征上均存在显著差异,特别婴幼儿的肺在SP的合成与代谢方面尚未完全成熟,对损伤的耐受和恢复有极大的影响[5]。过去研究大多数为成熟肺,而对未成熟肺与成熟肺之间的差异缺乏深入研究。本研究通过建立动物模型对未成熟肺与成熟肺重度冲击伤的病理生理特点及其SP-B变化进行研究,旨在探讨SP-B等功能及发育程度对损伤耐受和康复的影响及其机制,为肺冲击伤的救治提供依据。
1 材料与方法 1.1 实验动物与致伤设备 1.1.1 实验动物4周龄健康幼年新西兰白兔,雌雄不限,共40只为幼年兔组,体质量(442.10±55.30)g;24周龄成年新西兰白兔,雌雄不限,共40只为成年兔组,体质量(2018.15±145.80)g。
1.1.2 致伤设备采用陆军军医大学野战外科研究所研制的BST-I型生物激波管,采用闭口方式(加挡板)致伤,所有动物均以右侧朝向冲击波源。
1.2 动物致伤与分组 1.2.1 幼年兔组致伤参数激波管超压段的驱动压力为4.5 MPa,动物致伤处压力峰值为(384.32±10.87)kPa、正压作用时间为(624.15±45.03)ms[6]。
1.2.2 成年兔组致伤参数激波管超压段的驱动压力为4.0 MPa,动物致伤处压力峰值为(354.16±6.54)kPa、正压作用时间为(554.05±60.13)ms[6]。
1.2.3 分组幼兔和成年兔分别随机分为8组(各5只),在保证伤情一致情况下,分别于伤后即刻(0 h),2、4、6、12、24、48、72 h时间点用1.5%戊巴比妥钠溶液麻醉后,左心室穿刺取血检查血氧饱和度和血常规等,然后放血死亡后解剖。解剖观察记录各重要脏器大体病理情况,取一半的肺组织做支气管肺泡灌洗,另一半用于取肺组织取光镜病理、测肺组织测肺含水量。
1.3 观测指标及方法 1.3.1 动物一般情况观察及肺损伤程度评估观察记录动物致伤前后神志、发绀、口鼻分泌物、鼓膜情况、排便、排尿的情况及生存状况、心率、体温。记录肺脏组织大体损伤病理情况、出血面积占总面积的百分比、胸腔积血情况等病理特征;取左上肺叶区域的肺组织,用5%多聚甲醛溶液固定,做石蜡切片,行HE染色,进行光镜病理观察。采用2种方法对肺损伤程度进行评估:①依据脏器损伤分级的伤情评定方法对肺脏损伤严重程度进行评估,将肺损伤等级分为Ⅰ~Ⅵ级[7-9];②依据《简明损伤定级标准》[10]和肺出血程度和面积将肺损伤评分限定1~6分[4]。
1.3.2 支气管肺泡灌洗与肺泡灌洗液中SP-B含量测定 1.3.2.1 支气管肺泡灌洗用4 ℃的0.9%氯化钠注射液进行灌洗(成年兔1 mL,幼年兔0.5 mL),反复冲洗支气管肺泡5次,收集支气管肺泡灌洗液置于2 mL EP管中,记录回收的肺泡灌洗液的量,而后于-80 ℃冻存。
1.3.2.2 支气管肺泡灌洗液中SP-B含量检测采用ELISA法(兔肺表面活性物质相关蛋白B(SPTPB)酶联免疫试剂盒、武汉华美生物工程有限公司),将解冻后的支气管肺泡灌洗液于4 ℃采用高速离心机(1 000×g)离心15 min,取上层清液,按说明书应用双抗体夹心法测定标本中肺表面活性物质相关蛋白B(SP-B)水平。用酶标仪在450 nm波长下测定吸光度D(450)值,通过标准曲线计算样品中肺表面活性物质相关蛋白B(SP-B)浓度(ng/mL)。
1.3.3 肺含水率肺干湿比值测定:将去气管和支气管的肺组织称量,烤72 h后再称量,肺含水率=(肺湿重-肺干重)︰肺湿重×100%。
1.3.4 其他采集心尖动脉血后,将血样注入雅培血气分析片(3+),并用血气分析仪检测,选择能反映肺呼吸功能的血氧饱和度[11]作为代表性指标。其余血液1.5 mL装入紫色(EDTA)真空采血管后轻轻摇匀,进行血常规检测,选取能反映炎症程度的中性粒细胞百分比作为代表性指标。
1.4 统计学分析实验数据采用SPSS 19.0系统对资料进行统计学处理,计数资料采用χ2检验,计量资料采用配对和独立样本t检验。
2 结果 2.1 致伤后动物基本情况伤后72 h内所有动物未出现死亡;均出现短暂的精神萎靡、活动明显减少的情况,持续时间约30 min左右;未出现神志淡漠、发绀及血尿等情况;随后精神状态逐渐有所恢复。出现口鼻血性分泌物:幼年兔组6例(15%),成年兔组4例(10%);血便:幼年兔组5例(12.5%),成年兔组7例(17.25%);外耳道出血:幼年兔组5例(12.5%),成年兔组6例(15%)。
致伤后:幼年兔组心率迅速上升,于2 h左右达到最高峰之后逐渐下降至正常;成年兔心率迅速下降,在6 h左右达到最低后迅速上升,于12~24达到最高,而后又逐步下降至正常。两组体温变化趋势较一致,均迅速降低,于致伤后0.5~2.0 h达到最低,后逐步恢复正常,组间差异无统计学意义(P>0.05)。
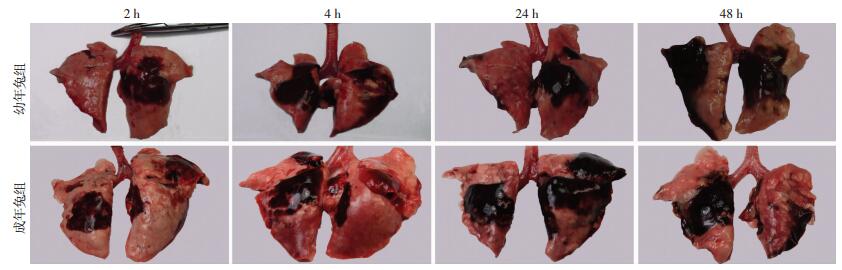
2.2 组织损伤大体解剖观察结果所有动物胸腔积血发生率为82.5%,未发现肝脏裂伤、腹腔出血及肋骨骨折的发生。伤后均出现不同程度的肺出血水肿,出血斑、块、点同时存在,部分出血波及整个肺叶;出血区域的组织切面呈红色实样变、有红色泡沫样液体溢出。肺出血表现为左肺较右肺重,下肺较上肺重,部分肺脏表现为中央较周围重。幼年组[(40.25±6.78)%]与成年组[(38.95±8.33)%]肺出血面积比较差异无统计学意义(P>0.05,图 1)。
|
| 图 1 幼、成年兔冲击伤后肺解剖大体观察结果 |
2.3 组织损伤病理特征
光镜下(图 2):两组兔肺组织损伤病理表现相似,有广泛的间质内出血和肺泡内出血,肺泡壁有断裂、破碎,肺间质及肺泡腔水肿、渗出、大量粒细胞浸润,肺泡毛细血管内红细胞淤滞、白细胞附壁,局部肺组织肺不张。幼年兔以肺泡壁的断裂和损伤更为明显,成年兔以肺泡及间质内出血及炎症细胞的浸润更为明显。

|
| ①肺大量出血、肺不张;②肺间质增厚;③肺泡内出血;④炎细胞浸润; A:幼年兔×40;B:成年兔×100;C:幼年兔×200;D:成年兔×200 图 2 不同放大倍数HE染色观察幼、成年兔冲击伤后肺组织病理改变 |
2.4 肺损伤程度评估
两组伤情较为一致,肺损伤程度间无明显差异(P>0.05)。幼年兔组肺脏器损伤严重程度分布为:Ⅲ级(中度损伤)3例、Ⅳ级(重度损伤)36例、Ⅴ级(极重度损伤)1例,Ⅳ级以上的损伤到92.5%。肺损伤的简明损伤评分(abbreviated injury scale,AIS)为(4.12± 0.74)分。成年兔组肺脏器损伤严重程度分级分布为:Ⅲ级4例、Ⅳ级34例、Ⅴ级2例;Ⅳ级以上的损伤占90%;AIS评分为(4.03±0.65)分。
2.5 肺泡灌洗液中SP-B含量在保证肺损伤伤情一致条件下,幼年组兔各时间点肺泡灌洗液中SP-B的浓度值均低于成年兔组,差异有统计学意义(P < 0.05,图 3)。

|
| a:P < 0.05,与成年兔组比较 图 3 两组兔冲击伤后各时间点肺泡灌洗液中SP-B含量变化(n=40,x±s) |
2.6 两组兔肺含水率及其他指标变化
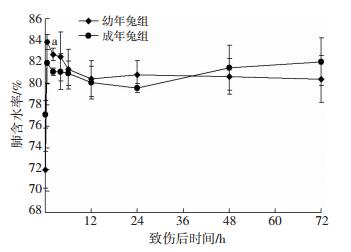
伤后2 h幼年组肺含水率高于成年组[(82.58±0.68)% vs(81.06±1.34%),P < 0.001],差异有统计学意义;其他各时间点差异无统计学意义(P>0.05);伤后幼年组兔肺含水率增高的速度较快,2~4 h左右达峰值,较成年组兔的峰值(伤后4~6 h)出现早(图 4)。
|
| a:P < 0.05,与成年兔组比较 图 4 两组兔冲击伤后各时间点肺含水率变化(n=40,x±s) |
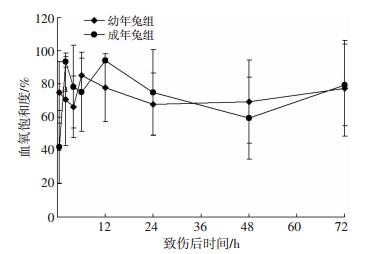
伤后0.5 h幼年兔组血氧饱和度显著高于成年兔组(P < 0.05),其他时相点两组差异无统计学意义(P>0.05)。幼年组血氧饱和度在伤后6~12 h恢复80%左右,成年组伤后4~6 h恢复80%左右(图 5)。
|
| a:P < 0.05,与成年兔组比较 图 5 两组兔冲击伤后各时间点血氧饱和度变化(n=40,x±s) |
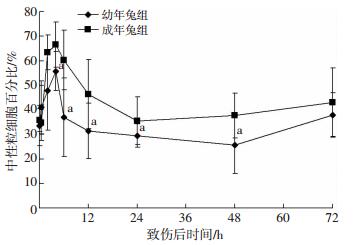
采用中性粒细胞百分比对炎症反应程度进行评估:两组兔中性粒细胞百分比均于致伤后4 h左右达到高峰,此后慢慢下降至基础水平(图 6)。幼年兔伤后4、6、12、24、48 h中性粒细胞百分比低于成年组(P < 0.05),其余时相点两组差异均无统计学意义(P>0.05)。
|
| a:P < 0.05,与成年兔组比较 图 6 两组兔冲击伤后各时间点中性粒细胞百分比变化(n=40,x±s) |
3 讨论
肺是冲击波作用的主要靶器官之一,其受损后主要表现为不同程度肺出血、肺水肿和气肿、炎细胞浸润等,有时可发生血性肺大泡和肺破裂[12]。婴幼儿的肺发育不完善,受冲击波损伤时其生物力学特点、损伤机制和伤后病理生理机制等与成年肺差异显著[4]。而目前对于冲击波所致幼年肺/未成熟肺损伤的关注较少。因此本研究在以往成熟肺冲击伤的基础上增加对未成熟肺冲击伤的探索,以幼、成年兔肺模拟未成熟和成熟肺,探讨重度肺冲击伤后肺泡灌洗液中SP-B变化与意义,同时比较未成熟和成熟肺冲击伤后的各指标变化特点。
为了保证所有家兔伤情的稳定性和一致性,使本研究肺冲击伤相关特点具有可比性,本实验构建在不同压力强度的冲击波致伤下伤情一致的动物模型[6]。根据两组动物重度肺冲击伤AIS评分、并发症的发生率和总体肺出血面积等均无明显差异,可以推测两组肺脏所受冲击波致伤后的损伤程度相当一致,因此可进行成年兔与幼年兔冲击伤疾病变化特点的比较。
SP-B是由肺泡Ⅱ型细胞合成并分泌到肺泡表面的同型二聚体,其中64~79 bp序列在降低肺泡表面张力、提高肺的顺应性方面有至关重要的作用,能促进气-液表面磷脂的吸附,参与管状髓磷脂的形成,也具备抗菌和保护肺免受肺损伤[13-14]。SP-B缺乏是导致急性呼吸窘迫综合征(ARDS)的重要因素,会导致急性呼吸衰竭[14],而冲击波造成的肺损伤属于急性肺损伤中的一种,因此研究SP-B含量对PS活性情况变化进行评估、探索肺功能恢复等具有重大意义。本研究中幼年兔组SP-B在伤后每一相同时间点上的含量明显低于成年兔组,且于致伤后迅速降低在4~6 h左右达到最低,伤后72 h仍未能恢复至正常水平,这可能是由于幼年兔肺脏发育未完全,PS活性、合成和分泌功能均较成年兔差,因此同等程度致伤条件下,其含量迅速降低,而成年兔组SP-B含量在致伤后0.5~2 h之间有一个较小的稳定期,这可能是由于机体自身的保护作用暂时维持一定稳态,致伤后2 h各种炎症反应开始发生故SP-B含量也开始减少,但减少幅度小于幼年兔组,后期恢复较快,于48~72 h疾病恢复正常水平。虽然成年兔受伤后炎症反应较强,也会影响PS的合成、分泌及其活性,但其恢复情况仍较幼年兔更快,肺功能的恢复也相对较快。因此,对于PS合成和分泌不足的未成熟肺,致伤后若能及时接受治疗并有效提高PS的恢复速度将可能会有助于肺呼吸功能改善,减少并发症、改善预后。
虽然成年兔组炎症反应更重,肺水肿更持久,但作为评价呼吸功能的血氧饱和度仍较幼年兔组恢复较快。幼年兔肺含水率在致伤后与2~4 h达到高峰,后逐渐恢复正常,成年兔于至伤后4~6 h肺含水率达到最高,后逐渐降低至正常,说明幼年兔未成熟肺伤后出血以及发生炎症反应的速度要快于成年兔成熟肺。幼年兔组中性粒细胞百分比在2~4 h达到高峰,而后迅速下降,而成年兔组于4~6 h达到高峰,之后缓慢降至正常,且峰值明显高于幼年兔组。因此,未成熟肺炎症反应较成熟肺轻,且持续时间较短。幼年兔肺组织较薄且发育不完全,在遇到冲击波后和成年兔相同伤情条件下更容易发生损伤、出血水肿等,因此冲击波致伤后肺水水肿程度较成年兔组高,但因其炎症反应较轻,所以恢复较成年兔组更快。
综上所述,在相同程度的重度肺冲击伤模型中,幼年兔未成熟肺与成年兔成熟肺相比肺水肿恢复较快、炎症反应较轻;但SP-B含量较低、合成和分泌功能恢复较慢,可能导致其呼吸功能恢复较慢,因此在临床救治冲击伤等原因所致的急性肺损伤时可以考虑增加SP-B含量来促进呼吸功能的恢复,从而用以指导不同成熟度肺损伤的临床救治。
志谢 感谢陆军特色医学中心生物激波管助理实验师廖志康、向洪义协助课题组开展动物致伤实验,感谢检验中心实验员胡波等在血常规等检查方面提供帮助| [1] |
胡泉, 柴家科, 杨红明. 烧冲复合伤肺损伤的研究进展[J].
解放军医学杂志, 2013, 38(5): 428–432.
HU Q, CAI J K, YANG H M. Research progress on burn-blast lung injury[J]. Med J Chin PLA, 2013, 38(5): 428–432. |
| [2] | BURNHAM G, LAFTA R, DOOCY S, et al. Mortality after the 2003 invasion of Iraq: a cross-sectional cluster sample survey[J]. Lancet, 2006, 368(9545): 1421–1428. DOI:10.1016/s0140-6736(06)69491-9 |
| [3] | OLMEDA B, GARCLA-ÁLVARE B, GÓMEZ M J, et al. A model for the structure and mechanism of action of pulmonary surfactant protein B[J]. Faseb J, 2015, 29(10). DOI:10.1096/fj.15-27345 |
| [4] |
闫亚敏, 王志红, 卢健. 肺表面活性蛋白B(SP-B)在肺损伤中的研究进展[J].
临床肺科杂志, 2010, 15(6): 849–851.
YAN Y M, WANG Z H, LU J. Progress in research of pulmonary surfactant protein B (SP-B) in lung injury[J]. J Clin Pulm Med, 2010, 15(6): 849–851. DOI:10.3969/j.issn.1009-6663.2010.06.051 |
| [5] | REUTER S, MOSER C, BAACK M. Respiratory distress in the newborn[J]. Pediatr Rev, 2014, 35(10): 417–429. DOI:10.1542/pir.35-10-417 |
| [6] |
梁毅, 代维, 麻超, 等. 幼兔重度肺冲击伤动物模型的建立[J].
局解手术学杂志, 2016, 25(5): 318–322.
LIANG Y, DAI W, MA C, et al. Establishment of animal model of severe lung injury in young rabbits[J]. J Region Anat Oper Surg, 2016, 25(5): 318–322. DOI:10.11659/jjssx.03E016015 |
| [7] | MOORE E E, MALANGONI M A, COGBILL T H, et al. Organ injury scaling.Ⅳ: Thoracic vascular, lung, cardiac, and diaphragm[J]. J Trauma, 1994, 36(3): 299–300. DOI:10.1097/00005373-199403000-00002 |
| [8] |
梁毅, 邱俊, 袁丹凤, 等. 脏器损伤分级及应用评价[J].
伤害医学(电子版), 2015, 4(3): 44–47.
LIANG Y, QIU J, YUAN D F, et al. Organ damage classification and application evaluation[J]. Injury Med (Electr Ver), 2015, 4(3): 44–47. |
| [9] |
孙海晨, 朱佩芳. 脏器损伤分级[J].
中华创伤杂志, 1998, 14(3): 143–147.
SUN H C, ZHU P F. Organ damage classification[J]. Chin J Trauma, 1998, 14(3): 143–147. DOI:10.3760/j:issn:1001-8050.1998.03.006 |
| [10] |
周继红, 刘宝华, 许明辉, 等. 创伤评分学[M]. 北京: 科学出版社, 2018: 88-92.
ZHOU J H, LIU B H, XU M H, et al. Trauma Scoreology[M]. Beijing: Science Press, 2018: 88-92. |
| [11] |
钱桂生. 急性肺损伤和急性呼吸窘迫综合征研究现状与展望[J].
解放军医学杂志, 2003, 28(2): 97–101.
QIAN G S. The status quo and pospect of acute lung injury and acute respiratory distress syndrome[J]. Med J Chin PLA, 2003, 28(2): 97–101. DOI:10.3321/j.issn:0577-7402.2003.02.001 |
| [12] |
黄跃生, 粟永萍, 周继红. 中华战创伤学(第8卷):特殊致伤原因战创伤[M]. 郑州: 郑州大学出版社, 2016: 88-89.
HUANG Y S, SU Y P, ZHOU J H. Chinese War Traumatology (Volume Eight)[M]. Zhengzhou: Zhengzhou University Press, 2016: 88-89. |
| [13] | MAZELA J, MERRITT TA, GADZINOWSKI J, et al. Evolution of pulmonary surfactants for the treatment of neonatal respiratory distress syndrome and pediatric lung diseases[J]. Acta Pediatrica, 2006, 95(9): 1036–1048. DOI:10.1080/08035250600615168 |
| [14] |
王鹏, 王万能, 吕婧, 等. 疏水性肺表面活性蛋白SP-B结构类似物的研究进展[J].
华西药学杂志, 2013(6): 636–639.
WANG P, WANG W L, LYU J, et al. Progress in the study of hydrophobic pulmonary surfactant protein SP-B structural analogues[J]. West China J Pharm Sci, 2013(6): 636–639. DOI:10.13375/j.cnki.wcjps.2013.06.039 |



