痛风是一种原发或继发性因素导致的体内嘌呤代谢紊乱而引起的一组慢性代谢性疾病,其主要临床表现为有或无症状的高尿酸血症[1],其典型发作症状则为预先无明显征兆而反复出现的痛风性关节炎、痛风肾及痛风石等[2-3]。由于长期的高尿酸水平,机体内尿酸盐结晶可沉积于关节液、关节滑膜和骨关节等处,继而引发关节肿胀、疼痛[4]。慢性痛风病导致尿酸盐结晶沉积[5],进而形成痛风石[6]。痛风石是痛风的特征性病变[7]。
目前临床上对于痛风石的治疗主要以保守治疗[8]或者手术治疗为主,但由于人体高尿酸血症的反复性,上述手段均难以彻底清除尿酸石;且对于高尿酸血症的患者,大部分存在血管循环系统的亚损害,机体术后抗感染能力及愈合能力相对健康人群较低,不利于术后恢复。超声治疗可提高静脉溃疡等疾病的愈合率[9]。而超声清创联合负压吸引术能通过超声波的空化作用使清创更彻底,同时,通过热效应使伤口组织温度升高,改善血液循环,促进组织修复。
因此,我们采取超声清创联合负压吸引治疗痛风石破溃创面,并与常规清创换药进行临床疗效的随机对照观察研究,探讨此种方法治疗痛风石创面的临床疗效及安全性。以期寻找及掌握一种较为有效、安全、快捷的新的治疗方法。
1 对象与方法 1.1 临床资料该研究经我院伦理委员会批准(2016年[技]002),选择2014年9月至2017年12月我院内分泌科住院的痛风合并痛风石破溃的患者96例,分别记录患者的年龄、性别、血常规、CRP、肝功、血肌酐、尿酸、尿素氮、伤口分泌物培养结果。依据就诊顺序采用随机数字表法将患者分为试验组和对照组(n=48),试验组年龄(51.3±7.6)岁,病程(6.8±1.1)年,BMI(25.7± 1.2),破溃创面面积(1.62±0.23)cm2。对照组年龄(52.4±6.9)岁,病程(6.5±1.3)年,BMI(26.1±1.4),破溃创面平均面积(1.65±0.21)cm2,两组患者在性别、年龄、病程、BMI指数及痛风石破溃面积上均未见显著差异,具有可比性(P>0.05)。
1.2 纳入标准① 所有入选患者均参照2012年美国风湿病协会痛风性关节炎的诊断标准;②所有患者既往均确诊有高尿酸血症,且尿酸值检测结果>480 μmol/L,病程>5年;③影像学检查结合临床查体可发现患者骨关节有痛风石,且所有患者患处分泌物试验室检查细菌培养阳性;④患者的临床表现主要为单发性的痛风石破溃伴感染,关节红肿、疼痛、活动受限等症状,具有明确的治疗适应证。
1.3 排除标准① 合并严重的感染、坏疽,心脑血管疾病、肝肾功能障碍的患者;②合并血液系统疾病、精神性疾病的患者,及对疗效有干扰的基础性疾病患者,如糖尿病、动脉炎及血管闭塞等;③多发性痛风石表皮破溃患者。
1.4 治疗方法对两组患者均进行系统的内科基础治疗,包括低嘌呤饮食、戒烟酒、全身营养状况、改善微循环,预防创面感染加重和(或)播撒。根据伤口分泌物细菌培养结果及全身情况选取敏感抗生素静脉输注,剂量选择为中度感染剂量(具体根据使用抗生素而定),每7天为一个疗程,治疗2~4个疗程。同时使用前列地尔10 μg/d,静脉输注,每7天为一个疗程,治疗2~4个疗程。
1.4.1 试验组① 超声清创机(USI超声清创机,北京速迈医疗科技有限公司,山东创康生物科技有限公司)的使用:先对较大块的坏死组织进行剪除,再以0.9%氯化钠液作为超声载体,参数设置为50 kHz频率,70~106 kPa压强,喷射出水流冲洗创面,清创范围应达到溃烂病灶周围半径2 cm。②负压吸引装置的使用(ZN100智能创伤负压综合治疗仪):按照创面的大小和形状修剪敷料[聚乙醇(PVF)医用海绵,北京英佳麦迪克医用材料有限公司],使其恰好能充填破溃腔体或覆盖于破溃口,然后将泡沫材料上的2根硅胶管从创口引出,将破溃灶周围消毒后,以一次性透明贴膜封闭创面及其周围半径3 cm内的正常皮肤,引出的硅胶管连接负压装置,作为引流管道。负压吸引术每个疗程治疗时间为3~7 d,治疗慢性创面一般需(6±2)个疗程。
1.4.2 对照组0.9%氯化钠液冲洗创面,冲出或挤出痛风石或结晶,待肉眼确定清除干净后使用双氧水、0.9%氯化钠液冲洗破溃腔体,去除坏死软组织,再消毒,以无菌纱布覆盖患处,每日换药,以5 d为1个疗程。
1.5 观察指标数码相机垂直于破溃面,对治疗前后的患处进行拍照,采用图像处理软件Image计算面积大小,分析治疗前后患处面积变化。创面愈合率=创面上皮覆盖面积/初始创面面积。根据创面愈合率判定治疗效果:展开治疗30天内创面愈合95%以上为治愈;展开治疗30天后,创面愈合面积高于80%(包含80%)为显效;创面愈合面积介于50%到80%(包含50%)之间为有效,创面愈合面积低于50%则为无效。总有效率包括愈合率、显效率和有效率;记录两组治疗前及治疗后10天患处的视觉模拟疼痛评分(VAS)情况,并记录两组治疗终结时的住院费用;观察患者治疗结束后30天内全身及局部并发症(关节畸形、延迟愈合、术口疼痛等)发生情况。
1.6 统计学方法数据分析采用SPSS 22.0软件;计数资料以频数和百分比表示,对于非正态分布数据,采用Mann-Whitney U检验进行组间差异比较,若为正常分布数据,则采用χ2检验进行比较;计量资料采用x±s对各时间点的伤口愈合情况进行统计,在满足正态性结果的条件下,采用独立样本t检验对各个时间点上的疗效差异进行分析,否则采用Mann-Whitney U检验进行分析;另外,采用两组间重复测量的方差分析,对治疗效果与时间的交互效应进行分析。所有分析方法检验水平为α=0.05。
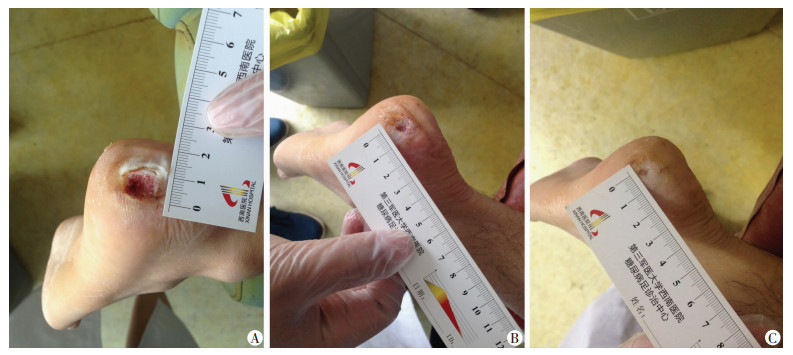
2 结果 2.1 两组创面愈合率比较通过试验观察,超声清创联合负压吸引治疗痛风石破溃创面疗效优于普通常规换药。如典型病例所示(图 1):患者治疗后第5、10天与治疗前的创面比较明显缩小,达到治愈标准。各时间差异性分析结果显示,除第25天外,其余时间点的试验组与对照组之间的平均创面愈合率都存在统计学差异(P<0.05,图 2)。经重复测量的时间×组别交互作用分析显示,两组不同治疗方式之间存在显著差异(F=48.813,P<0.05);不同分组的测量时间有显著差异(F=25.666,P<0.05);治疗方式与测量时间存在交互效应(F=1.523,P<0.05)。
|
| A:治疗前;B:治疗第5天;C:治疗后第10天 图 1 典型痛风石破溃病例治疗前后比较 |

|
| a:P<0.05,与常规清创(对照)组比较 图 2 两组痛风石破溃创面愈合率各时间差异性分析(n=48,x±s) |
2.2 治疗效果
试验组第5天总有效率为87.5%,明显高于对照组的48.34%,有统计学意义(Z=-2.570,P<0.05);试验组10 d总有效率为89.58%,明显高于对照组的66.67%,有统计学意义(Z=-2.126,P<0.05);试验组15 d总有效率为93.75%,明显高于对照组的77.08%,有统计学意义(Z=-2.255,P<0.05);试验组20 d总有效率为95.84%,明显高于对照组的77.069%,有统计学意义(Z=-2.241,P<0.05);试验组25 d总有效率为93.75%,明显高于对照组的81.24%,有统计学意义(Z=-2.348,P<0.05);试验组30 d总有效率为95.83%,明显高于对照组的81.25%,有统计学意义(Z=-2.757,P<0.05)。试验组随访第5天的显效率和第10、15、20、25、30天的治愈率与对照组比较有显著差异(P<0.05),见表 1。
| 随访时间 | 组别 | 治愈 | 显效 | 有效 | 无效 | Z | P |
| 5 d | 试验组 | 3(6.25) | 25(52.08) | 14(29.17) | 6(12.50) | -2.570 | 0.010 |
| 对照组 | 2(4.17) | 17(25.42) | 9(18.75) | 20(41.67) | |||
| 10 d | 试验组 | 8(16.67) | 25(52.08) | 10(20.83) | 5(10.42) | -2.126 | 0.033 |
| 对照组 | 5(10.42) | 20(41.67) | 7(14.58) | 16(33.33) | |||
| 15 d | 试验组 | 13(27.08) | 27(56.25) | 5(10.42) | 3(6.25) | -2.255 | 0.024 |
| 对照组 | 7(14.58) | 25(52.08) | 5(10.42) | 11(22.92) | |||
| 20 d | 试验组 | 17(35.42) | 24(50.00) | 5(10.42) | 2(4.17) | -2.241 | 0.025 |
| 对照组 | 11(22.92) | 21(43.75) | 5(10.42) | 11(22.92) | |||
| 25 d | 试验组 | 25(52.08) | 14(29.17) | 6(12.50) | 3(6.25) | -2.348 | 0.019 |
| 对照组 | 13(27.08) | 22(45.83) | 4(8.33) | 9(18.75) | |||
| 30 d | 试验组 | 33(68.75) | 9(18.75) | 4(8.33) | 2(4.17) | -2.757 | 0.006 |
| 对照组 | 20(41.67) | 15(31.25) | 4(8.33) | 9(18.75) |
2.3 患者患处疼痛及住院费用对比
试验组与对照组治疗前VAS评分比较,差异无统计学意义[(3.60±0.70)分vs(3.50±0.50)分,P>0.05],治疗10天后两组VAS评分均显著低于治疗前,且试验组(1.60±0.60)VAS评分低于对照组(2.20±0.60),差异有统计学意义(P<0.05);两组患者均治疗终结,两组住院费用对比,差异无统计学意义[(36 872.70±4 912.50)元vs(34 965.90±4 588.90)元,P>0.05]。
2.4 两组治疗后并发症比较两组患者治疗后30天内均未见全身不良反应,试验组超声清创过程中,2例感觉局部疼痛需要注射或创面喷施镇痛药物止痛,不良反应发生率4.2%;对照组治疗中有3例出现延迟愈合,不良反应发生率6.3%,两组不良反应发生率比较,差异无统计学意义(χ2=0.00,P>0.05)。
3 讨论痛风是以高尿酸血症为首要表现的代谢紊乱性疾病[10]。由于机体嘌呤代谢的障碍,导致体内长期持续性的尿酸水平升高,使机体的尿酸盐在关节囊、肌腱等部位形成结晶并沉积,导致发生无菌性炎症,由于关节腔内滑膜受累,致使关节出现红、肿、热、痛等炎性表现[10]。尿酸盐结晶可刺激产生慢性异物反应,其周围被上皮细胞、巨核细胞所包围,有时还有分叶核细胞的浸润,形成异物结节,即所谓痛风石[11]。临床上痛风石具有不完全孤立,无完整包膜,呈泥沙状沉积附着,侵及范围广,随着尿酸水平波动而反复形成等特点[12],由于尿酸盐结晶逐渐增多,关节腔内痛风石由小变大,腔内压增高,常常会使局部皮肤膨胀、张力变高且表皮被撑薄,加上尿酸盐结晶本身具有侵蚀性,而致使关节腔周围皮肤抗损害能力下降,抗牵拉的顺应性也降低,一旦因摩擦、受压、受冻以及创伤等原因可发生溃烂[13]。当破溃处皮肤结构和营养均遭到破坏时,由于高尿酸血症患者血液循环差,细胞再生力弱,血管长期处于慢性损害状态等因素,后期可导致细菌在破溃处滋生,引发痛风性细菌感染性关节炎,且极难自行愈合。严重者可引起脓毒血症,导致死亡[14]。
超声清创联合负压吸引是一种新的被应用于创口处理的治疗方式,已广泛在糖尿病足的治疗中显示出其优越性,但关于这两种技术在痛风石破溃创面的应用报道尚少[15]。负压吸引的核心技术为负压引流和创面封闭。在创面封闭方面,本组研究通过在覆盖局部创面后以半透膜进行相关创面封闭,从而隔绝细菌接触途径,制造相对密闭环境而减少二次感染的机会,并且保持低张力的封闭还能在一定程度上减少患者的痛苦,防止伤口表皮的挛缩,减少医务工作者工作量,减少医疗成本、缩短住院时间[16]。在负压吸引方面,本组研究中持续性的负压吸引有利于创面引流,可及时彻底清除创面坏死组织及渗液,减少细菌数量,去除细菌的存活环境,阻止细菌向深部组织侵袭[17],显著增加了痛风石患处的清创效果,促进了创面的恢复,另外负压吸引还可增加创面周围组织毛细血管血液流量,改善微循环,为患处提供充足血供的同时利于肉芽组织的形成,促进伤口愈合[18]。
本研究中,试验组痛风石破溃创面疗效优于普通常规换药。试验组第5天的显效率和第10、15、20、25、30天的治愈率均高于对照组,同时未出现全身不良反应,说明超声清创联合负压治疗痛风石破溃创面具有较好的治疗效果,其负压吸引时,持续负压状态刺激毛细血管再生,从而促进肉芽组织生长改善病灶部位微循环;且超声清创机通过空化、乳化作用,去除创面表面和深层的细菌和真菌,加上负压吸引技术,创面与外界分隔,防止细菌侵入。相对于传统的每日消毒、换药、物理性阻隔等手段,这均能更加有利于创面的愈合,减轻患者痛苦,降低感染率,甚至是病情恶化后截肢的概率,其在并不增加不良反应发生率及总得住院费用的前提下,相对于传统痛风石破溃创面的治疗中具有明显的优势。因此,本研究认为,超声清创联合负压吸引治疗痛风石破溃创面具有较好的治疗效果,能够改善患处的血供,改进微循环状态,促进愈合,预防及清除细菌感染等,有利于痛风石创面患者的局部功能恢复,减轻患者痛苦,降低感染率和截肢率,且不增加不良反应发生率及总住院费用,值得推广应用。
| [1] | HUI M, CARR A, CAMERON S, et al. The british society for rheumatology guideline for the management of gout[J]. Rheumatology (Oxford), 2017, 56(7): e1–e20. DOI:10.1093/rheumatology/kex156 |
| [2] | DABETH N, MERRMAN T R, STAMP L K. Gout[J]. Lancet, 2016, 388(10055): 2039–2052. DOI:10.1016/S0140-6736(16)00.46-9 |
| [3] | PEREZ-RUIZ F, CASTILLO E, CHINCHILLA S P, et al. Clinical manifestations and diagnosis of gout[J]. Rheum Dis Clin North Am, 2014, 40(2): 193–206. DOI:10.1016/j.rdc.2014.01.003 |
| [4] | Richette P, Bardin T. Gout[J]. Lancet, 2010, 375(9711): 318–28. DOI:10.1016/S0140-6736(09)60883-7 |
| [5] | PASCUAL E, ADDADI L, ANDRES M, et al. Mechanisms of crystal formation in gout-a structural approach[J]. Nat Rev Rheumatol, 2015, 11(12): 725–30. DOI:10.1038/nrrheum.2015.125 |
| [6] | HARRIS R P, MCLEAN R M, QASEEM A. Management of acute and recurrent Gout[J]. Ann Intern Med, 2017, 166(10): 760. DOI:10.7326/L17-0146 |
| [7] | DALBETH N, POOL B, GAMBLE G D, et al. Cellular characterization of the gouty tophus: a quantitative analysis[J]. Arthritis Rheum, 2010, 62(5): 1549–56. DOI:10.1002/art.27356 |
| [8] | KHANNA D, FITZGERALD J D, KHANNA P P, et al. 2012 American College of Rheumatology guidelines for management of gout. Part 1: systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia[J]. Arthritis Care Res (Hoboken), 2012, 64(10): 1431–46. DOI:10.1002/acr.21772 |
| [9] | MADHOK B M, VOWDEN K, VOWDEN P. New techniques for wound debridement[J]. Int Wound J, 2013, 10(3): 247–51. DOI:10.1111/iwj.2013.10.issue-3 |
| [10] | WONG W D, SHAH S, MURRAY N, et al. Advanced Musculoskeletal Applications of Dual-Energy Computed Tomography[J]. Radiol Clin North Am, 2018, 56(4): 587–600. DOI:10.1016/j.rcl.2018.03.003 |
| [11] | BOSSART S, SIDLER D, BLUM R, et al. Gout tophi on the soles resembling viral warts[J]. Clin Case Rep, 2018, 6(6): 1121–1123. DOI:10.1002/ccr3.1539 |
| [12] | CHHANA A, DALBETH N. The gouty tophus: a review[J]. Curr Rheumatol Rep, 2015, 17(3): 19. DOI:10.1007/s11926-014-0492-x |
| [13] | XU J, ZHU Z, ZHANG W. Clinical characteristics of infectious ulceration over tophi in patients with gout[J]. J Int Med Res, 2018, 46(6): 2258–2264. DOI:10.1177/0300060518761303 |
| [14] | XU J, LIN C, ZHANG P, et al. Risk factors for ulceration over tophi in patients with gout[J]. Int Wound J, 2017, 14(4): 704–707. DOI:10.1111/iwj.12680 |
| [15] | HAN L Y, FU M X, HUANG Y L, et al. Application of ultrasonic debridement machine combined by vacuum aspirationon diabetic foot[J]. Mod Prev Med, 2012, 39(21): 5713–5714. |
| [16] |
何敏, 郑焱玲, 邓武权, 等. 超声清创刀联合负压创面系统治疗糖尿病足溃疡的疗效观察[J].
局解手术学杂志, 2015, 24(1): 1–3.
HE M, ZHENG Y L, DENG W Q, et al. Clinical observation on treatment effect of negative pressure wound therapy followed by ultrasonic debridement surgical system in patients with diabetic foot[J]. J Region Anat Oper Surg, 2015, 24(1): 1–3. |
| [17] |
施劭锋, 苏广瑞, 林日昌, 等. 超声清创术联合简易负压封闭引流技术在糖尿病足溃疡中的应用[J].
白求恩医学杂志, 2016, 14(2): 186–188.
SHI S F, SU G R, LIN R C, et al. Application of drainage technology in diabetic foot ulcers in the ultrasonic debridement Joint Improvised vacuum sealing[J]. J Bethune Med Sci, 2016, 14(2): 186–188. DOI:10.16485/j.issn.2095-7858.2016.02.024 |
| [18] |
陈伟彬, 聂运修, 等. 超声清创术联合负压封闭引流技术治疗糖尿病足溃疡效果分析[J].
白求恩医学杂志, 2017, 15(2): 243–244.
CHEN W B, NIE Y X. Analysis of the effect of ultrasonic debridement combined with vacuum sealing drainage on diabetic foot ulcer[J]. J Bethune Med Sci, 2017, 15(2): 243–244. DOI:10.16485/j.issn.2095-7858.2017.02.054 |



