门静脉血栓(portal vein thrombosis, PVT)形成是发生在门静脉系统, 包括门静脉主干及分支、肠系膜上下静脉和脾静脉的深部血管阻塞性疾病。PVT起病隐匿, 可表现为门脉压力进行性升高, 导致曲张静脉破裂出血的风险增加和顽固性胸腹水的发生, 当血栓延伸到肠系膜静脉分支时, 可以出现高热、持续性腹部绞痛、腹泻及随后的肠缺血性梗死。肝硬化患者PVT的患病率文献[1-6]报道在0.6%~16%之间, 并随肝硬化严重程度的增加而升高。肝硬化合并有PVT患者的临床表现有更加严重的倾向[7-8], 而且影响肝硬化脾切除患者的预后[9]。PVT的发生增加了将来肝移植的难度[10-13], 并影响移植后的预后[14]。肝硬化合并严重的PVT治疗选择, 目前存在极大的争论, 常规的抗凝治疗往往对慢性血栓效果欠佳, 而TIPS用于该类疾病的治疗已经彰显出特有的优势, 特别在食管、胃曲张静脉破裂出血的二级预防上, 较经典的内镜下套扎+口服普奈洛尔治疗患者更加受益[15]。同时, TIPS能重塑门静脉系统, 使其通畅性增加, 降低门静脉压力, 使门静脉高压导致的症候群均得到缓解, 但在严重门静脉系统血栓, 特别是完全性门静脉血栓、门静脉海绵样改变、血栓纤维化的患者, TIPS实施是困难的, 而且面临腹腔大出血等致命性风险。在既往的研究中, 主要集中关注门静脉主干血栓, 较少关注合并有门静脉左、右支、肠系膜静脉栓塞。同时TIPS能否使肝硬化合并门静脉血栓的患者生存受益仍是一个等待回答的问题。虽然有学者认为其并不能使该类患者生存获益[15], 但仍需要不断扩大病例, 以求获得更可靠的结论。本研究, 我们尝试回答了TIPS用于肝硬化合并严重门静脉血栓的短期及长期疗效, 报告如下。
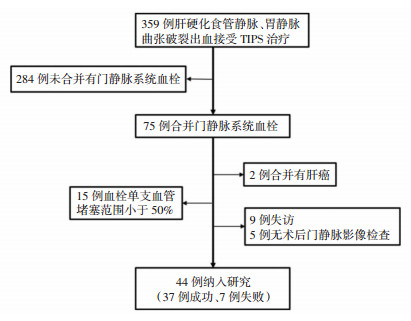
1 资料与方法 1.1 一般资料收集2013年1月至2017年10月本科住院明确诊断为肝硬化食管、胃静脉曲张破裂出血且接受TIPS治疗的患者共359例, 所有患者于术前签订《TIPS同意书》, 充分告知其利弊(TIPS该项技术于2012年7月通过医院准入, 同意开展)。该组患者TIPS的适应证为:①肝硬化食管、胃静脉曲张破裂出血; ②顽固性胸腹水。其禁忌证为:①严重肝功能异常, Chlid评分>13分; ②严重右心衰和(或)肺动脉高压; ③胆管重度扩张; ④多囊肝; ⑤合并有肝癌; ⑥全身或者肝内感染未得到控制; ⑦全身衰竭, 一般情况差。359例患者均行腹部增强CT检查, CT扫描可见管腔狭窄、充盈缺损或者完全闭塞。慢性门静脉阻塞后, 可发现海明样改变, 表现为多发迂曲的侧枝形成, 血栓可出现条索样改变, 有时可看到钙化灶。增强CT扫描可见横断面上明确划分出血管堵塞程度, 我们分为4级, Ⅰ级<25%, Ⅱ级25% ~50%, Ⅲ级51% ~75%, Ⅳ级76% ~100%[16]。由于<50%对于血流无明显影响[17], 故本研究只关注大于50%的患者, 所有影像学指标由两位有丰富经验的医师独立测得, 再对比其差异, 如果数值相同就采用, 如果不相同就共同商议后, 再次测量得出结果, 保证了测量数值的可靠性。共发现有PVT者75例, 31例被排除在外, 其中因为血栓单支血管堵塞范围小于50%(n=15), 或者合并有肝癌(n=2), 术后随访无门静脉系统影像学检查(n=5), 失访(n=9), 最后44例患者纳入该研究中(图 1)。44例患者中, 年龄(55.77±18.60)岁, 身高(164.16±6.60)cm, 体质量(60.53±6.32)kg, 病毒感染性肝硬化26例, 非病毒感染18例。
|
| 图 1 纳入流程图 |
1.2 TIPS治疗策略
根据血栓的栓塞程度和堵塞部位采取不同的治疗策略。术中先做间接门静脉造影了解门静脉主干及左、右支的通畅程度, 再结合CT图像评估在决定手术方式。主要有以下几种治疗策略:①当左、右支无血栓或者血栓尚未完全堵塞, 有穿刺成功可能性时, 我们尝试常规的TIPS。②当门静脉左、右支均完全堵塞, 通过CT等图像判断血栓的硬度, 如果血栓质地较软尚, 可经皮肝穿, 穿刺中左支或者右支(有学者从脾静脉入路探查)[17], 通过导丝探查进入门静脉主干, 则引导球囊扩张成型后, 再行TIPS (图 2)。③若左、右完全堵塞且无法通过经皮肝穿, 球囊成型, 而门静脉主干尚通畅, 则行门静脉主干与肝静脉“支架搭桥术”(图 3)。④如果门静脉主干及左、右完全堵塞, 且无法开通, 同时存在巨大的侧枝血管, 可以尝试肝静脉与该侧枝建立支架链接。所有患者均采用直径8 mm覆膜支架(2016年前用Fluency, Bard Peripheral Vascular, Tempe, Arizona, USA; 2017年开始用Viatorr; W.L. Gore & Associates, Flagstaff, Arizona, USA)。
|
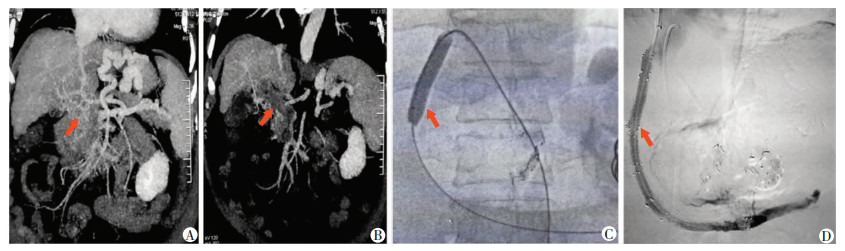
| A、B:术前CT扫描见门静脉主干完全堵塞、肠系膜上静脉部分堵塞(红色箭头); C:术中超声引导下经皮肝脏穿刺门静脉左支, 做球囊扩张后再行TIPS(红色箭头); D:术后见支架覆盖血栓, 门静脉系统重塑成功, 引流通畅(红色箭头) 图 2 完全门静脉堵塞患者TIPS开通过程 |

|
| A:CT扫描可见门静脉主干大量血栓(红色箭头); B:穿刺中门静脉主干造影:门静脉左、右分支未见显影, 主干残留伴充盈缺损(红色箭头); C:导管进入肠系膜上静脉远端造影可见:完全堵塞, 未见造影剂回流到门静脉(红色箭头); D:行TIPS后, 可见门静脉系统引流通畅 图 3 门静脉节段堵塞患者TIPS治疗过程 |
对于门静脉系统血栓的处理:术中将尽可能清除血栓, 通过导管、导丝、血栓切割装置等捣毁门静脉系统血栓, 然后抽吸出尽可能多的血栓, 残余血栓加用球囊扩张、压迫, 覆膜支架覆盖等, 使血管腔尽可能通畅。术后3 d内给予门冬氨酸鸟氨酸注射液静脉注射, 1个月内口服门冬氨酸鸟氨酸颗粒+乳果糖用于预防肝性脑病, 不使用抗凝药物预防支架堵塞。
1.3 随访患者都在门诊接受临床、生化和多普勒超声评估, 最初是在术后1个月, 然后是3、6个月, 然后每6个月复诊1次。当超声提示门静脉血栓严重时, 加做腹部增强CT扫描, 了解血栓范围。在随访中评估的终点包括门静脉系统的血栓的转归、支架功能、食管、胃静脉变化、胃肠道出血、腹水、肝性脑病、肝细胞癌、肝移植和死亡。
1.4 统计学分析采用SPSS 25.0统计软件进行数据分析。正态分布计量资料采用x±s表示, 组间比较采用t检验; 非正态分布计量资料采用中位数(25%, 75%分位数)表示, 组间比较采用非参数Wilcoxon检验; 计数资料组间比较采用χ2或Fisher’s精确概率检验。生存率采用Kaplan-Merier法计算, 不同组间的生存率的比较采用Log-rank检验, 采用Cox回归分析对生存的预后因素进行评估。检验水准:α=0.05。
2 结果44例患者接受TIPS治疗, 均有食管、胃静脉曲张破裂出血病史, 既往有脾切除史9例, 占20%, 血管栓塞程度较重, 大部分患者伴有顽固性胸和(或)腹水, 平均年龄是55.77(18.60)岁, 肝功能Child评分平均8.07(1.63)分, 其中A级:8例, B级:26例, C级:10例, 乙肝后肝硬化24例, 不明原因8例, 自身免疫性4例, 酒精肝6例, 丙肝2例, 其中TIPS成功组37例, 失败组7例, 手术成功概率是84%, 术中无严重并发症, 随访时间为术后6个月到3年, 44例患者随访时间均达6个月, 其中随访终点时间达12个月时31例, 18个月时25例, 24个月时23例, 30个月15例, 36个月9例(由于接受TIPS术时间前后不一致, 故随访时间长短不一致), 至随访终点, 一共6例死亡, 总体存活率86%。TIPS成功组:术前门静脉压力(33.28±4.00)mmHg, 术后(20.50±3.59)mmHg, 术后静脉曲张改善明显(P < 0.01), 复发出血3例, 给予内镜下套扎治疗, 出血复发率8%, 支架功能障碍3例, 考虑支架成角诱发血栓形成, 行支架矫正术恢复其功能2例, 1例口服华法林治疗, 效果欠佳, 顽固性胸腹水消失明显, 肝性脑病8例, 发病概率22%, 主要集中在术后1~3个月内, 给予对症处理后恢复。患者术前详细特征见表 1。
| 组别 | n | 年龄/岁 | 病毒/非病毒 | 身高/cm | 体质量/kg | 腹痛 | 静脉出血 | 胸水 | 腹水 | Chlid评分 |
| 全部患者 | 44 | 55.77±18.60 | 26/18 | 164.16±6.60 | 60.53±6.32 | 5 | 44 | 21 | 31 | 8.00(7.00, 9.00) |
| TIPS成功组 | 37 | 55.59±18.94 | 21/16 | 164.11±6.92 | 60.75±6.73 | 5 | 37 | 19 | 27 | 8.00(7.00, 9.25) |
| TIPS失败组 | 7 | 56.71±18.09 | 5/2 | 164.43±4.93 | 59.36±3.59 | 2 | 7 | 2 | 4 | 9.00(7.00, 9.00) |
| 组别 | n | AST/ U·L-1 | TBIL/ U·L-1 | 总胆酸/μmo1·L-1 | 前蛋白/g·L-1 | 白蛋白/g·L-1 | WBC/109·L-1 | |||
| 全部患者 | 44 | 43.05(28.40, 76.25) | 28.20(20.55, 46.50) | 22.45(10.05, 39.35) | 68.00(42.50, 88.00) | 33.00(29.55, 36.05) | 4.72(3.50, 5.86) | |||
| TIPS成功组 | 37 | 44.30(29.37, 73.88) | 28.10(20.68, 44.65) | 23.00(9.52, 39.83) | 67.00(41.75, 89.50) | 33.00(29.23, 35.23) | 4.75(3.41, 5.83) | |||
| TIPS失败组 | 7 | 23.60(20.60, 111.38) | 37.50(12.65, 55.70) | 15.50(11.70, 38.25) | 69.00(57.75, 73.00) | 36.50(32.03, 38.67) | 4.44(3.77, 5.76) | |||
| 组别 | n | PLT/109·L-1 | RBC/1012·L-1 | 血清Na/mmol·L-1 | 尿素/μmol·L-1 | 肌酐/μmol·L-1 | INR | |||
| 全部患者 | 44 | 65.00(51.00, 130.50) | 3.22(2.83, 3.67) | 137.65(135.35, 139.45) | 6.45(4.93, 9.01) | 71.00(57.00, 80.70) | 1.17(1.06, 1.33) | |||
| TIPS成功组 | 37 | 70.00(51.50, 134.75) | 3.26(2.83, 3.69) | 137.70(135.30, 139.43) | 6.41(4.93, 9.83) | 69.50(57.40, 80.05) | 1.15(1.06, 1.33) | |||
| TIPS失败组 | 7 | 58.00(51.00, 109.75) | 3.13(2.59, 3.26) | 137.60(135.75, 139.60) | 6.89(5.05, 7.49) | 73.00(58.03, 85.75) | 1.20(1.07, 1.33) | |||
| 组别 | n | PT/s | APTT/s | MVP-Ⅲ/Ⅳ | RPV-Ⅲ/Ⅳ | LPV-Ⅲ/Ⅳ | SMV-Ⅲ/Ⅳ | SV-Ⅲ/Ⅳ | 脾切(例) | |
| 全部患者 | 44 | 13.65(12.25, 15.35) | 39.15(32.55, 44.50) | 18/19 | 4/14 | 2/11 | 18/4 | 3/1 | 9 | |
| TIPS成功组 | 37 | 13.60(12.17, 15.43) | 38.80(32.72, 43.90) | 16/18 | 3/12 | 1/10 | 16/3 | 1/1 | 8 | |
| TIPS失败组 | 7 | 14.00(12.50, 15.28) | 39.50(31.93, 46.97) | 2/1 | 1/2 | 1/1 | 2/1 | 2/0 | 1 | |
| MPV:门静脉主干; RPV:门静脉右支; LPV:门静脉左支; SV:脾静脉; SMV:肠系膜上静脉; Ⅲ/Ⅳ:栓塞程度51% ~75%/76% ~100% | ||||||||||
2.1 门静脉系统血栓的变化
37例TIPS成功组中, 术前34例有MVP血栓, (Ⅲ级16例, Ⅳ级18例), 术后到例随访终点时, 1例无缓解, 1例缓解后复发加重, 其余均得到有效缓解或消失, 其整体缓解率达94%。伴有LVP栓塞11例(Ⅲ级1例, Ⅳ级10例), 由于该支血管血栓处理较困难, 只有3例患者术后缓解, 缓解率达27%。有15例伴有RVP血栓(Ⅲ级3例, Ⅳ级12例), 在随访终点有11例栓塞程度有效缓解, 缓解率73%。伴发SMV血栓19例(Ⅲ级16例, Ⅳ级3例)在随访终点均得到有效缓解, 但有1例新发血栓形成。在7例TIPS失败组中, MVA血栓3例, RVP+LVP血栓3例(Ⅳ级), SMV血栓3例, 至随访终点, 患者血栓全无缓解。
2.2 曲张静脉的缓解与再发出血44例患者术前均为胃食管静脉重度曲张, 红色征(+), 有出血病史, 37例TIPS组中, 术后短期内(1~6个月), 曲张静脉轻度-消失21例, 占57%, 中度曲张14例, 占38%, 重度曲张, 无缓解2例, 占5%。于术后12、18、36个月复发出血各1例, 再发出血率为8%, 内镜检查提示曲张静脉破裂出血, 并行内镜下套扎治疗。至随访终点, 曲张静脉未缓解共5例, 占14%, 其中包含1例支架堵塞而未行支架开通术患者, 其余患者曲张静脉均明显好转, 总体缓解率达86%。7例TIPS失败组患者, 在TIPS失败后, 随访过程中, 2例于6、30个月出血, 给予内镜下套扎治疗, 出血停止。2例于12月复发出血死亡, 总体再发出血率为57%。至随访终点, 7例患者曲张静脉仍为重度, 红色征(+)。
2.3 手术中及术后相关并发症本组病例中, 无手术相关死亡者。在3例患者术中穿刺到肝外, 腹腔内抽出血性液体, 术后给予积极输血、静脉输入止血药、补充凝血因子治疗, 生命体征平稳, 3例患者发生误穿刺中胆管, 术后未发现明显胆道出血症状。1例PVT完全堵塞的患者中, 穿刺中扩张的肝动脉, 行肝动脉造影, 未发现明显异常。3例患者术后出现发热, 伴有白细胞升高, 给予抗生素治疗后, 体温恢复正常。大部分患者术后第2天查肝功可发现丙氨酸氨基转移酶(ALT)水平不同程度的升高, 给予保肝治疗后, 术后1个月内逐渐下降到正常水平。在随访过程中, TIPS成功组一共发生肝性脑病8例, 发病概率22%, 主要集中在术后1~3个月内, 在长期随访中(1~3年), 未发现有肝性脑病。其中3例与进食大量动物蛋白, 伴有长时间便秘有关, 其余5例与肝功能基础较差有关, 给予门冬氨酸鸟氨酸颗粒口服+口服乳果糖等治疗后恢复正常。TIPS失败组, 未发现有肝性脑病发生。
2.4 总体生存情况44例患者致随访终点, 6例死亡, 总体存活率86%。TIPS成功组: 2例于术后2年死于肝癌, 1例18个月时发现肝癌, 行TACE(经肝动脉灌注化疗栓塞术)治疗, 至今存活。2例分别于术后13、25个月死于肝功能衰竭, 短期生存率100%(术后6个月), 长期生存率89%(术后1~3年)。TIPS失败组: 2例于12个月死于静脉曲张破裂再发出血, 短期生存率100%(术后6个月), 长期生存率71%(术后1~3年)。TIPS成功组存活率较失败组要高, 但差异无统计学意义(P>0.05, 图 4)。

|
| 图 4 TIPS成功组的生存情况 |
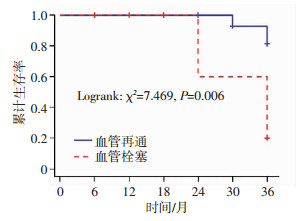
在单因素分析中, 多部位曲张静脉、血清Na、血管再通是肝硬化患者的生存预测因子(选取P < 0.05), 而没有TIPS。在多变量分析中, 血管再通是生存的唯一独立预测因子(HR 10.309, 95%CI 1.138~93.348, 表 2)。TIPS术后大部分患者实现了血管再通, 与血管未通患者比较, 生存率提高, 且差异有统计学意义(P < 0.05, 图 5)。
| 变量 | 单因素分析 | 多因素分析 | |||||
| HR | 95% CI | P值 | HR | 95% CI | P值 | ||
| 年龄/岁 | 1.013 | 0.945~1.086 | 0.719 | ||||
| 性别(男/女) | 2.417 | 0.442~13.215 | 0.309 | ||||
| TIPS(成功/失败) | 1.686 | 0.305~9.308 | 0.549 | ||||
| 病毒(有/无) | 1.059 | 0.194~5.796 | 0.947 | ||||
| 多部位曲张静脉(是/否) | 0.113 | 0.022~0.575 | 0.009 | 0.117 | 0.007-2.084 | 0.144 | |
| 术前胸水程度(无/有) | 1.349 | 0.269~6.778 | 0.716 | ||||
| 术前腹水程度(无/有) | 1.691 | 0.197~14.496 | 0.632 | ||||
| ALT | 0.972 | 0.928~1.018 | 0.228 | ||||
| AST | 0.990 | 0.968~1.011 | 0.341 | ||||
| TBIL | 1.019 | 0.990~1.050 | 0.196 | ||||
| 白蛋白 | 0.994 | 0.868~1.138 | 0.934 | ||||
| WBC | 1.125 | 0.747~1.694 | 0.573 | ||||
| PLT | 0.973 | 0.938~1.008 | 0.130 | ||||
| RBC | 1.183 | 0.348~4.024 | 0.787 | ||||
| 血清Na | 1.484 | 1.017~2.166 | 0.041 | 1.176 | 0.773-1.790 | 0.449 | |
| PT | 0.966 | 0.721~1.295 | 0.817 | ||||
| 门脉再通(是/否) | 6.881 | 1.246~38.006 | 0.027 | 10.309 | 1.138-93.348 | 0.038 | |
| LPV(Ⅰ/Ⅱ/Ⅲ/Ⅳ) | 0.855 | 0.157~4.673 | 0.857 | ||||
| RPV(Ⅰ/Ⅱ/Ⅲ/Ⅳ) | 0.713 | 0.130~3.925 | 0.698 | ||||
| MPV(Ⅰ/Ⅱ/Ⅲ/Ⅳ) | 1.691 | 0.197~14.496 | 0.632 | ||||
| SMV(Ⅰ/Ⅱ/Ⅲ/Ⅳ) | 0.654 | 0.068~6.283 | 0.713 | ||||
| SV(Ⅰ/Ⅱ/Ⅲ/Ⅳ) | 1.144 | 0.132~9.890 | 0.903 | ||||
| 脾切除术(是/否) | 0.791 | 0.142~4.422 | 0.790 | ||||
| MPV:门静脉主干; RPV:门静脉右支; LPV:门静脉左支; SV:脾静脉; SMV:肠系膜上静脉; Ⅰ/Ⅱ/Ⅲ/Ⅳ:栓塞程度<25%/25% ~50%/51% ~75%/76% ~100%;血管再通:定义为TIPS成功并且维持门静脉系统血流通畅; 多部位曲张静脉:食道或者胃静脉曲张=否, 二者均有=是 | |||||||
|
| 图 5 再通组和血栓组的存活率比较 |
3 讨论
该组病例选取的特点是:①血栓程度较重, 单支血管堵塞程度均>50%, 且是多支栓塞为主, 而现有文献关注单支血管栓塞的较多, 复合血栓的较少。这组病例更贴近临床中实际遇到的情况即多样、复杂而难于治疗。在处理血栓上, 我们尽可能解除或减少血栓的堵塞, 而文献[17-18]报道并未行血栓的处理, 只是植入分流支架。虽然文献[17]报道有肝外穿刺至死亡的病例, 但总体来讲, 基于充分的术前评估、熟练而小心的术中操作、得力的术后处理, TIPS治疗门静脉高压伴严重血栓者是较安全的, 值得尝试。静脉曲张是肝硬化的一种危及生命的并发症, 其6周死亡率约为15%, 伴有PVT者更高[19-20]。在大多研究报道中, 采用内镜下套扎治疗在没有合并PVT的患者中1~2年的复发率在29%~57%[21-23], 合并有PVT的复发率在45%~50%。本研究中, TIPS成功组曲张静脉再发出血率为8%, 失败组为57%。研究表明[19, 24], TIPS在预防静脉曲张再出血方面较内镜下套扎治疗效果更好, 并且在门脉再通和预防继发性血栓形成方面也是效果显著, 更重要的是, 肝性脑病的风险并不会增加[20, 25], 可能与TIPS前由于门静脉血栓堵塞致灌注减少, 而术后并未明显分流原门脉血流有关。更何况我们采用的是直径8 mm的支架, 可达到足够分流与减少肝脏脑病的发生[26]。TIPS除了在术中可以直接抽吸、捣毁、溶解血栓外, 术后血流速度的增加, 可以持续冲刷残余血栓达到血栓减少或者消失的目的[16, 27-29], 使门静脉再通率提高, 对于等待肝移植的患者有极大的价值[28-29]。从本组结果来看, 曲张静脉消失程度、再出血率、门静脉再通程度, TIPS成功组, 得到的临床疗效均较失败组要好, 进一步证明TIPS的有效性。本研究发现, 在PVT患者中, 唯一的独立预测因素是门静脉再通。血管再通的原因是:①TIPS后支架连通了门静脉与肝静脉; ②术中对血栓进行捣毁、抽吸、导管局部溶栓、球囊扩张以恢复门静脉系统通畅。这也是为什么在我们的研究中可以看到, 在TIPS成功组中, 患者的生存率高于失败组, 血管再通组较闭塞组生存率高, 且差异有统计学意义(P < 0.05)。这就提示我们, 使闭塞的门静脉系统得到最大程度的再通可以提高患者的生存时间, 而TIPS是使门静脉血栓再通的主要手段, 虽然手术难度较大, 但仍然是我们应该努力的方向。
本研究局限性:由于本研究是“回顾性的”和“相对较小的样本规模”, 需要一个前瞻性的、与自然病程对比、与内镜下标准治疗+药物溶栓对比得出更科学的结论。除此之外, 该研究中患者长期随访病例较少, 这可能会显著降低肝脏功能对预测生存率的影响。因此, 在肝脏功能相对较差的患者中, 生存分析需要进一步验证。
总之, 通过对PVT-TIPS患者的大量研究, 建议如下:①TIPS应该被视为一个安全可行的治疗PVT的方法, 在实施时间上, 我们倾向于血栓处于亚急性、慢性而尚未发生纤维条索状完全性堵塞阶段。②在PVT患者中, 唯一生存预测因素是门静脉再通, 这具有重大临床指导意义, 在今后对该类患者将通过TIPS致力于重塑门静脉系统, 但我们需要一个前瞻性的、与自然病程对比、与内镜下标准治疗+药物溶栓对比得出更科学的结论。
| [1] | DEBNATH C R, DEBNATH M R, ALAM M M, et al. Cirrhosis of liver and portal vein thrombosis-a review article[J]. Mymensingh Med J, 2014, 23(3): 606–608. |
| [2] | PARIKH S, SHAH R, KAPOOR P. Portal vein thrombosis[J]. Am J Med, 2010, 123(2): 111–119. DOI:10.1016/j.amjmed.2009.05.023 |
| [3] | AMITRANO L, GUARDASCIONE M A, BRANCACCIO V, et al. Risk factors and clinical presentation of portal vein thrombosis in patients with liver cirrhosis[J]. J Hepatol, 2004, 40(5): 736–741. DOI:10.1016/j.jhep.2004.01.001 |
| [4] | VALLA D C, CONDAT B, LEBREC D. Spectrum of portal vein thrombosis in the west[J]. J Gastroenterol Hepatol, 2002, 17(Suppl 3): S224–S227. DOI:10.1046/j.1440-1746.17.s3.4.x |
| [5] | VILLA E, CAMMC, MARIETTA M, et al. Enoxaparin prevents portal vein thrombosis and liver decompensation in patients with advanced cirrhosis[J]. Gastroenterology, 2012, 143(5): 1253–1260. DOI:10.1053/j.gastro.2012.07.018 |
| [6] | QI X, HAN G, HE C, et al. CT features of non-malignantportal vein thrombosis: a pictorial review[J]. Clin Res HepatolGastroenterol, 2012, 36(6): 561–568. DOI:10.1016/j.clinre.2012.05.021 |
| [7] | PONZIANI F R, ZOCCO M A, GARCOVICH M, et al. What we should know about portal vein thrombosis in cirrhotic patients: a changing perspective[J]. World J Gastroenterol, 2012, 18(36): 5014–5020. DOI:10.3748/wjg.v18.i36.5014 |
| [8] |
吴勤, 楚金东, 金波, 等. 肝硬化后门静脉血栓形成的临床特点研究[J].
传染病信息, 2013, 26(3): 164–167.
WU Q, CHU J D, JIN B, et al. Clinical characteristics of portal vein thrombosis in patients with liver cirrhosis[J]. Infect Dis Info, 2013, 26(3): 164–167. DOI:10.3969/j.issn.1007-8134.2013.03.010 |
| [9] | LI M X, ZHANG X F, LIU Z W, et al. Risk factors and clinical characteristics of portal vein thrombosis after splenectomy in patients with liver cirrhosis[J]. HBPD INT, 2013, 12(5): 512–519. DOI:10.1016/s1499-3872(13)60081-8 |
| [10] | FRANCOZ C, VALLA D, DURAND F. Portal vein thrombosis, cirrhosis, and liver transplantation[J]. J Hepatol, 2012, 57(1): 203–212. DOI:10.1016/j.jhep.2011.12.034 |
| [11] | LUCA A, CARUSO S, MILAZZO M, et al. Natural course of extrahepatic nonmalignant partial portal vein thrombosis inpatients with cirrhosis[J]. Radiology, 2012, 265(1): 124–132. DOI:10.1148/radiol.12112236 |
| [12] | LISMAN T. Low molecular weight heparin in management and prevention of portal vein thrombosis[J]. Thromb Res, 2014, 134(4): 761–762. DOI:10.1016/j.thromres.2014.08.003 |
| [13] | RODRIGUEZ-CASTRO K I, SIMIONI P, BURRA P, et al. Anticoagulation for the treatment of thrombotic complications in patients with cirrhosis[J]. Liver Int, 2012, 32(10): 1465–1476. DOI:10.1111/j.1478-3231.2012.02839.x |
| [14] | ENGLESBE M J, KUBUS J, MUHAMMAD W, et al. Portal vein thrombosis and survival in patients with cirrhosis[J]. Liver Transpl, 2010, 16(1): 83–90. DOI:10.1002/lt.21941 |
| [15] | LV Y, QI X, HE C, et al. Covered TIPS versus endoscopic band ligation plus propranolol for the prevention of varicealrebleeding in cirrhotic patients with portal vein thrombosis: a randomised controlled trial[J]. Gut, 2017: gutjnl-2017-314634. DOI:10.1136/gutjnl-2017-314634 |
| [16] | LUCA A, MIRAGLIA R, CARUSO S, et al. Short- andlong-term effects of the transjugular intrahepatic portosystemicshunt on portal vein thrombosis in patients with cirrhosis[J]. Gut, 2011, 60(6): 846–852. DOI:10.1136/gut.2010.228023 |
| [17] | HAN G, QI X, HE C, et al. Transjugular intrahepatic portosystemic shunt for portal vein thrombosis with symptomatic portal hypertension in liver cirrhosis[J]. J Hepatol, 2011, 54(1): 78–88. DOI:10.1016/j.jhep.2010.06.029 |
| [18] | WANG Z, JIANG M S, ZHANG H L, et al. Is Post-TIPS Anticoagulation therapy necessary in patients with cirrhosis and portal vein thrombosis? A randomized controlled trial[J]. Radiology, 2016, 279(3): 943–951. DOI:10.1148/radiol.2015150369 |
| [19] | GARCIA-TSAO G, BOSCH J. Management of varices and variceal hemorrhage in cirrhosis[J]. N Engl J Med, 2010, 362(9): 823–832. DOI:10.1056/NEJMra0901512 |
| [20] | JALAN R, HAYES P C. UK guidelines on the management of variceal haemorrhage in cirrhotic patients. British society of gastroenterology[J]. Gut, 2000, 46(Suppl 3-4): Ⅲ1–Ⅲ15. DOI:10.1136/gutjnl-2015-309262 |
| [21] | HOLSTER I L, TJWA E T, MOELKER A, et al. Covered transjugular intrahepatic portosystemic shunt versus endoscopic therapy+β-blocker for prevention of variceal rebleeding[J]. Hepatology, 2016, 63(2): 581–589. DOI:10.1002/hep.28318 |
| [22] | SAUER P, HANSMANN J, RICHTER G M, et al. Endoscopic variceal ligation plus propranolol vstransjugular intrahepatic portosystemic stent shunt: a long-term randomized trial[J]. Endoscopy, 2002, 34(9): 690–697. DOI:10.1055/s-2002-33565 |
| [23] | POMIER-LAYRARGUES G, VILLENEUVE J P, DESCH NES M, et al. Transjugular intrahepatic portosystemic shunt (TIPS) versus endoscopic variceal ligation in the prevention of variceal rebleeding in patients with cirrhosis: a randomised trial[J]. Gut, 2001, 48(3): 390–396. DOI:10.1136/gut.48.3.390 |
| [24] | LUO X, WANG Z, TSAUO J, et al. Advanced cirrhosis combined with portal vein thrombosis: a randomized trial of TIPS versus endoscopic band ligation plus propranolol for the prevention of recurrent esophageal variceal bleeding[J]. Radiology, 2015, 276(1): 286–293. DOI:10.1148/radiol.15141252 |
| [25] | R SSLE M. TIPS: 25 years later[J]. J Hepatol, 2013, 59(5): 1081–1093. DOI:10.1016/j.jhep.2013.06.014 |
| [26] | WANG Q, LV Y, BAI M, et al. Eight millimetre covered TIPS does not compromise shunt function but reduces hepatic encephalopathy in preventing variceal rebleeding[J]. J Hepatol, 2017, 67(3): 508–516. DOI:10.1016/j.jhep.2017.05.006 |
| [27] | HAN G, QI X, HE C, et al. Reply to:tips for portal vein thrombosis (pvt) in cirrhosis: not only unblocking a pipe[J]. Journal of Hepatology, 2011, 55(4): 947–948. DOI:10.1016/j.jhep.2011.03.003 |
| [28] | SALEM R, VOUCHE M, BAKER T, et al. Pretransplant portal vein recanalization-transjugular intrahepatic portosystemic shunt in patients with complete obliterative portal vein thrombosis[J]. Transplantation, 2015, 99(11): 2347–2355. DOI:10.1097/TP.0000000000000729 |
| [29] | THORNBURG B, DESAI K, HICKEY R, et al. Portal vein recanalization and transjugular intrahepatic portosystemic shunt creation for chronic portal vein thrombosis: technical considerations[J]. Tech Vasc Interv Radiol, 2016, 19(1): 52–60. DOI:10.1053/j.tvir.2016.01.006 |



