心脏再同步化治疗(cardiac resynchronization therapy,CRT)能够改善心室运动不同步心衰患者的症状,提高运动耐量和生活质量,减少心衰再入院率,提高总体生存率[1-2]。但是,不同的患者对CRT的反应存在较大差异,约30%的患者不能从CRT获益[3]。因此,识别哪些因素可以提高CRT的反应性非常重要。有研究提出女性、QRS波较宽、缺血性心肌病、较小的左心室等可预测CRT有反应[4],还有研究提出较短的心衰病程、缺血性心肌病、女性、QRS波较宽、左束支传导阻滞、较小的肺动脉收缩压(pulmonary artery systolic pressure,PASP)、较小的左心房和左心室可预测CRT超反应[4-6],目前存在较大争议。约2/3的慢性心衰患者可能合并PASP升高[7],研究表明PASP升高影响心衰患者的临床预后[7-8]。因此,PASP对心衰患者CRT术后反应性及预后的影响是值得探讨的课题。
1 资料与方法 1.1 研究对象回顾性分析2014年6月至2017年12月因心衰收住本院心血管内科行心脏再同步化治疗起搏器/除颤器(cardiac resynchronization therapy-Pacemaker/Defibrillator, CRT-P/D)的73例患者资料,男性52例,女性21例,年龄(60.32 ± 9.78)岁,53例植入心脏再同步化治疗起搏器(CRT-P),20例植入心脏再同步化治疗除颤器(CRT-D)。患者均满足2016年欧洲心脏病学会(European Society of Cardiology, ESC)急慢性心力衰竭诊治指南中CRT-P/D植入标准[9]:①症状性心衰患者,窦性心率,至少充分抗心衰药物治疗3个月后QRS波宽度≥130 ms,左室射血分数(left ventricular ejection fraction,LVEF)≤35%;②房颤,至少充分抗心衰药物治疗3个月后LVEF≤35%,纽约心脏协会(New York Heart Association, NYHA)心功能分级Ⅲ~Ⅳ级,QRS≥130 ms;③术前和术后6个月随访资料完整。排除标准:①术前3个月内曾患急性心肌梗死;②有精神类疾病不配合者。患者及家属均知情同意本研究并签署知情同意书。2018年6月6日通过陆军军医大学第二附属医院伦理委员会审查。
1.2 观察指标收集所有患者的术前临床资料,包括:年龄、性别、NYHA分级、合并疾病(高血压、糖尿病、肾功能不全)、超声心动图[LVEF、左心房内径(left atrial dimension,LAD)、左心室舒张末期内径(left ventricular end-diastolic dimension,LVEDD)、右心房内径(right atrial dimension,RAD)、右心室舒张末期内径(right ventricular end-diastolic dimension,RVEDD)、二尖瓣返流面积、三尖瓣返流面积]、心电图(心脏节律、QRS波宽度)、抗心衰治疗用药情况[血管紧张素转换酶抑制剂/血管紧张素Ⅱ受体拮抗剂(ACEI/ARB)、β受体阻滞剂、螺内酯]。术后随访资料包括:NYHA分级、超声心动图、心电图、起搏器程控参数、复合终点事件(心衰再入院或全因死亡)。
1.3 超声心动图检查超声心动图由心脏超声专业医师采集,患者取左侧卧位,采用Simpson双平面法在心尖四腔切面测得LVEF,使用M型超声心动图在胸骨旁长轴切面和心尖四腔切面测得各心腔大小和各瓣膜返流面积。有三尖瓣返流的患者,PASP由估测的三尖瓣返流压差(测得三尖瓣最大返流速度V,根据Bernouli方程Grad=4V2计算)加上右房压(10 mmHg)[10]得出,没有三尖瓣返流的患者,我们将术前PASP设定为25 mmHg[11]。根据估测的PASP将患者分成两组:肺动脉高压组(PASP≥50 mmHg)和非肺动脉高压组(PASP < 50 mmHg)。CRT有反应定义为:术后6个月LVEF增加幅度 > 5%,CRT超反应定义为:术后6个月NYHA分级较术前下降≥1级,LVEF≥50%[12],逆转左心室重构定义为左心室缩小。
1.4 CRT植入过程CRT由本科室起搏电生理团队植入,局麻后行左锁骨下静脉穿刺,先行冠状静脉窦逆行造影,首选的靶静脉为侧静脉或侧后静脉,若左心室电极导线放置于靶静脉困难时,可选择其他分支。右心房和右心室电极导线固定于右心耳和右室心尖部。测试起搏器参数满意后,将脉冲发生器与电极导线连接并置于左胸前囊袋内,缝合切口。
1.5 统计学分析采用SPSS 20.0统计软件。正态分布的计量资料用x±s表示,采用独立样本t检验比较组间差异;不符合正态分布的计量资料用中位数(四分位数)表示,采用Mann-Whitney U检验比较组间差异。组内术后与术前差异用配对样本t检验比较。分类变量采用计数或百分数表示,采用χ2检验比较计数资料组间差异。P < 0.05为差异具有统计学意义。用受试者工作特征曲线(ROC曲线)及曲线下面积(AUC)评价术前PASP对CRT有反应或超反应的预测价值,并计算截断值。以Kaplan-Meier法进行生存分析,并绘制生存曲线,同时用Log-rank法检验。用单因素Cox回归分析影响CRT术后预后的危险因素,P < 0.1纳入多因素Cox回归模型分析。
2 结果 2.1 两组患者基线特征的比较共纳入73例患者,年龄(60.32±9.78)岁,男性52例,女性21例,平均NYHA分级3(3,3)级,QRS波宽度(164.00±20.99)ms,平均LVEF[32%(27%,34%)],合并高血压16例,糖尿病8例,肾功能不全11例,使用抗心衰治疗药物ACEI/ARB、β受体阻滞剂、螺内酯的比例分别为91.78%、90.41%、83.56%。
肺动脉高压组27例(37%),非肺动脉高压组46例(63%),两组在年龄、性别、NYHA分级、合并高血压、糖尿病、肾功能不全的比例、术前QRS波宽度、房颤比例、LVEF、LVEDD、使用抗心衰治疗药物ACEI/ARB、β受体阻滞剂、螺内酯的比例差异均无统计学意义(P > 0.05),而与非肺动脉高压组相比,肺动脉高压组有更大的LAD、RAD、RVEDD、二尖瓣返流面积和三尖瓣返流面积(P < 0.001,表 1)。
| 组别 | n | 年龄/岁 | 女性 | NYHA分级 | 高血压 | 糖尿病 | 肾功能不全 |
| 肺动脉高压组 | 27 | 59.93±10.06 | 7.00(25.93) | 3.00(3.00,4.00) | 7.00(25.93) | 5.00(18.52) | 3.00(11.11) |
| 非肺动脉高压组 | 46 | 60.54±9.72 | 14.00(30.43) | 3.00(3.00,3.00) | 9.00(19.57) | 3.00(6.52) | 8.00(17.39) |
| 合计 | 73 | 60.32±9.78 | 21.00(28.77) | 3.00(3.00,3.00) | 16.00(21.92) | 8.00(10.96) | 11.00(15.07) |
| P值 | 0.797 | 0.681 | 0.097 | 0.526 | 0.137 | 0.736 | |
| 组别 | 房颤 | QRS波宽度/ms | LVEF/% | LAD/mm | LVEDD/mm | RAD/mm | |
| 肺动脉高压组 | 3.00(11.11) | 161.90±23.26 | 31.00(25.00,34.00) | 46.00(45.00,50.00) | 71.10±7.96 | 45.00(42.00,47.00) | |
| 非肺动脉高压组 | 6.00(13.04) | 165.30±19.68 | 32.00(27.53,34.00) | 41.75(38.50,46.08) | 69.70±8.03 | 37.00(34.00,41.50) | |
| 合计 | 9.00(12.33) | 164.00±20.99 | 32.00(27.00,34.00) | 45.00(39.75,47.00) | 70.22±7.98 | 40.20(36.0,45.25) | |
| P值 | 1.000 | 0.501 | 0.765 | < 0.001 | 0.472 | < 0.001 | |
| 组别 | RVEDD/mm | 二尖瓣返流面积/cm2 | 三尖瓣返流面积/cm2 | ACEI/ARB | β受体阻滞剂 | 螺内酯 | |
| 肺动脉高压组 | 42.00(36.00,44.00) | 9.70(6.90,13.30) | 5.50(3.70,7.30) | 24.00(88.89) | 25.00(92.59) | 23.00(85.19) | |
| 非肺动脉高压组 | 35.00(33.00,40.18) | 6.00(4.07,8.23) | 1.40(0.00,2.60) | 43.00(93.48) | 41.00(89.13) | 38.00(82.61) | |
| 合计 | 36.00(34.00,42.50) | 7.00(4.50,9.98) | 2.10(1.00,5.35) | 67.00(91.78) | 66.00(90.41) | 61.00(83.56) | |
| P值 | < 0.001 | < 0.001 | < 0.001 | 0.664 | 1.000 | 1.000 | |
| 计量资料以x±s或中位数(四分位数)表示,计数资料以例(%)表示 | |||||||
2.2 两组患者CRT术后6个月心功能、PASP和心脏超声检查情况
CRT术后6个月,肺动脉高压组NYHA分级、LVEF较术前有改善(P < 0.05),LVEDD无改善(P > 0.05),而非肺动脉高压组在NYHA分级、LVEF和LVEDD方面均有改善(P < 0.05),且NYHA分级、LVEF和LVEDD改善程度显著优于肺动脉高压组(P < 0.05)。CRT术后肺动脉高压组PASP较术前下降(P < 0.001),非肺动脉高压组较术前无变化(P > 0.05,表 2)。
| 组别 | n | NYHA分级 | LVEF/% | △LVEF/% | LVEDD/mm | △LVEDD/mm | PASP/mmHg | △PASP/mmHg |
| 肺动脉高压组 | 27 | 3.00(0.00,8.20) | 2.00 (-5.50,7.00) | 26.00(17.60,32.00) | ||||
| 术前 | 3.00 (3.00,4.00) | 31.00 (25.00,34.00) | 71.10±7.96 | 63.00 (55.30,69.00) | ||||
| 术后 | 2.00 (2.00,3.00) | 34.00 (29.00,38.00) | 69.30±9.53 | 34.00 (25.00,49.00) | ||||
| P值 | < 0.001 | 0.028 | 0.265 | < 0.001 | ||||
| 非肺动脉高压组 | 46 | 11.50(3.75,20.75) | 4.30 (0.00,10.40) | < 0.01(-6.25,7.03) | ||||
| 术前 | 3.00 (3.00,3.00) | 32.00 (27.53,34.00) | 69.70±8.03 | 29.00 (25.00,39.08) | ||||
| 术后 | 2.00 (2.00,2.00) | 44.00 (35.00,56.00) | 63.28±10.46 | 26.00 (25.00,34.25) | ||||
| P值 | < 0.001 | < 0.001 | < 0.001 | 0.969 | ||||
| Pa值 | 0.014 | 0.001 | 0.002 | 0.017 | 0.034 | 0.009 | < 0.001 | |
| △LVEF:LVEF变化值;△LVEDD:LVEDD变化值;△PASP:PASP变化值; a:术后6个月两组比较; 计量资料以x±s或中位数(四分位数)表示 | ||||||||
2.3 术前PASP对CRT有反应和超反应的预测
CRT术后6个月,73例患者中CRT有反应和超反应的发生率分别为60.3%(44/73)、23.3%(17/73)。非肺动脉高压组CRT有反应和超反应的发生率均高于肺动脉高压组[71.7%(33/46)、32.6%(15/46)vs 40.7%(11/27)、7.4%(2/27),P < 0.05]。
术前PASP不能预测CRT有反应(P > 0.05),但是对CRT超反应有预测价值(AUC=0.709,95%CI为0.575~0.843,P < 0.05),取PASP≤35 mmHg为最佳截断值时,Youden指数最大,预测CRT超反应的灵敏度、特异度分别为76.5%、64.3%。
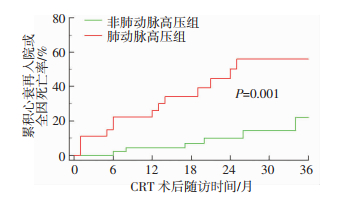
2.4 肺动脉高压对预后的影响术后随访1~36(22.56±10.38)个月,共有6例(8.2%)死亡,11例(15.1%)因心衰再入院。肺动脉高压组3例(11.1%)死亡,9例(33.3%)因心衰再入院;而非肺动脉高压组3例(6.5%)死亡,2例(4.3%)因心衰再入院。Kaplan-Meier生存曲线(图 1)提示:CRT术后3年肺动脉高压组复合终点事件(心衰再入院或全因死亡)发生率显著高于非肺动脉高压组(P < 0.05)。
|
| 图 1 两组患者CRT术后3年的生存曲线分析 |
2.5 发生复合终点事件的危险因素
单因素Cox回归分析提示肺动脉高压、LAD、LVEDD、RAD、RVEDD是影响复合终点事件发生的危险因素,但是多因素Cox回归模型分析校正了术前LVEF、LAD、LVEDD、RAD、RVEDD后提示肺动脉高压(HR:3.64,95%CI,1.25~10.61,P < 0.05)、LAD(HR:1.10,95%CI:1.01~1.20,P < 0.05)是影响预后的独立危险因素(表 3)。
| 统计学分析 | 肺动脉高压 | 女性 | 年龄/岁 | NYHA分级 | 高血压 | 糖尿病 | 肾功能不全 | 房颤 | QRS波宽度/ms | |
| 单因素Cox回归分析 | ||||||||||
| HR | 5.09 | 0.34 | 1.01 | 1.44 | 1.51 | 2.4 | 1.18 | 0.41 | 0.98 | |
| 95%CI | 1.79~14.48 | 0.08~1.50 | 0.96~1.06 | 0.67~3.07 | 0.53~4.29 | 0.69~8.40 | 0.34~4.10 | 0.05~3.08 | 0.96~1.00 | |
| P值 | 0.002 | 0.155 | 0.694 | 0.349 | 0.440 | 0.170 | 0.797 | 0.384 | 0.103 | |
| 多因素Cox回归分析 | ||||||||||
| HR | 3.64 | |||||||||
| 95%CI | 1.25~10.61 | |||||||||
| P值 | 0.018 | |||||||||
| 统计学分析 | LVEF/% | LAD /mm | LVEDD /mm | RAD /mm | RVEDD /mm | 二尖瓣返流面积/cm2 | 三尖瓣返流面积/cm2 | ACEI/ARB | β受体阻滞剂 | 螺内酯 |
| 单因素Cox回归分析 | ||||||||||
| HR | 0.92 | 1.12 | 1.08 | 1.07 | 1.08 | 1.03 | 1.1 | 0.99 | 0.93 | 1.31 |
| 95%CI | 0.83~1.02 | 1.04~1.21 | 1.01~1.14 | 1.00~1.13 | 1.01~1.16 | 0.97~1.08 | 0.98~1.12 | 0.13~7.65 | 0.21~4.08 | 0.30~5.78 |
| P值 | 0.100 | 0.003 | 0.017 | 0.040 | 0.020 | 0.370 | 0.104 | 0.988 | 0.919 | 0.720 |
| 多因素Cox回归分析 | ||||||||||
| HR | 1.1 | 1.06 | 0.94 | 1.05 | ||||||
| 95%CI | 1.01~1.20 | 1.00~1.13 | 0.80~1.10 | 0.97~1.14 | ||||||
| P值 | 0.033 | 0.059 | 0.415 | 0.247 | ||||||
3 讨论
20世纪90年代初期开始应用CRT治疗心衰,目前CRT已成为伴有心室收缩不同步心衰患者的标准疗法。CRT术后最亟待解决的问题是约30%的患者不能从CRT获益,且40%~50%的患者术后不能逆转心室重构[13]。因此,研究如何通过常规术前检测预测CRT术后的反应,对提高CRT植入后的疗效有重要的临床意义。
失代偿期左心衰会引起左心充盈压升高,左房压升高使肺静脉回流障碍,压力升高,从而导致继发性肺动脉高压,在2015 ESC/ERS肺动脉高压诊疗指南分类中属于第2大类左心疾病相关性肺动脉高压[14],肺动脉高压进一步引起右心充盈压升高,右心衰竭。植入CRT的患者中,PASP升高的发病率是35.0%~ 50.3%[11, 15-16],本研究中PASP升高的发病率是37.0%,与之前的研究一致。本研究中肺动脉高压组较非肺动脉高压组在术前有更大的LAD、RAD、RVEDD、二尖瓣返流面积和三尖瓣返流面积,可能是由于长期左心衰导致左心房扩大,引起肺动脉高压,从而导致右心衰。
关于合并肺动脉高压的心衰患者CRT术后能否逆转左室重构,目前的研究较少,且结论并不一致。CHATTERJEE等[17]发现肺动脉高压组与非肺动脉高压组在逆转心室重构方面差异无统计学意义;同样地,STERN等[16]发现术前PASP与逆转心室重构无关。但是,WANG等[15]、汪菁峰等[18]和WANG等[19]对中国人群的研究发现CRT术后,术前PASP升高组LVEDD较术前差异无统计学意义,并不能逆转心室重构。本研究发现肺动脉高压组术后LVEDD较术前差异无统计学意义(P > 0.05),我们推测与CHATTERJEE等[17]和STERN等[16]研究不同的原因可能是存在种族差异,但尚需大样本、多中心的数据进一步验证。
现有有限的研究大多证实术前PASP值对CRT术后的反应性有一定的预测价值。WANG等[15]和汪菁峰等[18]证实术前PASP值能预测术后对CRT有反应。KILLU等[6]观察到较低的术前PASP是CRT超反应的独立预测因素。刘丹等[20]证实术前PASP≤30 mmHg的患者更容易发生超反应。本研究发现术前PASP不能预测CRT有反应,与WANG等[15]和汪菁峰等[18]研究不同的原因可能是定义CRT有反应的标准不同,我们将术后6个月LVEF增加幅度 > 5%定义为有反应,而WANG等[15]定义术后6个月NYHA下降≥1级为CRT临床有反应,左室收缩末容积(LVESV)较术前缩小≥15%为超声心动图有反应,汪菁峰等[18]定义LVESV较术前缩小≥10%为CRT治疗有效。本研究发现术前PASP对CRT超反应有预测价值,与KILLU等[6]和刘丹等[20]研究结果基本一致,但是取PASP≤35 mmHg为截断值时预测的灵敏度、特异度(76.5%、64.3%)不高,可能原因是影响CRT超反应的术前因素较多,单一的PASP预测CRT超反应有一定的局限性。
目前的研究认为术前PASP升高是全因死亡、心脏移植或心衰再入院的独立危险因素[11, 15-17]。本研究的结果与上述研究结果一致,术前PASP≥50 mmHg的患者预后差,全因死亡或心衰再入院的风险几乎增加3倍,PASP是全因死亡或心衰再入院的独立预测因素。STERN等[16]发现右心功能衰竭可能与CRT临床预后不良有关,但是在Cox回归分析中无统计学意义(P=0.31)。CHATTERJEE等[17]报道右室扩张与预后有关。本研究单因素Cox回归模型分析发现右心室内径是心衰再入院或全因死亡的危险因素(HR:1.08,95% CI:1.01~1.16,P < 0.05),遗憾的是在Cox多因素回归分析中差异无统计学意义。关于右心功能与CRT预后的关系还需进一步研究。REANT等[21]观察到左心室容积 < 55 mL是CRT超反应的独立预测因素,STEFAN等[22]同样发现较小的LAD可预测CRT超反应。本研究发现LAD是CRT术后预后的弱危险因素(HR:1.10,95%CI:1.01~1.20,P < 0.05),提示LAD越大,CRT术后预后越差。
本研究观察到CRT术后肺动脉高压组患者PASP下降,证明CRT可以降低PASP,但是术前PASP升高的患者预后仍较差,这提示应该对符合CRT植入术标准的患者尽早植入CRT,如果患者进一步发展成肺动脉高压,则术后获益有限。
本研究的主要局限性是单中心研究,且样本量较少,有些患者由于随访资料不全没有纳入研究,可能会出现偏倚;另外,本研究为回顾性研究,缺少对照组,且随访时间较短,仍需多中心、前瞻性研究进一步验证本研究结论。
综上所述,CRT术后,与非肺动脉高压组相比,肺动脉高压组逆转左室重构的效应明显减低;术前PASP不能预测CRT有反应,但是PASP≤35 mmHg对CRT超反应有预测价值;CRT术后3年肺动脉高压组复合终点事件(心衰再入院或全因死亡)发生率高于非肺动脉高压组;肺动脉高压、LAD是影响CRT术后预后的独立危险因素。
| [1] | CLELAND J G, DAUBERT J C, ERDMANN E, et al. The effect of cardiac resynchronization on morbidity and mortality in heart failure[J]. N Engl J Med, 2005, 352(15): 1539–1549. DOI:10.1056/NEJMoa050496 |
| [2] | BRISTOW M R, SAXON L A, BOEHMER J, et al. Cardiac-resynchronization therapy with or without an implantable defibrillator in advanced chronic heart failure[J]. N Engl J Med, 2004, 350(21): 2140–2150. DOI:10.1056/NEJMoa032423 |
| [3] | ABRAHAM W T, FISHER W G, SMITH A L, et al. Cardiac resynchronization in chronic heart failure[J]. N Engl J Med, 2002, 346(24): 1845–1853. DOI:10.1056/NEJMoa013168 |
| [4] | ELLENBOGEN K A, HUIZAR J F. Foreseeing super-response to cardiac resynchronization therapy: a perspective for clinicians[J]. J Am Coll Cardiol, 2012, 59(25): 2374–2377. DOI:10.1016/j.jacc.2011.11.074 |
| [5] | GOLDENBERG I, MOSS A J, HALL W J, et al. Predictors of response to cardiac resynchronization therapy in the Multicenter Automatic Defibrillator Implantation Trial with Cardiac Resynchronization Therapy (MADIT-CRT)[J]. Circulation, 2011, 124(14): 1527–1536. DOI:10.1161/CIRCULATIONAHA.110.014324 |
| [6] | KILLU A M, GRUPPER A, FRIEDMAN P A, et al. Predictors and outcomes of "super-response" to cardiac resynchronization therapy[J]. J Card Fail, 2014, 20(6): 379–386. DOI:10.1016/j.cardfail.2014.03.001 |
| [7] | GUAZZI M, BORLAUG B A. Pulmonary hypertension due to left heart disease[J]. Circulation, 2012, 126(8): 975–990. DOI:10.1161/CIRCULATIONAHA.111.085761 |
| [8] | SZWEJKOWSKI B R, ELDER D H J, SHEARER F, et al. Pulmonary hypertension predicts all-cause mortality in patients with heart failure: a retrospective cohort study[J]. Eur J Heart Fail, 2012, 14(2): 162–167. DOI:10.1093/eurjhf/hfr159 |
| [9] | PONIKOWSKI P, VOORS A A, ANKER S D, et al. 2016 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure[J]. Rev Esp Cardiol (Engl Ed), 2016, 69(12): 1167. DOI:10.1016/j.rec.2016.11.005 |
| [10] | CURRIE P J, SEWARD J B, CHAN K L, et al. Continuous wave doppler determination of right ventricular pressure: a simultaneous doppler-catheterization study in 127 patients[J]. J Am Coll Cardiol, 1985, 6(4): 750–756. DOI:10.1016/s0735-1097(85)80477-0 |
| [11] | SHALABY A, VOIGT A, EL-SAED A, et al. Usefulness of pulmonary artery pressure by echocardiography to predict outcome in patients receiving cardiac resynchronization therapy heart failure[J]. Am J Cardiol, 2008, 101(2): 238–241. DOI:10.1016/j.amjcard.2007.07.064 |
| [12] | GASPARINI M, REGOLI F, CERIOTTI C, et al. Remission of left ventricular systolic dysfunction and of heart failure symptoms after cardiac resynchronization therapy: temporal pattern and clinical predictors[J]. Am Heart J, 2008, 155(3): 507–514. DOI:10.1016/j.ahj.2007.10.028 |
| [13] | HOLZMEISTER J, LECLERCQ C. Implantable cardioverter defibrillators and cardiac resynchronisation therapy[J]. Lancet, 2011, 378(9792): 722–730. DOI:10.1016/S0140-6736(11)61228-2 |
| [14] | GALIÈ N, HUMBERT M, VACHIERY J L, et al. 2015 ESC/ERS guidelines for the diagnosis and treatment of pulmonary hypertension: the joint task force for the diagnosis and treatment of pulmonary hypertension of the european society of cardiology (ESC) and the european respiratory society (ERS): endorsed by: association for european paediatric and congenital cardiology (AEPC), International society for heart and lung transplantation (ISHLT)[J]. Eur Respir J, 2015, 46(4): 903–975. DOI:10.1183/13993003.01032-2015 |
| [15] | WANG J, SU Y, BAI J, et al. Elevated pulmonary artery pressure predicts poor outcome after cardiac resynchronization therapy[J]. J Interv Card Electrophysiol, 2014, 40(2): 171–178. DOI:10.1007/s10840-014-9890-2 |
| [16] | STERN J, HEIST E K, MURRAY L, et al. Elevated estimated pulmonary artery systolic pressure is associated with an adverse clinical outcome in patients receiving cardiac resynchronization therapy[J]. Pacing Clin Electrophysiol, 2007, 30(5): 603–607. DOI:10.1111/j.1540-8159.2007.00719.x |
| [17] | CHATTERJEE N A, UPADHYAY G A, SINGAL G, et al. Pre-capillary pulmonary hypertension and right ventricular dilation predict clinical outcome in cardiac resynchronization therapy[J]. JACC Heart Fail, 2014, 2(3): 230–237. DOI:10.1016/j.jchf.2014.02.004 |
| [18] |
汪菁峰, 秦胜梅, 宿燕岗, 等. 肺动脉压力与心脏再同步化治疗疗效的相关性研究[J].
中国心脏起搏与心电生理杂志, 2013, 27(6): 507–510.
WANG J F, QIN S M, SU Y G, et al. Associations between pulmonary artery systolic pressure and clinical outcome of cardiac resynchronization therapy[J]. Chin J Cardiac Pacing Electrophysiol, 2013, 27(6): 507–510. DOI:10.7695/zgxzqb201306010 |
| [19] | WANG D, HAN Y, ZANG H, et al. Prognostic effects of pulmonary hypertension in patients undergoing cardiac resynchronization therapy[J]. J Thorac Dis, 2010, 2(2): 71–75. DOI:10.1136/hrt.2010.208967.553 |
| [20] |
刘丹, 吴冬燕, 许静. 心脏再同步化治疗超反应患者临床特征分析[J].
临床心血管病杂志, 2016, 32(11): 1087–1091.
LIU D, WU D Y, XU J. Research of clinical characteristics of super-responders to cardiac resynchronization therapy[J]. J Clin Cardiol, 2016, 32(11): 1087–1091. DOI:10.13201/j.issn.1001-1439.2016.11.005 |
| [21] | REANT P, ZAROUI A, DONAL E, et al. Identification and characterization of super-responders after cardiac resynchronization therapy[J]. Am J Cardiol, 2010, 105(9): 1327–1335. DOI:10.1016/j.amjcard.2009.12.058 |
| [22] | STEFAN L, SEDLÁ ČEK K, ČERNÁ D, et al. Small left atrium and mild mitral regurgitation predict super-response to cardiac resynchronization therapy[J]. Europace, 2012, 14(11): 1608–1614. DOI:10.1093/europace/eus075 |



