心脏瓣膜病因其病史较长,术中体外循环时间及主动脉阻断时间较单纯冠脉搭桥长,心肌受损较重,加之术前易合并房颤以及其他脏器功能不全,是术后出现药物难以矫治的低心排血量综合征(low cardiac output syndrome,LCOS)而致术后早期死亡的重要原因。而主动脉内球囊反搏(intra-aortic balloon pump,IABP)是目前较为广泛应用的左心室辅助装置,对IABP的远期效果目前仍存在争议,而且国内外大部分的研究集中于冠心病相关的心脏疾病使用IABP的疗效,对于瓣膜疾病相关的心功能不全时IABP的疗效尚未深入探讨[1]。本研究采用回顾性病例对照研究,分析IABP用于瓣膜置换术患者的置入时机、术后心功能恢复、术后并发症和病死率等,探讨IABP对于瓣膜术后LCOS的临床疗效。
1 资料与方法 1.1 一般资料本研究选取2015-2017年陆军军医大学(第三军医大学)第二附属医院全军心血管外科研究所围手术期使用IABP的患者。排除病史资料不齐、先心病患者、冠心病搭桥患者以及单纯主动脉夹层的患者,纳入瓣膜置换术患者共98例,其中行单纯二尖瓣置换27例,单纯主动脉瓣置换18例,行双瓣置换术53例。死亡20例。最终排除死亡患者后,对78例患者资料进行统计分析。
1.2 手术及麻醉方法所有患者均在气管插管、全身麻醉下行胸部正中切口,常规建立体外循环,浅低温阻断主动脉心脏停搏下完成瓣膜置换手术,均为常规的二尖瓣置换、主动脉瓣置换或是双瓣置换术。
1.3 主动脉内球囊反搏置入术前患者心功能差以及术中复跳后体外循环无法停机的患者术中置入IABP的34例,术后早期因各种原因引起的药物难以纠正的LCOS而置入IABP的44例。常规选择右侧股动脉经皮穿刺术。根据患者身高选择合适的球囊导管(身高<158 cm选择34号双腔导管,身高>162 cm选择40号双腔导管),以患者胸骨角经脐至穿刺点的距离来估算导管置入深度,置入球囊导管后,连接IABP装置。预防性置入组术中食道超声评估确认球囊位置,球囊尖端应位于降主动脉下锁骨远端开口以下2 cm,术中及术后返回ICU途中使用压力触发,回ICU后改为心电触发,开始均按1 :1反搏。治疗性置入组ICU床旁置入IABP后选择心电触发,按1 :1反搏,床旁胸片检查确认球囊位置。常规给予每30分钟肝素盐水(500 U/500 mL)冲管直至停机。
1.4 统计学分析首先将所选患者按照IABP置入时机不同分为预防性置入组与治疗性置入组。预防性治疗组患者IABP于术中置入,而治疗性置入组的IABP是于术后早期置入。我们将死亡患者剔除后,比较两组患者术前各项指标以及术后早期恢复情况。采用SPSS 25.0统计学软件,对各组的数据采用单因素方差分析、独立样本t检验以及χ2检验进行分析,检验水准:α=0.05。
2 结果 2.1 两组患者术前一般情况比较结果两组患者术前一般情况差异无统计学意义(P>0.05,表 1、2),而治疗性置入组术前合并房颤者较多。预防性置入组患者术前心功能较差,术前血清B型尿钠肽(brain natriuretic peptide,BNP)水平较高。分析患者术中的情况,发现预防性置入组的转流时间较长,差异有统计学意义(P=0.009,表 3)。
| 组别 | n | 性别(男/女) | 年龄/岁 | 体质量/kg | BMI/kg·m-2 | 高血压 | 糖尿病 | 吸烟史 | 手术史 |
| 预防性置入组 | 34 | 24(70.59)/10(29.41) | 50.65±8.82 | 59.64±10.61 | 22.53±3.55 | 6(17.65) | 2(5.89) | 13(38.24) | 4(11.76) |
| 治疗性置入组 | 44 | 20(45.45)/24(54.55) | 53.68±9.54 | 56.75±11.02 | 22.28±4.53 | 5(11.36) | 1(2.27) | 12(27.27) | 3(6.82) |
| 组别 | n | 房颤/例 (%) |
心脏超声(x±s) | NYHA心功能分级/例 | 术前血清BNP/pg·mL-1 (x±s) | |||||||
| LA/mm | LV/mm | LVFS/% | LVEF/% | Ⅰ | Ⅱ | Ⅲ | Ⅳ | |||||
| 预防性置入组 | 34 | 5(14.71) | 47.63±8.51 | 65.04±13.88 | 24.01±7.75 | 46.13±12.83 | 0 | 6 | 9 | 19 | 1172.18±1301.02 | |
| 治理性置入组 | 44 | 23(52.27) | 51.48±9.01 | 54.45±12.24 | 31.53±7.52 | 58.33±11.69 | 0 | 5 | 30 | 9 | 727.54±835.53 | |
| P值 | 0.001 | 0.059 | 0.001 | <0.001 | <0.001 | 0.001 | 0.014 | |||||
| NYHA:纽约心脏病协会 | ||||||||||||
| 组别 | n | 转流时间/min | 阻断时间/min | 术中出血/mL | 电击复跳 | 起搏器使用 |
| 预防性置入组 | 34 | 166.76±62.56 | 102.56±45.75 | 410.88±172.51 | 10(29.41) | 18(52.94) |
| 治疗性置入组 | 44 | 133.18±40.57 | 91.64±31.66 | 452.68±466.77 | 7(15.91) | 19(43.18) |
| P值 | 0.009 | 0.239 | 0.621 | 0.152 | 0.392 |
2.2 两组患者术后短期心功能相关指标分析
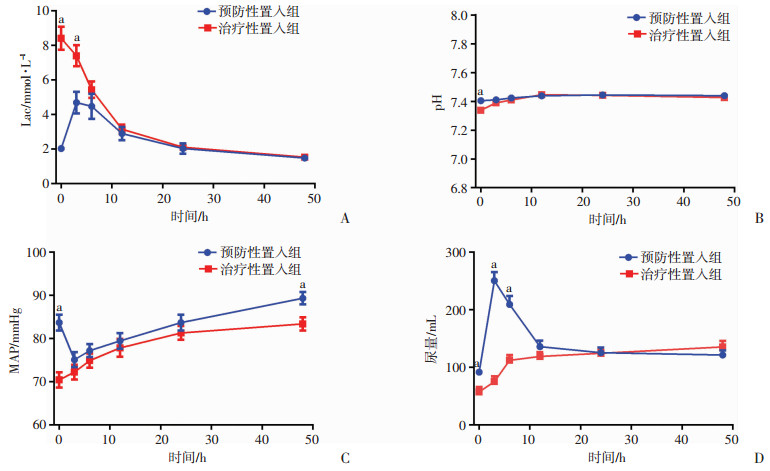
统计患者IABP置入后0、3、6、12、24、48 h的乳酸(Lac)、pH值、平均动脉压(MAP)及尿量,其中0 h以置入IABP前的最后一个血气时间为准。预防性置入IABP患者术后Lac值在0、3 h较治疗性置入组明显较低,差异具有统计学意义(P<0.05,图 1A);预防性置入组pH值及MAP在置入时的0 h较治疗性置入组明显较高,并且MAP在预防性置入组第48小时较治疗性置入组明显较高(图 1B、C);预防性置入组尿量在0、3、6 h较治疗性置入组明显较高,差异具有统计学意义(P<0.05,图 1D)。
|
| a:P<0.05, 与治疗性置入组比较 图 1 术后早期两组患者Lac(A)、pH(B)、MAP(C)及尿量(D)48 h内的变化 |
2.3 主动脉内球囊反搏置入时机两组患者术后早期恢复情况
预防性置入组的有创呼吸机时间较治疗性置入组明显减少(P=0.001),ICU的住院时间明显缩短(P<0.001,表 4)。
| 组别 | n | 有创呼吸机辅助时间/h | 无创呼吸机辅助时间/h | IABP使用时间/h | 住院时间/d | ICU时间/d | 术后LA/mm | 术后LV/mm | 术后LVFS/% | 术后LVEF/% |
| 预防性置入组 | 34 | 48.82±15.00 | 15.01±20.88 | 90.06±27.35 | 26.09±8.73 | 5.62±1.67 | 38.25±5.76 | 54.22±10.52 | 29.59±7.19 | 55.11±10.63 |
| 治疗性置入组 | 44 | 85.18±62.60 | 30.05±53.44 | 109.66±47.7 | 26.59±7.05 | 8.05±3.27 | 39.35±6.30 | 48.94±7.03 | 32.42±6.23 | 59.75±10.01 |
| P值 | 0.001 | 0.095 | 0.054 | 0.779 | <0.001 | 0.432 | 0.014 | 0.067 | 0.052 |
2.4 两组死亡患者讨论分析
预防性置入IABP的患者中死亡7例(17.07%),其中3例(7.32%)死于术后短期无法纠正的顽固性LCOS,2例(4.88%)死于恶性心律失常,2例(4.88%)死于术中。治疗性置入IABP的患者中死亡13例(22.81%),其中2例(3.51%)死于术后短期无法纠正的顽固性LCOS,2例(3.51%)严重肺部感染,4例(7.02%)死于多器官功能衰竭,5例(8.77%)死于恶性心律失常。78例患者中1例出现短期下肢动脉血栓,经治疗后痊愈出院。
3 讨论 3.1 瓣膜手术围手术期低心输出量综合征多种原因可导致瓣膜疾病患者尤其是重症瓣膜疾病患者在行瓣膜置换术后围手术期内发生LCOS[2-3],如自身心功能受损较重、心肌肥厚、心脏严重扩大和术中体外循环损伤、术中心肌保护不当、排气不充分等因素。而普通的强心利尿等药物治疗措施对于该情况的发生也收效甚微。IABP作为目前临床上较常使用的左心系统循环辅助装置,在心脏术后发生药物无法纠正的LCOS中起到了重要的作用[4]。IABP的球囊位于降主动脉,球囊在心脏舒张期充气膨胀而在心脏收缩期排气,以减轻左室后负荷同时增加了冠脉供血。不同患者基础心输出量不同,IABP可增加左室近40 mL的每搏量,心输出量可增至1 L/min(提高15%~30%)。但同时IABP的长期使用也会增加并发症的风险,如肢体缺血、血栓形成、感染以及血小板破坏等[1]。
尽管治疗性置入组患者术前心功能明显较好,但该组的死亡率明显较高。且治疗性置入组患者多器官功能障碍及严重肺部感染较多,这与IABP置入时机的选取是否也存在一定的关联,如何在有效地辅助左心功能的同时,减少并发症的发生率以及降低死亡率,需要我们对IABP置入时机进一步进行深入探讨。
3.2 早期应用主动脉内球囊反搏辅助支持可明显改善术后早期患者心功能的恢复瓣膜疾病尤其是联合瓣膜病变的病理生理发展过程十分复杂。我们对于术前巨大左室、心功能较差及术中发现左室功能较差、手术时间长、术后出现LCOS概率大的选择预防性置入IABP,尤其是严重主动脉瓣疾病的患者和较复杂的联合病变患者,更应该预防性置入IABP。从本组患者术后早期心功能的恢复中可以看出,预防性置入组与治疗性置入组术后早期心功能无明显统计学差异,而术前血清BNP及心功能检查结果提示预防性置入组明显较差,说明预防性置入IABP可使术前心功能较差的患者术后心功能得到显著的提高。
3.3 围手术期早期应用主动脉内球囊反搏辅助支持维持重症瓣膜病患者术后早期循环稳定术后早期的Lac、pH、MAP及尿量可综合反映患者术后早期心功能的水平[5-6],从本组患者数据中可以看出术中预防性置入IABP的患者术后早期的Lac、pH、MAP较为平稳,且术后48 h的MAP恢复较术后治疗性置入IABP组好;预防性置入IABP患者术后早期未出现因心功能受损的尿量减少,这些结果综合反映了预防性置入IABP可维持术后早期心功能的相对平稳,并且可以维持一定的循环稳定从而减少肾功能损伤。术后有创呼吸机使用时间、IABP使用时间及ICU住院时间术后治疗性置入IABP组是明显增加的,有创呼吸机时间延长会大大增加呼吸机相关肺炎的发生率,也是ICU住院时间延长的重要因素[7]。此外,IABP使用时间的延长也增加了IABP并发症发生的可能。由此可见,对重症瓣膜病患者尽早IABP干预能有效地恢复患者早期心功能,减少有创呼吸机使用时间及IABP使用时间,可尽量减少其他系统并发症及IABP使用相关并发症的发生。
3.4 主动脉内球囊反搏置入时机的思考本研究对术前心功能较差的患者在术中预防性置入IABP,以预防术后LCOS的发生。同时发现术后置入IABP的患者术前左房较大以及有房颤病史的比例是明显增加的。房颤作为临床上十分常见的心律失常,对患者血流动力学及凝血系统都产生重要的影响[8-9]。而术后心律失常可能导致的血流动力学不稳定也是IABP置入的一个重要的参考指征。对于合并房颤的瓣膜疾病患者,IABP置入的时机与指征是否应适当放宽,我们将在后续的工作中进行进一步的研究。
综上所述,IABP作为广泛应用的左心辅助装置,不仅对冠脉疾病相关的LCOS疗效显著,对于瓣膜疾病围手术期出现药物无法纠正的LCOS的预防和治疗也有显著的作用,并且对于术前合并较大左室、左心功能差、术中手术难度大、合并房颤的高危瓣膜病患者可考虑术中预防性置入IABP,以求达到满意的效果。
| [1] | WERDAN K, GIELEN S, EBELT H, et al. Mechanical circulatory support in cardiogenic shock[J]. Eur Heat J, 2014, 35(3): 156–167. DOI:10.1093/eurheartj/eht248 |
| [2] |
中国医师协会心脏重症专家委员会. LCOS血量综合征中国专家共识[J].
解放军医学杂志, 2017, 42(11): 933–944.
Chinese Medical Doctor Association Cardiac Critical Expert Committee. The Chinese expert consensus on the low cardiac output syndrome[J]. Med J Chin PLA, 2017, 42(11): 933–944. DOI:10.11855/j.issn.0577-7402.2017.11.01 |
| [3] | THIELE H, OHMAN E M, DESCH S, et al. Management of cardiogenic shock[J]. Eur Heat J, 2015, 36(20): 1223–1230. DOI:10.1093/eurheartj/ehv051 |
| [4] |
熊健宪, 李文通. 28例瓣膜置换术后顽固性LCOS应用IABP的临床分析[J].
赣南医学院学报, 2014(2): 183–185.
XIONG J X, LI W T. The therapy of low cardiac output syndrome (LCOS) after cardiac valve replacement with application of the Intra-aortic balloon pump (IABP)[J]. J Gannan Med Univ, 2014(2): 183–185. |
| [5] | ANDERSEN L W, HOLMBERG M J, DOHERTY M, et al. Postoperative lactate levels and hospital length of stay after cardiac surgery[J]. J Cardiothorac Vasc Anesth, 2015, 29(6): 1454–1460. DOI:10.1053/j.jvca.2015.06.007 |
| [6] | PARK S J, KIM J B, JUNG S H, et al. Outcomes of extracorporeal life support for low cardiac output syndrome after major cardiac surgery[J]. J Thorac Cardiov Surg, 2014, 147(1): 283–289. DOI:10.1016/j.jtcvs.2012.11.006 |
| [7] | DAMAS P, FRIPPIAT F, ANCION A, et al. Prevention of ventilator-associated pneumonia and ventilator-associated conditions:a randomized controlled trial with subglottic secretion suctioning[J]. Crit Care Med, 2015, 43(1): 22–30. DOI:10.1097/CCM.0000000000000674 |
| [8] | STAERK L, SHERER J A, KO D, et al. Atrial fibrillation:epidemiology, pathophysiology, and clinical outcomes[J]. Circ Res, 2017, 120(9): 1501–1517. DOI:10.1161/CIRCRESAHA.117.309732 |
| [9] | HEIJMAN J, GUICHARD J B, DOBREV D, et al. Translational challenges in atrial fibrillation[J]. Circ Res, 2018, 122(5): 752–773. DOI:10.1161/CIRCRESAHA.117.311081 |



