2. 610072 成都,四川省医学科学院·四川省人民医院皮肤科
2. Department of Dermatology, Sichuan Academy of Medical Science & Sichuan Provincial People' Hospital, Chengdu, Sichuan Province, 610072, China
隆突性皮肤纤维肉瘤(dermatofibrosarcoma protuberans,DFSP)是真皮及皮下组织的低度恶性肉瘤,临床表现为结节状皮肤肿物,生长缓慢,具有局部侵袭性,极易原位复发却很少远处转移。通常发生在成年人,最常见于躯干、肢体近端、头颈部、乳腺等部位[1, 2]。DFSP呈局部侵袭性生长,因此肿瘤边界的术前确定非常重要。有文献报道DFSP单纯局部肿块切除术后肿瘤复发率高达50%~70%[3],为减少术后复发,本研究拟利用超声造影(contrast-enhanced ultrasound, CEUS)对DFSP进行成像,探讨其造影特征和CEUS对提高手术切除精度的价值。
1 资料与方法 1.1 研究对象收集2016年10月至2017年12月于四川省人民医院皮肤科门诊因体表包块就诊并行传统超声及CEUS检查, 病灶经穿刺活检和手术切除后得到病理结果的DFSP患者共23名(23个病例),其中男性9名,女性14名,年龄17~76岁(40.7±11.5)岁。23例DFSP均为单发,发生于躯干15例,上臂及后枕部各2例,乳腺4例。病变均位于皮肤及皮下组织,最大直径1.0~5.8 cm,平均(3.85±1.82)cm;19例为原发,4例为术后原位复发。纳入标准:体格检查发现皮肤病灶, 最终经穿刺或手术取得病理和免疫组化诊断。排除标准:直径<1.0 cm,>8.0 cm的病灶;有造影剂过敏史等严重CEUS禁忌证的患者;病灶未能获得病理及免疫组化诊断;病灶切除后病理发现切缘及基底缘存在残余瘤细胞需再次手术者。
1.2 仪器与方法23个DFSP病例,由我院皮肤科医师首诊后对病灶行经皮穿刺活检,得到病理诊断结果为DFSP。
术前采用GE Logiq E9彩色多普勒超声诊断仪,高频线阵探头9L(频率9 MHz),造影剂采用Bracco SonoVue(主要成分为六氟化硫),部分病灶过于靠近皮肤表面时使用超声垫。选用浅表组织条件设置,用传统超声依次观察病变部位、边界、内部回声、与皮肤层次的关系、病灶内部及周缘血流情况;在最大长轴切面上(一般均要显示部分周围正常组织作对照)冻结分别测量病灶的长、宽(cm), 在最大短轴切面上冻结测量病灶的厚(cm),每一病灶分别测量3次,取平均值为最终结果。随即切换至造影模式,MI:0.05,经肘正中静脉快速团注法注射造影剂2.4 mL尾随5 mL生理盐水冲洗。观察DFSP内造影剂灌注过程,待肿瘤轮廓清晰显示至最大时选择最大长轴切面测量其长、宽(cm),最大短轴切面测量其厚值(cm),同样每一病灶分别测量3次,取平均值为最终结果。储存动态图像及数据120 s,记录时间3 min。以上操作由2名具备3年以上CEUS和皮肤超声检查经验的医师进行。23例病灶于CEUS后第2天行手术切除,切除范围参考CEUS测量结果,术后病理证实为完整的包膜切除且切缘阴性,术前传统超声测量大小和CEUS测量大小分别与术后的病理切除大小相比较。
所有操作患者均知情同意并获得医院伦理委员会认可。
1.3 统计学分析应用SPSS 20.0进行统计学分析。计量资料采用x±s表示, 采用独立样本t检验比较术后病理和传统超声,术后病理和CEUS的测量结果的差值,以P<0.05为差异有统计学意义。
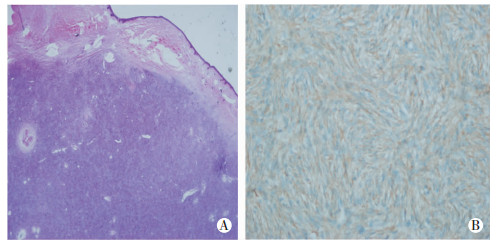
2 结果 2.1 DFSP的传统超声和CEUS表现23例经病理和免疫组化证实为DFSP的病灶(图 1),在二维声像图上表现为皮肤层和皮下组织内边界欠清的低回声灶,形态较规则,内部回声欠均匀;彩色多普勒超声显示病灶周边及内部丰富的血流信号(图 2)。
|
| A:术后病理切片(HE染色,400×);B:术后免疫组化,CD34强阳性 图 1 26岁女性患者,左乳上象限皮肤层内结节,术后病理结果 |
|
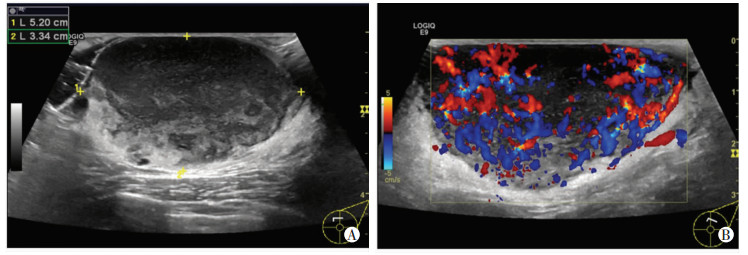
| A:二维图像示一大小约5.20 cm×3.34 cm低回声结节位于真皮和皮下组织;B:彩色多普勒示结节周边及内部丰富的血流信号 图 2 同一患者的传统超声图像 |
23例DFSP的CEUS灌注特点如下:与周围正常皮下组织的增强时间对照,造影剂整体呈现出快进慢退,即“速升缓降”型。其中17例(73.9%)表现为快进弥漫性均匀性高增强(图 3);4例(17.4%)为快进弥漫性非均匀性高增强,内部伴充盈缺损;2例(8.7%)为快进均匀性等增强。增强后肿瘤边界清晰,形态较规则,范围均增大,3例病灶内出现增强后周边血管的穿入支。
|
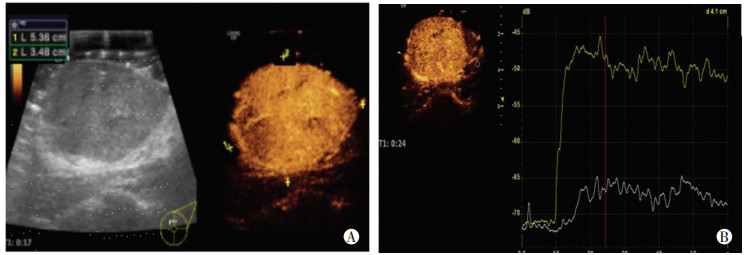
| A:造影后病灶轮廓更加清晰,大小测量较二维增大(5.36 cm×3.48 cm);B:与周围组织相比,病灶呈快进均匀性高增强,造影剂缓慢廓清 图 3 同一患者术前超声造影图像 |
2.2 传统超声和CEUS测量与术后病理测量结果的比较
23例病灶切除范围参考CEUS的测量结果被完整切除,术后病理显示标本四周切缘及基底缘为完整的包膜切除无残余瘤细胞。以病理测量结果为“金标准”,用独立样本t检验比较传统超声与病理测量值的差值和CEUS与病理测量值的差值。经统计分析,长、宽、厚三个差值的比较差异均具有统计学意义(P<0.05),较于传统超声,CEUS与病理的测量差距更接近(表 1)。
| 指标 | 测量值差 | n | 差值 | t值 | P值 |
| 长度 | 病理测量-CEUS测 | 23 | 0.72±0.18 | -3.486 | 0.001 |
| 病理测量-二维测量 | 23 | 0.96±0.28 | |||
| 宽度 | 病理测量-CEUS测量 | 23 | 0.30±0.13 | -8.319 | 0.000 |
| 病理测量-二维测 | 23 | 0.86±0.29 | |||
| 厚度 | 病理测量-CEUS测 | 23 | 0.17±0.10 | -3.726 | 0.001 |
| 病理测量-二维测 | 23 | 0.33±0.17 |
3 讨论
近年来,CEUS已广泛应用于评估各类皮肤软组织肿瘤的良、恶性, 对于此类肿瘤的诊断和鉴别诊断具有重要的价值[4-5]。本研究发现大多数(17/23)DFSP的CEUS增强特征呈快进弥漫性均匀性高增强,且造影后病灶范围扩大。由此推论DFSP为富血供类皮肤软组织肿瘤,其周缘和内部具有丰富的微循环,此造影特征和增强表现也与肿瘤呈“蟹足样”侵袭性生长方式密切相关[6]。本研究有4例(4/23)的CEUS表现为快进弥漫性非均匀性高增强,内部伴有充盈缺损,术后病理证实为肿瘤内部的出血坏死区,此声像在传统超声中未被发现。4例伴有坏死区的DFSP中有2例(2/4)为原位复发性DFSP,说明CEUS对发现肿瘤内部的液化坏死优于传统超声;同时结合术后的病理诊断结果发现2例复发性DFSP恶性程度明显增加、分化程度差,出血、坏死、黏液变性现象更严重。23例DFSP中有3例病灶内出现增强后周边血管的穿入支,后证实均为原位复发的病灶,此结果说明复发病灶周边有大的滋养血管生成。由于首次手术的切除不尽,残存的瘤细胞不断增殖扩散而在原位形成复发性DFSP,其周边的新生血管生成现象较之前更加显著。因此在临床诊断工作中结合患者的DFSP病史,在二维及彩色多普勒超声检查的基础上,利用CEUS增强后肿瘤内部伴充盈缺损,出现周边血管的穿入支,病灶范围扩大等特征,可以对原位复发性DFSP提供一个明确的诊断。此外,穿刺前的CEUS可以提供有价值的信息,如在术前穿刺活检中,利用肿瘤造影增强后的表现有效避开局部坏死区进行穿刺,还可以明显提高穿刺活检的阳性率。
由于DFSP的侵袭性生长,其周缘存在大量的新生血管,故利用传统超声无法识别肿瘤周缘的微循环,也无法准确测量其边界;即使行广泛切除术后,仍有局部复发可能性,这也很好地解释了DFSP手术切除后复发率较高的特点。据相关文献报道并结合本研究的病理诊断发现,随着复发次数增多,手术切除次数增多,肿瘤细胞可发生分化、异型性增加,其恶性度、侵袭性、远端转移率也随之增高[7]。同时,外科切除DFSP,切缘通常为2~3 cm[8],过大范围的手术可导致大量正常组织被不必要地切除,甚至可导致外观残缺或功能丧失。因此,如何精确地对DFSP的边界进行术前评估,达到既彻底清除肿瘤切缘残余瘤细胞,又可以保留更多的健康组织,是手术治疗和减少复发的首要任务。MA等[9]首次应用CEUS测量1例DFSP患者的皮损大小,手术切除后冷冻切片病理检查,病理检查提示与CEUS测得大小基本相同且手术切缘周围未见肿瘤累及。本研究将传统超声和CEUS测量DFSP的长、宽、厚值与病理测量值的差值进行比较分析,得到两者的差异均具有统计学意义,同时CEUS增强后的测量值与病理的测量差距更小,说明CEUS与病理的结果更接近,更精确地显示肿瘤的实际边界和肿瘤周边的微血管灌注范围进一步论证了术前利用CEUS评估DFSP手术切缘的可行性和应用价值。
本研究同时也存在不足,如纳入的病例还较少,CEUS是否能精确地对DFSP进行术前评估,进而有效避免二次手术还需长期大样本量的研究和对病人进行跟踪随访。此外,超声与MRI成像各有优势及不足,两者对DFSP术前评估的比较影像学研究可进一步深入。
综上所述,CEUS可显示DFSP内部及周缘丰富的微循环,还可清晰显示造影后恶性肿瘤扩大的边缘,与传统超声相比,CEUS测量结果与术后病理的测量结果更接近。因此利用CEUS对于提高DFSP的手术切除精度具有重要的辅助价值。
| [1] | BICHAKJIAN C K, OLENCKI T, ALAM M, et al. Dermatofibrosarcoma protuberans, version 1.2014[J]. J Natl Compr Canc Netw, 2014, 12(6): 863–868. DOI:10.6004/jnccn.2014.0081 |
| [2] | ZHENG Z, PIAO J, LEE J H, et al. Dermatofibrosarcoma protuberans: a study of clinical, pathologic, genetic, and therapeutic features in Korean patients[J]. Yonsei Med J, 2015, 56(2): 440–446. DOI:10.3349/ymj.2015.56.2.440 |
| [3] | BAGUE S, FOLPE A L. Dermatofibrosarcoma protuberans presenting as a subcutaneous mass: A clinicopathological study of 15 cases with exclusive or near-exclusive subcutaneous involvement[J]. Am J Dermatopathol, 2008, 30(4): 327–332. DOI:10.1097/dad.0b013e31817d32b2 |
| [4] | KLEINERMAN R, WHANG T B, BARD R L, et al. Ultrasound in dermatology: principles and applications[J]. J Am Acad Dermatol, 2012, 67(3): 478–487. DOI:10.1016/j.jaad.2011.12.016 |
| [5] |
杜燕然, 陈曼. 超声造影在乳腺小肿块诊断中的应用[J].
中国超声医学杂志, 2016, 32(6): 500–502.
DU Y R, CHEN M. Application of contrast-enhanced ultrasound in diagnosis of small breast lesions[J]. Chin J Ultrasound Med, 2016, 32(6): 500–502. DOI:10.3969/j.issn.1002-0101.2016.06.008 |
| [6] |
王坚, 朱雄增. 2013版WHO软组织肿瘤新分类解读[J].
中华病理学杂志, 2013, 42(006): 363–365.
WANG J, ZHU X Z. Interpretation of the new classification of WHO soft tissue tumors in 2013[J]. Chin J Pathol, 2013, 42(006): 363–365. |
| [7] | SANMARTíN O, LLOMBART B, LóPEZ-GUERRERO J A, et al. Dermatofibrosarcoma protuberans[J]. Actas Dermosifiliogr, 2007, 98(2): 77–87. DOI:10.1016/s1578-2190(07)70400-6 |
| [8] | BOGUCKI B, NEUHAUS I, HURST E A. Dermatofibrosarcoma protuberans: a review of the literature[J]. Dermatol Surg, 2012, 38(4): 537–551. DOI:10.1111/j.1524-4725.2011.02292.x |
| [9] | MA C, SUN Y, YANG X, et al. Improving precision of resection by pre-surgery inspections with contrast-enhanced ultrasound for dermatofibrosarcoma protuberans[J]. Dermatol Ther, 2016, 29(6): 473–475. DOI:10.1111/dth.12401 |



