硅橡胶(silicone rubber, SR)因其稳定的理化特性、生物惰性、易加工和耐腐蚀性成为整形外科中常用的填充材料。然而, 硅橡胶具有强烈的疏水性, 与组织细胞的相容性较差, 易导致植入材料区域形成包膜, 长此以往包膜易出现挛缩畸形等问题; 同时硅橡胶材料不具备抗菌性, 使其存在较大感染风险。已有不少研究通过对材料表面改性从而优化材料的表面性能。表面处理技术在制备具有良好生物相容性的医用生物材料方面具有代价小、耗时少等优势[1]。尤其是离子注入技术, 它不影响基体材料的力学性能, 注入层和基体无明显界限。为了探究离子注入对硅橡胶材料的影响, 课题组前期采用构成人体生命基本元素的碳元素, 以碳离子注入方式对硅橡胶进行了改性处理, 结果显示其亲疏水性及生物相容性显著提升[2]。但是其他离子如氮离子和有抗菌功效的银离子, 注入硅橡胶后材料表面的性能相关研究缺乏, 且离子注入硅橡胶对组织周围干细胞的调控作用并不清楚。干细胞作为组织工程的种子细胞, 对其周围环境的变化较为敏感, 影响干细胞生物学行为的因素包括化学因素如可溶性和不可溶性的因子[3-4], 表面化学[5], 物理因素包括基质弹性[6-7]、机械拉力[8]、表面电荷[9]、表面拓扑结构[10-11]等。近年来, 材料与干细胞的相互作用成为研究热点。本研究选用大鼠骨髓间充质干细胞为模式细胞, 通过对普通硅橡胶的表面改性, 研究离子注入后硅橡胶对大鼠骨髓间充质干细胞的粘附、增殖及分化的影响, 以期研发出一种能较好满足临床需求的整形外科填充材料。
1 材料与方法 1.1 材料 1.1.1 实验材料采用双组分医用液体硅橡胶(深圳红叶杰科技有限公司), 按模具制作100 mm×100 mm×1 mm大小的硅橡胶片, 其后硅橡胶片采用核工业西南物理研究院研发的多功能离子注入机向硅橡胶表面注入剂量为1×1016 ions/cm2的碳离子、银离子和氮离子。其后分别标记为C-SR, Ag-SR和N-SR, 普通未注入硅橡胶标记为SR。研究采用8只雄性SD大鼠, 体质量约130 g, 由本院实验动物中心提供, 提取的干细胞后经鉴定合格后选用P2~P5代用于后续实验。
1.1.2 主要试剂与仪器试剂有:α-MEM培养基(HyClone, 美国), 胎牛血清(Gibco, 美国), 胰酶(HyClone, 美国), CCK-8试剂盒(DOJINDO, 日本), Actin-Tracker Green试剂(碧云天, 中国), BSA封闭液(碧云天, 中国), Runx2抗体(博士德生物, 中国), PPAR-γ抗体(博士德生物, 中国), GAPDH抗体(巴傲德生物, 中国)。仪器:全波长多功能酶标仪(Thermo Fisher, 美国), 倒置显微镜(Leica, 德国), 激光共聚焦显微镜(Leica TCS SP5, 德国)。
1.2 实验方法 1.2.1 大鼠骨髓间充质干细胞的制备及原代细胞培养大鼠脱颈处死, 浸入体积分数为75%的乙醇5 min, 无菌条件下取出两侧股骨, 切除股骨两端, 用α-MEM培养基(含10%胎牛血清和1%双抗)从股骨上端向下冲出骨髓, 将悬浮液吸入培养瓶中, 放入37 ℃, 5%CO2培养箱中静置培养。接种24 h后半定量换液, 72 h全量换液, 7~9 d后首次传代, 经鉴定合格后采用2~5代细胞进行实验。
1.2.2 普通光镜下细胞形态观察取SR、C-SR、Ag-SR和N-SR硅橡胶材料铺板于6孔板底, 37 ℃, 5%CO2培养箱静置培养, 于第1、7、14、21、28天在普通光学显微镜下观察细胞粘附, 细胞形态变化。
1.2.3 CCK-8实验将SR、C-SR、Ag-SR和N-SR硅橡胶材料铺板于96孔板底, 取第2代BMSCs以5×104/mL的密度接种于含离子注入硅橡胶96孔板各孔, 各组设5个复孔, 每48小时换液1次, 采用CCK-8法分别检测各组第24、48、72、96小时的细胞增殖情况。
1.2.4 细胞骨架染色实验将SR、C-SR、Ag-SR和N-SR硅橡胶材料铺板于24孔板底, 取第2代BMSCs以5×104/mL的密度接种于含离子注入硅橡胶24孔板各孔。在37 ℃, 5%CO2培养箱中静置培养24、48 h后进行实验, 室温孵育Actin-Tracker Green试剂(1 :100, 碧云天公司, 中国)2 h, Hoechest33342(碧云天公司, 中国)室温下染核5 min。置于激光共聚焦显微镜下观察, 其后采用Image-Pro Plus软件对细胞粘附数目及细胞粘附面积进行半定量分析。
1.2.5 Western blot检测将SR、C-SR、Ag-SR和N-SR硅橡胶材料铺板于6孔板底, 取第2代BMSCs以1×104/mL的密度接种于含普通硅橡胶及离子注入硅橡胶的6孔板。分别于第7、14、21、28天提取细胞总蛋白, 其后进行SDS-PAGE电泳, 转膜, 室温下封闭1.5 h, 4 ℃孵育一抗过夜, 抗体稀释的比例分别是Runx2(1 :100), PPAR-γ(1 :200)以及GAPDH(1 :10 000)。其后二抗孵育2 h, 显影, 采用Image J软件进行分析。
1.3 统计学分析计量数据以x±s形式表示, 采用GraphPad Prism 5进行单因素方差分析, 其后采用LSD法进行两两比较。检验水准:α=0.05。
2 结果 2.1 细胞粘附将BMSCs以1×105/mL接种在各组材料上, 分别在第1、7、14、21天及28 d时观察细胞在材料上的粘附生长情况, 结果见图 1。细胞能较好粘附在各组材料上, 细胞形态均为长梭形或多角形, 伸展较好。离子注入材料上的细胞生长状态与在SR材料上的细胞并无明显差异, 表明离子注入材料对细胞无明显毒性, 不会抑制BMSCs的粘附。

|
| 图 1 大鼠骨髓间充质干细胞在各组材料表面的粘附情况(LM×100) |
2.2 细胞增殖
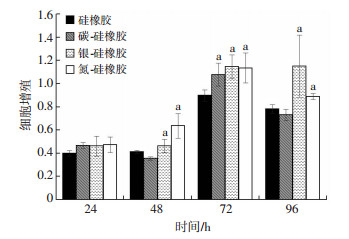
用CCK-8法检测各材料表面细胞增殖情况, 结果如图 2。实验结果显示, 从48 h开始, Ag-SR和N-SR组与SR组细胞增殖差异有统计学意义(P < 0.01)。而C-SR组在24、48 h时, 细胞增殖与SR组比较没有明显差异, 直至72 h时, C-SR组开始对BMSCs的增殖产生明显影响(P < 0.01)。
|
| a: P < 0.01, 与硅橡胶比较 图 2 大鼠骨髓间充质干细胞在各组材料上的增殖情况(n=5, x±s) |
2.3 细胞骨架染色
通过F-actin细胞肌动蛋白微丝染色, 激光共聚焦显微镜下观察细胞骨架变化, 结果见图 3。实验结果显示, SR上细胞内的F-actin呈弥散分布, 很少形成成束的应力纤维, 即使出现应力纤维也显得纤细, 多数应力纤维沿细胞长轴分布。而24 h时, 在Ag-SR组培养的细胞就出现明显成束的应力纤维, 纤维方向沿着细胞长轴分布。

|
| A:大鼠骨髓间充质干细胞在各组材料上的细胞骨架染色观察(激光共聚焦显微镜×400);B:细胞粘附数目比较(n=3, x±s); C:细胞在各组材料上的铺展面积比较(n=3, x±s) a: P < 0.05, 与24 h比较 图 3 激光共聚焦下观察各组材料上间充质的细胞骨架变化 |
N-SR组也出现应力纤维, 纤维较细, 但是没有Ag-SR明显, 其他组材料上则较少应力纤维。到48 h时, N-SR组细胞也出现较明显的成束的应力纤维, 而C-SR还不是很明显。本研究发现, 几乎所有材料上出现明显应力纤维的细胞形状多为多角形, F-actin均匀分布的细胞为长梭形, 这一现象在Ag-SR上尤其明显。通过荧光强弱对比发现, 24 h的细胞骨架染色, SR组细胞的荧光非常弱, 而Ag-SR, N-SR以及C-SR组细胞出现较强的荧光。由此说明, 在SR组细胞F-actin表达较弱, 而改性后的材料更有利于细胞骨架的重组, 进一步影响细胞的粘附或分化。
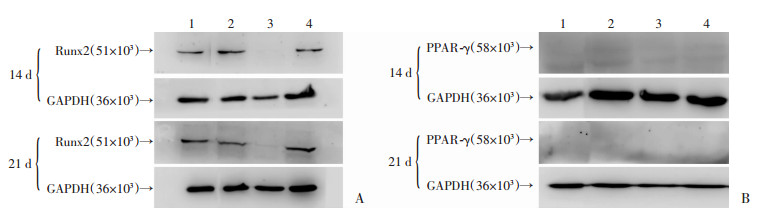
2.4 细胞分化通过将骨髓间充质干细胞在改性材料表面培养7、14、21、28 d后, 提取蛋白质, Western blot检测干细胞成骨和成脂分化指标Runx2、PPAR-γ的表达变化, 实验结果见图 4。结果显示N-SR和C-SR对干细胞成骨有一定的促进作用, 并且不会促进细胞成脂肪分化。
|
| 1:硅橡胶; 2:碳-硅橡胶; 3:银-硅橡胶; 4氮-硅橡胶 图 4 Western blot检测硅橡胶及离子注入硅橡胶上培养的干细胞中Runx2、PPAR-γ表达变化 |
3 讨论
硅橡胶因其独特的生物惰性、易加工成型等特点在临床上各个科室都有广泛应用, 可作为角膜接触眼镜、视网膜植入物应用于眼科, 并可作为人工手指、手掌关节、人工肌腱等在骨科广泛应用, 临床常有的静脉导管、导尿管和腹膜透析管等都是硅橡胶制成[12-13], 在整形修复方面, 更是可以作为软组织填充材料用以修复填充。但是, 硅橡胶由相对分子质量较高的线性聚甲基硅氧烷组成, 分子极性很低, 所以硅橡胶表面具有强烈的疏水性、耐氧化及抗老化性[14]。正是由于硅橡胶表面呈强烈的疏水性, 硅胶假体植入体内后, 周围容易形成纤维包膜, 从而产生包膜挛缩畸形, 则可以通过对硅橡胶表面改性, 提高材料表面亲水性, 改善其组织相容性[15-18]。有研究表明在硅橡胶表面接枝两性离子聚合物, 提高了材料表面的湿润性, 并且显著改善血液相容性[15]。许脉等[16]采用紫外光亲水改性法在硅橡胶表面接枝亲水聚合物PEG1000及表面活性剂OP-10, 发现改性后材料表面亲水性增加, 并且降低了其细菌粘附性。离子注入技术是将电离的原子经电场加速后, 使离子具有较高能量, 轰击材料表面, 引起材料表面结构和成分发生改变并在一定程度上扰动原子环境和电子组态等微观状态, 使材料表面产生纳米级的变化, 此方法相较于等离子体注入、表面接枝改性、仿生涂层等改性方法, 可以精确地控制离子掺杂的深度和浓度[19]。我们前期的实验已经成功地将不同剂量的离子注入硅橡胶, 且发现剂量为1×1016 ions/cm2时, 材料具有较好的细胞相容性。
前期研究表明, 通过碳离子注入改性硅橡胶, 改性后的硅橡胶机械性能并没有改变, 并且具有良好的生物安全性[20]。我们通过将大鼠骨髓间充质干细胞培养在离子注入硅橡胶上发现, 改性后的硅橡胶可以在早期促进间充质干细胞的增殖, 尤其以Ag-SR和N-SR较为明显, 并在改性硅橡胶上培养的间充质干细胞的细胞骨架形态以及F-actin分布发生改变, Ag-SR和N-SR上的干细胞铺展得更开, 应力纤维更明显, 而在C-SR上的细胞伸展较差。细胞中应力纤维的空间分布和密度可能是细胞骨架中应力的反映, 应力纤维在各种生物进程中发挥着关键作用, 从细胞形状, 细胞极性以及对力的反应, 到干细胞分化和癌症发展过程[23]。本实验结果显示, 干细胞在不同组材料上产生的应力纤维不同, 这对干细胞的进一步细胞行为变化具有重要意义。有研究表明, 细胞骨架F-actin在机械感知和机械传导中起重要作用[21-23], 机械力可以通过生物分子将机械信号转化为生化信号(非直接机械信号传导), 也可以通过细胞骨架传播到细胞核中以直接改变细胞核形状和可能的染色体(直接机械信号传导)[24]。本实验观察到不同组材料上细胞骨架中应力纤维的变化, 而后细胞的黏附增殖和分化也产生了不同的变化。这说明, 离子注入硅橡胶相对普通硅橡胶对细胞的生物学行为产生了一定的影响, 可以改善细胞的粘附增殖。本研究采用离子注入技术对硅橡胶材料表面进行改性, 并初步研究了改性材料对干细胞生物学行为的影响, 我们观察到了C-SR和N-SR相对于干细胞具有更好的细胞生物相容性, 目前尚处于初步研究阶段, 对于细胞粘附增殖和分化的具体机制, 我们将进行进一步的完善和补充。
硅橡胶在临床上应用广泛, 但作为植入物长期植入体内, 材料周围形成包膜容易挛缩畸形。我们通过对硅橡胶的表面改性, 已经成功制得3种改性的离子注入硅橡胶, 保持其原有的良好的理化稳定性以及生物惰性的同时, 提高了其表面与细胞组织的生物相容性, 这对于进一步提高硅橡胶在临床上的应用, 以期减少临床不良反应具有重要作用。
| [1] |
赵治国, 万怡灶, 王玉林, 等. 生物材料的离子注入表面改性[J].
金属热处理, 2006, 31(8): 4–7.
ZHAO Z G, WAN Y Z, WANG Y L, et al. Review of surface modification of biomaterials by on implantation[J]. Heat Treatment Metals, 2006, 31(8): 4–7. DOI:10.13251/j.issn.0254-6051.2006.08.002 |
| [2] |
杨芷, 沈丽如, 石小花, 等. 碳离子硅橡胶改性材料的表面性能检测及其细胞相容性评价[J].
第三军医大学学报, 2013, 35(2): 123–126.
YANG Z, SHEN L R, SHI X H, et al. Surface properties and cell compatibility of carbon ion implanted silicone rubber[J]. J Third Mil Med Univ, 2013, 35(2): 123–126. DOI:10.16016/j.1000-5404.2013.02.028 |
| [3] | PITTENGER M F, MACKAY A M, BECK S C, et al. Multilineage potential of adult human mesenchymal stem cells[J]. Science, 1999, 284(5411): 143–147. DOI:10.1126/science.284.5411.143 |
| [4] | FAN V H, TAMAMA K, AU A, et al. Tethered epidermal growth factor provides a survival advantage to mesenchymal stem cells[J]. Stem Cells, 2007, 25(5): 1241–1251. DOI:10.1634/stemcells.2006-0320 |
| [5] | BENOIT D S, SCHWARTZ M P, DURNEY A R, et al. Small functional groups for controlled differentiation of hydrogel-encapsulated human mesenchymal stem cells[J]. Nat Mater, 2008, 7(10): 816–823. DOI:10.1038/nmat2269 |
| [6] | JIANG J, PAPOUTSAKIS E T. Stem-cell niche based comparative analysis of chemical and nano-mechanical material properties impacting ex vivo expansion and differentiation of hematopoietic and mesenchymal stem cells[J]. Adv Healthc Mater, 2013, 2(1): 25–42. DOI:10.1002/adhm.201200169 |
| [7] | EVEN-RAM S, ARYM V, YAMADA K M. Matrix control of stem cell fate[J]. Cell, 2006, 126(4): 645–647. DOI:10.1016/j.cell.2006.08.008 |
| [8] | CULVER J C, DICKINSON M E. The effects of hemodynamic force on embryonic development[J]. Microcirculation, 2010, 17(3): 164–178. DOI:10.1111/j.1549-8719.2010.00025.x |
| [9] | IWAI R, NEMOTO Y, NAKAYAMA Y. The effect of electrically charged polyion complex nanoparticle-coated surfaces on adipose-derived stromal progenitor cell behaviour[J]. Biomaterials, 2013, 34(36): 9096–9102. DOI:10.1016/j.biomaterials.2013.08.027 |
| [10] | YIM E K F, DARLING E M, KULANGARA K, et al. Nanotopography-induced changes in focal adhesions, cytoskeletal organization, and mechanical properties of human mesenchymal stem cells[J]. Biomaterials, 2010, 31(6): 1299–1306. DOI:10.1016/j.biomaterials.2009.10.037 |
| [11] | JANA S, LEUNG M, CHANG J, et al. Effect of nano- and micro-scale topological features on alignment of muscle cells and commitment of myogenic differentiation[J]. Biofabrication, 2014, 6(3): 035012. DOI:10.1088/1758-5082/6/3/035012 |
| [12] |
武卫莉, 李佳. 硅橡胶的生物医学材料特性[J].
中国组织工程研究与临床康复, 2007, 11(1): 145–147.
WU W L, LI J. Biomedical characteristics of silicon rubber[J]. J Clin Rehabil Tissue Eng Res, 2007, 11(1): 145–147. DOI:10.3321/j.issn:1673-8225.2007.01.040 |
| [13] |
张承焱. 医用高分子材料的应用研究及发展(二)[J].
中国医疗器械信息, 2005, 11(6): 17–22.
ZHANG C Y. Application and development of medical polymeric materials(2)[J]. China Med Device Inform, 2005, 11(6): 17–22. DOI:10.3969/j.issn.1006-6586.2005.06.006 |
| [14] |
张一鸣, 王科, 樊东力. 医用硅橡胶生物相容性改性研究进展[J].
重庆医学, 2006, 35(3): 274–276.
ZHANG Y M, WANG K, FAN D L. Medical silicone rubber modification research progress of biological compatibility[J]. Chongqing Med, 2006, 35(3): 274–276. DOI:10.3969/j.issn.1671-8348.2006.03.044 |
| [15] | LIU P, CHEN Q, YUAN B, et al. Facile surface modification of silicone rubber with zwitterionic polymers for improving blood compatibility[J]. Mater Sci Eng C Mater Biol Appl, 2013, 33(7): 3865–3874. DOI:10.1016/j.msec.2013.05.025 |
| [16] |
许脉, 赵亚群, 李洪敏. 医用硅橡胶紫外光亲水改性后的抗菌黏附能力研究[J].
科学技术与工程, 2014, 14(28): 265–268.
XU M, ZHAO Y Q, LI H M. Study on antibacterial adhesion ability of medical silicone rubber UV-hydrophilic modification[J]. Sci Tech Eng, 2014, 14(28): 265–268. DOI:10.3969/j.issn.1671-1815.2014.28.052 |
| [17] | AZIZ T, WATES M, JAGGER R. Surface modification of an experimental silicone rubber maxillofacial material to improve wettability[J]. J Dent, 2003, 31(3): 213–216. DOI:10.1016/S03005712(02)00131-8 |
| [18] |
张琳.医用硅橡胶表面的PEG接枝改性及生物相容性评价[D].天津大学, 2012.
ZHANG L. Preparation and biocompatibility evaluation of PEG-grafted surface modification of silicone elastomer[D]. Tianjin University, 2012. |
| [19] |
高仁伟. 医用硅橡胶材料改性研究[J].
中国医疗器械杂志, 2015, 39(2): 122–124.
GAO R W. Research for modification of medical silicone rubber material[J]. Chin J Med Instrumentation, 2015, 39(2): 122–124. DOI:10.3969/j.issn.1671-7104.2015.02.012 |
| [20] |
陈兴, 周鑫, 张一鸣, 等. 碳-硅橡胶机械性能和生物安全性的初步研究[J].
第三军医大学学报, 2015, 37(8): 730–735.
CHEN X, ZHOU X, ZHANG Y M. Mechanical properties and bio-safety evaluation of carbon ion implanted silicone rubber[J]. J Third Mil Med Univ, 2015, 37(8): 730–735. DOI:10.16016/j.1000-5404.201411093 |
| [21] | TREISER M D, YANG E H, GORONOV S, et al. Cytoskeleton-based forecasting of stem cell lineage fates[J]. Proc Natl Acad Sci U S A, 2010, 107(2): 610–615. DOI:10.1073/pnas.0909597107 |
| [22] | MATHIEU P S, LOBOA E G. Cytoskeletal and focal adhesion influences on mesenchymal stem cell shape, mechanical properties, and differentiation down osteogenic, adipogenic, and chondrogenic pathways[J]. Tissue Eng Part B Rev, 2012, 18(6): 436–444. DOI:10.1089/ten.TEB.2012.0014 |
| [23] | DE R, ZEMEL A, SAFRAN S A. Theoretical concepts and models of cellular mechanosensing[J]. Methods Cell Biol, 2010, 98: 143–175. DOI:10.1016/S0091-679X(10)98007-2 |
| [24] | DOBBENGA S, FRATILA-APACHITEI L, ZDPOR A A. Nanopattern-induced osteogenic differentiation of stem cells-a systematic review[J]. Acta Biomaterialia, 2016, 46: 3. DOI:10.1016/j.actbio.2016.09.031 |



