2. 400038 重庆,重庆市公共卫生医疗救治中心:感染门诊;
3. 400038 重庆,重庆市公共卫生医疗救治中心:信息科
2. Clinic of Infective Diseases, Chongqing Public Health Medical Center, Chongqing, 40038, China;
3. Department of Information, Chongqing Public Health Medical Center, Chongqing, 40038, China
艾滋病和结核病是人类面临的两大传染性疾病,艾滋病与结核病合并感染则对两种疾病的防控提出了更大的挑战[1]。2011年,在全球发现结核病的870万人中,有110万人(13%)感染艾滋病毒[2]。反之,结核病是艾滋病病毒感染者的头号杀手,死亡的艾滋病患者中约30%由结核病导致[3]。WHO在2012年强调世界各国应当重视监测结核患者中艾滋病毒感染情况以及艾滋病毒感染者中活动性结核病患者的情况[4]。
重庆市艾滋病综合防治系统中有针对接受抗病毒治疗的艾滋病患者发生肺结核的监测数据[5]。我们应用该系统数据分析抗病毒治疗的艾滋病患者合并肺结核的感染率,分析艾滋病患者发生肺结核合并感染的相关因素,旨在揭示发生两种疾病合并感染的危险因素,为艾滋病合并肺结核感染的防治工作提供科学依据。
1 资料与方法 1.1 数据来源本研究数据来自于艾滋病综合防治系统——抗病毒治疗管理系统,该系统收集了重庆市2004-2015年各艾滋病治疗定点医院中接受抗病毒治疗患者的基本信息。患者均通过HIV确诊实验确诊为HIV-RNA阳性,自愿接受抗病毒治疗和随访,定期前往定点医院领取治疗药物,同时随访人员对患者随访情况进行信息更新。所有研究参与者签订了保密协议并对患者的信息进行严格保密。本研究已经经过医院伦理委员会批准(2018年)。
1.2 研究方法纳入标准:①研究对象均通过HIV确诊实验确诊为HIV-RNA阳性,且接受抗病毒治疗;②研究对象均自愿接受定期随访,在随访过程中进行结核分枝杆菌合并感染的检测;③随访人员针对艾滋病患者的随访信息进行完善的更新记录。排除标准:拒绝参与随访或随访信息不全的患者。
本研究采用病例对照研究,将合并肺结核感染的艾滋病患者纳入病例组,肺结核诊断标准参照《肺结核诊断和治疗指南》[6],结合患者临床症状、影像学诊断以及病原学检测进行确诊。将没有合并肺结核感染的艾滋病患者纳入对照组。分析病例组和对照组患者间年龄、性别、HIV感染途径、婚姻状况、WHO临床分期以及基线CD4值等因素的分布差异,通过单因素分析和多因素分析探索艾滋病患者合并肺结核感染的危险因素。
1.3 统计学分析采用SPSS 19.0统计软件,单因素分析采用χ2检验或Mann-Whitney U检验;将单因素分析中差异有统计学意义的变量纳入多因素Logistic回归分析。Logistic回归分析中,将年龄和WHO临床分期进行哑变量设置。检验水准:α=0.05。
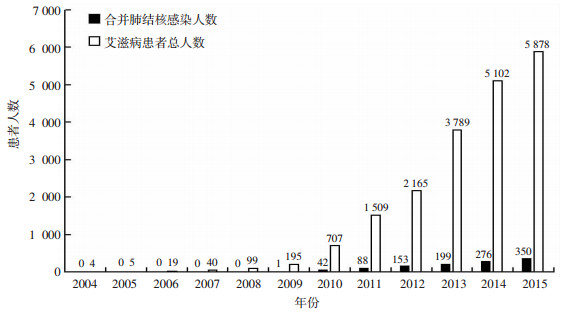
2 结果 2.1 艾滋病患者的基本情况2004-2015年重庆市累计登记艾滋病患者20 397例。共有19 512例患者确认是否患有肺结核,将这19 512例艾滋病患者纳入后续研究。在时间分布方面,艾滋病患者总人数以及合并肺结核感染患者人数逐年增加(图 1)。19 512例艾滋病患者年龄为30~45岁,以男性为主;在感染途径方面,主要通过性传播途径感染HIV;多数患者为已婚;WHO分期为Ⅰ期艾滋病患者居多,其次为Ⅱ期艾滋病患者;多数艾滋病患者基线CD4值>200(表 1)。
|
| 图 1 2004-2015年艾滋病患者总人数及合并肺结核感染人数 |
| 因素 | 合计 | HIV合并肺结核感染 | P值 | |
| 是 | 否 | |||
| 年龄/岁 | ||||
| <30 | 4 964(25.4) | 206(18.6) | 4 758(25.9) | <0.001 |
| 30~45 | 6 819(34.9) | 453(40.8) | 6 366(34.6) | |
| >45~60 | 4 743(24.3) | 317(28.6) | 4 426(24.1) | |
| >60 | 2 986(15.3) | 133(12.0) | 2 853(15.5) | |
| 性别 | ||||
| 男性 | 14 683(75.3) | 918(82.8) | 13 765(74.8) | <0.001 |
| 女性 | 4 829(24.7) | 191(17.2) | 4 638(25.2) | |
| 感染途径 | ||||
| 血液传播 | 1 407(7.8) | 86(9.1) | 1 321(7.7) | 0.259 |
| 性传播 | 16 653(92.2) | 859(90.9) | 15 794(92.3) | |
| 母婴传播 | 4(0) | 0(0) | 4(0) | |
| 婚姻状况 | ||||
| 未婚 | 5 120(26.5) | 266(24.0) | 4 854(26.6) | 0.125 |
| 已婚 | 10 846(56.0) | 650(58.7) | 10 196(55.9) | |
| 离异或丧偶 | 3 389(17.5) | 191(17.3) | 3 198(17.5) | |
| WHO临床分期 | ||||
| Ⅰ期 | 6 740(34.5) | 184(16.6) | 6 556(35.6) | <0.001 |
| Ⅱ期 | 4 850(24.9) | 133(12.0) | 4 717(25.6) | |
| Ⅲ期 | 3 391(17.4) | 249(22.5) | 3 142(17.1) | |
| Ⅳ期 | 4 531(23.2) | 543(49.0) | 3 988(21.7) | |
| 基线CD4值 | ||||
| ≤200 | 7 897(42.6) | 881(81.7) | 7016(40.2) | <0.001 |
| >200 | 10 634(57.4) | 197(18.3) | 10 437(59.8) | |
| 抗病毒治疗时间/月 | 20.98±19.41 | 21.64±21.18 | 20.94±19.30 | 0.292 |
2.2 艾滋病患者合并肺结核感染影响因素的单因素分析
19 512例艾滋病患者中,1 109例患有肺结核,HIV感染患者中合并肺结核的感染率为5.68%。艾滋病合并肺结核感染患者的年龄主要集中在30~45岁,以男性、已婚居多。从HIV病毒感染途径来看,合并肺结核感染的艾滋病患者主要通过性传播感染HIV病毒;艾滋病合并肺结核感染主要为WHO Ⅳ期艾滋病患者,其次为Ⅲ期艾滋病患者。大多数艾滋病合并肺结核感染患者基线CD4值<200(表 1)。
分析年龄、性别、感染途径、婚姻状况、WHO临床分期以及基线CD4值在两组间的分布,发现感染途径和婚姻状况在两组间的分布差异无统计学意义(P>0.05),此外,抗病毒治疗时间在两组间差异也无统计学意义(P>0.05)。年龄、性别、WHO临床分期以及基线CD4值在两组间分布差异有统计学意义(P<0.05,表 1)。
2.3 艾滋病患者合并肺结核感染影响因素的多因素分析将单因素分析中有统计学差异的因素均作为协变量,同时纳入多因素Logistic回归模型进行分析。结果显示:在校正了其他协变量的情况下,与<30岁的人群相比,年龄在30~45岁的人群更容易合并肺结核感染(校正后OR=1.238,95%CI:1.035~1.481);男性艾滋病患者更容易合并肺结核感染(校正后OR=1.645,95%CI: 1.393~1.942);WHO临床分期为Ⅲ期、Ⅳ期的艾滋病患者比Ⅰ期患者更容易合并肺结核感染(Ⅲ期患者校正后OR=2.734,95%CI=2.235~3.345;Ⅳ期患者校正后OR=3.144,95%CI:2.630~3.759);基线CD4值<200的艾滋病患者更容易合并肺结核感染(校正后OR=5.244,95%CI=4.444~6.188,表 2)。
| 因素 | β值 | SE值 | Wald χ2 | P值 | OR值(95%CI) |
| 年龄/岁 | |||||
| <30 | 参照 | ||||
| 30~45 | 0.214 | 0.091 | 5.455 | 0.020 | 1.238(1.035~1.481) |
| >45~60 | 0.156 | 0.098 | 2.543 | 0.111 | 1.169(0.965~1.416) |
| >60 | -0.387 | 0.120 | 10.416 | 0.001 | 0.679(0.537~0.859) |
| 性别 | |||||
| 女性 | 参照 | ||||
| 男性 | 0.498 | 0.085 | 34.431 | <0.001 | 1.645(1.393~1.942) |
| WHO临床分期 | |||||
| Ⅰ期 | 参照 | ||||
| Ⅱ期 | 0.071 | 0.119 | 0.355 | 0.551 | 1.073(0.851~1.354) |
| Ⅲ期 | 1.006 | 0.103 | 95.618 | <0.001 | 2.734 (2.235~3.345) |
| Ⅳ期 | 1.146 | 0.091 | 157.957 | <0.001 | 3.144 (2.630~3.759) |
| 基线CD4值 | |||||
| >200 | 参照 | ||||
| ≤200 | 1.657 | 0.084 | 384.647 | <0.001 | 5.244(4.444~6.188) |
3 讨论
艾滋病患者的免疫系统受到HIV病毒的破坏,容易发生机会性感染,结核病是艾滋病患者人群中最常见的机会性感染之一,也是造成艾滋病患者死亡的主要原因之一[7-8]。艾滋病患者合并结核病并非HIV病毒与结核分枝杆菌简单的合并感染,艾滋病毒可以促进潜伏期结核分枝杆菌进展为活动进展阶段,促进结核病的发生率[9]。反过来,结核病也会对艾滋病患者产生影响,促进HIV感染者疾病发生的进程,影响艾滋病患者的治疗效果、生存质量和生存时间[10]。因此,探索艾滋病患者合并感染结核病的危险因素,对于有效降低结核病合并感染起着重要的作用。
在本研究中,艾滋病患者合并肺结核的感染率为5.68%。与国内其他地区相关研究相比,本研究结果中肺结核合并感染率与广西2011年的结果(5.31%)近似[11],高于浙江省温州市的结果(2.21%)[12]。与国外研究相比,本研究结果与坦桑尼亚部分地区(8.5%)相近[13],低于埃塞俄比亚地区(27.7%)[14]。不同国家、同一国家不同地区艾滋病/肺结核合并感染率的差异可能是由于不同的诊断方法、疾病检测覆盖率等原因导致的。
目前,国内关于艾滋病患者发生肺结核合并感染危险因素的研究相对较少,本研究结果显示:艾滋病患者的年龄(30~45岁)、性别(男性)、WHO临床分期(Ⅲ期、Ⅳ期)以及基线CD4值(≤200)均为艾滋病/肺结核合并感染的独立危险因素。CD4细胞是人体免疫系统中最重要的免疫细胞种类之一,而且CD4细胞是HIV病毒的主要攻击对象。因此,在艾滋病患者中,CD4淋巴细胞计数下降,人体的防御机制被破坏,导致各种机会性感染更容易发生。本研究结果显示:与CD4淋巴细胞计数超过200相比,CD4淋巴细胞计数少于200的患者发生结核病的可能性为1.657倍。本研究结果与埃塞俄比亚的一项研究结果类似,该结果显示:随着CD4淋巴细胞计数下降,艾滋病患者CD4淋巴细胞计数<200时,发生结核病的可能性将增加2倍[14]。
本研究还发现30~45岁的艾滋病患者以及男性艾滋病患者更容易发生肺结核合并感染。这可以解释为30~45岁的艾滋病患者属于青壮年人群,此类人群由于工作、生活等原因经常发生较大的人口流动,更有可能接触并感染结核分枝杆菌,特别是男性。有趣的是,本研究结果还发现>60岁的艾滋病患者合并肺结核感染的风险有所降低,这也可能是由于老龄人群居住稳定,接触人群单一,感染结核分枝杆菌的机会减少。此外,本研究另一个重要的发现是艾滋病患者的WHO临床分期与合并肺结核感染相关。与WHO临床分期Ⅰ期患者相比,Ⅲ期和Ⅳ期合并肺结核感染的风险分别增加为2.7倍和3.1倍。这一结果与国外的报道一致[15-16],这可以解释为患者一旦进入艾滋病晚期阶段,免疫保护能力将会很小,这将使他们容易发生肺结核合并感染。
本研究存在一定的局限性,如国外的一些研究报道中吸烟、饮酒以及教育程度也是艾滋病患者发生结核病合并感染的危险因素[17-18],由于我们收集数据的局限性,并没有将吸烟和饮酒等因素纳入研究。因此,吸烟以及饮酒在重庆地区艾滋患者群中是否影响肺结核的合并感染有待于进一步研究。
综上所述,本研究发现30~45岁人群、男性、Ⅲ期和Ⅳ期艾滋病患者以及基线CD4值≤200的患者更容易发生肺结核合并感染。因此,在今后的艾滋病患者临床管理中,应重点针对此类人群进行肺结核感染的防控,将这些艾滋病患者纳入结核病合并感染的重点易感人群进行保护,有效减少结核病的合并感染。
| [1] | TIBERI S, CARVALHO A C, SULIS G, et al. The cursed duet today:tuberculosis and HIV-coinfection[J]. Presse Med, 2017, 46(2 Pt 2): e23–e39. DOI:10.1016/j.lpm.2017.01.017 |
| [2] | GAO J, ZHENG P, FU H. Prevalence of TB/HIV co-infection in countries except China:a systematic review and meta-analysis[J]. PLoS ONE, 2013, 8(5): e64915. DOI:10.1371/journal.pone.0064915 |
| [3] |
张湘玲. 2005-2012年凭祥市结核病和艾滋病(TB/HIV)双重感染人群资料分析[J].
医学动物防制, 2014, 30(6): 624–626.
ZHANG X L. Double infection population data analysis of Tuberculosis and HIV/AIDS (TB/HIV) of Pingxiang city during 2005-2012[J]. J Med Pest Control, 2014, 30(6): 624–626. |
| [4] | CHANDA-KAPATA P, KAPATA N, KLINKENBERG E, et al. The prevalence of HIV among adults with pulmonary TB at a population level in Zambia[J]. BMC Infect Dis, 2017, 17(1): 236. DOI:10.1186/s12879-017-2345-5 |
| [5] |
聂欢, 肖文秀, 唐德谊, 等. 分析重庆市HIV/AIDS患者合并HBV、HCV感染状况[J].
第三军医大学学报, 2017, 39(21): 2140–2144.
NIE H, XIAO W X, TANG D Y, et al. Retrospective analysis of HBV and HCV infection in HIV/AIDS patients in Chongqing[J]. J Third Mil Med Univ, 2017, 39(21): 2140–2144. DOI:10.16016/j.1000-5404.201705085 |
| [6] |
中华医学会结核病分会. 肺结核诊断和治疗指南[J].
中华结核和呼吸杂志, 2001, 24(2): 70–74.
Chinese Society for Tuberculosis, Chinese Medical Association. Guidelines for the diagnosis and treatment of tuberculosis[J]. Chin J Tuberc Respir Dis, 2001, 24(2): 70–74. DOI:10.3760/j:issn:1001-0939.2001.02.002 |
| [7] |
霍飞, 方彦. 2005-2014年艾滋病合并结核病国际研究状况文献计量学分析[J].
中国艾滋病性病, 2016, 22(7): 536–538.
HUO F, FANG Y. Bibliometric analysis of domestic and overseas literature on co-infected with TB and HIV[J]. Chin J AIDS STD, 2016, 22(7): 536–538. DOI:10.13419/j.cnki.aids.2016.07.14 |
| [8] |
孙月, 郜桂菊, 李兴旺. 艾滋病合并结核病研究进展[J].
中国艾滋病性病, 2013, 8(08): 619–621.
SUN Y, GAO G J, LI X W. Novel developments in AIDS/TB coinfection[J]. Chin J AIDS STD, 2013, 8(08): 619–621. DOI:10.13419/j.cnki.aids.2013.08.027 |
| [9] | NANTA S, KANTIPONG P, PATHIPVANICH P, et al. Screening scheme development for active TB prediction among HIV-infected patients[J]. Southeast Asian J Trop Med Public Health, 2011, 42(4): 867–875. |
| [10] | JALAL T M T, ABDULLAH S, WAHAB F A, et al. Prevalence and factors associated with tuberculosis treatment success among TB/HIV co-infection in North-east Malaysia[J]. Malays J Med Sci, 2017, 24(6): 75–82. DOI:10.21315/mjms2017.24.6.9 |
| [11] |
崔哲哲, 冯启明, 林玫, 等. 2010~2013年广西TB/HIV双重感染监测数据分析与评价[J].
广西医学, 2015, 37(3): 364–367.
CUI Z Z, FENG Q M, LIN M, et al. Analysis and evaluation on TB/HIV coinfection monitoring result in Guangxi from 2010 to 2013[J]. Guangxi Med J, 2015, 37(3): 364–367. |
| [12] |
张淑兰, 单志力, 毛玲琼, 等. 2011-2013年浙江省温州市结核菌/艾滋病病毒双重感染筛查与治疗资料分析[J].
疾病监测, 2015, 30(1): 42–45.
ZHANG S L, SHAN Z L, MAO L Q, et al. Screening and treatment of Mycobacterium tuberculosis/HIV co-infection in Wenzhou, Zhejiang, 2011-2013[J]. Dis Surveillance, 2015, 30(1): 42–45. |
| [13] | NGOWI B J, MFINANGA S G, BRUUN J N, et al. Pulmonary tuberculosis among people living with HIV/AIDS attending care and treatment in rural northern Tanzania[J]. BMC Public Health, 2008, 8: 341. DOI:10.1186/1471-2458-8-341 |
| [14] | MITKU A A, DESSIE Z G, MULUNEH E K, et al. Prevalence and associated factors of TB/HIV co-infection among HIV infected patients in Amhara region, Ethiopia[J]. Afr Health Sci, 2016, 16(2): 588–595. DOI:10.4314/ahs.v16i2.29 |
| [15] | AKANBI M O, ACHENBACH C J, FEINGLASS J, et al. Tuberculosis after one year of combination antiretroviral therapy in Nigeria:a retrospective cohort study[J]. AIDS Res Hum Retroviruses, 2013, 29(6): 931–937. DOI:10.1089/AID.2012.0231 |
| [16] | SCHABLON A, BECKMANN G, HARLING M, et al. Prevalence of latent tuberculosis infection among health care workers in a hospital for pulmonary diseases[J]. J Occup Med Toxicol, 2009, 4: 1. DOI:10.1186/1745-6673-4-1 |
| [17] | LIENHARDT C, FIELDING K, SILLAH J S, et al. Investigation of the risk factors for tuberculosis:a case-control study in three countries in West Africa[J]. Int J Epidemiol, 2005, 34(4): 914–923. DOI:10.1093/ije/dyi100 |
| [18] | TAHA M, DERIBEW A, TESSEMA F, et al. Risk factors of active tuberculosis in people living with HIV/AIDS in Southwest Ethiopia:a case control study[J]. Ethiop J Health Sci, 2011, 21(2): 131–139. DOI:10.4314/ejhs.v21i2.69053 |



