蛋白质在细胞结构、行为、信号传递、生化反应中起关键作用,获取蛋白数量和活性信息有助于理解细胞的生理病理机制。目前蛋白质分析方法,如凝胶电泳、免疫测定法、色谱法和质谱法等,都需要收集大量组织细胞进行研究,忽略了细胞异质性将导致生物信息不可逆的丢失或稀释,更难以发现细胞群体中的“异类”。且传统Western blot步骤繁多,引入的误差在低丰度蛋白含量测定中影响更大。目前还缺乏简便有效的方法解决上述问题。若能从精确位置收集特定细胞,以及提高检测方法精密度、灵敏度入手,可有助于增强蛋白定量信息的可靠性。
激光显微切割在显微镜下通过激光切割标记细胞,可获取组织切片中的特定细胞,展示出良好的精确收集细胞样本的能力。另一方面,毛细管Western blot因其在纳升级毛细管中分离和免疫测试,以及全自动标准化的上样、分离、免疫杂交、曝光,使其具备高灵敏度、高精确性和重复性的特点。本研究结合上述两种方法优势,联合使用激光显微切割和全自动毛细管Western blot,同时实现了样本收集的精确性、特异性以及微量蛋白定量检测的可靠性。通过激光显微切割收集小鼠海马CA1和DG区微量神经元细胞,应用全自动毛细管Western blot系统检测颅脑创伤(traumatic brain injuries,TBI)中对继发损伤和修复起重要作用的磷酸化蛋白激酶A(phosphorylated protein kinase A,p-PKA)含量,为研究组织标记细胞的微量蛋白奠定基础。
1 材料与方法 1.1 材料主要仪器:颅脑损伤仪(PSI TBI-0310,美国),激光显微切割系统(Leica LMD7000,德国),全自动毛细管Western blot (ProteinSimple Wes,美国),酶标仪(BioTek ELx800,美国), 化学发光成像系统(Fusion FX5,法国),超声破损仪(Epigentek EpiSonic1100,美国)。主要试剂:RIPA Lysis and Extraction Buffer (ThermoFisher美国),蛋白酶和磷酸酶抑制(ThermoFisher美国),Bis-tris 4%~20%预制胶(GenScript ExpressPlus,中国),p-PKA抗体(Abcam美国),α-tubulin抗体(Bioworld中国),山羊抗兔二抗(Bioworld中国), Wes Separation[(12~230)×103] 8×13 Capillary Cartridges(ProteinSimple美国),Anti-Rabbit Detection Module (ProteinSimple美国),Standard Pack1 (ProteinSimple美国),MembraneSlides PEN-Membrane 2.0 μm(Leica德国),硫堇(Solarbio中国)。实验动物:SPF级20~25 g的C57BL/6雄性小鼠由陆军军医大学第三附属医院野战外科研究所实验动物中心提供。
1.2 方法 1.2.1 全自动毛细管Western blot检测p-PKA和α-tubulin实验按照ProteinSimple公司提供的Wes用户指南操作。将蛋白和5×的反应混合液(DTT,荧光标签Marker,SDS)按1 :4比例混合后95 ℃孵育5 min。分别按每孔3 μL样品、3 μL蛋白ladder、10 μL封闭液、10 μL一抗(p-PKA浓度为1 :250,α-tubulin为1 :500)、10 μL兔二抗、15 μL发光液和500 μL洗涤缓冲液加入独立微孔组成的上样板。室温2 500 r/min离心5 min,将上样板和毛细管放入Wes全自动毛细管Western blot仪器,后续实验将自动完成(上述实验中试剂耗材除一抗以外,均来自Wes全自动毛细管Western blot仪器配套试剂盒)。Wes全自动毛细管Western blot实验设置参数:分离时间25 min,分离电压375 V,封闭5 min,一抗孵育30 min,二抗孵育30 min。
1.2.2 传统Western blot检测p-PKA和α-tubulin蛋白加入5×Loading buffer 100 ℃孵育5 min,使用4%~20%梯度预制凝胶电泳分离。湿转蛋白至PVDF膜,室温封闭3 h后加入一抗(p-PKA浓度为1 :2 000,α-tubulin为1 :5 000),4 ℃孵育12 h后室温复温30 min,加入1 :5 000抗兔的二抗。增强型化学发光法(enhanced chemiluminescent,ECL)显示结果。Labworks4.6图像分析软件分析条带灰度值。
1.2.3 轻度颅脑创伤模型建立使用1.5%戊巴比妥钠(50 mg/kg)腹腔注射麻醉小鼠,在小鼠左侧顶叶前囟及后囟间开4 mm×4 mm骨窗,使用颅脑损伤仪对左侧顶叶骨窗处进行撞击,撞击直径3 mm,速度3.5 m/s,停留时间100 ms,深度1 mm。伤后复原骨片,缝合皮肤。
1.2.4 激光显微切割海马神经元细胞将未灌注的新鲜脑组织冰冻切片贴于MembraneSlides PEN-Membrane 2.0 μm玻片,放入干燥器干燥30 min后,75%酒精2 min×3次清洗包埋剂(optimal cutting temperature compound,OCT),0.5%的硫堇对神经元尼氏体染色0.5~1 min,75%酒精清洗2 min×3次,放入干燥器干燥30 min后,在显微镜下找到兴趣部位的染色细胞,操作软件进行激光切割。
1.2.5 微量细胞蛋白提取向收集到微量细胞的0.2 mL EP管盖中加入含蛋白酶磷酸酶抑制剂的RIPA溶液6 μL,倒立关盖后4 ℃离心12 000 r/min,30 s,4 ℃超声破碎(振幅档位:13;处理时长20 s;每次脉冲开启1 s;脉冲间隔2 s),4 ℃离心12 000 r/min,10 min,取上清保存于-80 ℃。
1.3 统计学分析实验数据采用x±s表示,应用SPSS 19.0统计软件,采用t检验进行分析,检验水准α=0.05。
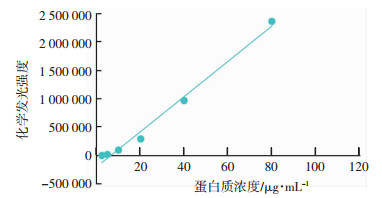
2 结果 2.1 毛细管Western blot检测低浓度蛋白的α-tubulin线性关系使用总蛋白浓度为100、50、25、12.5、6.25、3.125 μg/mL脑组织蛋白,按毛细管Western blot步骤操作后,检测α-tubulin,结果R2为0.988 5(图 1)。
|
| 图 1 全自动毛细管Western blot检测梯度浓度总蛋白中α-tubulin的线性关系 |
2.2 全自动毛细管Western blot检测低浓度蛋白p-PKA的重复性
使用全自动毛细管Western blot,上样3 μL浓度为50 μg/mL的脑组织蛋白,1 d内重复检测3次p- PKA(3 748.00 ±93.82),得到日内精密度RSD%为2.50%。同样方法重复检测3 d,每天3次测量p-PKA (3 596.33±147.14),得到日间精密度RSD%为4.09%。
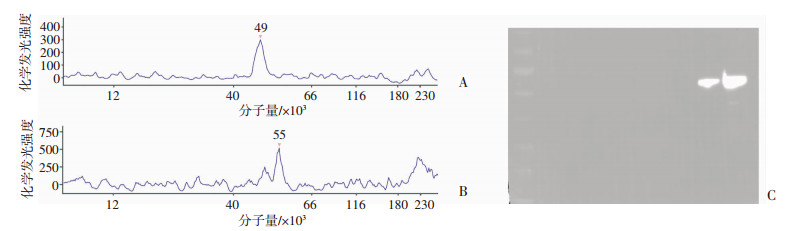
2.3 毛细管Western blot与传统Western blot灵敏度比较使用总蛋白浓度为500、50和5 μg/mL以及500、50和5 ng/mL脑组织蛋白,按毛细管Western blot步骤操作后,检测p-PKA和α-tubulin。结果总蛋白高于50 μg/mL浓度,上样3 μL可检出p-PKA(图 2A),总蛋白高于5 μg/mL,上样3 μL可检出α-tubulin(图 2B)。
|
| A:全自动毛细管Western blot检测50 μg/mL总蛋白中p-PKA;B:全自动毛细管Western blot检测5 μg/mL总蛋白中α-tubulin;C:传统Western blot检测梯度浓度总蛋白中p-PKA结果(为检测到低信号,采用过度曝光参数进行曝光) 图 2 两种Western blot方法检测低浓度总蛋白中p-PKA和α-tubulin的结果 |
使用总蛋白浓度为3.125、6.25、12.5、25、50、100、2 500 μg/mL脑组织蛋白,按传统Western blot步骤操作,前6个泳道分别是浓度3.125、6.25、12.5、25、50、100 μg/mL上样3 μL,第7、8泳道分别是100、2 500 μg/mL上样20 μL。结果显示总蛋白高于100 μg/mL上样20 μL可检出p-PKA(图 2C)。
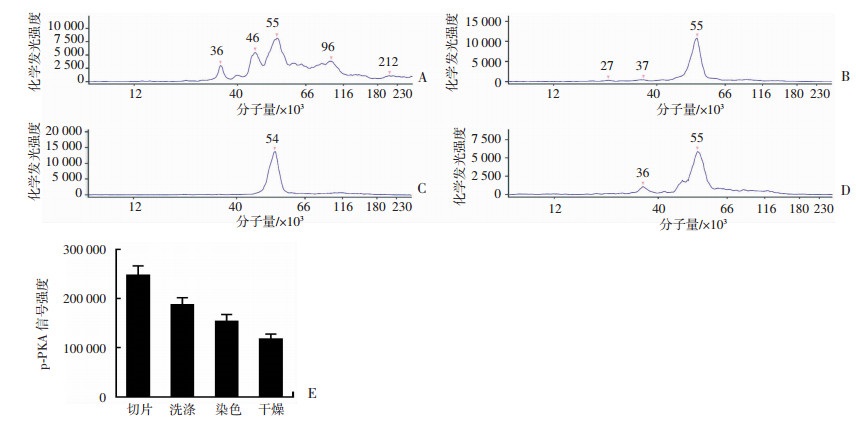
2.4 激光显微切割预处理条件优化取新鲜脑组织,修剪组织块后包埋于OCT中,快速放入-80 ℃冷冻2 h,使用冰冻切片机做16 μm厚度切片。根据切割操作步骤,分别在切片、干燥洗涤、染色、干燥后,使用10 μL含蛋白酶抑制剂的组织裂解液收集一片脑组织切片(均取相邻切片),提取蛋白并使用全自动毛细管Western blot检测p-PKA。结果显示未洗涤去除的OCT对蛋白分离干扰较大,蛋白降解持续发生,从切片到开始切割之间的预处理发生约50%的p-PKA蛋白降解(图 3)。
|
| A:切片;B:洗涤;C:染色;D:干燥;E:上述结果信号强度汇总 图 3 激光显微切割每步预处理检测p-PKA所得信号面积 |
2.5 检测颅脑创伤小鼠海马亚区神经元胞体p-PKA
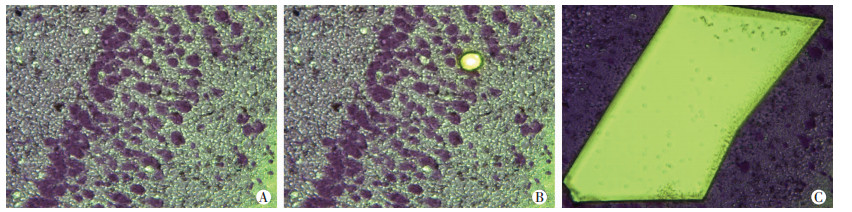
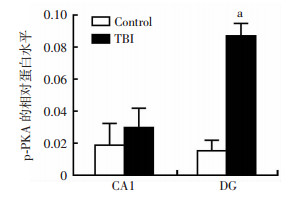
建立小鼠轻度颅脑创伤模型,24 h取脑组织以50 μm冰冻切片, 尼氏体染色后使用激光显微切割收集30片脑组织的伤侧海马CA1和DG区神经元(图 4),全自动毛细管Western blot检测各组p-PKA和α-tubulin。结果显示轻度颅脑创伤后24 h海马CA1神经元的p-PKA没有显著变化(P>0.05),而伤侧DG区神经元的p-PKA显著增高(P < 0.01,图 5)。
|
| A:切割前;B:单颗细胞切割;C:区域切割 图 4 激光显微切割海马(×20) |
|
| a: P < 0.01,与Control比较 图 5 全自动毛细管Western blot检测轻度TBI急性期海马CA1和DG区神经元的p-PKA蛋白水平 |
3 讨论
本研究使用全自动毛细管Western blot检测海马亚区微量神经元p-PKA含量,结果显示全自动毛细管Western blot的最低浓度检测限高于传统Western blot一个数量级。全自动毛细管Western blot是通过光照将分离的蛋白固定在毛细管壁,暴露的抗原抗体结合位点可能与固定在PVDF膜上的蛋白存在差异,影响了蛋白抗原抗体结合效率,因此对不同蛋白灵敏度可能存在差异。另一方面全自动毛细管Western blot实验全程都在一根毛细管中进行,减少转膜可能带来的蛋白损失,也可提高灵敏度。本实验在低蛋白浓度水平仍具有4.09%的RSD,与该仪器检测常规浓度结果相似[1],表现出良好的精密度,小于传统Western blot的30%[2]。因毛细管Western blot从进样到最后检测结果都是全自动操作,避免了传统Western blot繁琐的人工操作和仪器切换带入的误差,这些误差将严重干扰微量定量结果的差异性分析。本实验中全自动毛细管Western blot上样体积为3 μL(实际进入毛细管体积仅为nL级);另据报道毛细管Western blot能一次性对同一样品分子量相差大于10%的多种蛋白进行分离检测[3],这些特性为微量低浓度样品的检测提供了有利条件。全自动毛细管Western blot相较于传统Western blot技术,优势体现在更高的精密度和重复性上,使低浓度样本的检测结果更稳定可信。但在灵敏度上的提升有限,仍需少量富集低浓度样本,富集过程的特异性问题可由激光显微切割解决。
不同脑区的细胞蛋白质组差异巨大,目前对大脑研究时空精确性已提升至单细胞水平。激光显微切割可收集标记兴趣单细胞后进行核酸研究。但蛋白质无法扩增,低丰度蛋白质对后续检测方法要求很高[4]。本研究采用激光显微切割收集海马亚区标记的神经元,富集蛋白同时尽量减少引入非同类细胞的干扰,达到降低后续定量难度同时提高结果可信度。显微切割预处理中值得注意的是,冰冻切片包埋剂OCT对后续全自动毛细管Western blot的蛋白分离干扰较大,需要洗涤干净。但OCT并不影响传统Western blot的结果[5],其中一个原因可能是OCT易溶于水,上样时样本中的OCT已溶于大量的电泳液中。而全自动毛细管Western blot电泳体系只有纳升级,样本直接吸入液态电泳胶中,没有大量电泳液对其溶解稀释,且未对微量蛋白样本进行稀释,均可能放大OCT的干扰作用。本实验通过洗涤OCT可消除杂峰,降低基线。另外发现蛋白降解持续发生,提示蛋白降解除了与操作步骤有关以外,可能也与处理时间有关,应尽量在低温的情况快速操作。
本方法应用于轻度TBI小鼠模型,急性期海马DG区p-PKA水平显著升高,而CA1没有明显变化,提示海马亚区神经元对TBI反应不一致。与报道的CA1和DG在缺氧损伤后p-PKA变化规律一致,DG区的高水平p-PKA促进一氧化氮过量生成,产生损害作用[6]。另外,p-PKA在DG区的神经发生具有重要作用[7],在这里可能参与创伤修复。
目前对分子机制研究的时空及细胞类型精细度要求日益增高,尤其在脑科学领域广泛应用的单细胞RNA测序,以及光遗传学等技术的推动下。本研究应用激光显微切割收集的CA1和DG微量神经元使用全自动毛细管Western blot检测p-PKA和α-tubulin,为标记并收集特定部位兴趣细胞的微量蛋白定量检测提供了新的思路,将有助于在细胞类型及功能众多,且混杂分布的组织(如脑组织)中开展细胞和分子水平研究。
| [1] | XU D, MARCHIONNI K, HU Y, et al. Quantitative analysis of a biopharmaceutical protein in cell culture samples using automated capillary electrophoresis (CE) western blot[J]. J Pharm Biomed Anal, 2017, 145: 10–15. DOI:10.1016/j.jpba.2017.06.025 |
| [2] | KOLLER A, WATZIG H. Precision and variance components in quantitative gel electrophoresis[J]. Electrophoresis, 2005, 26(12): 2470–2475. DOI:10.1002/elps.200500024 |
| [3] | XU D, MANE S, SOSIC Z. Characterization of a biopharmaceutical protein and evaluation of its purification process using automated capillary Western blot[J]. Electrophoresis, 2015, 36(2): 363–370. DOI:10.1002/elps.201400380 |
| [4] | WU M, SINGH A K. Single-cell protein analysis[J]. Curr Opin Biotechnol, 2012, 23(1): 83–88. DOI:10.1016/j.copbio.2011.11.023 |
| [5] | TIAN Y, BOVA G S, ZHANG H. Quantitative glycoproteomic analysis of optimal cutting temperature-embedded frozen tissues identifying glycoproteins associated with aggressive prostate cancer[J]. Anal Chem, 2011, 83(18): 7013–7019. DOI:10.1021/ac200815q |
| [6] | WADA K, OSUKA K, WATANABE Y, et al. Subarachnoid hemorrhage induces neuronal nitric oxide synthase phosphorylation at Ser1412 in the dentate gyrus of the rat brain[J]. Nitric Oxide, 2017, 8603(17): 30163–30165. DOI:10.1016/j.niox.2017.10.007 |
| [7] | NAKAGAWA S, KIM J E, LEE R, et al. Regulation of neurogenesis in adult mouse hippocampus by cAMP and the cAMP response element-binding protein[J]. J Neurosci, 2002, 22(9): 3673–3682. DOI:10.1523/JNEUROSCI.22-09-03673.2002 |



