2. 400016 重庆,重庆医科大学 附属第一医院检验科
2. Department of Clinical Laboratory, the First Affiliated Hospital of Chongqing Medical University, Chongqing, 400016, China
肺炎克雷伯菌(Klebsiella pneumoniae)属于肠杆菌科克雷伯菌属,是重要的条件致病菌与医院内感染的病原菌,可以引起严重或致死性感染;碳青霉烯类抗菌药物因对超广谱β-内酰胺酶(ESBLs)和头孢菌素酶(AmpC酶)具有高度稳定性,是目前治疗该类细菌严重感染最主要的抗菌药物之一。近年来随着碳青霉烯类抗生素的广泛使用,已经出现碳青霉烯耐药肺炎克雷伯菌(CR-KP),该类细菌可以导致包括碳青霉烯类在内的多种不同类型抗菌药物耐药,成为临床治疗失败的主要原因[1-4]。2015年中国耐药监测网CHINET数据调查显示肺炎克雷伯菌对碳青霉烯类的耐药率呈逐年上升趋势[5],值得注意的是,在CR-KP基础上的广泛耐药的肺炎克雷伯菌(extensively drug-resistant Klebsiella pneumoniae, XDR-KP)更应值得关注和重视。由于该类细菌的出现,使临床医师对抗菌药物的选择进一步减少,给临床治疗带来更为严峻的挑战[6]。
本研究拟对重庆医科大学附属第一医院2012-2015年收集到的XDR-KP感染的临床菌株进行相关临床特征、分子流行病学和危险因素分析,为临床合理诊治,控制耐药细菌传播提供理论依据。
1 材料与方法 1.1 研究对象2012年1月至2015年12月我院从住院患者送检标本中共分离到肺炎克雷伯菌株2 932株,均为非重复菌株,其中共分离到39株XDR-KP,作为病例组。XDR-KP指除对1~2类抗菌药敏感外,对其他的所有类别抗菌药物均耐药者。同时按1 :2的比例配对随机选择78例同期非XDR-KP感染作为对照组。从送检科室来看,病例组标本主要来源于泌尿外科7份(17.9%)、肝胆外科6份(15.4%)、呼吸内科6份(15.4%)、神经外科5份(12.8%)、重症医学科3份(7.7%)等;对照组标本主要来源于肝胆外科13份(16.7%)、胃肠外科8份(10.3%)、泌尿外科7份(9.0%)、重症医学科7份(9.0%)、老年病科6份(7.7%)等。
1.2 细菌鉴定及药物敏感实验采用法国生物梅里埃公司生产的Vitek2 Compact全自动细菌鉴定系统和配套的药敏鉴定卡对病例组和对照组的所有菌株进行19种常见抗生素的药敏检测。判读标准和结果解释均参考CLSI M100-S26文件。替加环素药敏折点参照2012年美国FDA标准中肠杆菌科细菌的折点[7]。质控菌株为大肠埃希菌ATCC25922、铜绿假单胞菌ATCC27853和肺炎克雷伯菌ATCC700603。
1.3 危险因素数据收集回顾性分析入选患者的资料,所有病例资料均收集于我院电子病历系统和检验科LIS系统。统计变量包括:(1)患者基本情况(性别,高龄,入住ICU等);(2)基础疾病(糖尿病,高血压,实体肿瘤等);(3)侵入性操作(肠外营养,动静脉置管,感染前手术史等);(4)细菌检出前抗生素使用情况(青霉素类、头孢菌素,碳青霉烯类,氨基糖苷类等);(5)糖皮质激素使用、输血史等。
1.4 脉冲场凝胶电泳本研究采用脉冲场凝胶电泳(PFGE)对病例组39株XDR-KP菌株进行同源性分析,实验结果采用Tenover等(1995)提供的参考标准进行染色体DNA条带分型解释。具体解释标准如下:(1)相同:酶切图谱间有同样的条带数,且相应条带大小相同, 流行病学上则认为相同菌株。(2)紧密相关:由单一基因事件的改变,如点突变、插入或DNA缺失等情况下导致2~3条带的差异,则判断为紧密相关菌株。(3)可能相关:由两个独立的基因情况所致的一致的差异,导致出现了4~6条带差异,则判断为可能相关菌株。(4)不相关:分离茵株通过3个或更多个独立的基因事件所致的一致的改变,导致有7个或更多个条带的差异,则判断为与暴发克隆株不相关。
1.5 统计学分析采用SPSS 21.0软件进行危险因素统计分析。关联性数据分析采用比值比(OR)和95%置信区间(95%CI)分析,通过卡方检验或Fisher精确概率法对计数资料进行单因素分析,并计算相关统计量,计数资料采用百分率(%)表示。将单因素分析中P≤0.1的变量纳入二元Logistic回归模型中采用逐步前进法(条件)进行多因素分析,检验水准α=0.05。
2 结果 2.1 病例组与对照组的耐药率分析从药敏结果来看,XDR-KP对包括碳青霉烯类在内的常见抗生素的耐药率达到100%(39/39)。显示病例组菌株的耐药率非常高,仅对替加环素敏感。从病例组与对照组药敏结果对比来看,病例组菌株的耐药率明显高于对照组,差异具有统计学意义(P < 0.05,表 1)。
| 抗生素名称 | 病例组(n=39) | 对照组(n=78) | P值 | |||||
| 敏感 | 中介 | 耐药 | 敏感 | 中介 | 耐药 | |||
| 氨苄西林 | 0(0) | 0(0) | 39(100) | 9(11.5) | 2(2.6) | 67(85.9) | 0.014 | |
| 氨苄西林/舒巴坦 | 0(0) | 0(0) | 39(100) | 41(52.6) | 1(1.3) | 36(46.1) | < 0.001 | |
| 哌拉西林/他唑巴坦 | 0(0) | 0(0) | 39(100) | 43(55.1) | 8(10.3) | 27(34.6) | < 0.001 | |
| 头孢唑啉 | 0(0) | 0(0) | 39(100) | 33(42.3) | 4(5.1) | 41(52.6) | < 0.001 | |
| 头孢曲松 | 0(0) | 0(0) | 39(100) | 54(69.2) | 2(2.6) | 22(28.2) | < 0.001 | |
| 头孢他啶 | 0(0) | 0(0) | 39(100) | 53(68.0) | 4(5.1) | 21(26.9) | < 0.001 | |
| 头孢吡肟 | 0(0) | 0(0) | 39(100) | 57(73.1) | 8(10.3) | 13(16.6) | < 0.001 | |
| 头孢西丁 | 0(0) | 0(0) | 39(100) | 59(75.6) | 4(5.1) | 15(19.3) | < 0.001 | |
| 氨曲南 | 0(0) | 0(0) | 39(100) | 40(51.3) | 13(16.6) | 25(32.1) | < 0.001 | |
| 环丙沙星 | 0(0) | 0(0) | 39(100) | 52(66.7) | 0(0) | 26(33.3) | < 0.001 | |
| 左氧氟沙星 | 0(0) | 0(0) | 39(100) | 53(67.9) | 3(3.9) | 22(28.2) | < 0.001 | |
| 庆大霉素 | 0(0) | 0(0) | 39(100) | 52(66.7) | 7(9.1) | 19(24.2) | < 0.001 | |
| 妥布霉素 | 0(0) | 0(0) | 39(100) | 59(75.6) | 8(10.3) | 11(14.1) | < 0.001 | |
| 阿米卡星 | 0(0) | 0(0) | 39(100) | 72(92.3) | 2(2.6) | 4(5.1) | < 0.001 | |
| 厄他培南 | 0(0) | 0(0) | 39(100) | 76(97.4) | 0(0) | 2(2.6) | < 0.001 | |
| 亚胺培南 | 0(0) | 0(0) | 39(100) | 76(97.4) | 0(0) | 2(2.6) | < 0.001 | |
| 美罗培南 | 0(0) | 0(0) | 39(100) | 76(97.4) | 0(0) | 2(2.6) | < 0.001 | |
| 复方新诺明 | 0(0) | 0(0) | 39(100) | 58(74.3) | 4(5.1) | 16(20.6) | < 0.001 | |
| 替加环素 | 39(100) | 0(0) | 0(0) | 78(100) | 0(0) | 0(0) | - | |
2.2 XDR-KP感染的单因素分析
通过回顾性分析入选患者的病例资料,我们对病例组和对照组进行危险因素调查分析,其单因素分析结果显示:入住ICU(OR:4.52, 95%CI: 1.96-10.43, P < 0.001)、转院(OR: 2.32, 95%CI: 1.01-5.30, P=0.044)、肺部感染(OR: 3.09, 95%CI: 1.01-9.68, P=0.044)、内置引流管(OR: 3.81, 95%CI:1.54-9.43, P=0.003)、碳青霉烯类抗生素使用(OR: 6.72, 95%CI: 2.33-19.38, P < 0.001)是导致XDR-KP感染的主要危险因素(表 2)。
| 危险因素 | 病例组(n=39) | 对照组(n=78) | OR(95% CI) | P值 |
| 患者基本情况 | ||||
| 男性 | 24(61.5) | 41(52.6) | 1.44(0.66-3.16) | 0.357 |
| 高龄a | 19(48.7) | 31(39.7) | 1.44(0.66-3.12) | 0.355 |
| 吸烟 | 18(46.2) | 33(42.3) | 1.17(0.54-2.53) | 0.692 |
| 饮酒 | 22(56.4) | 38(48.7) | 1.36(0.63-2.95) | 0.433 |
| 入住ICU | 21(53.8) | 16(20.5) | 4.52(1.96-10.43) | < 0.001 |
| 转院 | 16(41.0) | 18(23.1) | 2.32(1.01-5.30) | 0.044 |
| 基础疾病及并发症 | ||||
| 高血压 | 14(35.9) | 21(26.9) | 1.52(0.67-3.46) | 0.318 |
| 糖尿病 | 10(25.6) | 16(20.5) | 1.33(0.54-3.30) | 0.529 |
| 冠心病 | 3(7.7) | 11(14.1) | 0.51(0.13-1.93) | 0.314 |
| 实体肿瘤 | 9(23.1) | 10(12.8) | 2.04(0.75-5.53) | 0.156 |
| 呼吸疾病 | 13(33.3) | 22(28.2) | 1.27(0.56-2.91) | 0.568 |
| 肝胆疾病 | 10(25.6) | 17(21.8) | 1.23(0.50-3.03) | 0.642 |
| 胃肠疾病 | 11(28.2) | 15(19.2) | 1.65(0.67-4.04) | 0.271 |
| 肾脏疾病 | 15(38.5) | 19(24.4) | 1.94(0.85-4.43 | 0.113 |
| 心血管疾病 | 6(15.4) | 8(10.3) | 1.59(0.51-4.96) | 0.420 |
| 尿路感染 | 7(17.9) | 10(12.8) | 1.48(0.52-4.26) | 0.458 |
| 肺部感染 | 8(20.5) | 6(7.7) | 3.09(1.01-9.68) | 0.044 |
| 腹腔内感染 | 2(5.1) | 2(2.6) | 2.05(0.28-15.16) | 0.472 |
| 低蛋白血症b | 14(35.9) | 21(26.9) | 1.52(0.67-3.46) | 0.318 |
| 重度贫血c | 2(5.1) | 3(3.8) | 1.35(0.22-8.44) | 0.747 |
| 低钾血症d | 9(23.1) | 11(14.1) | 1.83(0.68-4.87) | 0.224 |
| 侵入性操作(细菌检出前4周) | ||||
| 肠外营养 | 7(17.9) | 6(7.7) | 2.63(0.82-8.43) | 0.096 |
| 机械通气 | 7(17.9) | 10(12.8) | 1.48(0.52-4.26) | 0.458 |
| 导尿管 | 14(35.9) | 25(32.1) | 1.18(0.53-2.66) | 0.677 |
| 内置引流管 | 15(38.5) | 11(14.1) | 3.81(1.54-9.43) | 0.003 |
| 气管插管 | 5(12.8) | 3(3.8) | 3.68(0.83-16.27) | 0.070 |
| 感染前手术史 | 20(51.3) | 32(41) | 1.51(0.69-3.27) | 0.293 |
| 静脉置管 | 8(20.5) | 10(12.8) | 1.76(0.63-4.87) | 0.277 |
| 动脉置管 | 7(17.9) | 12(15.4) | 1.20(0.43-3.34) | 0.723 |
| 抗生素使用情况(细菌检出前3个月) | ||||
| 青霉素类 | 9(23.1) | 15(19.2) | 1.26(0.49-3.21) | 0.627 |
| 头孢菌素类 | 26(66.7) | 38(48.7) | 2.11(0.95-4.69) | 0.066 |
| 碳青霉烯类 | 14(35.9) | 6(7.7) | 6.72(2.33-19.38) | < 0.001 |
| 氨基糖苷类 | 6(15.4) | 10(12.8) | 1.24(0.41-3.69) | 0.704 |
| 喹诺酮类 | 8(20.5) | 14(17.9) | 1.18(0.45-3.11) | 0.738 |
| 大环内酯类 | 5(12.8) | 4(5.1) | 2.72(0.68-10.77) | 0.141 |
| 抗厌氧类 | 9(23.1) | 20(25.6) | 0.87(0.35-2.14) | 0.762 |
| 糖肽类 | 5(12.8) | 6(7.7) | 1.76(0.50-6.19) | 0.370 |
| 糖皮质激素 | 4(10.3) | 6(7.7) | 1.37(0.36-5.17) | 0.640 |
| 输血 | 9(23.1) | 14(17.9) | 1.37(0.53-3.52) | 0.511 |
| a:高龄,年龄>65岁;b:低蛋白血症,血清总蛋白 < 60 g/L或白蛋白 < 25 g/L;c:重度贫血,血红蛋白 < 60 g/L;d:低钾血症,血清钾 < 3.5 mmol/L | ||||
2.3 XDR-KP感染的Logistic多因素回归分析
将上述单因素分析结果中P≤0.1的所有变量纳入二元Logistic回归模型中采用逐步前进法(条件)进行多因素分析,结果显示:入住ICU(OR:3.01, 95%CI: 1.12-8.07, P=0.029)、内置引流管(OR:3.24, 95%CI:1.11-9.45, P=0.032)和碳青霉烯类抗生素使用(OR:5.08, 95%CI:1.42-18.16, P=0.012)是导致XDR-KP感染的独立危险因素(表 3)。
| 危险因素 | B | S.E. | Walds | P值 | OR | 95% CI |
| 入住ICU | 1.101 | 0.504 | 4.777 | 0.029 | 3.01 | 1.12-8.07 |
| 内置引流管 | 1.174 | 0.547 | 4.613 | 0.032 | 3.24 | 1.11-9.45 |
| 碳青霉烯类抗生素使用 | 1.624 | 0.650 | 6.239 | 0.012 | 5.08 | 1.42-18.16 |
2.4 流行病学调查分析
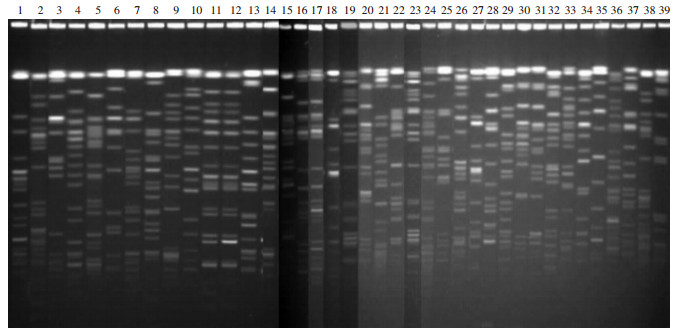
根据Tenover等(1995)提出的参考标准对PFGE结果进行判读,结果显示:39株XDR-KP可分为35个克隆型别,其中有4个克隆型别分别由2株紧密相关的菌株组成,但均来自不同科室,提示菌株间不存在各科室间的暴发流行(图 1)。
|
| 1~39号为菌株编号,分属35个克隆型别;其中11号和12号、02号和38号、19号和23号、20号和30号为同一克隆型别 图 1 XDR-KP菌株的PFGE分型 |
3 讨论
肺炎克雷伯菌是医院院内感染的最常见条件致病菌之一,可以引起严重或致死性感染。随着临床抗菌药物的广泛使用,目前已出现广泛耐药肺炎克雷伯菌(XDR-KP),且呈逐年上升趋势,从而使抗感染治疗极为棘手,因此积极寻找导致细菌广泛耐药的原因已迫在眉睫[8-10]。本研究对我院2012至2015年XDR-KP感染的流行病学和危险因素的基本情况进行了统计分析,从PFGE结果来看,XDR-KP菌株呈现克隆多样性,并未出现某一克隆型别的暴发流行,且科室分布较为分散,提示XDR-KP菌株在各科室间呈现散在流行。
本研究通过分析XDR-KP感染的危险因素发现,入住ICU、转院、肺部感染、内置引流管、碳青霉烯类抗生素使用均与XDR-KP感染相关。从病例资料分析来看,入住ICU和内置引流管是导致XDR-KP感染的独立危险因素。本研究中,病例组入住ICU的比例明显高于对照组,这可能与入住ICU的患者自身疾病严重,机体免疫力低下,对XDR-KP菌株更具有人群易感性有关;同时,ICU病房的患者长期使用呼吸机等辅助设备,这些设备均易导致患者继发各种细菌感染,经过长期或轮替使用多种抗菌药物作用下,更易筛选出XDR-KP菌株的感染。本研究与国内外相关报道一致[11-14]。另外,有文献报道中心静脉置管、人工气道是肠杆菌科细菌感染的独立危险因素[15],而本研究显示病例组内置引流管的使用比例明显高于对照组,故在病情允许的情况下,尽量避免使用内置引流管,如病情需要应严格按照无菌操作要求执行,加强伤口护理并合理使用抗菌药物以降低耐药菌感染风险。
从抗菌药物的使用情况来看,碳青霉烯类抗生素使用是导致XDR-KP感染的独立危险因素。对于病情危重的患者,碳青霉烯类抗生素是临床医师经验性用药的首选。通常认为在碳青霉烯类抗生素压力作用下,敏感菌株被抑制或杀灭,造成耐药菌株的大量增殖而成优势菌,耐药菌株所携带的耐药基因可以通过质粒水平传播给敏感菌株,从而造成更严重的耐药菌株的流行。本研究显示,耐药菌株检出前应用碳青霉烯类抗生素与XDR-KP感染密切相关,这与以前的报道结果相似[16]。因此,临床医师应当合理应用抗菌药物,尤其要避免碳青霉烯类抗生素的滥用,根据细菌培养及药敏结果有针对性地使用抗菌药物,减少经验性用药,注重联合用药,以减少XDR-KP感染的发生。
本研究的局限性在于仅收集到39株XDR-KP,菌株数量偏少,且均来自同一家医院,未能进行多中心研究试验以避免单一研究可能存在的局限性。本研究通过回顾性分析我院XDR-KP感染住院患者的病例资料,初步探究了我院XDR-KP感染的临床特征、流行病学和危险因素,发现入住ICU、内置引流管和碳青霉烯类抗生素使用是导致XDR-KP感染的独立危险因素。建议临床规范使用内置引流管,严格执行无菌操作,根据药敏结果有针对性地使用抗菌药物,且ICU病房应加强院内感染的监控,以预防和控制XDR-KP感染的产生及流行。
| [1] | TUMBARELLO M, TRECARICHI E M, DE ROSA F G, et al. Infections caused by KPC-producing Klebsiella pneumoniae: differences in therapy and mortality in a multicentre study[J]. J Antimicrob Chemother, 2015, 70(7): 2133–2143. DOI:10.1093/jac/dkv086 |
| [2] | DASS R, DEKA N M, BARMAN H, et al. Empyema thoracis: analysis of 150 cases from a tertiary care centre in North East India[J]. Indian J Pediatr, 2011, 78(11): 1371–1377. DOI:10.1007/s12098-011-0416-y |
| [3] | SCHWABER M J, LEV B, ISRAELI A, et al. Containment of a country-wide outbreak of carbapenem-resistant Klebsiella pneumoniae in Israeli hospitals via a nationally implemented intervention[J]. Clin Infect Dis, 2011, 52(7): 848–855. DOI:10.1093/cid/cir025 |
| [4] | SBRANA F, MALACARNE P, BASSETTI M, et al. Risk factors for ventilator associated pneumonia due to carbapenemase-producing Klebsiella pneumoniae in mechanically ventilated patients with tracheal and rectal colonization[J]. Minerva Anestesiol, 2016, 82(6): 635–640. |
| [5] |
胡付品, 朱德妹, 汪复, 等. 2015年中国CHINET细菌耐药性监测[J].
中国感染与化疗杂志, 2016, 16(6): 685–694.
HU F P, ZHU D M, WANG F, et al. Report of CHINET antimicrobial resistance surveillance program in 2015[J]. Chin J Infect Chemother, 2016, 16(6): 685–694. |
| [6] | MAGIORAKOS A P, SRINIVASAN A, CAREY R B, et al. Multidrug-resistant, extensively drug-resistant and pandrug-resistant bacteria: an international expert proposal for interim standard definitions for acquired resistance[J]. Clin Microbiol Infect, 2012, 18(3): 268–281. DOI:10.1111/j.1469-0691.2011.03570.x |
| [7] | SADER H S, FARRELL D J, JONES R N. Tigecycline activity tested against multidrug-resistant Enterobacteriaceae and Acinetobacter spp. isolated in US medical centers(2005- 2009)[J]. Diagn Microbiol Infect Dis, 2011, 69(2): 223–227. DOI:10.1016/j.diagmicrobio.2010.10.020 |
| [8] | FRAENKEL-WANDEL Y, RAVEH-BRAWER D, WIENER-WELL Y, et al. Mortality due to blaKPC Klebsiella pneumonia bacteraemia[J]. J Antimicrob Chemother, 2016, 71(4): 1083–1087. DOI:10.1093/jac/dkv414 |
| [9] | SCHWABER M J, CARMELI Y. An ongoing national intervention to contain the spread of carbapenem-resistant enterobacteriaceae[J]. Clin Infect Dis, 2014, 58(5): 697–703. DOI:10.1093/cid/cit795 |
| [10] | VAN DUIN D, DOI Y. Outbreak of colistin-resistant, carbapenemase-producing Klebsiella pneumoniae: are we at the end of the road?[J]. J Clin Microbiol, 2015, 53(10): 3116–3117. DOI:10.1128/JCM.01399-15 |
| [11] | CHIA J H, SU L H, LEE M H, et al. Development of high-level carbapenem resistance in Klebsiella pneumoniae among patients with prolonged hospitalization and carbapenem exposure[J]. Microb Drug Resist, 2010, 16(4): 317–325. DOI:10.1089/mdr.2009.0048 |
| [12] | BORER A, SAIDEL-ODES L, ESKIRA S, et al. Risk factors for developing clinical infection with carbapenem-resistant Klebsiella pneumoniae in hospital patients initially only colonized with carbapenem-resistant K pneumoniae[J]. Am J Infect Control, 2012, 40(5): 421–425. DOI:10.1016/j.ajic.2011.05.022 |
| [13] | HUSSEIN K, RAZ-PASTEUR A, FINKELSTEIN R, et al. Impact of carbapenem resistance on the outcome of patients' hospital-acquired bacteraemia caused by Klebsiella pneumoniae[J]. J Hosp Infect, 2013, 83(4): 307–313. DOI:10.1016/j.jhin.2012.10.012 |
| [14] | WU D, CAI J, LIU J. Risk factors for the acquisition of nosocomial infection with carbapenem-resistant Klebsiella pneumoniae[J]. South Med J, 2011, 104(2): 106–110. DOI:10.1097/SMJ.0b013e318206063d |
| [15] | SCHECHNER V, KOTLOVSKY T, KAZMA M, et al. Asymptomatic rectal carriage of blaKPC producing carbapenem-resistant Enterobacteriaceae: who is prone to become clinically infected[J]. Clin Microbiol Infect, 2013, 19(5): 451–456. DOI:10.1111/j.1469-0691.2012.03888.x |
| [16] | GÓMEZ RUEDA V, ZULETA TOBóN J J. Risk factors for infection with carbapenem-resistant Klebsiella pneumoniae: a case-case control study[J]. Colomb Med(Cali), 2014, 45(2): 54–60. |



