近几十年来,椎弓根螺钉内固定已经成为脊柱退行性疾病、创伤、肿瘤等引起的不稳定脊柱手术治疗的金标准[1]。然而,对于骨质疏松症(osteoporosis,OP)患者,普通椎弓根螺钉难以对其脆弱的骨质提供足够的把持力,常导致内固定失败。大量研究发现,可以采取多种策略提高螺钉把持力,包括增加螺钉的长度和直径[2]、优化螺杆及螺纹设计[3-4]、选择适当的置钉角度及钉道[5]、双皮质固定[6]、应用可膨胀椎弓根螺钉[1, 7-8]及骨水泥强化椎弓根螺钉[9]。但这些策略均存在一定的缺陷,例如,螺钉松动甚至拔出、椎弓根骨折、血管或脏器损伤以及骨水泥渗漏引起的并发症等[10-12]。因此,需要探索提高安全性、有效性的新技术。传统的空心椎弓根螺钉存在几个缺点,包括骨水泥弥散不满意[13-14]、固定钉头不便于操作[14]、骨水泥注射系统的安装与拆卸过于繁琐等。针对这些弊端,本研究小组研究设计出一种新型可注射骨水泥椎弓根螺钉(bone cement-injectable cannulated pedicle screw,CICPS),并在之前的生物力学实验及初期临床应用中证明其具有较高的安全性及有效性[15-16]。本研究旨在通过对较多病例研究CICPS在临床应用中的中长期临床安全性及有效性。
1 资料与方法 1.1 临床资料选取2011年3月至2015年3月本院骨科收治的符合纳入标准的患者128例,均使用聚甲基丙烯酸甲酯(polymethylmethacrylate,PMMA)强化的CICPS系统实施脊柱内固定手术,包括男性29例,女性99例,年龄35~83(60.7±11.0)岁。其中术前诊断腰椎滑脱症53例(41.4%)、腰椎间盘突出症/腰椎管狭窄症44例(34.4%)、椎体骨折19例(14.8%)、强直性脊柱炎伴脊柱后凸畸形12例(9.4%)。患者平均骨密度T值为-5.40~-2.50(-3.20±0.66)。纳入标准:①术前对腰椎进行双光子骨密度检查诊断为OP(骨密度T值≤-2.5);②术前诊断为腰椎滑脱症、腰椎间盘突出症/腰椎管狭窄症、椎体骨折、脊柱后凸畸形,具有后路经椎弓根脊柱内固定手术治疗的明确指征。排除标准:①出凝血功能障碍;②不能耐受手术;③局部或全身感染;④对植入物过敏;⑤有其他明显手术禁忌证。本研究经本院伦理委员会审查批准(2014年)实施,在术前均向患者及家属充分告知研究内容并签署知情同意书。
1.2 术前准备术前对所有病例行腰椎双光子骨密度检查;对腰椎滑脱症、腰椎间盘突出症/腰椎管狭窄症患者行腰椎正侧过伸过屈位X线片、CT三维重建、MRI检查;对椎体骨折患者行相应节段正侧位X线片、CT三维重建及MRI检查;对脊柱后凸畸形患者行脊柱全长正侧位X线片、CT三维重建及MRI检查。完善术前检查后,进行全科病例讨论,确定手术方案。术前告知患者手术风险及注意事项并签署知情同意书。
1.3 手术方案总体设计手术麻醉方式均采用静吸复合全麻,手术体位俯卧位。手术由我科3名经验丰富的高年资(副)主任医师实施。对腰椎滑脱症、腰椎间盘突出症/腰椎管狭窄症采取后路腰椎滑脱复位、腰椎间盘摘除、椎管减压、椎间植骨融合、椎弓根螺钉内固定术;对椎体骨折采取后外侧植骨融合、椎弓根螺钉内固定术,酌情行椎管减压;对脊柱后凸畸形采取后路截骨矫形、后外侧植骨融合、椎弓根螺钉内固定术。术中视情况给予止血粉充分止血,对有椎管减压的手术常规放置防粘黏膜覆盖硬膜囊,常规放置1根或2根皱襞引流管。
1.4 术后管理术后常规给予预防感染、止痛等治疗。术后按时换药、观察引流情况及术口愈合情况,注意活动性出血及脑脊液漏发生,引流量少于50 mL时拔除引流管。预防坠积性肺炎、血栓形成及褥疮。术后3 d后穿戴支具下床活动,促进康复。复查血常规、血沉、C反应蛋白、降钙素原及术后X线片, 如无明显异常,则可出院康复。
1.5 随访与评价术后1、3、6、12个月及以后每年门诊复查。随访内容包括:①每次随访均进行腰腿痛视觉模拟评分法(Visual Analogue Scale/Score, VAS)评分、Oswestry功能障碍指数问卷表(ODI)评分;②术后1个月正侧位X线片,术后3个月及以上复查腰椎正侧过伸过屈位X线片、腰椎CT三维重建(脊柱后凸畸形、椎体骨折病例查脊柱全长正侧位X线片、CT三维重建)。主要评价指标:①临床指标:腰腿痛VAS评分、ODI评分;②影像学指标:椎体高度、椎间隙高度、滑脱角、Taillard指数、螺钉位移情况(钉尖至椎体前缘及上终板的距离,分别记为x, y)、融合率;③并发症:骨水泥渗漏情况、血管栓塞、肺栓塞(有临床症状的肺栓塞,术后不常规检查胸片及CT)、感染。
1.6 统计学分析采用SPSS 18.0统计软件,使用平均值及标准差的方法描述正态分布变量,以x±s表示,采取配对t检验进行统计分析。以P<0.05为差异具有统计学意义。
2 结果 2.1 手术基本情况128例患者274个椎体中共使用418颗CICPS(表 1),平均每颗螺钉使用骨水泥(1.51±0.13)mL。
| 术前诊断 | 例数 (百分比) |
CICPS (例) |
CPS (例) |
使用CICPS的椎体数 |
| 椎体滑脱症 | 53(41.4%) | 178 | 52 | 109 |
| LDH/LSS | 44(34.4%) | 120 | 95 | 100 |
| 椎体骨折 | 19(14.8%) | 68 | 41 | 37 |
| 脊柱后凸畸形 | 12(9.4%) | 52 | 68 | 28 |
| 合计 | 128(100.0%) | 418 | 256 | 274 |
| LDH/LSS:腰椎间盘突出症/腰椎管狭窄症;AS:强直性脊柱炎;CICPS:骨水泥椎弓根螺钉;CPS:普通椎弓根螺钉 | ||||
2.2 并发症情况
术中无神经、血管及内脏损伤,在注射骨水泥过程中手术区域无骨水泥污染。在20例(15.63%)患者中共发现25个(9.12%)椎体27处(6.46%)骨水泥渗漏,但均未引起任何临床症状。住院期间未出现活动性出血、感染及有症状的血管栓塞形成(表 2)。
| 诊断 | 渗漏数 | 渗漏椎体 | 渗漏病例数 |
| 腰椎滑脱症 | 3(1.69%) | 3(2.75%) | 3(5.66%) |
| LDH/LSS | 7(5.83%) | 6(6.00%) | 5(11.36%) |
| 椎体骨折 | 15(22.06%) | 15(40.54%) | 11(57.89%) |
| 强直性脊柱后凸畸形 | 2(3.85%) | 1(3.57%) | 1(8.33%) |
| 合计 | 27(6.46%) | 25(9.12%) | 20(15.63%) |
| 此组骨水泥渗漏均发生于椎体前静脉;LDH/LSS:腰椎间盘突出症/腰椎管狭窄症 | |||
2.3 随访情况
病例均获随访,随访时间23~71(42.4±13.4)个月。患者腰腿痛症状均得到不同程度的缓解。
2.3.1 评分量表结果末次随访腰痛VAS评分、腿痛VAS评分及ODI评分较术前分别下降了83.2%、93.3%、90.1%(P<0.05,表 3)。
| 评分 | n | 术前 | 末次随访 |
| 腰痛VAS评分 | 128 | 4.34±1.38 | 0.73±0.78a |
| 腿痛VAS评分* | 87 | 3.45±1.49 | 0.23±0.45b |
| ODI评分(%) | 128 | 52.20±17.27 | 5.19±10.33a |
| a:P < 0.05,与术前比较 | |||
2.3.2 影像学检查结果
腰椎滑脱患者均获满意复位,脊柱后凸畸形得到矫正,术中及术后随访未发现螺钉松动、移位、拔出及断裂(表 4)。术后3个月CT显示椎间及螺钉周围出现新骨形成,末次随访病例均获骨融合,融合率达到100%。无一例出现螺钉切割椎体及椎弓根,随访过程中未发现需要翻修病例。
| 时相点 | 椎间隙高度/mm | 椎体高度/mm | 滑脱角/° | Taillard指数/% | x/mm | y/mm |
| 术前 | 9.04±3.11 | 16.16±6.23 | 7.09±5.67 | 27.02±12.14 | — | — |
| 术后 | 12.26±1.90a | 22.08±5.01a | 10.75±4.87a | 6.11±8.30a | 4.71±2.94 | 8.37±2.96 |
| 末次随访 | 11.89±1.93ab | 22.32±5.21ab | 10.16±5.00ab | 6.19±7.74ab | 4.82±2.98b | 8.48±2.91b |
| a:P < 0.05,与术前比较;b:P < 0.05,与术后比较;x:钉尖至椎体前缘距离;y:钉尖至上终板距离 | ||||||
2.4 典型病例
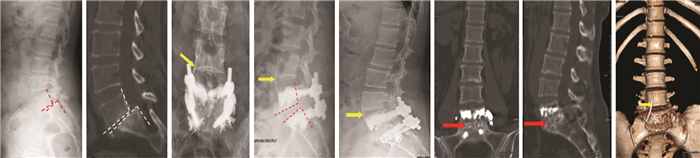
患者女性,51岁,术前诊断:①L5椎体滑脱症(峡部裂型,Ⅱ度);②重度骨质疏松症(骨密度T值:-2.9)。术前腰痛及左下肢疼痛VAS评分分别为6、5分,ODI评分31.11%。术前X线片、CT检测见图 1A、B。L5/S1椎间隙高度4.35 mm,滑脱角7.23°,滑脱指数46.68%。给予手术治疗:经后路L5椎体滑脱复位、L5/S1椎间盘摘除、椎管减压、椎间植骨融合、椎弓根螺钉内固定术。术后复查X线片显示L5椎体完全复位,骨水泥弥散满意,少量骨水泥向椎体前方静脉渗漏(图 1C、D),患者无不适主诉。术后L5/S1椎间隙高度13.49 mm,滑脱角10.31°,滑脱指数7.65%。术后1、3、6、12、36、71个月分别随访,腰腿痛症状逐步缓解(表 5)。术后1个月腰痛VAS评分、腿痛VAS评分、ODI评分分别为2分、0分、27.78%;术后3个月腰痛VAS评分、腿痛VAS评分、ODI评分分别为1分、0分、13.44%;术后6个月至末次随访腰腿痛症状完全缓解,VAS评分均为0分,ODI评分2.22%;末次随访L5/S1“椎间隙”高度9.24 mm,滑脱角11.95°,滑脱指数8.38%,椎体高度较术后即刻有所丢失(图 1E~H)。
|
| A、B:术前X线片、CT示L5椎体向前Ⅱ度滑脱,峡部裂;C、D:术后即刻复查X线片见L5椎体完全复位,骨水泥弥散满意,少量骨水泥向椎体前方静脉渗漏;E~H:末次随访(术后71个月)X线片示螺钉无明显移位,椎体无明显滑脱,CT示L5/S1椎间骨性融合 图 1 应用CICPS的典型病例影像学检查 |
| 时间 | 腰痛VAS评分 | 左下肢痛VAS评分 | ODI/% | 椎间隙高度/mm | 滑脱角/° | Taillard指数/% | x/mm | y/mm |
| 术前 | 6 | 5 | 31.11 | 4.35 | 7.23 | 46.68 | - | - |
| 术后 | 4 | 2 | 35.56 | 13.49 | 10.31 | 7.65 | 11.87 | 3.59 |
| 术后1个月 | 2 | 0 | 27.78 | 13.2 | 10.69 | 7.78 | 12.03 | 3.32 |
| 术后3个月 | 1 | 0 | 13.44 | 13.02 | 11.32 | 7.53 | 11.56 | 3.65 |
| 术后6个月 | 0 | 0 | 2.22 | 12.93 | 10.86 | 7.42 | 11.9 | 3.44 |
| 术后12个月 | 0 | 0 | 2.22 | 13.03 | 11.03 | 7.28 | 11.22 | 3.98 |
| 术后36个月 | 0 | 0 | 2.22 | 12.57 | 11.51 | 8.01 | 11.55 | 3.87 |
| 术后71个月 | 0 | 0 | 2.22 | 9.24 | 11.95 | 8.38 | 11.24 | 3.64 |
| x:钉尖至椎体前缘距离;y:钉尖至上终板距离 | ||||||||
3 讨论
OP是指一种以普遍骨量减少,骨小梁结构组成下降,从而引起骨强度减低、骨折风险升高的全身性骨病。根据世界卫生组织的诊断标准,将骨密度T值≤-2.5定义为OP。虽然椎弓根螺钉已成为成人脊柱内固定系统中的核心[1],但是当脊柱内固定手术遇到OP时,椎弓根螺钉松动、拔出却成了最大的、最常见的问题。尽管使用更粗、更长的椎弓根螺钉或者不同螺杆、螺纹设计的椎弓根螺钉能提高其在所置入椎体内的把持力[4, 17-19], 骨水泥强化的椎弓根螺钉仍被认为更适用于恢复和维持退行性脊柱的稳定性[20-21]。多个生物力学研究及临床研究显示,PMMA强化可提高螺钉在OP椎体及正常椎体内的抗拔出力[15, 21]。本研究小组自行研究设计的这款新型可注射CICPS,具有三个大小、形态、位置各异的侧孔、可活动钉头,在生物力学实验及初期临床应用中均显示出其显著的优点。本研究通过对较多病例较长时间的随访,从临床症状、并发症、影像学检查多个方面的不同指标对其安全性、有效性进行综合评估。研究结果表明,这种新型的椎弓根螺钉在OP患者的脊柱内固定手术应用中安全有效。
在不同种类的骨水泥中,PMMA因其价格便宜、容易生产、机械性能好而被广泛应用于临床[1]。PMMA骨水泥的常用注射方式通常有两种,在经皮椎体成形术(percutaneous vertebroplasty,PVP)中直接或通过空心螺钉注射入椎体,在经皮后凸成形术(percutaneous kyphoplasty,PKP)中则是先置入球囊扩张撑开椎体,再向空腔内注入骨水泥,恢复和维持椎体高度及脊柱后凸[1]。总的来说前者较后者好,其抗拔出力较未强化的骨水泥螺钉增加80%[22]。置钉前注射骨水泥其分布难以控制,置钉时螺钉会将骨水泥挤出钉道甚至椎体外,因此存在较高的渗漏风险[11]。而经空心椎弓根螺钉注射骨水泥可控性更好,当发现有骨水泥渗漏迹象时立即停止注射,减少渗漏风险及脊髓、神经、血管等软组织损伤。因此我们认为经空心螺钉注射PMMA骨水泥安全有效。
在螺钉的设计中,侧孔的存在可提高抗拔出力。CHEN等[3]研究发现,增加侧孔数目可提高椎弓根螺钉最大轴向抗拔出力,骨水泥溢出的主要部位是近端侧孔,而非远端侧孔。研究表明,空心螺钉的侧孔离钉头越近螺钉的抗拔出力越大,是因为这种螺钉可在更短时间内有更多骨水泥溢出、分布更广。但是,增加侧孔数量可能增加螺钉断裂风险,而侧孔位置太靠近钉头又会增加骨水泥向椎管内渗漏的风险。为了解决这些问题,我们设计出了一款新型可注射骨水泥椎弓根螺钉,即CICPS,在螺钉前2/5(即近钉尖一端)设计3个侧孔,由小到大纵向分布,空心螺钉尖端是封闭的。这种设计可使得在注射骨水泥时各个侧孔的阻力大小基本一致,骨水泥可均匀分布螺钉远端周围。已通过影像学检查证实这一设想[3]。骨水泥均匀分布可有效减少甚至避免骨水泥向椎管内渗漏所引起的临床并发症。可以断定,这种空心螺钉明显优于现有的其他空心螺钉[15-16]。
除此之外,骨水泥用量与螺钉抗拔出力及骨水泥渗漏风险均密切相关。理论上,在一定范围内,骨水泥用量越多,所能提供的抗拔出力就越大。但是,在保证螺钉足够的抗拔出力的前提下,尽量减少骨水泥用量具有很多优点,例如降低骨水泥渗漏风险及相关并发症,减少PMMA单体甲基丙烯酸甲酯(methylmethacrylate,MMA)的毒性。本研究中每颗CICPS的PMMA用量为1.2~1.7(1.51±0.13) mL,显著低于FRANKEL等[23]报道的2.0~5.0(2.89±0.72)mL及MOON等[14]报道的1.7~2.0(1.83±0.11)mL。骨水泥渗漏率(15.63%)亦明显低于JANSSENA等[11]报道的66.7%。CICPS万向活动钉头及单轴旋转钉头设计、专用骨水泥注射器及连接装置使得手术操作更为简便,可有效缩短手术时间、减少术中及术后出血,减少术后相关并发症的发生,有利于患者术后康复,这是CICPS系统又一优势。因患者病种、手术方式、手术节段各异,无法横向或纵向比较手术时间、术中出血量。本研究中患者腰腿症状术后均得到不同程度的减轻,功能均明显改善,主要得益于坚强的内固定。螺钉松动、拔出是内固定失败的主要原因,其发生率达0.6%~11%[24]。而在我们平均随访时间长达42个月的随访过程中,未发现1例螺钉松动、拔出。术后X线片也未发现螺钉明显移位,CT显示所有病例末次随访(≥2年)均获骨融合,融合率100%,无钉棒断裂及内固定失败情况发生。术后X线片示腰椎滑脱病例的滑脱角及Taillard指数较术前均有明显改善,末次随访较术后即刻无明显变化,提示PMMA强化的CICPS对纠正腰椎滑脱、维持滑脱椎体稳定性是可靠的。对AS伴脊柱后凸畸形病例,CICPS内固定系统可有效矫正后凸畸形并维持手术节段的稳定性,即使AS病情进展,手术节段也不会出现明显后凸畸形。对所有病例,CICPS内固定系统均可维持椎体高度及椎间隙高度。
需要说明的是,本研究尚存在以下几方面不足和局限:第一,本研究不是对照研究。无法进行对照研究的原因,一是病例性别、年龄、体质量指数、骨密度、病种、手术方式、手术节段等可变因素较多且各不相同,病例选择时很难实现同质性;二是OP患者因骨质差,普通螺钉在其椎体内抗拔出强度差,松动、拔出风险高,不宜作为对照组,也是伦理所不允许的。第二,骨密度不能代表骨强度。骨密度检查提示OP并不意味着骨强度差,不代表螺钉在椎体内抗拔出力差。双光子骨密度检查亦不能准确反映骨密度尤其是钉道骨密度。仅凭术中医师手感判断又缺乏客观性,且不能量化。因此,根据双光子骨密度T值评估是否使用CICPS不够严谨,需进一步寻求评估骨强度的方法及技术。第三,术后随访过程中影像学检查结果存在偏差。因为病例较多、随访节点不一致、随访时间较长,术后影像学检查可能因为患者体位不完全相同、投射角度不同等原因出现影像学结果偏差。但因病例较多,统计分析可部分消除系统误差,因此影响不大。
| [1] | LIU D, SHI L, LEI W, et al. Biomechanical comparison of expansive pedicle screw and polymethylmethacrylate-augmented pedicle screw in osteoporotic synthetic bone in primary implantation: an experimental study[J]. Clin Spine Surg, 2016, 29(7): E351–357. DOI:10.1097/BSD.0b013e31828bfc85 |
| [2] | SCHMID S L, BACHMANN E, FISCHER M, et al. Pedicle screw augmentation with bone cement enforced Vicryl mesh[J]. J Orthop Res, 2018, 36(1): 212–216. |
| [3] | CHEN L H, TAI C L, LEE D M, et al. Pullout strength of pedicle screws with cement augmentation in severe osteoporosis: a comparative study between cannulated screws with cement injection and solid screws with cement pre-filling[J]. BMC Musculoskelet Disord, 2011, 12: 33. DOI:10.1186/1471-2474-12-33 |
| [4] | KIM Y Y, CHOI W S and RHYU K W. Assessment of pedicle screw pullout strength based on various screw designs and bone densities-an ex vivo biomechanical study[J]. Spine J, 2012, 12(2): 164–168. DOI:10.1016/j.spinee.2012.01.014 |
| [5] | YU T, ZHANG X, LIU J, et al. Superior cortical screw in osteoporotic lumbar vertebrae: A biomechanics and microstructure-based study[J]. Clin Biomech, 2018, 53: 14–21. DOI:10.1016/j.clinbiomech.2018.01.017 |
| [6] | ZHUANG X M, YU B S, ZHENG Z M, et al. Effect of the degree of osteoporosis on the biomechanical anchoring strength of the sacral pedicle screws: an in vitro comparison between unaugmented bicortical screws and polymethylmethacrylate augmented unicortical screws[J]. Spine, 2010, 35(19): 925–931. DOI:10.1097/BRS.0b013e3181c5fb21 |
| [7] | SHI L, WANG L, GUO Z, et al. A study of low elastic modulus expandable pedicle screws in osteoporotic sheep[J]. J Spinal Disord Tech, 2012, 25(2): 123–128. DOI:10.1097/BSD.0b013e31820ef9f7 |
| [8] | KIYAK G, BALIKCI T, HEYDAR A M, et al. Comparison of the Pullout Strength of Different Pedicle Screw Designs and Augmentation Techniques in an Osteoporotic Bone Model[J]. Asian Spine J, 2018, 12(1): 3–11. DOI:10.4184/asj.2018.12.1.3 |
| [9] | LIU D, SHENG J, LUO Y, et al. Biomechanical comparative study of the stability of injectable pedicle screws with different lateral holes augmented with different volumes of polymethylmethacrylate in osteoporotic lumbar vertebrae[J]. Spine J, 2018. DOI:10.1016/j.spinee.2018.03.009 |
| [10] | BECKER S, CHAVANNE A, SPITALER R, et al. Assessment of different screw augmentation techniques and screw designs in osteoporotic spines[J]. Eur Spine J, 2008, 17(11): 1462–1469. DOI:10.1007/s00586-008-0769-8 |
| [11] | JANSSEN I, RYANG Y M, GEMPT J, et al. Risk of cement leakage and pulmonary embolism by bone cement-augmented pedicle screw fixation of the thoracolumbar spine[J]. Spine J, 2017, 17(6): 837–844. DOI:10.1016/j.spinee.2017.01.009 |
| [12] | MARTIN-FERNANDEZ M, LOPEZ-HERRADON A, PINERA A R, et al. Potential risks of using cement-augmented screws for spinal fusion in patients with low bone quality[J]. Spine J, 2017, 17(8): 1192–1199. DOI:10.1016/j.spinee.2017.04.029 |
| [13] | STADELMANN V A, BRETTON E, TERRIER A, et al. Calcium phosphate cement augmentation of cancellous bone screws can compensate for the absence of cortical fixation[J]. J Biomech, 2010, 43(15): 2869–2874. DOI:10.1016/j.jbiomech.2010.07.025 |
| [14] | MOON B J, CHO B Y, CHOI E Y, et al. Polymethylmethacrylate-augmented screw fixation for stabilization of the osteoporotic spine: a three-year follow-up of 37 patients[J]. J Korean Neurosurg Soc, 2009, 46(4): 305–311. DOI:10.3340/jkns.2009.46.4.305 |
| [15] | LIU Y, XU J, SUN D, et al. Biomechanical and finite element analyses of bone cement-Injectable cannulated pedicle screw fixation in osteoporotic bone[J]. J Biomed Mater Res Part B Appl Biomater, 2016, 104(5): 960–967. DOI:10.1002/jbm.b.33424 |
| [16] | DAI F, LIU Y, ZHANG F, et al. Surgical treatment of the osteoporotic spine with bone cement-injectable cannulated pedicle screw fixation: technical description and preliminary application in 43 patients[J]. Clinics, 2015, 70(2): 114–119. DOI:10.6061/clinics/2015(02)08 |
| [17] | PATEL P S, SHEPHERD D E, HUKINS D W. The effect of screw insertion angle and thread type on the pullout strength of bone screws in normal and osteoporotic cancellous bone models[J]. Med Eng Phys, 2010, 32(8): 822–828. DOI:10.1016/j.medengphy.2010.05.005 |
| [18] | VARGHESE V, SARAVANA KUMAR G, KRISHNAN V. Effect of various factors on pull out strength of pedicle screw in normal and osteoporotic cancellous bone models[J]. Med Eng Phys, 2017, 40: 28–38. DOI:10.1016/j.medengphy.2016.11.012 |
| [19] | LORENZ A, LEICHTLE C I, FRANTZ S, et al. Pull out Strength of Dual Outer Diameter Pedicle Screws Compared to Uncemented and Cemented Standard Pedicle Screws: A Biomechanical in vitro Study[J]. Orthop Surg, 2017, 9(2): 229–236. DOI:10.1111/os.12322 |
| [20] | CHANDRA V V, PRASAD B C, JAGADEESH M A, et al. Segmental polymethylmethacrylate-augmented fenestrated pedicle screw fixation for lumbar spondylolisthesis in patients with osteoporosis-A case series and review of literature[J]. Neurol India, 2017, 65(1): 89–95. DOI:10.4103/0028-3886.198229 |
| [21] |
孙浩林, 李淳德, 杨泽川, 等. 多孔中空椎弓根螺钉骨水泥加强固定治疗合并骨质疏松症的腰椎退变性疾病[J].
北京大学学报(医学版), 2016, 48(6): 1019–1025.
SUN H L, LI C D, YANG Z C, et al. Polymethylmethacrylate augmentation of bone cement-injectable cannulated pediclescrews for the treatment of degenerative lumbar diseases with osteoporosis[J]. J Peking Univ (Health Sciences), 2016, 48(6): 1019–1025. DOI:10.3969/j.issn.1671-167X.2016.06.017 |
| [22] | SHEA T M, LAUN J, GONZALEZ-BLOHM S A, et al. Designs and techniques that improve the pullout strength of pedicle screws in osteoporotic vertebrae: current status[J]. Biomed Res Int, 2014, 2014: 748393. DOI:10.1155/2014/748393 |
| [23] | FRANKEL B M, JONES T, WANG C. Segmental polymethylmethacrylate-augmented pedicle screw fixation in patients with bone softening caused by osteoporosis and metastatic tumor involvement: a clinical evaluation[J]. Neurosurgery, 2007, 61(3): 531–537. DOI:10.1227/01.NEU.0000290899.15567.68 |
| [24] | MUMMANENI P V, HADDOCK S M, LIEBSCHNER M A, et al. Biomechanical evaluation of a double-threaded pedicle screw in elderly vertebrae[J]. J Spinal Disord Tech, 2002, 15(1): 64–68. DOI:10.1097/00024720-200202000-00012 |



