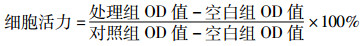2. 400010 重庆,重庆医科大学超声分子影像研究所;
3. 400010 重庆,重庆医科大学附属第二医院妇产科
2. Institute of Ultrasound Imaging, Chongqing Medical University, Chongqing, 400010;
3. Department of Obstetrics and Gynecology, the Second Affiliated Hospital of Chongqing Medical University, Chongqing, 400010, China
类风湿关节炎(rheumatoid arthritis,RA)是一种以对称性的多关节滑膜炎症性病变为主要病理特征的慢性自身免疫性疾病[1]。尽管RA的确切病理机制尚未完全阐明,但病变关节滑膜组织中异常增殖的成纤维样滑膜细胞(fibroblast-like synoviocytes,FLSs)在关节炎的发生与发展过程中起着至关重要的作用[2]。靶向抑制或破坏病变关节滑膜组织中异常增殖的FLSs,可有效阻止RA的发生与发展。声动力疗法(sonodynamic therapy,SDT)是基于低强度超声介导声敏性物质产生声动力学效应而发挥治疗作用的一种新兴治疗方法,具有靶向定位以及可对体内深部病变组织产生治疗作用的优点[3-4]。SDT在实体肿瘤[5-6]以及动脉粥样硬化[7]等增生性疾病的研究中已取得显著的治疗效果。司帕沙星(sparfloxacin)为氟喹诺酮类抗菌药,通过作用于细胞内DNA回旋酶发挥杀菌作用。经全身用药后,司帕沙星在骨关节组织中有较多的分布,被广泛用于全身抗感染治疗。研究报道司帕沙星具有良好的声敏特性,其介导的声动力治疗显示出显著的抗肿瘤细胞毒性[8]。本研究通过体外探讨司帕沙星介导SDT对FLSs的损伤作用,阐明其可能的作用机制,旨在为司帕沙星介导SDT靶向治疗RA提供前期研究基础。
1 材料与方法 1.1 材料 1.1.1 主要试剂与细司帕沙星为上海源叶生物科技有限公司产品,经适量N, N-dimethylformamide(DMF)助溶,配置成浓度为1.00 mmol/L的母液。过滤除菌,避光冷藏保存备用。MTT、组氨酸、甘露醇购自Sigma公司。2’, 7’-dichlorodihydrofluorescein diacetate (DCFH-DA)购自上海碧云天生物技术有限公司。Annexin V-FITC/propidium iodide凋亡试剂盒购自杭州隆基生物技术有限公司。DMEM和FBS购自Hyclone公司。人类风湿关节炎成纤维样滑膜细胞株MH7A从BioVector NTCC公司引进,培养于含15% FBS和1%青霉素-链霉素的DMEM培养液中,置于温度为37 ℃、5% CO2恒温孵育箱中培养。取指数生长期细胞进行相关实验。
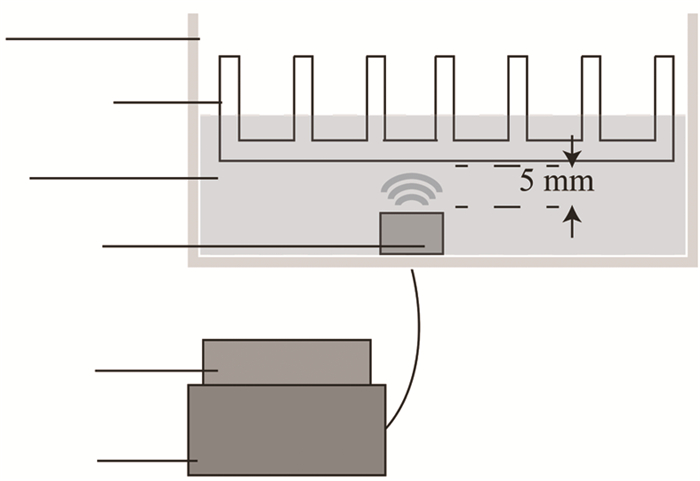
1.1.2 超声装置实验用超声装置(图 1)根据重庆医科大学超声分子影像研究所研制的UGT 1025机型超声装置[9]定制。超声探头为非聚焦探头,直径为20 mm,频率为1.0 MHz。超声辐照采用脉冲模式。为避免超声热效应对实验结果的影响,超声探头被垂直地固定在水槽底部,细胞培养板被固定在探头正上方5 mm处。探头与培养板之间充满预制冷的脱气水。超声辐照前后,培养板中培养液的温度均无明显变化(±1 ℃)。
|
| 图 1 超声装置简易图 |
1.2 方法 1.2.1 司帕沙星浓度筛选
将MH7A细胞接种于96孔板中过夜贴壁。分别予以浓度为0.01~100.00 μmol/L的司帕沙星孵育24 h。然后严格按照标准的MTT法进行操作,并在多功能酶标仪(ELx800,Bio-TEK,USA)中测定各组的吸光度(OD)值[10]。依据细胞活力筛选出司帕沙星的最适药物浓度。
1.2.2 超声参数筛选将MH7A细胞接种于96孔板中过夜贴壁。将超声辐照强度分别设置为0.5、1.0、2.0 W/cm2,然后在每一辐照强度下分别辐照30、60、90 s。经不同参数超声辐照处理后,继续培养24 h。严格按照标准的MTT法测定各组的细胞活力。依据细胞活力筛选出最适超声参数。
1.2.3 声动力治疗处理将MH7A细胞接种于培养板后,根据随机数字表法将其分为对照组、司帕沙星组、超声组以及SDT组。司帕沙星组和SDT组分别加入1.00 μmol/L司帕沙星;超声组和对照组分别加入等体积的无血清培养基。在37 ℃孵箱中避光孵育4 h后,超声组和SDT组分别被频率为1.0 MHz,强度为1.0 W/cm2的超声辐照60 s。随后,各组细胞被置于37 ℃孵箱中继续培养,以备后续实验。在活性氧物质(reactive oxygen species,ROS)清除剂的阻抗实验中,各组细胞在超声辐照前分别经等体积的ROS清除剂组氨酸(终浓度为10.00 mmol/L)或甘露醇(终浓度为100.00 mmol/L)孵育1 h。所有指标在室温下避光检测,并重复测定3次。
1.2.4 细胞活力检测将MH7A细胞接种于96孔板中过夜贴壁。经不同措施处理24 h后,严格按照标准的MTT法测定各组的细胞活力。
1.2.5 细胞凋亡检测将MH7A细胞接种于24孔板中过夜贴壁。经不同措施处理24 h后,严格按照Annexin V-FITC/propidium iodide凋亡试剂盒的操作说明书进行染色处理,然后采用流式细胞仪(BD Biosciences,USA)测定各组细胞的凋亡率[11]。
1.2.6 细胞内ROS检测DCFH-DA是一种非特异性的ROS指示剂,其自身无荧光特性,可自由地穿过细胞膜。当细胞内存在ROS时,DCFH-DA可被迅速地氧化生成具有强荧光特性的DCF(荧光素)。DCF不能穿过细胞膜,从而可用于检测细胞内的ROS含量[12]。将MH7A细胞接种于96孔板中过夜贴壁。经司帕沙星处理3.5 h后,各组分别加入等量DCFH-DA溶液(终浓度为10.00 μmol/L),在室温下避光孵育30 min,予以超声处理。继续培养0.5 h后,经PBS溶液充分清洗,在多功能荧光酶标仪(Varioskan Flash,Thermo Fisher Scientific,USA)中测定各组细胞内的ROS含量。检测所用的激发波长和发射波长分别为488 nm和525 nm。
1.3 统计分析利用Graphpad Prism 5.01软件对实验数据进行分析。计量资料数据以x±s表示,进行单因素方差分析。以P < 0.05为差异有统计学意义。
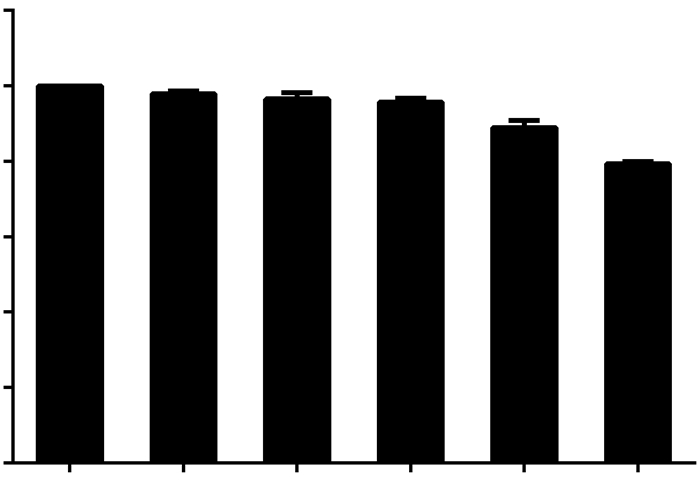
2 结果 2.1 司帕沙星对MH7A细胞活力的影响如图 2所示,MH7A细胞的活力随着司帕沙星浓度的增加而逐渐降低。为使司帕沙星的声动力细胞毒性最大,而其自身的药理毒性最小,1.00 μmol/L司帕沙星被选为最适宜的药物浓度以备后续实验。
|
| a:P < 0.01,与0.00 μmol/L组比较 图 2 不同浓度司帕沙星对MH7A细胞活力的影响 |
2.2 超声对MH7A细胞活力的影响
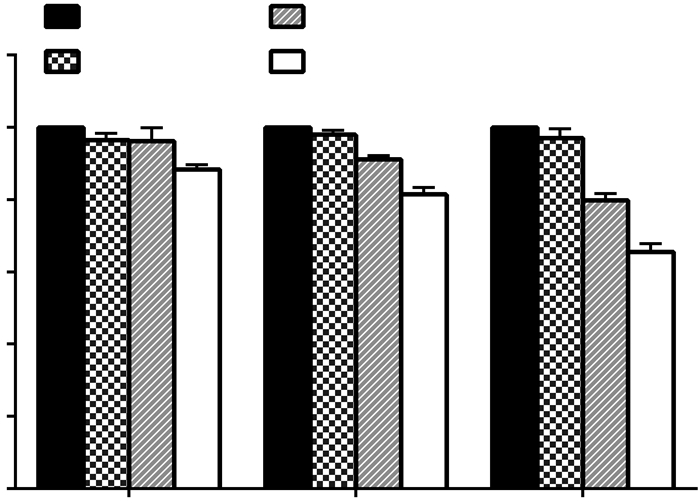
如图 3示,随着超声辐照强度增加或辐照时间延长,MH7A细胞的活力逐渐降低。为使声动力细胞毒性最大,而超声机械损伤作用最小,辐照强度为1.0 W/cm2,辐照时间为60 s被选为最适宜的超声参数以备后续实验。
|
| a:P < 0.01,与0.0 W/cm2辐照组比较 图 3 不同参数超声对MH7A细胞活力的影响 |
2.3 司帕沙星介导SDT诱导MH7A细胞活力降低
如图 4所示,与对照组相比,司帕沙星组的细胞活力无明显变化,差异无统计学意义(P>0.05),超声组的细胞活力轻微降低(P < 0.01)。然而,当司帕沙星联合超声作用于MH7A细胞时,细胞活力显著下降,与对照组相比,差异具有统计学意义(P < 0.01)。提示司帕沙星介导SDT显著地诱导MH7A细胞活力降低。
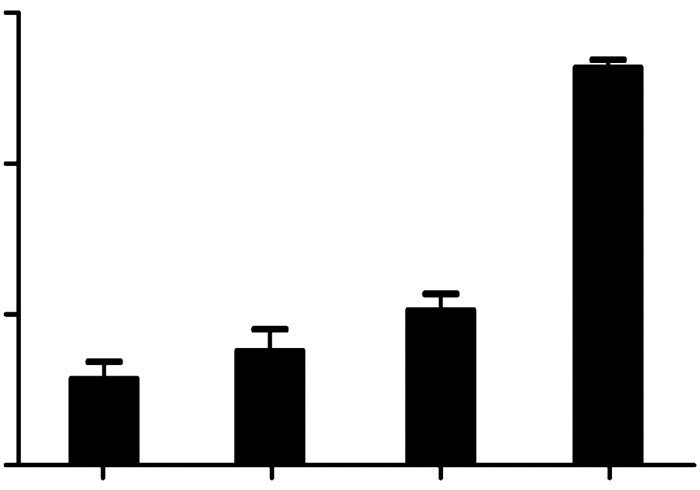
2.4 司帕沙星介导SDT诱导MH7A细胞凋亡增加如图 5所示,与对照组相比,司帕沙星组的细胞凋亡率无明显增加(P>0.05),超声组的细胞凋亡率轻微增加(P < 0.01)。然而,当司帕沙星联合超声作用于MH7A细胞时,凋亡率显著增加,与对照组相比,差异具有统计学意义(P<0.01)。提示司帕沙星介导SDT显著地诱导MH7A细胞凋亡增加。

|
|
1:对照组;2:司帕沙星组;3:超声组;4:SDT组 a:P < 0.01,与对照组比较 图 4 司帕沙星介导SDT对MH7A细胞活力的影响 |
|
|
1:对照组;2:司帕沙星组;3:超声组;4:SDT组 a:P < 0.01,与对照组比较 图 5 司帕沙星介导SDT对MH7A细胞凋亡的影响 |
2.5 司帕沙星介导SDT诱导MH7A细胞内产生过量ROS
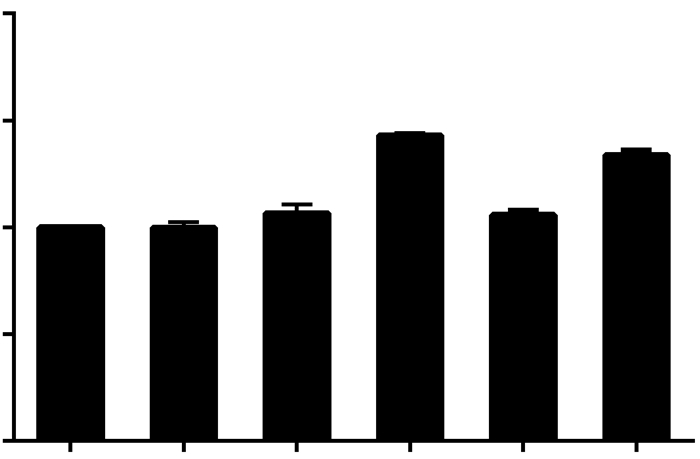
如图 6所示,与对照组相比,司帕沙星组和超声组中DCF的荧光值均无明显变化(P>0.05)。然而,当司帕沙星联合超声作用于MH7A细胞时,DCF的荧光值显著地增加,与对照组相比,差异具有统计学意义(P < 0.01),提示司帕沙星介导SDT诱导MH7A细胞内产生过量的ROS。
|
|
1:对照组;2:司帕沙星组;3:超声组;4:SDT组;5:SDT+组氨酸组;6:SDT+甘露醇组 a:P<0.01,与对照组比较;b:P < 0.01,与SDT组比较 图 6 MH7A细胞内ROS的产生情况 |
2.6 ROS清除剂减轻司帕沙星介导SDT诱导MH7A细胞损伤
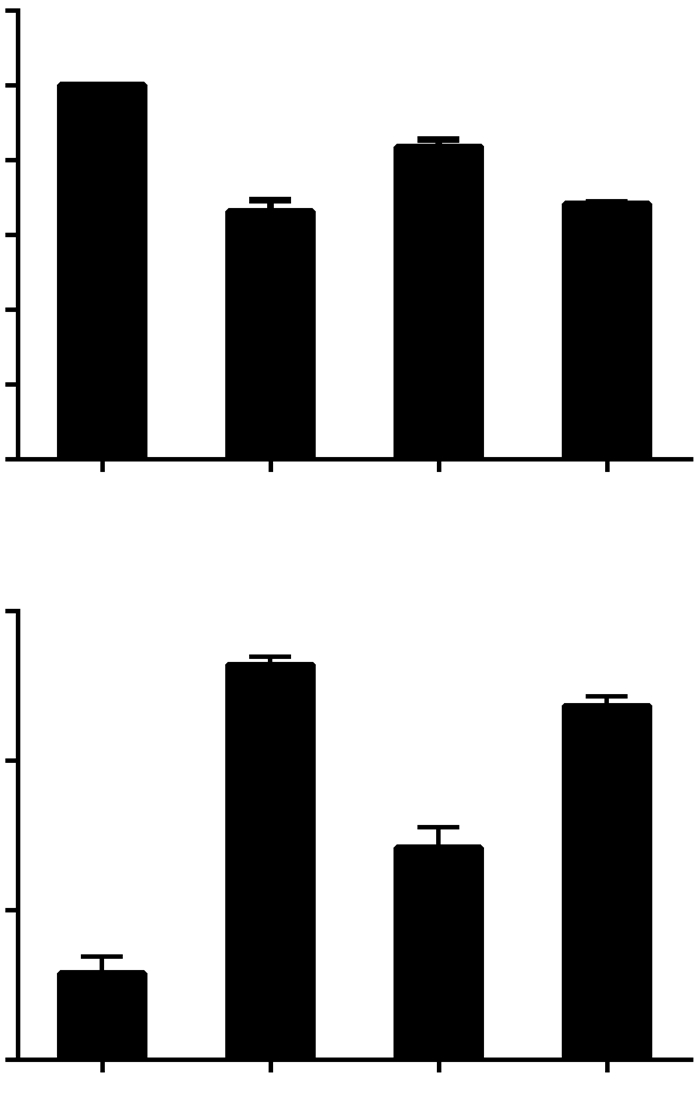
提前加入ROS清除剂组氨酸处理时,SDT组的细胞活力显著增加,与未加入组氨酸相比,差异具有统计学意义(P < 0.01);提前加入ROS清除剂甘露醇处理时,细胞活力轻微增加,与未加入甘露醇相比,差异无统计学意义(P>0.05,图 7A)。提前加入ROS清除剂组氨酸处理时,细胞凋亡率显著下降,与未加入组氨酸相比,差异具有统计学意义(P < 0.01);提前加入ROS清除剂甘露醇处理时,细胞凋亡率轻微下降,与未加入甘露醇相比,差异有统计学意义(P < 0.05,图 7B)。提示,与ROS清除剂甘露醇相比,ROS清除剂组氨酸有效地减轻司帕沙星介导SDT诱导MH7A细胞损伤。
|
|
A:细胞活力变化;B:细胞凋亡变化1:对照组;2:SDT组;3:SDT+组氨酸组;4:SDT+甘露醇组 a:P < 0.01,与对照组比较;b:P < 0.01,c:P < 0.05,与SDT组比较s 图 7 ROS清除剂对SDT诱导MH7A细胞损伤的影响 |
3 讨论
SDT是一种新兴的无创治疗方法,通过联合低强度超声和声敏性物质,协同发挥靶向治疗作用,主要用于治疗增生性疾病的研究。司帕沙星是一种氟喹诺酮类抗菌药,易进入细胞,并且具有显著的声敏特性。本课题旨在探索司帕沙星介导的SDT对FLSs的损伤作用,并阐明其可能的作用机制。
在本研究中,司帕沙星对MH7A细胞无明显的损伤作用,超声轻微地引起MH7A细胞活力降低,然而,当司帕沙星联合超声作用于MH7A细胞时,细胞活力显著降低,提示司帕沙星介导的SDT有效地诱导MH7A细胞损伤。本研究中使用的司帕沙星浓度(1.00 μmol/L,约为0.40 μg/mL)近似于在治疗剂量下药代动力学研究中所报道的司帕沙星的血药浓度(最大0.70 μg/mL)[13]。因此,若在此浓度下将司帕沙星应用于体内,对机体组织是安全的。
近年来,一系列研究发现超声和SDT均可诱导细胞凋亡增加[6, 14]。在细胞被暴露于超声环境之前,利用声敏剂对细胞进行预处理,显著地降低诱导细胞凋亡所需要的超声能量[15],提示SDT是一种相对比较安全和有效的治疗方法。在本研究中,SDT组细胞凋亡率显著高于对照组、司帕沙星组以及超声组,提示司帕沙星介导SDT显著地诱导MH7A细胞凋亡增加。SDT的机制非常复杂。当前较为公认的机制主要包括:诱导细胞内产生过量的ROS、高强度超声机械应激以及超声热效应[7]。在本研究中,超声辐照前后,细胞培养基中的温度无明显的变化(±1 ℃),因而排除了超声热效应引起细胞损伤的可能。另一方面,经相同参数超声单独处理时,未引起明显的MH7A细胞损伤,因而排除了超声引起的高强度机械应激诱导MH7A细胞损伤的可能。因此,我们重点研究了SDT诱导细胞损伤最可能的机制,即:诱导产生过量的ROS。尽管SDT的确切机制尚未完全明阐明,但一系列实验研究表明SDT诱导细胞损伤主要是通过诱导细胞内产生过量ROS[6, 16-17]。然而,由于SDT诱导产生ROS的机制与声敏剂类型、细胞种类以及超声参数等因素有关。因此,到目前为止国内外仍然没有明确统一是何种ROS在SDT中发挥主要作用。本研究为明确司帕沙星介导SDT是否可以诱导细胞内产生ROS,并探明ROS的种类,我们选用了非特异性的ROS荧光指示剂DCFH-DA进行研究,并选用两种ROS清除剂来进一步验证实验结果的可靠性,即:组氨酸(同时清除单线态氧和羟自由基)和甘露醇(特异性地清除羟自由基)。在本研究中,与对照组、司帕沙星组以及超声组相比,司帕沙星介导SDT显著诱导细胞内产生ROS,同时,与ROS清除剂甘露醇相比,ROS清除剂组氨酸显著减轻SDT对MH7A细胞的损伤作用。由此可知,司帕沙星介导SDT诱导MH7A产生大量的ROS,且主要为单线态氧物质。
本研究表明司帕沙星介导SDT对RA病变滑膜组织中异常增殖的FLSs具有显著的细胞毒性作用,其毒性损伤机制可能与诱导FLSs细胞内产生过量的ROS有关。
| [1] | MCINNES I B, SCHETT G. The pathogenesis of rheumatoid arthritis[J]. N Engl J Med, 2011, 365(23): 2205–2219. DOI:10.1056/NEJMra1004965 |
| [2] | BARTOK B, FIRESTEIN G S. Fibroblast-like synoviocytes: key effector cells in rheumatoid arthritis[J]. Immunol Rev, 2010, 233(1): 233–255. DOI:10.1111/j.0105-2896.2009.00859.x |
| [3] | BILMIN K, KUJAWSKA T, SECOMSKI W, et al. 5-Aminolevulinic acid-mediated sonosensitization of rat RG2 glioma cells in vitro[J]. Folia Neuropathol, 2016, 54(3): 234–240. DOI:10.5114/fn.2016.62233 |
| [4] | LI Y, WANG P, ZHAO P, et al. Apoptosis induced by sonodynamic treatment by protoporphyrin Ⅸ on MDA-MB-231 cells[J]. Ultrasonics, 2012, 52(4): 490–496. DOI:10.1016/j.ultras.2011.10.013 |
| [5] | SVIRIDOV A P, OSMINKINA L A, KHARIN A Y, et al. Cytotoxicity control of silicon nanoparticles by biopolymer coating and ultrasound irradiation for cancer theranostic applications[J]. Nanotechnology, 2017, 28(10): 105102. DOI:10.1088/1361-6528/aa5b7c |
| [6] | SU X, WANG X, ZHANG K, et al. Sonodynamic therapy induces apoptosis of human leukemia HL-60 cells in the presence of protoporphyrin Ⅸ[J]. Gen Physiol Biophys, 2016, 35(2): 155–164. DOI:10.4149/gpb_2015051 |
| [7] | GUO S, SUN X, CHENG J, et al. Apoptosis of THP-1 macrophages induced by protoporphyrin Ⅸ-mediated sonodynamic therapy[J]. Int J Nanomed, 2013, 8: 2239–2246. DOI:10.2147/IJN.S43717 |
| [8] | HUANG D, OKADA K, KOMORI C, et al. Ultrastructure of sarcoma 180 cells after ultrasound irradiation in the presence of sparfloxacin[J]. Anticancer Res, 2004, 24(3a): 1553–1559. |
| [9] | SUN J, YIN M, ZHU S, et al. Ultrasound-mediated destruction of oxygen and paclitaxel loaded lipid microbubbles for combination therapy in hypoxic ovarian cancer cells[J]. Ultrason Sonochem, 2016, 28: 319–326. DOI:10.1016/j.ultsonch.2015.08.009 |
| [10] | ZHANG F, CHANG M, YU Y, et al. Preparation and evaluation of lipid emulsified docetaxel-loaded nanoparticles[J]. J Pharm Pharmacol, 2015, 67(11): 1546–1555. DOI:10.1111/jphp.12472 |
| [11] | SUN J, YIN M, ZHU S, et al. Ultrasound-mediated destruction of oxygen and paclitaxel loaded lipid microbubbles for combination therapy in hypoxic ovarian cancer cells[J]. Ultrason Sonochem, 2016, 28: 319–326. DOI:10.1016/j.ultsonch.2015.08.009 |
| [12] | HAO D, SONG Y, CHE Z, et al. Calcium overload and in vitro apoptosis of the C6 glioma cells mediated by sonodynamic therapy (hematoporphyrin monomethyl ether and ultrasound)[J]. Cell Biochem Biophys, 2014, 70(2): 1445–1452. DOI:10.1007/s12013-014-0081-7 |
| [13] | SHIMADA J, NOGITA T, ISHIBASHI Y. Clinical pharmacokinetics of sparfloxacin[J]. Clin Pharmacokinet, 1993, 25(5): 358–369. DOI:10.2165/00003088-199325050-00002 |
| [14] | JIA Y, WANG X, LIU Q, et al. Sonodynamic action of hypocrellin B triggers cell apoptoisis of breast cancer cells involving caspase pathway[J]. Ultrasonics, 2017, 73: 154–161. DOI:10.1016/j.ultras.2016.09.013 |
| [15] | XIANG J, XIA X, JINAG Y, et al. Apoptosis of ovarian cancer cells induced by methylene blue-mediated sonodynamic action[J]. Ultrasonics, 2011, 51(3): 390–395. DOI:10.1016/j.ultras.2010.11.005 |
| [16] | YOU D G, DEEPAGAN V G, UM W, et al. ROS-generating TiO2 nanoparticles for non-invasive sonodynamic therapy of cancer[J]. Sci Rep, 2016, 6: 23200. DOI:10.1038/srep23200 |
| [17] | ZHENG X, WU J, SHAO Q, et al. Apoptosis of THP-1 Macrophages Induced by Pseudohypericin-Mediated Sonodynamic Therapy Through the Mitochondria-Caspase Pathway[J]. Cell Physiol Biochem, 2016, 38(2): 545–557. DOI:10.1159/000438649 |