幻肢痛是指主观感觉已被截除的肢体仍然存在,并且伴有不同程度、不同性质疼痛的幻觉现象[1],是截肢后主要并发症之一,其发病率很高,占截肢后患者的60%~80%[2]。截肢后幻肢痛严重影响患者的睡眠质量、情绪、日常生活活动及工作,若能给予有效地治疗对幻肢痛患者预后具有积极的意义[3]。近年研究表明,截肢后大脑皮质非适应性功能重组可能是幻肢痛发生的重要机制之一。这为临床缓解幻肢痛提供了新的思路,在临床上尝试应用镜像运动疗法来缓解截肢后幻肢痛[4-6]。目前镜像运动疗法因其低成本、无创伤、操作简单,被广泛应用于临床实践,很有可能成为截肢后幻肢痛治疗的一种很有前途的治疗方法,但是镜像运动在大脑中是如何发挥作用的,其神经机制目前尚不清楚。功能近红外光谱技术(functional near-infrared spectroscopy, fNIRS)是一种新兴的、无创的脑功能成像技术,由于该技术灵活、易用,对头动的容忍度高,比较适合运动类任务的脑机制研究[7]。为此,本研究采用fNIRS技术,考察被试在镜像运动过程中大脑皮层血氧浓度变化,并与运动执行任务进行比较,研究其大脑功能激活特征,初步探讨镜像运动的大脑神经机制,从而为镜像运动疗法治疗截肢后幻肢痛提供试验依据。
1 资料与方法 1.1 研究对象招募13名右利手健康被试作为研究对象,被试者均为本校在校师生,其中男性10名,女性3名,年龄为22~34(23.08±3.14)岁,受教育程度均为高中以上。要求被试既往无重要脏器疾病史,无脑部肿瘤或其他颅脑疾患,无精神病史或其他运动功能障碍疾病。采用运动想象能力问卷对其动觉想象和视觉想象能力进行评估[8],此量表主要是通过尝试没有真正运动时感觉自己正在做某个被要求动作和尝试尽可能清晰生动的看到自己做某个被要求动作的难易程度来评估被试运动想象能力,评分从1“非常难”到7“非常容易”。试验前告知被试试验内容和试验流程,被试对本研究知情并签署了知情同意书。该研究方案于2016年经第三军医大学医学伦理委员会批准通过。
1.2 试验任务设计试验任务设计为组块设计,每次试验有5个组块,每个组块包括30 s休息+30 s任务。每个被试需完成2个试验任务,包括左足的运动执行和右足的镜像运动。被试运动执行和镜像运动指令以声音的形式呈现,声音的频率为0.5 Hz/s。运动执行要求被试坐在椅子上,被试的双足置于地面,听到1次声音,左足完成1次背屈及跖屈运动,持续30 s。镜像运动是指利用平面镜成像原理,将右足运动的画面复制到左足,通过视错觉、视觉反馈让被试想象成自己的左足在运动。右足镜像运动时的运动动作、频率和左足运动执行一致。
1.3 数据采集采用NIRScout16×16系统记录大脑皮层血流动力学信息。本系统使用的近红外光波长为760 nm和850 nm。本试验使用了16个光源和16个探测器,左右两侧大脑分别为8个光源和8个探测器,探头间距为3 cm,构成48个光学探测通道,光学探测通道由光源-探测器构成,如光源1(S1)-探测器1(D1)构成光学探测通道1(Ch1)。光源探测器布局见图 1,探测通道见图 2。光源和探测器在被试头上安置时,参照国际脑电10-20系统,使光源、探测器定位于相应的脑电电极位置上,如S16定位于脑电电极C2位置,D14定位于脑电电极C4位置,通过这些脑电电极以及文献[9]报道的脑电电极与大脑MNI坐标的映射关系,可以定位出本研究中光源和探测器构成的光学探测通道主要位于大脑双侧感觉运动皮层区域,其中有部分通道覆盖了大脑的前额叶区域。本试验fNIRS信号采集频率为3.91 Hz。
|
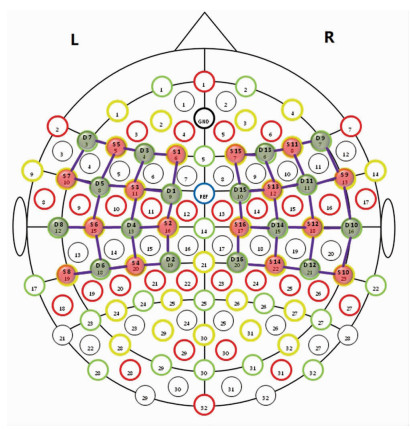
| 橙色圆球S:光源;浅绿色圆球D:探测器;光源和探测器之间紫色的连线:光学探测通道;L:大脑左侧;R:大脑右侧 图 1 被试双侧大脑感觉运动区域光源探测器布局图 |

|
| 1:ch1,由S1-D1构成;2:ch2,由S1-D3构成 图 2 由16个光源和16个探测器构成的48个光学探测通道示意图 |
1.4 试验数据分析 1.4.1 试验数据预处理
首先通过NIRS LAB软件对48通道的fNIRS数据进行预处理,包括去除坏的通道,数据裁剪,带通滤波(0.015~0.1 Hz)[10]。通过带通滤波进行去漂移处理,同时去除头动、心跳等噪声影响。然后根据修订后的比尔-朗伯(吸收)定律(modified Beer-Lambert law,MBLL)将每个通道2个波长的光强信号变化转化为含氧血红蛋白(HbO2)、脱氧血红蛋白(Hb)、总血红蛋白(total Hb)相对浓度变化。因HbO2指标对任务刺激的产生的大脑血氧信号变化更加敏感[11],所以本研究着重分析HbO2的变化。接下来,通过广义线性模型(general linear model, GLM)来建模,用于拟合运动任务效应,然后通过任务拟合参考波来估计GLM模型的参数(GLM模型中不同探测通道的权重值,即beta值)。
1.5 统计学分析通过SPSS 22.0软件进行统计学分析,分别对不同任务下获取的beta值进行单样本t检验或配对样本t检验。取两组任务中单样本t检验显著激活的右侧大脑主运动区和初级感觉皮层探测通道HbO2相对含量时间变化曲线中HbO2相对含量变化均值,其中每个时间点HbO2相对含量变化强度值用Z分数来描述[12],进行配对样本t检验。检验水准:α=0.05。
2 结果 2.1 运动想象能力问卷所有被试的动觉想象能力评分为6.00~7.00(6.50±0.46)分,视觉想象能力评分为5.50~7.00(6.35±0.58)分,所有被试运动想象能力问卷评分都在5分以上,表明所有被试都能容易完成视觉和动觉想象任务,具有较高运动想象能力,能够胜任此试验中镜像运动任务。
2.2 左足运动执行和右足镜像运动下大脑的激活模式对左足运动执行和右足镜像运动任务分别进行单样本t检验,根据各通道的T值绘制了单个任务的组分析的激活图(图 3)。

|
| A:左足运动执行;B:右足镜像运动红色点表示光源,黄色点表示探测器,右侧颜色条显示单样本t检验各通道T值大小,T值越大表明大脑激活越强 图 3 左足运动执行和右足镜像运动时大脑激活图 |
左足运动执行能显著激活大脑双侧感觉运动皮层,包括双侧大脑辅助运动区(BA6),主运动皮层(中央前回,BA4),以及初级感觉皮层(中央后回,BA1)。激活最强的区域主要位于右侧大脑的辅助运动区,主运动区及初级感觉皮层,对应于光学探测通道ch27、ch33、ch34、ch35、ch36、ch37、ch40、ch41、ch43、ch46、ch48(P < 0.01,未矫正,图 3A)。右足镜像运动与左足运动执行激活模式类似,激活范围略小于左足运动执行,主要激活的脑区包括双侧主运动区和初级感觉皮层,右侧大脑激活显著的区域主要位于主运动区和初级感觉皮层,对应于光学探测通道ch35、ch36、ch41、ch43(图 3B)。
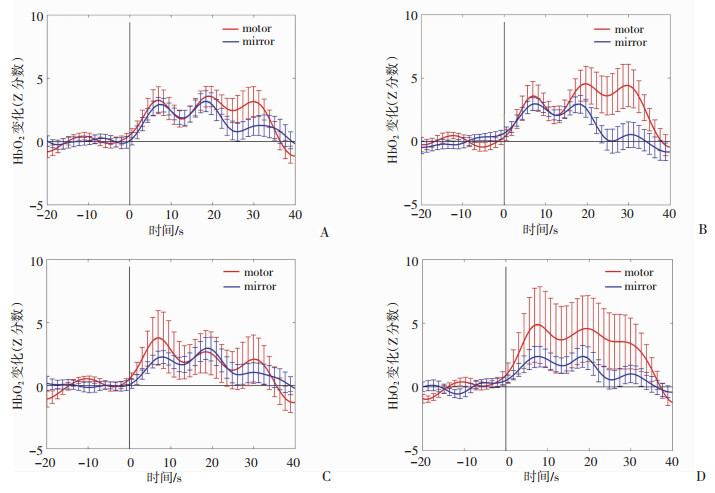
2.3 HbO2平均相对含量时间变化曲线图对左足运动执行和右足镜像运动各通道的beta值进行配对样本t检验,发现2种任务在所有光学探测通道间的差异无统计学意义(P>0.05)。在组间比较差异无统计学意义的前提下,我们进一步分析左足运动执行和右足镜像运动时镜像足对侧(即右侧)大脑主运动区和初级感觉皮层区域激活通道(ch35、ch36、ch41、ch43)HbO2相对含量变化曲线关系(图 4),发现镜像运动在主运动区和初级感觉运动皮层4个探测通道HbO2相对含量变化较运动执行低,但是整体变化趋势比较一致。两种任务均表现为:任务开始后,从基线水平开始上升,达到一定幅值后持续一段时间,在此期间有一定的波动,任务结束后,信号开始下降,经过一段时间HbO2浓度变化回归到基线水平。同时还发现相较于左足运动执行,右足镜像运动HbO2相对浓度时间变化曲线出现下降趋势时间(在18 s左右)早于运动执行,表明镜像运动对大脑激活的持续时间短于运动执行。但两种任务配对样本t检验结果显示,在整个信号变化曲线上HbO2浓度变化均值在两种任务间差异无统计学意义(P>0.05)。
|
| 红色为运动执行足曲线,蓝色为镜像足运动曲线,每条曲线分别标注了整组被试HbO2变化的方差线 图 4 左足运动执行和右足镜像运动时右侧大脑主运动区及初级感觉皮层的光学探测通道ch35(A)、ch36(B)、ch41(C)、ch43(D)HbO2相对含量变化曲线图 |
3 讨论
fNIRS作为一种无创性的光学成像技术,其成像原理是光与脑组织的相互作用。近红外区域(700~1 000 nm)的光对人体组织具有较好穿透性和散射性,而在这个光谱范围内,含氧血红蛋白和脱氧血红蛋白对不同波长近红外光的吸收率是不同的。当大脑在进行神经活动时,脑组织中血流动力学变化会带来含氧血红蛋白和脱氧血红蛋白变化,这些变化会影响近红外光在脑组织中的光学特性,影响脑组织对近红外光的吸收和散射,因此通过测定大脑某一区域内透过脑皮层的光强信号变化,就可以推知该区域含氧血红蛋白和脱氧血红蛋白变化,从而推测该大脑区域在神经活动中的功能状态。相比于现有的功能磁共振成像技术(functional magnetic resonance imaging,fMRI),fNIRS具有比较突出的两大优势:①fNIRS对被试试验过程中的运动不是特别敏感,对被试头动等具有较高的容忍性,因而为运动领域内大脑功能活动的研究开辟了1条新路[7];②fNIRS有相对较高的时间分辨率,这一特点有利于试验反映与神经元活动相关的大脑血流动力学信号,试验对大脑功能状态的时间变化信号特征的检测。基于fNIRS这两大技术优势,本研究采用fNIRS技术对镜像运动时大脑激活特征进行研究,研究结果显示右足镜像运动和左足运动执行均激活了大脑双侧主运动区和初级感觉皮层,同时激活最强区域在右侧大脑主运动区和初级感觉皮层,表明镜像运动和实际运动具有相似的大脑激活模式。从右侧大脑的4个探测通道的HbO2相对含量随刺激时间变化曲线上来看,HbO2浓度变化随任务时间变化的趋势也比较一致,仅存在镜像运动HbO2浓度变化略低于运动执行,且对大脑激活的持续时间短于运动执行,但整个运动过程中两种任务HbO2浓度变化均值差异无统计学意义。
3.1 右足镜像运动时fNIRS激活模式镜像运动疗法是在1995年由RAMACHANDRAN等[13]学者首次提出,并开始应用在截肢后幻肢痛患者的疼痛治疗中。镜像运动疗法是指利用平面镜成像原理,截肢后幻肢痛患者通过镜子观察自己健全肢体,产生被截除肢体仍然存在的视觉错觉,同时当幻肢痛患者运动健全肢体时会主观感觉自己在移动和控制幻肢运动,从而刺激幻肢对应的大脑的感觉运动皮层,从而激活调节那些引发幻肢痛的脑部神经中心,从而逐渐缓解截肢后患者的幻肢痛。在本研究中右足镜像运动时,我们发现了显著激活在左侧主运动区和初级感觉皮层,即实际运动(右足运动)对侧大脑区域激活,同时我们还发现右侧大脑主运动区和初级感觉皮层显著激活,即镜像肢体对侧大脑区域激活。这些结果和之前幻肢痛患者和正常被试fMRI镜像运动研究中激活结果相一致[14-17]。同时对比本研究两种运动任务,我们发现右足镜像运动和左足运动执行有相似的激活模式,均激活了右侧(镜像肢体对侧)大脑的感觉运动皮层。本研究这些研究结果为镜像运动疗法进一步应用于临床截肢后幻肢痛治疗提供了脑功能影像学方面的依据。
3.2 右足镜像运动时HbO2相对含量时间变化曲线目前国内外主要采用fMRI技术对镜像运动进行研究,包括正常被试中镜像运动过程中大脑激活模式研究[14-15],截肢后幻肢痛患者镜像运动大脑激活模式的研究[16-17],以及幻肢痛患者中镜像运动疗法作用效果评估研究[4]。相对于fMRI技术,fNIRS具有较高的时间分辨率,fNIRS这一成像优势能够帮助我们进一步对镜像运动中激活脑区血流动力学响应(血红蛋白浓度变化)的信号时间变化特征进行研究[18]。杜凯等[19]通过fNIRS对运动执行和运动想象过程中HbO2相对含量时间变化曲线进行研究,找出不同状态下被试HbO2浓度变化的时程特点,帮助研究者进一步探索运动想象的神经机制。也有研究者通过fNIRS血氧浓度信号时间特征研究大脑高级活动,如语言、认知、情绪处理等,通过HbO2时间变化曲线中特征指标,譬如曲线中信号峰值延时,来研究正常群体脑功能活动过程或区分正常和病患群体间差异[12, 20]。以上这些研究表明了fNIRS血氧信号的时间变化曲线在描述脑区功能状态变化过程以及临床疾病诊断方面具有很广的应用前景。
本研究对比左足运动执行HbO2相对含量时间变化曲线,发现镜像运动时,镜像肢体对侧大脑主运动区和初级感觉皮层区域的探测通道的HbO2浓度变化略低于左足运动执行,但任务间差异无统计学意义,表明镜像肢体运动能有效刺激其对侧大脑感觉运动区域,达到实际肢体运动执行的作用效果[17]。同时在本研究中,镜像运动在任务开始时,HbO2相对含量变化开始从基线水平0附近上升,达到一定程度后,虽存在一定的波动,但是一直保持在一个较高变化水平,但在18 s后,尽管右足镜像(镜子里的左足)运动仍在进行,但HbO2相对含量变化开始呈现下降趋势。镜像运动HbO2相对含量变化在18 s后开始呈现下降趋势,这一时间曲线特性指标提示我们,可能18 s是正常被试注意力比较集中,镜像肢体参与度最高的时间段,这一特性还有待进一步验证。目前在脑功能成像研究方面少见关于镜像运动疗法治疗时间选择的报道,这一时间特性指标很有可能对临床截肢后幻肢痛镜像运动治疗方案制定具有重要的参考价值。
3.3 研究的局限本研究中任务刺激持续时间尤其是镜像运动持续时间可能对两种任务HbO2相对含量时间变化曲线时间特性指标有一定的影响,这一指标具有较大的临床应用价值。因此,在今后的研究中,可以尽量制定多种试验任务范式,探讨任务持续时间对HbO2相对含量时间变化曲线和时间特性指标的影响。同时,我们研究镜像运动主要是用于截肢后幻肢痛患者临床治疗,因此后期还需要进行幻肢痛患者镜像运动fNIRS研究,进一步探讨镜像运动的神经机制和作用机制。
| [1] | FLOR H, DIERS M, ANDOH J. The neural basis of phantom limb pain[J]. Trends Cogn Sci (Regul Ed), 2013, 17(7): 307–308. DOI:10.1016/j.tics.2013.04.007 |
| [2] | HANLEY M A, EHDE D M, JENSEN M, et al. Chronic pain associated with upper-limb loss[J]. Am J Phys Med Rehabil, 2009, 88(9): 742–751. DOI:10.1097/PHM.0b013e3181b306ec |
| [3] | FOELL J, BEKRATER-BODMANN R, FLOR H, et al. Phantom limb pain after lower limb trauma: origins and treatments[J]. Int J Low Extrem Wounds, 2011, 10(4): 224–235. DOI:10.1177/1534734611428730 |
| [4] | FOELL J, BEKRATER-BODMANN R, DIERS M, et al. Mirror therapy for phantom limb pain: brain changes and the role of body representation[J]. Eur J Pain, 2014, 18(5): 729–739. DOI:10.1002/j.1532-2149.2013.00433.x |
| [5] | RAMADUGU S, NAGABUSHNAM SC, KATUWAL N, et al. Intervention for phantom limb pain: a randomized single crossover study of mirror therapy[J]. Indian J Psychiatry, 2017, 59(4): 457–464. DOI:10.4103/psychiatry.IndianJPsychiatry_259_16 |
| [6] | WITTKOPF P G, JOHNSON M I. Mirror therapy: a potential intervention for pain management[J]. Rev Assoc Med Bras (1992), 2017, 63(11): 1000–1005. DOI:10.1590/1806-9282.63.11.1000 |
| [7] |
白学军, 张琪涵, 章鹏, 等. 基于fNIRS的运动执行与运动想象脑激活模式比较[J].
心理学报, 2016, 48(5): 495–508.
BAI X J, ZHANG Q H, ZHANG P, et al. Comparison of motor execution and motor imagery brain activation patterns: A fNIRS study[J]. Acta Psychologica Sinica, 2016, 48(5): 495–508. DOI:10.3724/SP.J.1041.2016.00495-508 |
| [8] | HALL C R, MARTIN K A. Measuring movement imagery abilities: a revision of the movement imagery questionnaire[J]. Journal of Mental Imagery, 1997, 21: 143–154. |
| [9] | CUTINI S, SCATTURIN P, ZORZI M. A new method based on ICBM152 head surface for probe placement in multichannel fNIRS[J]. Neuroimage, 2011, 54(2): 919–927. DOI:10.1016/j.neuroimage.2010.09.030 |
| [10] | LUU S, CHAU T. Decoding subjective preference from single-trial near-infrared spectroscopy signals[J]. J Neural Eng, 2009, 6(1): 016003. DOI:10.1088/1741-2560/6/1/016003 |
| [11] | HOSHI Y, KOBAYASHI N, TAMURA M. Interpretation of near-infrared spectroscopy signals: a study with a newly developed perfused rat brain model[J]. J Appl Physiol, 2001, 90(5): 1657–1662. DOI:10.1152/jappl.2001.90.5.1657 |
| [12] | ICHIKAWA H, NAKATO E, KANAZAWA S, et al. Hemodynamic response of children with attention-deficit and hyperactive disorder (ADHD) to emotional facial expressions[J]. Neuropsychologia, 2014, 63: 51–58. DOI:10.1016/j.neuropsychologia.2014.08.010 |
| [13] | RAMACHANDRAN V S, ROGERS-RAMACHANDRAN D, COBB S. Touching the phantom limb[J]. Nature, 1995, 377(6549): 489–490. DOI:10.1038/377489a0 |
| [14] | DIERS M, KAMPING S, KIRSCH P, et al. Illusion-related brain activations: a new virtual reality mirror box system for use during functional magnetic resonance imaging[J]. Brain Res, 2015, 1594: 173–182. DOI:10.1016/j.brainres.2014.11.001 |
| [15] | MILDE C, RANCE M, KIRSCH P, et al. Do mirror glasses have the same effect on brain activity as a mirror box? Evidence from a functional magnetic resonance imaging study with healthy subjects[J]. PLoS ONE, 2015, 10(5): e0127694. DOI:10.1371/journal.pone.0127694 |
| [16] | LOTZE M, FLOR H, GRODD W, et al. Phantom movements and pain. An fMRI study in upper limb amputees[[J]. Brain, 2001, 124(Pt 11): 2268–2277. |
| [17] | DIERS M, CHRISTMANN C, KOEPPE C, et al. Mirrored, imagined and executed movements differentially activate sensorimotor cortex in amputees with and without phantom limb pain[J]. Pain, 2010, 149(2): 296–304. DOI:10.1016/j.pain.2010.02.020 |
| [18] | TAK S, YE J C. Statistical analysis of fNIRS data: a comprehensive review[J]. Neuroimage, 2014, 85(Pt 1): 72–91. DOI:10.1016/j.neuroimage.2013.06.016 |
| [19] |
杜凯, 王莉, 冯正权, 等. 应用fNIRS技术对运动执行与运动想象脑激活模式的研究[J].
第三军医大学学报, 2015, 37(20): 2017–2021.
DU K, WANG L, FENG Z Q, et al. Brain activation modes during motor execution and motor imagery in healthy individuals by functional near infrared reflectance spectroscopy[J]. J Third Mil Med Univ, 2015, 37(20): 2017–2021. DOI:10.3724/SP.J.1041.2016.00495-508 |
| [20] |
白学军, 周菘, 刘颖, 等. 中文音素言语流畅性任务的近红外脑功能成像研究[J].
心理科学, 2016, 39(3): 520–526.
BAI X J, ZHOU S, LIU Y, et al. Language-specific cortical activation patterns for phoneme verbal fluency task in Chinese assessed by functional near-infrared spectroscopy[J]. Psychol Sci, 2016, 39(3): 520–526. DOI:10.16719/j.cnki.1671-6981.20160302 |



