经典的牙本质粘接中常应用磷酸(Pi)、乙二胺四乙酸溶液(ethylene diamine tetraacetie acid,EDTA)等对牙本质表面进行脱矿,从而暴露牙本质表面的胶原纤维基质以便树脂粘接剂渗透并固化形成混合层,这也是现代牙本质粘接技术的基础。然而,不当的牙本质脱矿时间却往往造成牙本质胶原基质不能充分暴露[1]或深部暴露牙本质胶原基质无法被树脂完全渗透包被,形成纳米渗漏[2],导致即刻或远期粘接效果下降[2];此外,酸蚀脱矿还可以激活牙本质基质中的基质金属蛋白酶前体[3],造成界面胶原降解破坏,影响牙本质粘接界面的长期稳定性[4]。因此,本研究拟比较37% Pi和17% EDTA两种临床常用脱矿剂在牙本质粘接中对牙本质的脱矿动力学曲线,并探讨其对暴露的牙本质胶原基质酶降解速率的影响,从而为牙本质粘接中准确确定酸蚀脱矿时间提供进一步的证据。
1 材料与方法 1.1 主要试剂和仪器37%磷酸溶液(广东翁江化学试剂有限公司),17% EDTA溶液[陆军军医大学(第三军医大学)第一附属医院药剂中心],K555羟脯胺酸试剂盒(BioVision公司,美国),C0130 Ⅰ型胶原酶(Sigma公司,美国), AR0030 PBS缓冲液(武汉博士德生物工程有限公司)。
401A型低速齿科技工打磨机(上海齿科器械厂),切割机,BeadRuptor24样品研磨均质匀浆仪(OMNI公司,美国),FD-1A-50冷冻干燥机(北京博医康实验仪器有限公司),ST 40R离心机(Thermo公司,美国),AU5800全自动生化分析仪(BECKMA COULTR公司,美国), Varioskan flash酶标仪(Thermo公司),CPA225D万分之一分析天平(北京普林赛斯科技有限公司)。
1.2 酶溶液的配制精确称量Ⅰ型胶原酶20 mg,加入20 mL PBS缓冲液(pH 7.2),玻璃棒搅拌均匀,制成1.0g/L的Ⅰ型胶原酶溶液,现配现用。
1.3 标本收集收集陆军军医大学(第三军医大学)第一附属医院口腔科新鲜拔除(不超过1个月)无龋坏、无充填及修复体、发育完整的人第三磨牙及因正畸治疗拔除的双尖牙(患者知情同意),刮净所附牙周组织及牙结石,清洗后生理盐水浸泡,4 ℃保存。
用低速打磨机在4 ℃流水冲洗下,平齐牙合面中央窝底部水平,以金刚砂片垂直于牙体长轴方向切除冠部牙釉质,暴露牙本质,高速涡轮手机去除剩余冠部牙釉质,分割成牙本质组织小块。利用组织匀浆机(PROG 01,20 ℃,s=4.5,C=02,T=0 :10,D=0 :10)将牙本质块磨成牙本质粉,冻干,过筛(20~180 μm颗粒大小)。按照40 mg/管精确称取牙本质粉,分装至聚乙烯小管内4 ℃冰箱保存待用。
1.4 牙本质粉脱矿上述牙本质粉分别以37% Pi和17% EDTA进行脱矿处理。根据脱矿时相点,2组各分为7个时间点(n=5),分别脱矿10、15、30、60、90、120 s、72 h。另取5个样本,各加入1 mL去离子水作为阴性对照。荡洗3次,定容收集上清液10 mL。留存样本荡洗沉淀物。
1.5 两种脱矿液的脱矿效率与胶原溶脱效率 1.5.1 上清液离子计算及绘制脱矿曲线全自动生化分析仪检测EDTA组上清液磷浓度及Pi组钙浓度。Pi组根据所测钙及镁浓度与荡洗液体积,计算脱钙量及脱镁量,由于Pi本身的干扰,利用人牙本质羟基磷灰石(HAp)的钙磷(1.67)计算脱磷量。EDTA与钙镁离子反应生成可溶于水但不能发生电离的络合物,分析仪不能测定其浓度,故利用HAp钙磷比(1.670)及镁钙比(0.045)计算脱钙量及脱镁量。3种离子之和计算总脱矿量。分别绘制脱矿曲线,比较两种脱矿液的脱矿效率。
1.5.2 上清液胶原溶脱率曲线取100 μL脱矿上清液分装至1.5 mL离心管内,加入100 μL 12 mol/L盐酸120 ℃水解2 h,10 000 r/min离心3 min后,取10 μL水解上清液,利用羟脯胺酸试剂盒,通过酶标仪在波长560nm测定光密度值[D(560)]。分别绘制胶原溶脱曲线,比较两种脱矿液的溶脱胶原率。
1.6 酶解1、7 d后胶原降解的变化趋势上述样本荡洗沉淀物中加入1 g/L Ⅰ型胶原酶溶液300 μL,振荡混匀,放入37 ℃恒温孵箱。
1.6.1 羟脯胺酸标准曲线各取1 mg/mL HYP标准品10 μL分装至96孔板内,加入90 μL去离子水,混匀,制成0.1 mg/mL HYP标准品。加入0、2、4、6、8、10 μL上述溶液配制成0.2、0.4、0.6、0.8、1 μg/孔的HYP标准溶液,通过酶标仪在波长560 nm测定光密度值。绘制标准曲线,得出待测D(560)值=0.965 0× HYP(μg/孔)。
1.6.2 酶解1 d时HYP的变化趋势于酶解1 d时测定D(560)值,根据公式C=B/V×D(μg/μL)计算样本HYP含量, 其中B为标准曲线中HYP量,V为加入反应的样品体积,D为样品稀释因子。再根据待测样品总体积300 μL,计算酶解后释放HYP含量。绘制酶解后胶原降解的变化趋势图。
1.6.3 酶解7 d时HYP的变化趋势于酶解7 d时测定D(560)值,方法同前绘制酶解后胶原降解的变化趋势图。
1.7 统计学分析采用SPSS 20.0统计软件进行数据处理,组间同时间点比较采用两独立样本t检验;组内利用重复测量方差分析及两因素析因分析。Pearson相关系数分析相关性。检验水准:α=0.05。
2 结果 2.1 Pi组与EDTA组脱矿效率的比较Pi脱矿10~15 s时即可显著脱矿,随时间进一步延长无显著变化,脱矿反应较为迅速高效;而EDTA的螯合脱矿反应缓慢持续,30 s可见较明显脱矿。
经重复测量方差分析,组内效应分析结果显示脱矿总量随脱矿时间的变化差异有统计学意义(F=593.303,P < 0.05)。交互效应方差分析显示,脱矿总量随脱矿时间的变化而变化,且相同作用时间点脱矿总量随脱矿处理方式不同而不同(F=32.770,P < 0.05)。组间效应方差分析显示不同测量时间下磷酸和EDTA两种方式脱矿总量差异有统计学意义(F=38.234,P < 0.05,表 1)。
| 组别 | 0 s | 10 s | 15 s | 30 s | 60 s | 90 s | 120 s | 72 h |
| Pi组 | 1.41±0.02 | 196.65±12.65a | 206.65±9.85a | 207.41±9.94a | 209.56±8.68a | 211.21±9.64a | 213.65±9.30a | 236.14±24.11 |
| EDTA组 | 1.41±0.02 | 121.37±1.73 | 134.75±16.32 | 142.78±21.70 | 146.16±25.74 | 160.10±21.79 | 164.62±21.79 | 241.80±19.26 |
| a: P < 0.05, 与EDTA组比较 | ||||||||
2.2 Pi组与EDTA组胶原溶脱效率比较
Pi组胶原溶脱量10~30 s急剧增加,随着时间进一步延长无显著变化;EDTA组胶原溶脱在120 s内无显著变化。
经重复测量方差分析,组内效应分析结果显示胶原溶脱量随脱矿时间的变化差异有统计学意义(F=491.021,P < 0.05)。交互效应方差分析显示,胶原溶脱量随脱矿时间的变化而变化,且相同作用时间点胶原溶脱量随脱矿处理方式不同而不同(F=115.267,P < 0.05)。组间效应方差分析显示不同测量时间下磷酸和EDTA两种方式胶原溶脱量差异有统计学意义(F=558.915,P < 0.05,表 2)。
| 组别 | 0 s | 10 s | 15 s | 30 s | 60 s | 90 s | 120 s | 72 h |
| Pi组 | 0 | 142.68±45.89a | 202.67±7.64a | 292.18±8.64a | 313.32±7.62a | 321.17±9.11a | 337.58±12.94a | 363.04±7.00 |
| EDTA组 | 0 | 104.83±7.70 | 112.45±11.34 | 107.56±12.57 | 106.87±13.07 | 104.13±14.32 | 101.56±14.91 | 300.90±14.99 |
| a: P < 0.05, 与EDTA组比较 | ||||||||
2.3 脱矿总量与胶原溶脱的相关性分析
Pi组脱矿总量与胶原溶脱量呈显著相关(r=0.864,P=0.006);EDTA组脱矿总量与胶原溶脱量呈显著相关(r=0.894,P=0.003)。
2.4 Pi组与EDTA组胶原酶解1 d释放HYP量的比较Pi组酶解量各时间点差异无统计学意义;EDTA组酶解量随脱矿时间增长而增加,30 s后降低。
析因方差分析结果显示:不同脱矿时间下Pi和EDTA两种方式胶原降解量(酶解1 d)差异有统计学意义(P < 0.05)。同种脱矿方式胶原降解量(酶解1 d)随脱矿时间的变化差异有统计学意义(P < 0.05)。胶原降解量(酶解1 d)随脱矿时间的变化而变化,且相同作用时间点胶原降解量随脱矿处理方式不同而不同(P < 0.05,表 3)。
| 组别 | 0 s | 10 s | 15 s | 30 s | 60 s | 90 s | 120 s | 72 h |
| Pi组 | 29.19±2.28 | 21.83±1.45a | 27.68±3.18a | 22.06±2.62a | 21.32±2.12a | 19.70±0.77a | 17.56±1.16a | 7.76±0.07a |
| EDTA组 | 29.19±2.28 | 336.65±34.55 | 358.87±61.11 | 462.60±50.62 | 425.39±65.11 | 361.68±61.16 | 353.75±62.22 | 154.74±16.60 |
| a: P < 0.05, 与EDTA组比较 | ||||||||
2.5 脱矿总量与酶解1 d释放HYP的相关性分析
Pi组脱矿量与酶解7 d后释放HYP量不相关(r=-0.616,P=0.104);EDTA组脱矿量与酶解7 d后释放HYP量不相关(r=0.372,P=0.364)。
2.6 Pi组与EDTA组胶原酶解7 d释放HYP量的比较Pi组酶解量各时间点差异无统计学意义(P>0.05);EDTA组酶解量随脱矿时间增长而增加,30 s后降低。
析因方差分析结果显示:不同脱矿时间下Pi和EDTA两种方式胶原降解量(酶解7 d)差异有统计学意义(P < 0.05)。同种脱矿方式胶原降解量(酶解7 d)随脱矿时间的变化差异有统计学意义(P < 0.05)。胶原降解量(酶解7 d)随脱矿时间的变化而变化,且相同作用时间点胶原降解量随脱矿处理方式不同而不同(P < 0.05,表 4)。
| 组别 | 0 s | 10 s | 15 s | 30 s | 60 s | 90 s | 120 s | 72 h |
| Pi组 | 49.19±2.28a | 34.20±2.13a | 44.74±4.09a | 37.37±2.25a | 35.79±3.18a | 31.97±1.23a | 27.34±1.39a | 14.80±0.27a |
| EDTA组 | 49.19±2.28 | 359.91±34.69 | 385.09±61.55 | 493.06±50.43 | 461.86±65.18 | 389.22±60.98 | 375.25±62.24 | 170.93±17.00 |
| a: P < 0.05, 与EDTA组比较 | ||||||||
2.7 脱矿总量与酶解7 d释放HYP的相关性分析
Pi组脱矿量与酶解7 d后释放HYP量不相关(r=-0.662,P=0.074);EDTA组脱矿量与酶解7 d后释放HYP量不相关(r=0.358,P=0.384)。
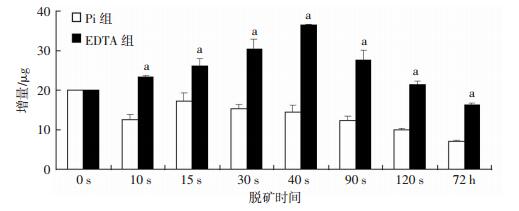
2.8 Pi组与EDTA组胶原降解增量的比较如图 1所示:Pi组0 s降解增量均大于其他各时间点,15 s后降低;EDTA组0s降解增量均小于其他各时间点,60 s开始降低。
|
| a: P<0.05, 与Pi组比较 图 1 Pi组与Pi组各时间点胶原降解增量比较 |
析因方差分析结果显示:不同脱矿时间下Pi和EDTA两种方式胶原降解增量差异有统计学意义(P < 0.05)。同种脱矿方式胶原降解增量随脱矿时间的变化差异有统计学意义(P < 0.05)。胶原降解增量随脱矿时间的变化而变化,且相同作用时间点胶原降解增量随脱矿处理方式不同而不同(P < 0.05)。
2.9 脱矿总量与胶原降解增量的相关性分析Pi组脱矿量与胶原降解增量呈显著相关(r=-0.713,P=0.047);EDTA组脱矿量与胶原降解增量不相关(r=-0.048,P=0.910)。
3 讨论临床上进行牙本质粘接时,常使用Pi或EDTA处理牙本质粘接面以获得较好的粘接强度。研究表明,牙本质粘接面以37% Pi酸蚀15s[5]或EDTA脱矿处理60s[6]后行湿粘接,粘接强度最高。但亦有研究表明,上述脱矿处理后的牙本质粘接界面残存暴露的牙本质胶原基质,在宿主来源或外源性的酶解作用下易于破坏,导致牙本质粘接界面的耐久性下降[7]。
牙本质的主要矿化结构为HAp,Pi与HAp相遇时以脱钙为主。随着反应的进行,溶液达到饱和或过饱和时,进一步脱钙受到抑制[8]。EDTA对牙本质脱矿的行为是具有自限性的,在某一时间点达平衡[9]。MISHRA等[10]认为这种自限性与脱矿过程中pH值不断下降有关。研究表明Pi较EDTA脱矿更为迅速高效,两种脱矿剂作用72 h脱矿效率差异无统计学意义。我们发现就脱矿效率而言,结合临床表面处理牙本质操作,其最佳时间分别为37% Pi 10~15 s,17% EDTA 60~120 s。
据HEDENBJÖRK-LAGER等[11]研究,Pi具有侵蚀性,脱矿后的胶原纤维对内外源性蛋白酶的酶解作用和水解作用敏感,进而可能发生结构改变。EDTA可通过顾不螯合Ca2+阻断激活MMP的Ca2+通道,抑制MMP活性。许强建等[12]研究认为EDTA作用到一定程度,Ca2+释放量持续增加,脱矿表面EDTA螯合Ca2+阻断激活MMP的Ca2+通道达到极限。研究表明Pi较EDTA造成胶原溶脱显著,且与脱矿量呈显著相关性(P < 0.05)。两种脱矿剂作用72 h胶原溶脱差异无统计学意义。我们发现就胶原溶脱而言,结合临床表面处理牙本质操作,其最佳时间分别为37% Pi 10~15 s,17% EDTA<120 s。
牙本质粘接界面因各种原因暴露的胶原可受到水分、温度、细菌及各种酶类的作用发生降解,引起牙本质粘接界面的退变,最终导致粘接稳定性降低[13]。为了更好地反映脱矿后牙本质胶原基质的稳定性,本研究采用了不同脱矿程度牙本质胶原基质酶解量及增量来评价其稳定性差异与脱矿剂脱矿时间的关系。结果显示EDTA脱矿作用后牙本质胶原基质酶解及增量较Pi显著,其稳定性弱于Pi。EDTA脱矿时间延长至30 s以后,牙本质胶原基质酶解减少,稳定性增强;而EDTA脱矿时间延长至60 s以后,酶解增量减少,稳定性增强。就脱矿后牙本质胶原基质的稳定性而言,结合临床表面处理牙本质操作,其最佳时间分别为37% Pi < 120 s,17% EDTA 60~90 s。
综上所述,37%磷酸较17% EDTA脱矿效率迅速、高效。结合临床脱矿效率、胶原溶脱及脱矿后牙本质胶原基质的稳定性而言,临床进行牙本质粘结前表面处理牙本质时,37% Pi酸蚀10~15s或17% EDTA脱矿处理60~90s是较为合理的。
| [1] |
赵三军, 陈吉华. 酸蚀时间对牙本质粘接界面纳米渗漏和粘接强度的影响[J].
实用口腔医学杂志, 2009, 25(1): 36–40.
ZHAO S J, CHEN J H. Effects of acid etching time on nanoleakage and microtensile bond strength of the adhesive-dentin bond[J]. J Pract Stomatol, 2009, 25(1): 36–40. DOI:10.3969/j.issn.1001-3733.2009.01.08 |
| [2] |
裴丹丹, 黄雪清, 黄翠. 牙本质混合层降解及其与牙本质粘接耐久性的关系[J].
中华口腔医学杂志, 2011, 46(1): 58–60.
PEI D D, HUANG X Q, HUANG C. Association of the degradation of the hybrid layer and the durability of dentin adhesion[J]. Chin J Stomatol, 2011, 46(1): 58–60. DOI:10.3760/cma.j.issn.1002-0098.2011.01.018 |
| [3] |
何恩宝, 王彦, 梁澜晨, 等. 聚乙烯磷酸对牙本质基质金属蛋白酶活性的影响[J].
中华口腔医学研究杂志(电子版), 2013, 7(4): 288–292.
HE E B, WANG Y, LIANG L C, et al. The influence of polyvinylphosphonic acid on matrix metalloproteinases activities in dentin[J]. Chin J Stomatol Res(Electron Ed), 2013, 7(4): 288–292. DOI:10.3877/cma.j.issn.1674-1366.2013.04.006 |
| [4] |
周恬, 朱梓园, 张保卫. 牙本质内基质金属蛋白酶的测定及其对牙本质胶原降解作用的研究[J].
口腔医学, 2012, 32(1): 25–28.
ZHOU T, ZHU Z Y, ZHANG B W. Study of measurement of matrix metalloproteinases in crown and root dentin and their effects on degradation of collagen fibers[J]. Stomatology, 2012, 32(1): 25–28. |
| [5] | SAURO S, TOLEDANO M, AGUILERA F S. Resin-dentin bonds to EDTA-treated vs. acid-etched dentin using ethanol wet-bonding. Part Ⅱ: Effects of mechanical cycling load on microtensile bond strengths[J]. Dent Mater, 2011, 27(6): 563–572. DOI:10.1016/j.dental.2011.02.010 |
| [6] | OSORIO R, ERHARDT M C, PIMENTA L A, et al. EDTA treatment improves resin-dentin bonds' resistance to degradation[J]. J Dent Res, 2005, 84(8): 736–740. DOI:10.1177/154405910508400810 |
| [7] | TJÄDERHANE L, NASCIMENTO F D, BRESCHI L, et al. Optimizing dentin bond durability: control of collagen degradation by matrix metalloproteinases and cysteine cathepsins[J]. Dent Mater, 2013, 29(1): 116–135. DOI:10.1016/j.dental.2012.08.004 |
| [8] | HENCH L L. An Introduction to Bioceramics[M]. 2nd Edition. Singapore: World Scientific Publishing, 2013: 150-151. |
| [9] | KUMAR Y, LOHAR J, BHAT S, et al. Comparative evaluation of demineralization of radicular dentin with 17% EDTA and MTAD at different time intervals——An in-vitro study[J]. Int Soc Prev Community Dent, 2016, 6(1): 44–48. DOI:10.4103/2231-0762.175412 |
| [10] | MISHRA V K, BHATTACHARJEE B N, KUMAR D, et al. Effect of a chelating agent at different pH on the spectroscopic and structural properties of microwave derived hydroxyapatite nanoparticles: a bone mimetic material[J]. New J Chemistry, 2016, 40(6): 5432–5441. DOI:10.1039/C5NJ03322E |
| [11] | HEDENBJÖRK-LAGER A, HAMBERG K, PÄÄKKÖNEN V, et al. Collagen degradation and preservation of MMP-8 activity in human dentine matrix after demineralization[J]. Arch Oral Biol, 2016, 68: 66–72. DOI:10.1016/j.archoralbio.2016.04.003 |
| [12] |
许强建, 李全利, 陈佳龙, 等. 多巴胺对基质金属蛋白酶活性及牙本质胶原纤维降解的影响[J].
中华口腔医学杂志, 2015, 50(3): 186–189.
XU Q J, LI Q L, CHEN J L, et al. Effect of dopamine on the activity of matrix metalloproteinases and degradation of dentin collagen[J]. Chin J Stomatol, 2015, 50(3): 186–189. DOI:10.3760/cma.j.issn.1002-0098.2015.03.015 |
| [13] | SAI K, SHIMAMURA Y, TAKAMIZAWA T, et al. Influence of degradation conditions on dentin bonding durability of three universal adhesives[J]. J Dent, 2016, 54: 56–61. DOI:10.1016/j.jdent.2016.09.004 |



