2. 400038 重庆,陆军军医大学(第三军医大学)第一附属医院放射科
2. Department of Radiology, First Affiliated Hospital, Army Medical University (Third Military Medical University), Chongqing, 400038, China
肺炎型肺癌(pneumonia type carcinoma of lung,PTCL)临床较少见[1],临床表现不典型,影像学表现与肺炎较为相似,因而误诊率高。18F-FDG PET/CT对原发性恶性肿瘤和转移病灶的探测具有重要价值[2],利用氟-18脱氧葡萄糖(18F-fluorodeoxyglucose,18F-FDG)进行正电子断层显像(positron emission tomography,PET)目前已广泛应用于诊断肺癌及其他肿瘤,可显示肿瘤组织的生物学特性,对恶性肿瘤的早期诊断较结构影像学具有其明显的特点,可以同时显示功能代谢信息和解剖形态信息,但也存在一定的假阳性和假阴性。18F-FDG PET/CT在肺癌诊断、分期、预后评价、疗效判断及对治疗计划的制定能起到指导作用[3]。目前尚少见采用双时相18F-FDG PET/CT显像联合CT增强扫描诊断PTCL并比较其正确诊断率的报道。收集我院经手术病理证实的19例PTCL的18F-FDG PET/CT及CT增强扫描资料,使用临床病理对照研究对比CT增强、单时相18F-FDG PET/CT、单时相18F-FDG PET/CT联合增强CT、双时相18F-FDG PET/CT、双时相18F-FDG PET/CT联合增强CT对肺炎型肺癌的诊断效能。
1 资料与方法 1.1 临床资料收集2013年1月至2017年6月在武警四川省总队医院行18F-FDG PET/CT、CT增强扫描后经手术病理证实的19例PTCL患者的临床资料。其中男性12例,女性7例,年龄30~79(58.8±13.2)岁,体质量43~82(57.3±11.4)kg。临床表现为刺激性咳嗽16例,咯大量白色黏液痰15例,痰中带血7例。本研究经武警四川省总队医院伦理委员会审批(2017)。
纳入标准:①CT表现为斑片状模糊影或实变影;②已行CT增强扫描及18F-FDG PET/CT显像。③经穿刺或外科手术得到病理证实。④实验室检查肿瘤5项(癌胚抗原、糖类抗原125、糖类抗原153、非小细胞肺癌相关抗原、神经元特异性烯醇化酶)中至少有1项增高。⑤随访病灶进展,淋巴结或远处出现转移。
排除标准:①已行放疗、化疗、靶向治疗的患者;②图像质量差,影响诊断的患者。
1.2 检查设备及显影剂18F-FDG PET/CT采用128层GE Discovery PET/CT Elite,显像剂为18F-FDG,放化纯度皆>95%。扫描参数如下,管电压:120 kV;管电流:150 mA;准直/层厚:5.00/3.75 mm;转速:0.5 s/r;螺距:1.250;扫描时间:20~30 s。CT增强扫描采用美国GE宝石能谱CT(Discovery750),造影剂采用非离子型造影剂碘海醇(30 g)。扫描层厚和层间距为0.625 mm,螺距1,矩阵为512×512。
1.3 检查前准备患者禁食8 h以上,给药前常规检测血糖并控制在7.2 mmol/L以下,平静休息10~15 min后按照体质量静脉注射显影剂18F-FDG(3.70~4.44 MBq/kg),活度为185~ 444 MBq,注射后静息平卧1 h。18F-FDG PET/CT检查需要排除在检查前1周内使用刺激骨髓造血药物的患者。
1.4 图像采集排尿后行18F-FDG PET/CT扫描,于首次显像后60~ 90 min行延迟期显像。检查中要求患者平静呼吸以保证CT图像和PET图像匹配满意。先采集CT图像后行PET发射扫描。扫描范围自颅顶到股骨中段,PET扫描采用3D采集,头部每个床位5 min,体部每个床位3 min,根据患者身高扫描6~8个床位,采集完成后利用CT数据对PET图像进行衰减、校正,进行图像重建和融合显示。CT增强扫描按照1 kg :1.5 mL确定注射量,采用高压注射器经肘中静脉按3.0 mL/s的速度注射造影剂,延迟45 s行胸部CT增强扫描。CT扫描范围为从胸廓入口水平到肺底水平。
1.5 图像分析首先判读同机CT图像,然后判读18F-FDG PET/CT图像,肉眼观察病变部位、大小、形态及放射性分布,使用感兴趣区工具自动测定病变部位最大标准摄取值(SUVmax),将SUVmax≥2.5作为诊断恶性病灶的参考指标之一[3],按照分组由两名工作15年以上经验丰富的核医学及CT副高级职称以上医师对各组进行独立分析,有争议的结果由共同讨论决定,诊断结果为肺癌、恶性肿瘤、肺癌可能性大或可能为阳性;诊断肺炎、感染性病变、良性病变可能性大或可能为阴性。
1.6 统计学处理采用SPSS 17.0统计软件处理数据,比较单独采用CT增强扫描、单时相18F-FDG PET/CT、单时相18F-FDG PET/CT联合CT增强、双时相18F-FDG PET/CT、双时相18F-FDG PET/CT联合CT增强扫描诊断PTCL的正确诊断率。采用行×列表的χ2检验进行比较(检验水准α=0.05),再用Fisher确切概率法进行两两比较(校正后检验水准α=0.005)。
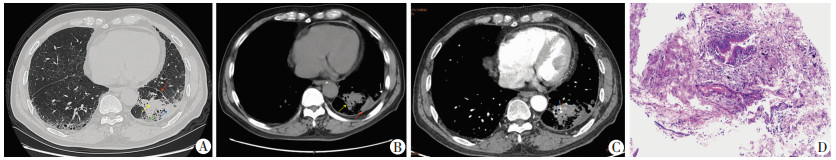
2 结果 2.1 PTCL的CT表现10例呈单肺单灶分布,6例呈单肺多灶分布,3例呈双肺分布。病灶位于右肺上叶尖段、后段4例,右肺中叶内侧段1例,右肺下叶6例(背段3例,后基底段5例,内侧基底段1例),左肺上叶5例(尖后段3例,舌段2例),左肺下叶7例(背段3例、后基底段5例、前内基底段2例)。19例病灶中均见实变,在实变的基础上15例见磨玻璃征,19例见小结节征,14例见空泡征,6例见蜂窝征,14例枯树枝征,16例见邻近胸膜增厚,增强扫描后所有病例见血管造影征。各种CT征象见图 1A~C。平扫CT值为(39.96±11.50)Hu,增强后CT值为(78.48±17.95)Hu。采用增强CT正确诊断5例,依据病理结果为金标准(图 1D)。
|
| A:胸部CT平扫肺窗示左下肺白色↑:示磨玻璃密度影;绿色↑:示空泡征及蜂窝征;黄色↑:示小结节征;蓝色↑:示实变征;红色↑:示胸膜增厚;B:胸部CT平扫纵隔窗示左下肺黄色↑:示小结节征;红色↑:示实变征;白色↑:胸膜增厚;C:胸部CT增强扫描示左下肺白色↑:示血管造影征;D:组织病理学检查结果为高分化腺癌(HE ×100) 图 1 肺炎型肺癌的胸部平扫、增强CT表现及其镜下病理表现(患者男性,67岁,左下肺肺炎型肺癌) |
2.2 18F-FDG代谢表现
19例患者均见不同程度的18F-FDG代谢升高(图 2),19例PTCL的18F-FDG摄取值SUVmax为(7.50±4.06);延时相SUVmax为(8.38±4.41)。病灶18F-FDG代谢升高主要位于实变区及结节内,磨玻璃密度区、部分小结节内无FDG摄取。

|
|
↑:示18F-FDG代谢增高;□:示感兴趣区;SUVmax为13.78,延时相SUVmax为14.62 A:轴位;B:冠状位;C:矢状位 图 2 肺炎型肺癌的PET/CT表现(患者男性,67岁,左下肺肺炎型肺癌) |
2.3 不同影像学方法组正确诊断率比较
5种不同方法组比较,差异有统计学意义(P<0.05),即5种不同诊断方法组之间可能存在差异。经过两两比较(Fisher确切概率法)后,得知只有双时相PET/CT联合增强CT组与增强CT组诊断结果差异有统计学意义(P<0.005),即双时相PET/CT联合CT增强扫描误诊率明显低于CT增强误诊率,而其他方法都不能表现出比CT增强明显低的误诊率,证明了双时相PET-CT联合增强CT的优势性(表 1)。
| 组别 | 正确诊断率/% | 误诊率/% |
| 增强CT组 | 26.3(5/19) | 73.7(14/19) |
| 单时相PET/CT组 | 63.2(12/19) | 36.8(7/19) |
| 单时相PET/CT联合增强CT组 | 78.9(15/19) | 21.1(4/19) |
| 双时相PET/CT组 | 73.7(14/19) | 26.3(5/19) |
| 双时相PET/CT联合增强CT组 | 94.7(18/19)a | 5.3(1/19) |
| a: P<0.005,与增强CT组比较 | ||
3 讨论
PTCL是一种表现为实变或炎症反应样的肿瘤,临床表现缺乏特异性,通常仅表现为咳嗽、咯痰、咯血、发热、胸痛等,加上影像学表现与肺炎极其相似,因而临床诊断困难。本研究单纯用CT增强诊断的误诊率达73.7%。临床诊断PTCL的病程都较长,抗炎治疗无效,并见病灶增多、增大才考虑到本病的可能性,不过文献[1]报道病变可以在2年内无明显变化。PTCL的CT表现与其病理特点有关,镜下可见肺泡壁结构完整,肿瘤细胞沿肺泡壁匍匐生长,CT上表现为斑片状模糊影,但其并非真实的炎症,对抗炎治疗无效并且会继续生长。过去认为弥漫性肺炎型肺癌病理上是黏液型细支气管肺泡癌(bronchioalveolar carcinoma,BAC)的常见形式,BAC是与乳头状腺癌、腺泡型腺癌并列的腺癌的一个亚型。因2011年肺腺癌新分类中弃用了BAC这个诊断术语[4],引入了“浸润性黏液腺癌”代替原来的黏液型BAC,所以从病理分类来讲PTCL是浸润性黏液腺癌。正是由于浸润性黏液腺癌的生长方式呈鳞屑样生长,因而CT表现多样。本研究中10例呈单肺单灶分布,6例呈单肺多灶分布,3例呈双肺分布,表现为团片状、斑片状高密度影,分布特点与AUSTIN等[5]的报道相似。PTCL的常见CT征象包括实变、磨玻璃征、小结节征、空泡征、蜂窝征、枯枝征、胸膜牵拉和增厚。本研究中19例均见实变,在实变的基础上15例见磨玻璃征,19例见小结节征,14例见空泡征,6例见蜂窝征,14例见枯枝征,16例见邻近胸膜增厚。本组病例的CT表现特点与张珣等[6]的研究一致,病灶平扫CT值为(39.96±11.50)Hu,增强后CT值为(78.48±17.95)Hu,全部病例见血管造影征。目前学者们对血管造影征的意义存在争议,而我们在其他肺实变中也能见到血管造影征。采用CT增强扫描仅正确诊断5例,分析其原因主要还是对本病的认识不足所致,影像学表现和平常所见肿块样肺癌差异大,导致误诊率高。LIU等[7]也认为X线及CT检查对诊断肺炎型肺癌意义不大,他认为误诊的原因为新生物太小、病变位于支气管内并合并肺炎及肺不张。找到提高正确诊断率的方法对于避免误诊意义重大。
18F-FDG PET/CT多用于肿瘤的诊断、分期、放疗计划制定及疗效愈后的评价[8-9]。18F-FDG PET/CT的作用还在于可以确定肿瘤与周围不张肺组织的边界[10]。研究表明,未诊断的肺结节中采用18F-FDG PET/CT在准确诊断及排除肿瘤,比传统的结构成像有显著改善[11]。18F-FDG PET/CT显像通过肿瘤内18F-FDG糖代谢的差异来判定恶性病变,主要通过观察病变的放射性浓聚,测定SUV值来了解18F-FDG的摄取程度,但是18 F-FDG PET显像有一定的假阳性和假阴性[12],感染性疾病、放射性肺炎等也常造成摄取升高。因此,对于肺部肿瘤的定性诊断需紧密结合临床资料和其他影像学表现综合分析。本组PTCL的18F-FDG PET/CT表现为所有患者见不同程度的18F-FDG代谢升高。病灶18F-FDG糖代谢升高主要位于实变区及小结节内,磨玻璃密度区、部分小结节内无FDG摄取。部分小结节见放射性浓聚,这部分结节考虑为初级肺小叶内肺泡腔内被肿瘤细胞填充,而部分结节表现为无放射性浓聚的结节,考虑这部分结节为肺泡腔内堵塞的黏液,除此以外肿瘤的恶性程度低、分化好、生长缓慢、代谢低也会表现为低摄取,增加了临床诊断难度。本研究的摄取特点与文献[13]报道基本一致。ALKHAWALDEH等[14]通过研究认为双时相PET/CT具有更高的准确性及特异性。恶性肿瘤的18F-FDG代谢表现为持久性增高,在本研究中延迟期都表现为SUVmax 进一步增高。本研究中单时相18F-FDG PET/CT正确诊断12例,误诊7例,正确诊断率为63.2%,而双时相18F-FDG PET/CT正确诊断14例,误诊5例,正确诊断率为73.7%。比较单时相18F-FDG PET/CT与双时相18F-FDG PET/CT的正确诊断率,两组数值的差异没有统计学意义。BARGER等[15]通过荟萃分析认为双时相18F-FDG PET/CT的敏感性和特异性分别为85%和77%,与单时相18F-FDG PET/CT的敏感性和特异性相似,并不能得到更多信息,与本研究结果相近。而双时相18F-FDG PET/CT联合CT增强组与CT增强组相比,差异具有统计学意义。本研究中采用双时相18F-FDG PET/CT联合CT增强正确诊断率为94.7%,其误诊率最低,虽然不能表现出与单时相18F-FDG PET/CT、单时相18F-FDG PET/CT联合增强CT、双时相18F-FDG PET/CT的差异,但是其他组均不能表现出与CT增强的差异,证实了双时相18F-FDG PET/CT结合CT增强的意义。所以在怀疑PTCL时宜采用双时相18F-FDG PET/CT结合CT增强来降低误诊率。PTCL的诊断中要结合CT征象来判定病变的良恶性,当CT征象中出现磨玻璃征、小结节征、空泡征、蜂窝征、枯枝征时,强烈提示肿瘤的可能性,结合SUVmax 增高,可考虑PTCL的可能,另外还要结合临床相关实验室检查结果。但是对于有上述CT征象并SUVmax<2.5的病例,不能轻易排除肿瘤,可早期行CT引导下穿刺活检证实,以免误诊。
本研究还存在一定的局限性:①因为PTCL是少见病,样本量较少,下一步计划扩大样本量继续研究提高准确性。②未引入需要和PTCL鉴别的其他病变,如肺炎、肺结核、肺肉芽肿,未进行灵敏度、特异度、阳性预测值、阴性预测值评价,下一步将进一步研究。
| [1] | MIR E, SAREEN R, KULSHRESHTHA R, et al. Bronchioloalveolar cell carcinoma presenting as a "non-resolving consolidation" for two years[J]. Pneumonol Alergol Pol, 2015, 83(3): 208–211. DOI:10.5603/PiAP.2015.0033 |
| [2] |
黎海涛, 王健, 陈伟, 等. 18F-FDG PET/CT显像在恶性肿瘤临床诊断中的应用[J].
第三军医大学学报, 2006, 28(7): 718–720.
LI H T, WANG J, CHEN W, et al. Clinical value of F-FDG PET/CT in diagnosis of malignant tumors[J]. J Third Mil Med Univ, 2006, 28(7): 718–720. |
| [3] |
崔社怀, 金榕兵, 曹国强, 等. FDG-PET对非小细胞肺癌分期的意义[J].
第三军医大学学报, 2005, 27(15): 1576–1578.
CUI S H, JIN R B, CAO G Q, et al. Significance of FDG-PET for staging of non-small cell lung cancer[J]. J Third Mil Med Univ, 2005, 27(15): 1576–1578. DOI:10.3321/j.issn:1000-5404.2005.15.014 |
| [4] | TRAVIS W D, BRAMBILLA E, NOGUCHI M, et al. Inter-national association for the study of lung cancer /American Thoracic Society/European Respiratory Society:international multidisciplinary classification of lung adenocarcinoma:executive summary[J]. Proc Am Thorac Soc, 2011, 8(5): 381–385. DOI:10.1513/pats.201107-042ST |
| [5] | AUSTIN J H, GARG K, ABERLE D, et al. Radiologic implications of the 2011 classification of adenocarcinoma of the lung[J]. Radiology, 2013, 266(1): 62–71. DOI:10.1148/radiol.12120240 |
| [6] |
张珣, 徐丽莹, 夏冰. 肺炎型肺癌的CT特点与病理对照分析[J].
临床放射学杂志, 2015, 34(8): 1220–1223.
ZHANG X, XU L Y, XIA B. Pneumonia type carcinoma of lung:CT pathologic correlation[J]. J Clin Radiol, 2015, 34(8): 1220–1223. |
| [7] | LIU X, ADAMS A L. Mucoepidermoid carcinoma of the bronchus:a review[J]. Arch Pathol Lab Med, 2007, 131(9): 1400–1404. |
| [8] | FISCHER B M, MORTENSEN J. The future in diagnosis and staging of lung cancer: positron emission tomography[J]. Respiration, 2006, 73(3): 267–276. DOI:10.1159/000092080 |
| [9] | SAHINER I, VURAL G U. Positron emission tomography/computerized tomography in lung cancer[J]. Quantit Imag Med Surg, 2014, 4(3): 195–206. |
| [10] | BRADLEY J, BAE K, CHOI N, et al. A phase II comparative study of gross tumor volume definition with or withoutPET/CTfusion in dosimetric planning for non-small-cell lung cancer (NSCLC): primary analysis of radiation therapy oncology group (RTOG) 0515[J]. Int J Radiat Oncol Biol Phys, 2012, 82(1): 435–441. DOI:10.1016/j.ijrobp.2010.09.033 |
| [11] | MACMANUS M P, HICKS R J. PET scanning in lung cancer: current status and future directions[J]. Semin Surg Oncol, 2010, 21(3): 149–155. |
| [12] | GUPTA G, GANDHI J S, SHARMA A, et al. A study of the pathological outcome of positron emission tomography-computed tomography 2(- 18F)-fluro-2-deoxy-D-glucose avid lesion:a 5 years retrospective study[J]. J Cancer Res Ther, 2017, 13(6): 1000–1006. |
| [13] | UESAKA D, DEMURA Y, ISHIZAKI T, et al. Evaluation of dual-time-point 18F-FDG PET for staging in patients with lung cancer[J]. J Nul Med, 2008, 49(10): 1577–1578. DOI:10.2967/jnumed.108.052142 |
| [14] | ALKHAWALDEH K, BIERSACK H J, HENKE A, et al. Impact of dual-time-point F-18 FDG PET/CT in the assessment of pleural effusion in patients with non-small-cell lung cancer[J]. Clin Nucl Med, 2011, 36(6): 423–428. DOI:10.1097/RLU.0b013e3182173823 |
| [15] | BARGER R L JR, NANDALUR K R. Diagnostic performance of dual-time 18F-FDG PET in the diagnosis of pulmonary nodules: a meta-analysis[J]. Acad Radiol, 2012, 19(2): 153–158. DOI:10.1016/j.acra.2011.10.009 |



