食管癌内镜黏膜下剥离术(endoscopic submucosal dissection, ESD)后导致食管狭窄的问题仍未解决, 严重影响患者术后生活质量。现普遍认为, 当病变位于食管颈段、剥离范围大于75%食管环周、纵向长度>40 mm[1]时, 术后狭窄的发生率明显增高。现存针对ESD术后食管狭窄的预防方法, 尚未形成共识。术后置入支架对食管狭窄有一定预防作用[2], 但长期效果欠佳; 预防性球囊扩张可能有用, 但严重影响患者生活质量; 自体细胞移植也显示出较好效果, 但技术、设备要求过高限制其应用。此外术后置入聚羟基乙酸薄片[3-4]和口服抗纤维化药物, 比如丝裂霉素C、N-乙酰半胱氨酸和曲尼司特也显示出一定效果。最被认可的是糖皮质激素的应用[5], 然而长期口服激素有严重感染风险[6]。所以如何有效地短期、低剂量应用糖皮质激素预防食管ESD术后狭窄值得研究[7]。生物蛋白胶在外科领域已被广泛应用于缓解纤维化导致的手术粘连, 且研究显示生物蛋白胶对药物有缓释作用[8]。因此, 本研究将生物蛋白胶和曲安耐德配成混悬液, 喷涂于犬食管ESD术后创面, 以期在减少曲安奈德用量的同时延长其局部作用时间, 发挥两种药物的效果, 预防食管术后狭窄。
1 材料与方法 1.1 实验动物及分组实验采用普通家犬20只, 由第三军医大学实验动物中心提供, 12月龄, 雌雄不限, 体质量12~15 kg。实验过程由第三军医大学实验动物伦理委员会审查并通过。将实验犬称量、编号, 以随机数字表法平分为4组:联合治疗组、生物蛋白胶组、曲安奈德组、对照组(n=5)。食管ESD术后立即应用不同药物:联合治疗组喷涂生物蛋白胶(含纤维蛋白原溶液和凝血酶溶液)和50 mg曲安奈德混悬液, 生物蛋白胶组仅喷涂生物蛋白胶, 曲安奈德组仅喷涂50 mg曲安奈德注射液, 对照组术后不用上述药物。所有实验犬于术后6周被处死。
1.2 器材与试剂电子胃镜(GIF-H260, Olympus)、内窥镜主机系统(CV-260, Olympus)、高频电设备(VIO300S, ERBE)。生物蛋白胶购自上海莱士血液制品公司。曲安奈德购自天津金耀药业。兔抗α-SMA购自Abcam公司。
1.3 食管ESD术后狭窄模型实验犬禁食1 d、禁水4 h后, 于术前30 min肌肉注射1 mg阿托品、400 mg戊巴比妥钠。待犬麻醉稳定后左侧卧位于操作台, 戴上牙垫并给予3 L/min鼻导管吸氧。采用ESD术于食管距门齿30~34 cm处剥离食管黏膜3/4环周, 建立创面。
1.4 术后药物处理将1盒生物蛋白胶(2 mL)置于37℃水浴10 min, 按说明书分别配置纤维蛋白原溶液、凝血酶溶液。取50 mg曲安奈德注射液注入上述纤维蛋白原溶液、凝血酶溶液中得到联合治疗组用药。生物蛋白胶组用药为纤维蛋白原溶液、凝血酶溶液。曲安奈德组用药为50 mg曲安奈德溶液。犬食管ESD术后, 立即取2支注射器分别抽取各组药物溶液1次用量, 连接插入胃镜活检孔道的双联混药系统, 同步、均匀地注入2支注射器中的溶液组分, 使溶液均匀喷涂于整个创面。术后各组只应用1次药物。
1.5 狭窄情况评估术后6周使用直径9.8 mm胃镜(GIF-H260, Olympus)检查狭窄处通过性, 观察狭窄情况。静脉注射10%氯化钾30 mL处死实验犬, 解剖食管后沿纵轴切开, 观察狭窄段情况, 测量最狭窄处及距其2 cm处周长并按文献[9]方法计算狭窄率。
1.6 病理学评估取得食管样本固定48 h, 石蜡包埋后制成5 μm切片, HE染色观察病理变化。为检测肌成纤维细胞和微血管数量评估黏膜下层纤维化程度, 切片置于4℃予兔抗α-SMA孵育12 h, 每张切片均随机选取5个视野测量阳性区域面积。
1.7 统计学分析数据以x ±s表示, 采用GraphPad Prism 6.0进行分析。总体差异采用单因素方差分析, 使用LSD-t检验比较组间差异。检验水准:α=0.05。
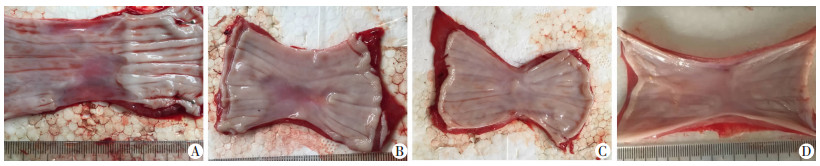
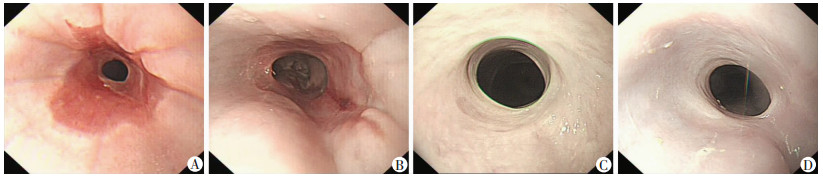
2 结果 2.1 狭窄情况评估术后6周胃镜下均可见最狭窄处黏膜皱襞向管腔中央聚拢且瘢痕皱襞相对非手术区域食管黏膜更紧张, 曲安奈德组、对照组相对其他两组更明显(图 1), 胃镜观察狭窄情况见表 1。食管大体病理可见(图 2):所有样本瘢痕处相比正常黏膜上皮更薄、黏膜颜色偏红。

|
| A:联合治疗组; B:生物蛋白胶组; C:曲安奈德组; D:对照组 图 1 家犬食管ESD术后局部喷涂生物蛋白胶和曲安奈德6周后胃镜下表现 |
|
| A:联合治疗组; B:生物蛋白胶组; C:曲安奈德组; D:对照组 图 2 家犬食管ESD术后局部喷涂生物蛋白胶和曲安奈德6周后狭窄情况 |
| 组别 | 可通过/不通过(例) | 狭窄率[(x ±s)%] | α-SMA阳性面积(x ±s)/μm2 |
| 联合治疗组 | 3/2 | 19.9±14.8ad | 7 030.3±5 142.6bd |
| 生物蛋白胶组 | 4/1 | 28.1±5.5c | 18 012.1±6 587.9bc |
| 曲安奈德组 | 1/4 | 45.7±20.1 | 46 326.6±20 806.1 |
| 对照组 | 2/3 | 51.4±17.3 | 37 306.0±13 623.6 |
| 统计值 | - | 4.54 | 9.29 |
| P值 | - | < 0.05 | < 0.01 |
| a:P < 0.05, b:P < 0.01, 与曲安奈德组比较; c:P < 0.05, d:P < 0.01, 与对照组比较 | |||
2.2 病理学评估
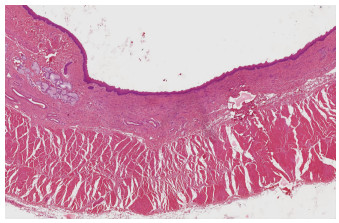
食管HE染色可见(图 3):新生上皮层相对正常食管上皮更毛糙, 术区被肌成纤维细胞及排列紊乱、致密的胶原纤维替代, 可见散在、个别成团的炎症反应细胞, 增生的纤维化组织渗入固有肌层, 局部可见固有肌层萎缩。非手术区域靠近手术区域边缘的食管壁相比手术区域更厚。
|
| 图 3 家犬食管ESD术后6周病理学观察结果(HE ×3) |
免疫组化染色(图 4)提示联合治疗组α-SMA表达量较曲安奈德组和对照组更低, 差异有统计学意义(P < 0.01);生物蛋白胶组表达量较曲安奈德组(P < 0.01)和对照组(P < 0.05)也更低, 差异也有统计学意义。

|
| A:联合治疗组; B:生物蛋白胶组; C:曲安奈德组; D:对照组 图 4 家犬食管ESD术后喷涂生物蛋白胶和曲安奈德6周后免疫组化检测α-SMA表达(S-P ×200) |
3 讨论
本研究于食管距门齿30~34 cm处剥离3/4环周食管黏膜, 并于术后6周行胃镜检查发现(图 1D):手术段明显变窄, 直径9.8 mm的胃镜不能通过, 同时实验犬进食后呕吐, 符合食管ESD术后狭窄的诊断。
不同研究者在评估食管ESD术后狭窄的时间不同。OHKI等[10]于术后4周评估, 更多研究者于术后8周评估[7, 11]。本研究为探索一个适宜的评估干预因素对ESD术后狭窄预防的时间点, 将1只实验犬如前所述方法建模后不应用药物, 于术后2、4、6、8周胃镜检查发现(图 5):术后2周见急性炎症期间所有的粉红色肉芽组织生成, 胃镜尚可通过; 术后4周见食管上皮覆盖术区, 局部黏膜仍比正常黏膜偏红, 瘢痕皱襞初步形成, 胃镜不能通过; 术后6周可见上皮颜色稍白, 瘢痕皱襞明显向管腔中央凸出, 胃镜不能通过; 术后8周与术后6周相比无明显变化。所以, 我们认为食管ESD术后6周可作为评估处理因素术后狭窄干预效果的理想时间。
|
| A:术后2周; B:术后4周; C:术后6周; D:术后8周 图 5 家犬食管ESD术后不同时间胃镜下表现 |
术后狭窄的病理机制包括黏膜上皮延迟愈合、黏膜下层炎症反应、细胞外基质沉积和固有肌层萎缩, 其中激活的肌成纤维细胞可分泌胶原纤维并过度沉积, 且肌成纤维细胞和胶原纤维有收缩效应[9], 而黏膜下层纤维化又可导致食管顺应性和弹性下降[6]。本研究同样观察到术后食管黏膜下层广泛的纤维化、肌成纤维细胞、胶原纤维、固有肌层萎缩(图 3), 也见到胃镜下术区瘢痕皱襞明显凸向管腔(图 5C、D), 但解剖食管后见此处黏膜相对正常黏膜更薄(图 2), HE染色也观察到手术区域食管壁更薄(图 3)。另外, 球囊扩张作为治疗术后狭窄重要而有效的方法之一, 可破坏狭窄处形成的黏膜皱襞, 但仍需反复进行扩张以缓解狭窄。因此, 术后管腔狭窄的主要原因可能是黏膜下层纤维化过程中肌成纤维细胞、胶原纤维收缩而不是术后上皮缺失、延迟愈合和固有肌层萎缩。
生物蛋白胶预防食管ESD术后狭窄的研究较少。IIZUKA等[12]将聚乙醇酸片置于术区并喷涂生物蛋白胶后出现吞咽困难比率为1/13, 与黏膜下注射糖皮质激素相比效果相当。KATAOKA等[13]报道1例局部应用曲安奈德、聚乙醇酸片和生物蛋白胶, 随访84 d未发现明显狭窄。SAKAGUCHI等[4]同样应用聚乙醇酸片和生物蛋白胶, 9.8 mm胃镜不能通过的占比为3/8。这些研究均不能阐明生物蛋白胶是否能预防术后狭窄。生物蛋白胶可抑制成纤维细胞浸润和血管形成、抑制胶原收缩进而抑制创面愈合[14]。而本研究也发现其可减少瘢痕组织中α-SMA表达(图 4), 减少局部瘢痕皱襞凸向管腔中央的程度(图 1), 进而提出生物蛋白胶在预防术后狭窄中的有效性。
糖皮质激素可减少成纤维细胞分化、迁移来缓解黏膜下层纤维化[15], 且黏膜下层注射糖皮质激素预防狭窄已经被证明有效[16], 但本实验显示曲安奈德组与对照组相比并未缓解食管狭窄(图 1), 也没有降低食管狭窄率(表 1、图 2)和减少α-SMA表达(图 4)。我们推测可能是药物喷涂后绝大部分进入胃腔, 局部保留的少量药物被消化道分泌物及术区渗出液冲刷, 致使创面局部起作用的曲安奈德量少, 并且单次应用药物疗效有限。生物蛋白胶与其他药物混合应用时具有对药物的缓慢释放作用, 我们将生物蛋白胶与曲安奈德混合后于食管ESD术后局部喷涂, 形成的曲安奈德缓释胶状载体, 预防术后狭窄的效果似乎比单用生物蛋白胶更有效, 但统计学分析其差异无统计学意义, 可能与单次应用药物效果有限、样本量少有关。
本研究存在一些局限性:①实验对象为动物且样本量小, 需进一步扩大样本量进行验证; 同时, 一部分观察指标也可能因此未能体现出统计学差异。②实验均为一次性给药, 多次给药可能效果更好, 特别是在2周内的急性炎症反应期间补充药物。③测量食管周长时管壁张力不一致, 获取的数据计算出的狭窄率可能存在偏倚。在光滑、水湿润的玻璃板上自然展开食管壁可能是一个更好的方法。
总之, 本研究显示术后6周是评估狭窄程度的适宜时间, 激活的肌成纤维细胞及胶原纤维的收缩在食管ESD术后狭窄中发挥重要作用。局部喷涂生物蛋白胶及联合曲安奈德可通过改善黏膜下层纤维化对术后狭窄产生预防效果, 是一种预防食管ESD术后狭窄的新方法。
| [1] | KOBAYASHI S, KANAI N, OHKI T, et al. Prevention of esophageal strictures after endoscopic submucosal dissection[J]. World J Gastroenterol, 2014, 20(41): 15098–15109. DOI:10.3748/wjg.v20.i41.15098 |
| [2] | WEN J, LU Z, LIU Q. Prevention and treatment of esophageal stenosis after endoscopic submucosal dissection for early esophageal cancer[J]. Gastroenterol Res Pract, 2014, 2014: 457101. DOI:10.1155/2014/457101 |
| [3] | IIZUKA T, KIKUCHI D, YAMADA A, et al. Polyglycolic acid sheet application to prevent esophageal stricture after endoscopic submucosal dissection for esophageal squamous cell carcinoma[J]. Endoscopy, 2015, 47(4): 341–344. DOI:10.1055/s-0034-1390770 |
| [4] | SAKAGUCHI Y, TSUJI Y, ONO S, et al. Polyglycolic acid sheets with fibrin glue can prevent esophageal stricture after endoscopic submucosal dissection[J]. Endoscopy, 2015, 47(4): 336–340. DOI:10.1055/s-0034-1390787 |
| [5] | BARRET M, BORDACAHAR B, BEUVON F, et al. Self-assembling peptide matrix for the prevention of esophageal stricture after endoscopic resection:a randomized controlled trial in a porcine model[J]. Dis Esophagus, 2017, 30(5): 1–7. DOI:10.1093/dote/dow015 |
| [6] | HONDA M, NAKAMURA T, HORI Y, et al. Feasibility study of corticosteroid treatment for esophageal ulcer after EMR in a canine model[J]. J Gastroenterol, 2011, 46(7): 866–872. DOI:10.1007/s00535-011-0400-3 |
| [7] | KATAOKA M, ANZAI S, SHIRASAKI T, et al. Efficacy of short period, low dose oral prednisolone for the prevention of stricture after circumferential endoscopic submucosal dissection (ESD) for esophageal cancer[J]. Endosc Int Open, 2015, 3(2): E113–117. DOI:10.1055/s-0034-1390797 |
| [8] | KIM B S, SHKEMBI F, LEE J. In vitro and in vivo evaluation of commercially available fibrin gel as a carrier of alendronate for bone tissue engineering[J]. Biomed Res Int, 2017, 2017: 6434169. DOI:10.1155/2017/6434169 |
| [9] | MIZUSHIMA T, OHNISHI S, HOSONO H, et al. Oral administration of conditioned medium obtained from mesenchymal stem cell culture prevents subsequent stricture formation after esophageal submucosal dissection in pigs[J]. Gastrointest Endosc, 2017: 10. |
| [10] | OHKI T, YAMATO M, OTA M, et al. Application of regenerative medical technology using tissue-engineered cell sheets for endoscopic submucosal dissection of esophageal neoplasms[J]. Dig Endosc, 2015, 27(2): 182–188. DOI:10.1111/den.12354 |
| [11] | HONDA M, HORI Y, NAKADA A, et al. Use of adipose tissue-derived stromal cells for prevention of esophageal stricture after circumferential EMR in a canine model[J]. Gastrointest Endosc, 2011, 73(4): 777–784. DOI:10.1016/j.gie.2010.11.008 |
| [12] | IIZUKA T, KIKUCHI D, HOTEYA S, et al. Polyglycolic acid sheet and fibrin glue for preventing esophageal stricture after endoscopic submucosal dissection:a historical control study[J]. Dis Esophagus, 2017, 30(11): 1–8. DOI:10.1093/dote/dox053 |
| [13] | KATAOKA Y, TSUJI Y, SAKAGUCHI Y, et al. Preventing esophageal stricture after endoscopic submucosal dissection:steroid injection and shielding with polyglycolic acid sheets and fibrin glue[J]. Endoscopy, 2015, 47(Suppl 1): E473–474. DOI:10.1055/s-0034-1392975 |
| [14] | PETRATOS P B, FELSEN D, TRIERWEILER G, et al. Transforming growth factor-beta2 (TGF-beta2) reverses the inhibitory effects of fibrin sealant on cutaneous wound repair in the pig[J]. Wound Repair Regen, 2002, 10(4): 252–258. DOI:10.1046/j.1524-475X.2002.10409.x |
| [15] | CHEN H C, YEN C I, YANG S Y, et al. Comparison of steroid and botulinum toxin type A monotherapy with combination therapy for treating human hypertrophic scars in an animal model[J]. Plast Reconstr Surg, 2017, 140(1): 43e–49e. DOI:10.1097/PRS.0000000000003426 |
| [16] | TAKAHASHI H, ARIMURA Y, OKAHARA S, et al. A randomized controlled trial of endoscopic steroid injection for prophylaxis of esophageal stenoses after extensive endoscopic submucosal dissection[J]. BMC Gastroenterol, 2015, 15: 1. DOI:10.1186/s12876-014-0226-6 |



