家族性渗出性玻璃体视网膜病变(familial exudative vitreoretinopathy,FEVR)是由Criswick和Schepens[1]于1969年首次提出并命名,是一种遗传性玻璃体视网膜疾病,特点是双侧缓慢进展的周边视网膜血管发育异常。早期可无任何症状,仅表现为周边视网膜无灌注区,随着病情进展,可出现眼内新生血管形成、黄斑移位、视网膜脱离等,引起视力下降,双侧进展可不对称[2-3]。临床FEVR患者常因晚期发生视网膜脱离而就诊。而晚期患者的手术难度高,视力预后不佳,易复发[4]。因此FEVR的早期诊断及治疗成为关键。临床上眼科医师靠肉眼检查和荧光素眼底血管造影(fluorescence fundus angiography,FFA)仅能发现部分视网膜结构改变,常常不能察觉黄斑部的轻微改变[5]。YONEKAWA等[6]通过频域光学相干断层扫描、(spectral-domain optical coherence tomography,SD-OCT)发现16%的FEVR患者黄斑区有永存中心凹胎儿结构和黄斑轮廓变小,推测这可能是一种先天性黄斑结构异常。近年研究发现,基因治疗能明显阻止早期Leber先天性黑矇疾病恶化进程,恢复术眼视觉功能[7-9]。
本研究通过SD-OCT观察早期FEVR患者的黄斑结构,测量其黄斑中心凹厚度(central foveal thickness)及最佳矫正视力(best corrected visual acuity,BCVA),分析FEVR早期的黄斑结构特征,探讨FEVR患者是否存在先天性黄斑发育异常,若存在可能的先天性黄斑发育异常,探究这些异常是否具有普遍性,以期为选择预防FEVR病程进展措施和介入时机提供临床依据。
1 资料与方法 1.1 一般资料收集2014年9月至2017年10月在本院就诊的FEVR患者。入选标准:①有一级亲属的阳性家族史;②FFA显示周边视网膜血管无灌注区;③无早产或出生后吸氧史;④至少有以下一项:新生血管形成、荧光素渗漏,动静脉吻合形成,视网膜血管数量增多、分布密集,视网膜血管被牵拉变直、向颞下方移位。排除标准:①累及后极部的视网膜脱离;②合并其他眼病,如眼外伤、青光眼、高度近视性弱视等。本研究获得陆军军医大学(第三军医大学)第一附属医院伦理委员会批准(2016年科研第29号),符合赫尔辛基宣言中的伦理学标准。根据PENDERGAST和TRESE[2]的国际分期法对所有入选FEVR患眼进行分期:1期,周边部视网膜无血管区,血管分支无明显增多;2期,周边部视网膜无血管区伴新生血管形成(A不伴渗出,B伴有渗出);3期,部分视网膜脱离,未累及黄斑(A渗出为主,B牵引为主);4期,部分视网膜脱离,累及黄斑中心凹(A渗出为主,B牵引为主);5期,视网膜全脱离(A开漏斗型,B闭漏斗型)。纳入研究的对象均接受小瞳验光检查、SD-OCT扫描(激光诊断仪,HRA+OCT SPECTRALIS,Heidelberg,德国;cirrus high definition OCT 5000, Carl Zeiss,德国)、FFA检查。
1.2 SD-OCT测量方法SD-OCT检查由同一名经验丰富的医师完成。检查过程中,受检者直视检查探头中的固视点,采用Cirrus macular cube 512×128扫描模式,对以黄斑中心凹为中心的6 mm×6 mm×2 mm的视网膜区域进行高密度扫描,生成黄斑地形图并测量黄斑中心凹厚度。
1.3 统计学方法采用SPSS 23.0统计软件进行数据分析。使用K-S检验参数是否符合正态分布,符合正态分布的计量资料采用x±s表示,使用t检验行差异性分析,偏态资料采用M(Q1,Q2)表示,使用非参数检验分析,检验水准α=0.05。
2 结果 2.1 一般情况研究入组61例(67眼),分为FEVR组和对照组。FEVR组31例(37眼),其中男性23例,女性8例,年龄7~64(31±16)岁。根据国际通用FEVR分期标准,1期12例15眼,2期18例19只眼,3A期3例3眼(因3A期患者视网膜脱离仅限于周边很小的范围,未累及黄斑区,对于本研究测量指标无影响,故也纳入)。对照组30例(30眼),均为我院非FEVR患者,其中15例为视网膜脱离患者的对侧眼,9例为外伤性视神经病变的对侧眼,6例为玻璃体积血的对侧眼。包括男性21例,女性9例,年龄13~52(31±12)岁。FEVR组和对照组在性别(P=0.56)、年龄(P=0.50)和等效球镜度数[-1.0(-4.75,0) vs-1.75(-5.5,0.06),P=0.89]上差异均无统计学意义。
2.2 黄斑中心凹厚度FEVR组和对照组的黄斑中心凹厚度分别为(234±53)、(234±21)μm,差异无统计学意义(P=0.996)。
2.3 黄斑特征根据SD-OCT图像上黄斑形态结构是否异常,将FEVR组37眼分为黄斑结构正常组和黄斑结构异常组(具体分布情况见表 1)。黄斑结构正常组26眼(70.3%);黄斑结构异常组11眼(29.7%),其中黄斑区脉络膜新生血管(choroidal neovascularization, CNV)2眼,玻璃体黄斑牵拉(vitreous macular traction, VMT)2眼,中心凹变浅3眼,黄斑区椭圆体带连续性中断3眼,同时伴有中心凹变浅及椭圆体带连续性中断1眼(图 1)。黄斑结构异常组、黄斑结构正常组的年龄(P=0.081)、性别(P=0.658)、屈光度(P=0.781)差异均无统计学意义,最佳矫正视力黄斑结构异常组低于黄斑结构正常组,差异有统计学意义(Z=-3.69,P=0.001)。黄斑结构正常组最佳矫正视力与对照组比较,差异无统计学意义(Z=-0.564,P=0.573,表 2)。
| 编号 | 年龄(岁) | 眼别 | 分期 | 视力 | 屈光度(D) | 黄斑中心凹厚度(mm) | 黄斑结构 |
| 1 | 51 | 左眼 | 2期 | 0.01 | 0 | 135 | 黄斑区脉络膜新生血管 |
| 2 | 28 | 左眼 | 2期 | 0.15 | -2.25 | 465 | 黄斑区脉络膜新生血管 |
| 3 | 49 | 右眼 | 1期 | 1.0 | 0.5 | 262 | 玻璃体黄斑牵拉 |
| 49 | 左眼 | 1期 | 1.0 | 0.5 | 251 | 玻璃体黄斑牵拉 | |
| 4 | 47 | 右眼 | 2期 | 0.9 | -4.75 | 225 | 中心凹变浅 |
| 5 | 26 | 右眼 | 3A期 | 0.8 | -5.25 | 195 | 椭圆体带连续性中断 |
| 6 | 24 | 右眼 | 3A期 | 0.6 | -8.5 | 180 | 中心凹变浅、椭圆体带连续性中断 |
| 7 | 14 | 右眼 | 1期 | 0.8 | 0.25 | 288 | 中心凹轻度变浅 |
| 14 | 左眼 | 1期 | 0.8 | 0.25 | 293 | 中心凹轻度变浅 | |
| 8 | 56 | 左眼 | 2期 | 1.0 | -0.5 | 221 | 椭圆体带连续性中断 |
| 56 | 右眼 | 2期 | 0.4 | -0.5 | 171 | 椭圆体带连续性中断 |
|
|
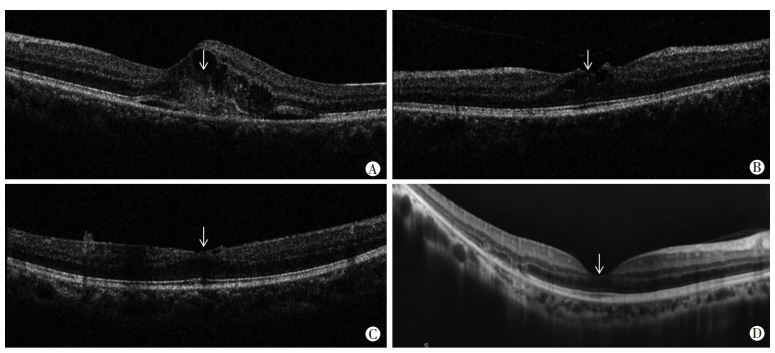
箭头示病变位置 A:黄斑区脉络膜新生血管;B:玻璃体黄斑牵拉;C:黄斑中心凹形态异常;D:黄斑区椭圆体带连续性中断 图 1 黄斑结构异常患者频域光学相干断层扫描观察 |
| 组别 | 例数 | 眼数 | 年龄(x±s,岁) | 屈光度[M(Q1,Q2)] | 最佳矫正视力[M(Q1,Q2)] |
| 黄斑结构异常组 | 8 | 11 | 37±5 | -0.5(-4.75, 0) | 0.8(0.4, 1.0)a |
| 黄斑结构正常组 | 25 | 26 | 28±3 | -1.25(-4.88, 0.063) | 1.0(1.0, 1.0) |
| 对照组 | 30 | 30 | 31±12 | -1.75(-5.5, 0.06) | 1.0(1.0, 1.2) |
| a: P < 0.05, 与黄斑结构正常组比较 | |||||
3 讨论
FEVR一般进展缓慢,早期可无任何临床症状,到中晚期,出现黄斑移位、玻璃体出血、视网膜脱离时可导致明显的视功能受损,患者往往这时才来就诊,同时检查其对侧眼,发现病程处于早期的对侧眼部分BCVA低于正常,甚至有明显下降,眼底检查均未见视力相关的眼底改变,SD-OCT检查发现部分患者存在黄斑结构异常。本研究FEVR组中4眼(4/37)有黄斑区椭圆体带连续性中断。TERAUCHI等[10]指出椭圆体带连续性中断可继发于孔源性视网膜脱离,在手术复位视网膜一段时间后恢复。因此我们推测本研究中的椭圆体带连续性中断可能继发于视网膜下液反复的形成和吸收,可见于FEVR进展引起颞侧视网膜牵引导致的视网膜下液,这种局限性浅脱离早期在休息后很不明显,临床上常常需反复三面镜检查才能发现。另外本研究中患者屈光度均大于5 D,高度近视也可能是导致椭圆体带中断的因素之一。本组4例椭圆体带断裂导致连续性中断的患者视力差异较大,因样本量太小无法统计,进一步的研究将扩大样本量并进行动态观察,并分析其与视力的相关性。4例患者出现黄斑中心凹变浅,其中2例较明显,推测为高度近视所致,另有1例患者表现为双眼黄斑中心凹轻度变浅,目前视力大致正常(0.8),可随访行动态观察。YONEKAWA等[6]发现16%早期FEVR患者伴有永存中心凹胎儿结构(持续存在的神经纤维、神经节细胞层、内丛状层、内核层、外丛状层)和黄斑轮廓变小,文中病例最小年龄2岁,作者认为这种异常随着年龄增大而消失,不能排除是一种发育迟缓。本研究中没有发现这种现象,推测与纳入的患者都在13岁以上有关。本研究中有1例双眼(2/37)FEVR1期的患者视力均为1.0,但SD-OCT检查显示有玻璃体黄斑牵拉。YONEKAWA等[6]也曾报道FEVR伴有玻璃体黄斑牵拉的病例,并且指出FEVR患者一般具有异常的玻璃体视网膜界面,同时伴有黏稠具有收缩倾向的玻璃体,随着病情进展,可能会出现玻璃体视网膜界面的异常结构,如玻璃体黄斑牵拉、玻璃体视盘牵拉等。该患者有轻度玻璃体黄斑牵拉,随着病情进展,可能会引起视力下降,因此对此类患者应密切随访,如果黄斑水肿进行性加重、视力进行性下降可手术治疗。本研究中有2眼(2/37)黄斑区CNV。CNV的发病机制较为复杂,目前尚未完全阐明。其重要的发病机制之一在于视网膜局部缺血缺氧以后继发新生血管的形成[11],而FEVR患者也因血管发育不良导致周边视网膜缺血缺氧继发新生血管形成,因此我们推测FEVR随着病情进展,可能继发CNV。但是FEVR患者一般仅累及周边视网膜,且目前国内外暂无FEVR合并CNV的报道,两者之间有无确切关联也需要进一步研究。因此我们认为:少数FEVR患者早期可出现黄斑结构异常,提示有些FEVR患者早期可出现黄斑结构的改变,引起视力下降,这些患者应定期复查,如果病变进行性发展,视力持续下降,则需密切观察,及早干预。对周边视网膜裂孔或视网膜渗漏早期发现,早期视网膜光凝治疗。因此,除FFA、三面镜检查之外,SD-OCT检查在监测FEVR病情发展上越来越重要。
本研究中,多数(26例,70.2%)FEVR患者早期黄斑结构正常,中心凹视网膜厚度与正常人相比差异无统计学意义,少数FEVR患者出现黄斑结构异常属于继发性改变,提示FEVR患者黄斑区视网膜没有发育异常。VMT、黄斑囊样水肿常由玻璃体视网膜界面异常累及黄斑区引起,椭圆体带中断、中心凹变浅等改变可能是由于患者同时伴有高度近视或继发于周边视网膜的牵拉。
早期FEVR患者黄斑与视力可无任何改变,晚期可因新生血管形成引起一系列继发性改变如视网膜脱离、玻璃体积血后导致视力明显下降。因此,预防FEVR的发展有重要意义。对于没有视力下降的FEVR患者,仍然需要重视,加强遗传咨询和对家族成员的诊断,告知他们,一旦视力出现下降,立即来院检查。FEVR是基因突变导致视网膜血管发育异常,随之继发一系列的病变,从本研究可得出结论:FEVR患者无黄斑发育异常,多数患者早期具有正常的黄斑结构和视力,这为基因治疗提供了治疗时机。目前国外在基因治疗视网膜遗传病上取得了重大进展,利用球内注射基因药物治疗Leber先天性黑矇,能阻止疾病恶化进程,恢复眼睛视觉功能,Ⅲ期临床研究发现,基因治疗后患者生活质量得到了明确改善[9]。目前已发现的FEVR致病基因有6种:LRP5、FZD4、NDP、TSPAN12、ZNF408及KIF11,Wnt信号途径与FEVR的发病密切相关,LRP5等4个蛋白组成的复合物共同参与Wnt信号途径,FEVR模型Lrp5敲除小鼠的视网膜血管发育明显延迟。锂盐能激活Wnt信号途径,绕开基因缺陷,恢复视网膜血管发育,部分恢复小鼠的视网膜功能[11]。基因和干预治疗为预防FEVR的发展提供了新的手段,基因诊断、基因和干预治疗研究将是我们进一步的研究方向。
视力下降是FEVR患者病情进展的敏感指标。OCT具有无创与快速获取图像的能力,能定量分析黄斑中心凹厚度,是监测FEVR进展的重要手段,在评估玻璃体视网膜牵拉异常上也非常有价值,能发现轻微和进行性的黄斑受累情况,已经成为确诊临床无法察觉的玻璃体黄斑牵引综合征的最终手段。OCT技术的进步,如光学相干断层扫描血管成像(optical coherence tomography angiography, OCTA),是一种新出现的高分辨率的血管成像技术,具有三维立体、分层成像的特点[12],相对于FFA,OCTA能帮助我们更好地诊断黄斑中心凹的毛细血管病变,特别是黄斑拱环的破坏以及毛细血管的丢失[13],因此通过OCTA检查FEVR患者,可获得更丰富、更具体的黄斑结构及功能的信息,并可以定量分析,将有助于进一步揭示FEVR患者黄斑改变的特征和发展规律,加深对玻璃体视网膜界面和黄斑关系的理解。
| [1] | CRISWICK V G, SCHEPENS C L. Familial exudative vitreoretinopathy[J]. Am J Ophthalmol, 1969, 68(4): 578–594. DOI:10.1016/0002-9394(69)91237-9 |
| [2] | PENDERGAST S D, TRESE M T. Familial exudative vitreoretinopathy. Results of surgical management[J]. Ophthalmology, 1998, 105(6): 1015–1023. DOI:10.1016/S0161-6420(98)96002-X |
| [3] | MIYAKUBO H, HASHIMOTO K, MIYAKUBO S. Retinal vascular pattern in familial exudative vitreoretinopathy[J]. Ophthalmology, 1984, 91(12): 1524–1530. DOI:10.1016/S0161-6420(84)34119-7 |
| [4] | CHEN S N, HUANG J F, LIN C J. Clinical characteristics and surgical management of familial exudative vitreoretinopathy-associated rhegmatogenous retinal detachment[J]. Retina, 2012, 32(2): 220–225. DOI:10.1097/IAE.0b013e31821c3ec5 |
| [5] | YUAN M, YANG Y, YAN H, et al. Increased posterior retinal vessels in mild asymptomatic familial exudative vitreoretinapathy eyes[J]. Retina, 2016, 36(6): 1209–1215. DOI:10.1097/IAE.0000000000000830 |
| [6] | YONEKAWA Y, THOMAS B J, DRENSER K A, et al. Familial exudative vitreoretinopathy: spectral-domain optical coherence tomography ofthevitreoretinal interface, retina, and choroid[J]. Ophthalmology, 2015, 122(11): 2270–2277. DOI:10.1016/j.ophtha.2015.07.024 |
| [7] | WELEBER R G, PENNESI M E, WILSON D J, et al. Results at 2 years after gene therapy for RPE65-deficient leber congenital amaurosis and severe early-childhood-onset retinal dystrophy[J]. Ophthalmology, 2016, 123(7): 1606–1620. DOI:10.1016/j.ophtha.2016.03.003 |
| [8] | CHACON-CAMACHOÓ JF, ZENTENO J C. Gene therapy for vision restoration in patients with Leber congenital amaurosis (LCA) due to RPE65 gene mutations: beginning the phase Ⅳ trial[J]. Gac Med Mex, 2017, 153(2): 276–278. |
| [9] | BAINBRIDGE J W, MEHAT M S, SUNDARAM V, et al. Long-term effect of gene therapy on Leber's congenital amaurosis[J]. N Engl J Med, 2015, 372(20): 1887–1897. DOI:10.1056/NEJMoa1414221 |
| [10] | TERAUCHI G, SHINODA K, MATSUMOTO C S, et al. Recovery of photoreceptor inner and outer segment layer thickness after reattachment of rhegmatogenous retinal detachment[J]. Br J Ophthalmol, 2015, 99(10): 1323–1327. DOI:10.1136/bjophthalmol-2014-306252 |
| [11] | GROSSNIKLAUS H E, GREEN W R. Pathologic findings in pathologic myopia[J]. Retina, 1992, 12(2): 127–133. DOI:10.1097/00006982-199212020-00009 |
| [12] | SPAIDE R F, KLANCNIK J M JR, COONEY M J. Retinal vascular layers imaged by fluorescein angiography and optical coherence tomography angiography[J]. JAMA Ophthalmol, 2015, 133(1): 45–50. DOI:10.1001/jamaophthalmol.2014.3616 |
| [13] | SOARES M, NEVES C, MARQUES I P, et al. Comparison of diabetic retinopathy classification using fluorescein angiography and optical coherence tomography angiography[J]. Br J Ophthalmol, 2017, 101(1): 62–68. DOI:10.1136/bjophthalmol-2016-309424 |



