腹主动脉瘤腔内修复术(endovascular aneurysm repair, EVAR)是指经非治疗区的血管入路置入人工血管支架达到治愈腹主动脉瘤的治疗方式。常规的血管入路包括股动脉、髂动脉及肱动脉等。血管入路的解剖形态在EVAR中起着关键作用[1],术中股、髂动脉钙化、狭窄、闭塞及瘤样变等复杂的血管入路常导致血管内膜损伤、血管破裂、支架闭塞、动脉血栓形成等并发症,危及患者的生命安全[2]。目前针对复杂的入路及其并发症的解决办法包括经腹膜后解剖髂动脉、切除扭曲血管、股股搭桥及支架置入血管矫形等[3-5]。当介入医师面对复杂的血管入路时,若处理不当,极易造成医源性损伤。本研究回顾性分析2015年5月至2017年5月我院57例EVAR血管入路并发症发生的原因及处理方法,报告如下。
1 资料与方法 1.1 临床资料收集2015年5月至2017年5月我科收治的肾下腹主动脉瘤患者,主要临床表现:腹部搏动性肿块,伴或不伴有腹部或腰背部疼痛。纳入标准:①经CT动脉造影(CTA)、数字减影血管造影(DSA)或核磁共振血管成像(MRA)检查;②主动脉瘤瘤体直径,男性>5 cm,女性>4.5 cm,或年增长率大于5 mm;③任意大小瘤体伴有腹部或/和腰背部疼痛。排除标准:因外伤,感染,梅毒或结缔组织病导致的腹主动脉瘤,大动脉炎合并腹主动脉瘤者。纳入66例患者中6例行开腹手术治疗,3例于手术前突发瘤体破裂,经抢救无效死亡,57例行EVAR治疗。EVAR病例中男性48例,女性9例,年龄(71.2±10.3)岁。本研究经重庆医科大学附属第一医院伦理委员会审核通过(2016年),患者签署知情同意书。
1.2 手术材料AXIOM Artis周围血管平板血管造影系统(西门子);21G微穿刺套件(COOK);6F Flexor Balkin对侧鞘(翻山鞘)和Shuttle Tibial膝下导引鞘(COOK);4F C2导管和多功能导管;Diver支持导管(INVATEC)和2.7F微导管(ev3);0.035 inch导丝(Terumo);0.018 inch V18及0.014 inch PT2 300 cm导丝(Boston Scientific);0.014 inch Miracle 180 cm系列冠脉CTO硬头导丝;小剖面长球囊(长度80~120 mm,工作直径1.5~4 mm);Amphirion Deep球囊(INVATEC);6 mm人工血管(Gore);VIABAHN覆膜支架(Gore);Endurant Ⅱ支架(Medtronic);Ankura Ⅱ支架(Lifetech)等。
1.3 手术方式在静脉麻醉下,常规全穿或于双侧腹股沟区切开皮肤暴露股动脉,采用塞丁格法穿刺股动脉,置入6F血管鞘,5F猪尾导管行主动脉造影,根据入路血管的不同情况预先处理后,准确测量瘤颈和瘤体的长度和直径、髂总动脉直径、肾动脉开口至髂内动脉开口的距离,并与术前螺旋CT结果对照,选择适当口径和长度的人工血管支架,常规肝素化后沿导丝置入支架主体并与肾动脉平面下方释放,对侧短臂位于瘤腔内,穿刺对侧股动脉,置入单支直筒血管支架与短臂锚定,远端根据不同的入路情况,确定锚定位置及方法,支架完全置入后再次行主动脉造影观察内漏情况及各个分支血管情况,必要时于瘤腔内填入弹簧圈促进瘤体内血栓形成,稳定支架[6]。
1.4 血管入路处理方法髂动脉扭曲者采用特殊加硬导丝(PA35153M,Terumo)支撑导入移植物或肱股牵张导丝技术纠正扭曲髂动脉从而置入支架主体[7];导入动脉过细者于腹膜外行小切口暴露髂动脉,经髂外或髂总动脉导入移植物;髂动脉狭窄者用6~10 mm球囊逐步扩张再行支架置入;髂动脉闭塞者采用同侧肱动脉穿刺入导丝至股动脉引出,采用6~10 mm球囊逐步扩张开通闭塞段再行支架主体置入[8]。单侧髂动脉瘤:累及髂内动脉者行髂内动脉主干栓塞,支架分支延长至髂外动脉锚定,未累及髂内动脉者锚定位于髂内动脉开口[9]。双侧髂动脉瘤者若瘤体直径均 < 25 mm,选择合适“喇叭口”髂腿支覆盖至髂内外动脉分叉处,保留双侧髂内动脉;若瘤体直径≥25 mm,栓塞该侧髂内动脉并将分支延伸至髂外动脉锚定,对侧选择“喇叭口”支架[10]。
1.5 术后随访EVAR术后30 d,患者于门诊复查,采用彩色多普勒检测观察瘤体内血栓形成、支架形态、支架内血流、各血管入路及双下肢动脉内血流情况,记录血液的流速、流量等指标。
2 结果 2.1 一般资料57例患者成功完成EVAR手术,无中转开放手术病例,无患者死亡。手术时间(112.25±21.30)min。经CTA及术中DSA造影发现入路血管中髂动脉扭曲(成角>90°)7例(12.28%),股动脉直径细(<7 mm) 3例(5.26%),一侧髂动脉闭塞4例(7.02%),合并髂动脉瘤5例(8.77%,双髂动脉瘤2例,单侧髂动脉瘤3例)。
2.2 不同血管入路的并发症及其处理19例复杂入路患者术中髂动脉破裂1例(5.26%),血管内支架闭塞2例(10.53%),股动脉内膜损伤3例(15.79%),髂股动脉血栓形成1例(5.26%)。髂动脉破裂采用血管内覆膜支架(VIABAHN)封堵;血管内支架释放后导致髂动脉闭塞者采用PTFE人工血管股股转流术,股动脉内膜损伤者实施毁损段切除人工血管移植及裸支架贴服内膜,术后重建血管通畅。下肢动脉血栓形成患者采用支架矫形狭窄段并配合Fogarty球囊导管取栓。
2.3 术后随访情况术后30 d失访2例,发生Ⅱ型内漏3例,术后30 d无患者死亡。髂动脉破裂者用覆膜支架封堵后,未出现支架断裂,移位及支架内血栓形成;髂动脉支架置入后闭塞者实施股股转流术,术后30 d双侧股动脉与人工血管吻合口愈合良好,无狭窄,人工血管内无血栓形成,患者下肢无缺血相关症状及体征;股动脉内膜损伤者采用人工血管移植或裸支架贴服内膜,1例出现吻合口狭窄,血液流速增加,流量减少,患者无缺血相关症状。余2例吻合口无渗漏,无狭窄,支架无移位及折叠,管腔血流通畅;下肢动脉血栓形成患者采用支架矫形及Fogarty球囊取栓,随访中支架帖服良好,无移位及断裂,下肢血供良好。
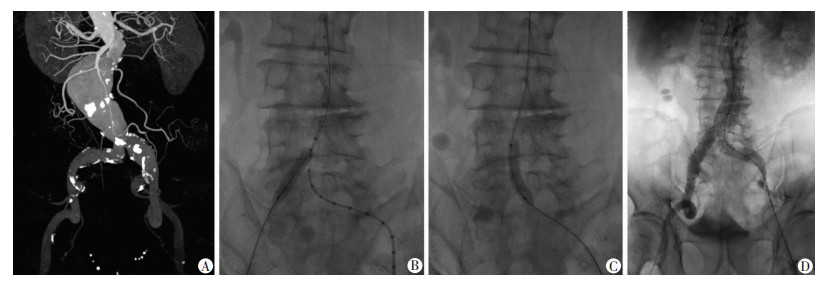
2.4 典型病例病例1:女性,64岁,因突发腹部疼痛2 h入院,体格检查可扪及腹部搏动性肿块,超声检查探及腹主动脉,双髂动脉管径增宽,行CTA检查诊断为腹主动脉瘤合并双侧髂动脉瘤,术中发现双髂动脉开口钙化,狭窄,支架主体无法置入,随即先行采用8 mm球囊行双侧髂动脉扩张后支架主体置入,术后30 d随访,支架稳定,支架内血流通畅(图 1)。
|
| A: CTA示腹主动脉瘤合并双髂动脉瘤,双髂动脉开口狭窄;B、C:DSA下采用8 mm球囊行左、右侧髂动脉扩张;D:DSA下置入支架主体 图 1 EVAR时球囊扩张双侧狭窄髂动脉入路后支架置入 |
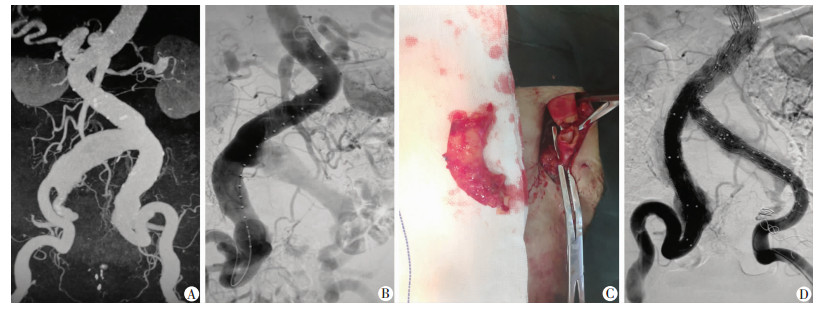
病例2:男性,67岁,因体检发现腹部搏动性肿块入院,CTA检查发现腹主动脉瘤合并双侧髂动脉瘤,双侧髂-股动脉扭曲, 扭曲呈“S”型,成角>90°,EVAR术中切开右腹股沟区,暴露扭曲的股动脉,沿股动脉向上解剖至髂外动脉扭曲节段,并切除扭曲髂外动脉约3 cm,经切口近端置入支架主体后,5-0普理灵缝线吻合髂-股动脉。术后30 d随访,吻合口无渗漏,无狭窄,血流通畅,下肢未出现缺血相关症状及体征(图 2)。
|
| A、B:CTA及DSA提示右侧髂股动脉严重扭曲,无法置入支架;C:分离并切除髂外动脉扭曲段;D:DSA下置入支架主体 图 2 切除扭曲的髂外动脉后DSA下行腹主动脉瘤支架置入 |
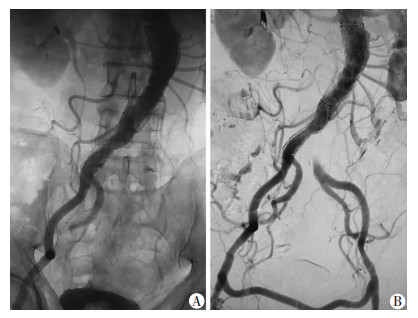
病例3:男性,73岁,因腹部搏动性肿块伴腹痛入院,CTA检查发现腹主动脉瘤合并双侧髂动脉钙化,EVAR术中成功释放支架主体,释放支架左侧腿支时出现左侧髂总动脉闭塞,左下肢出现皮肤苍白,皮温降低,下肢动脉搏动消失等症状及体征,立即采用6 mm PTFE人工血管,行股股转流术,术后下肢皮肤色泽恢复正常,皮温转暖,各动脉搏动点恢复搏动。术后30 d随访,吻合口血流通畅,双下肢血供良好,无缺血相关症状及体征(图 3)。
|
| A:DSA下支架主体置入后,左侧髂分支折叠闭塞;B:开放手术行股-股搭桥后造影观察 图 3 DSA下支架主体置入后左侧髂动脉分支折叠闭塞行股-股搭桥术 |
3 讨论
良好的血管入路是EVAR成功的基本保证。国内血管外科专家共识认为良好的血管入路主要是指:(1)主髂动脉、髂股动脉弯曲度均不得>90°;(2)双侧髂动脉、股动脉无广泛钙化及严重狭窄甚至闭塞;(3)双侧髂动脉、股动脉非瘤样变时直径>7 mm。反之则为复杂血管入路,常见的复杂入路主要包括:髂股动脉扭曲成角,髂股动脉纤细、狭窄及闭塞,髂动脉瘤样变等。复杂血管入路可直接导致支架置入困难或无法置入;需要对血管进行预处理或调整置入方式,若强行置入支架,极有可能造成严重并发症,如入路血管破裂、血管内支架闭塞、动脉内膜损伤、动脉断裂及动脉血栓形成等。
本研究发现导入血管中髂动脉扭曲成角>90°患者7例,占全部病例的12.28%。髂动脉极度的扭曲及髂血管闭塞是导致支架释放后血管内支架闭塞的重要原因[11-12]。本研究中血管内支架闭塞2例,其中1例是由血管扭曲角度大,在支架经过扭曲位置时发生折叠。2例髂血管内支架闭塞病例均通过股-股人工血管转流术,恢复下肢血流。随着经验的积累及支架工艺的进步,入路血管极度扭曲这一EVAR禁忌证逐渐得以破除,对于扭曲角度较小的病例可以使用超硬导丝配合柔顺性较好的支架主体尝试性的导入[13],对于角度>90°的病例则需要尝试以特殊加硬导丝为支撑,置入带亲水涂层的支架输送系统,多能顺利通过[14-15]。此外也有学者采用逐步更换普通硬度导丝、超硬导丝、特殊加硬导丝的方法改善入路血管的形态。还可以通过对扭曲段的切除整形以消除支架折叠的风险[16-17],或从肱动脉导入导丝,实现肱股牵拉技术使髂动脉的扭曲状态得到缓解,继而导入支架。
腹主动脉瘤是动脉硬化基础上的血管壁扩张,常伴有髂动脉硬化狭窄及闭塞[13]。本研究中发现一侧髂动脉闭塞4例,占7.02%。国外研究认为因髂股动脉闭塞导致约6%的患者无法顺利实施EVAR手术[18],本研究中髂动脉内支架闭塞2例,其中1例即是因为术前髂动脉闭塞,预扩不充分,分支支架在狭小的髂动脉内无法展开,导致支架塌陷闭塞。目前支架导入系统直径一般是14~25 F(1 F≈0.33 mm),髂动脉直径<7 mm一度被认为是EVAR的禁忌证。髂动脉闭塞患者首选的方式是先行球囊扩张,再导入支架。对于扩张无效的病例,特别是合并有对侧髂动脉瘤者,可以行主髂单臂支架置入,再行股-股人工血管搭桥及髂外动脉结扎[19-22]。一项为期12年的随访结果确定了主髂单臂支架在髂动脉闭塞患者中运用的优越性[23]。但对于严重钙化的患者,股-股搭桥有着较高的远期并发症风险,如吻合口狭窄,血栓形成及假性动脉瘤形成等。此外,在伴有硬化狭窄闭塞的血管中操作,血管破裂的风险增加,发生率约3%[24]。在4例髂动脉闭塞病例中,1例于球囊扩张时发生破裂出血,原因是球囊直径过大,DSA下表现为呈片状的造影剂快速弥散至血管外,本例及时给予VIABAHN腹膜支架置入覆盖破口,避免了灾难性的后果。对于DSA下难以止血者,应立即中转开放手术, 迅速找到动脉破裂口并予以修复。
既往将股动脉直径<6~7.5 mm定义为行EVAR时的股动脉狭窄[25]。目前,随着支架导入系统直径的减小,这一定义值逐渐降低。对于伴有硬化的狭窄段,可先行球囊扩张,若扩张后仍不能达到支架导入系统的要求时或股动脉先天发育纤细,如部分女性患者[24],可直接经腹膜外游离髂动脉,经髂外或髂总动脉直接置入支架。对于股动脉纤细、硬化狭窄及闭塞的患者,术中介入材料反复的导入,操作时间长,血流阻断时间增加,粗暴操作导致的髂股斑块脱落、夹层形成是动脉壁损伤和下肢动脉血栓形成的主要因素[4, 24]。在本研究中发生股动脉损伤3例,其原因是导入系统与动脉直径不匹配,置入过程中导致内膜损伤,分别采取动脉毁损段切除后行人工血管移植及裸支架将内膜贴壁等处理措施。此外,根据股内膜损伤程度不同还可以采用补片成型、内膜固定或覆膜支架覆盖等处理方法[26]。术后下肢血栓形成,还与术后髂股动脉恢复扭曲状态导致支架折叠扭结、流出道狭窄、血流减慢,及患者合并房颤等多因素相关[4]。国外报道其发生率为3.5%~5.5%[11, 27]。本研究中发生1例髂股动脉血栓形成,考虑与支架分支折叠成角所致的血管狭窄相关,及时给予球囊扩张,裸支架置入矫形,同时配合Fogarty导管取栓术,下肢血流恢复。早发现,早处理是支架置入后动脉血栓形成保全肢体及患者生命的重要原则,及时解除支架狭窄并配合Fogarty导管取栓、血管腔内接触性溶栓、机械性血栓切除等治疗措施可显著改善EVAR患者的预后[12]。
腹主动脉瘤合并髂动脉瘤在临床中较常见,腹主动脉瘤合并双侧髂动脉瘤者占15%~30%[28],髂动脉瘤样变并不会直接影响支架主体的置入,但在远端锚定区的选择上,为了既防止Ⅰ型内漏的发生又要保留盆腔脏器及臀部的血供,使得EVAR的难度增加[29]。我们分别使用了延长支架至髂外锚定、“喇叭口”支架置入及单侧髂内动脉栓塞等处理方案,无早期并发症的发生。
总之,EVAR的复杂入路及相关并发症的处理,有赖于术前CTA及术中DSA观察与评估。术前CTA充分地评估髂股动脉有无扭曲、成角、狭窄甚至闭塞,判断腹主动脉瘤能否行腔内治疗。术中放置支架时,仔细确定支架是否展开充分,是否存在扭曲折叠,流出道有无狭窄甚至闭塞,血液流速是否下降,发现问题及时腔内处理。当腔内解决不足时,可借助开放手术。本组中分别使用了人工血管移植,股-股人工血管搭桥及Fogarty导管取栓等经典的血管外科手术技巧,降低了复杂入路早期并发症的风险。精湛的腔内技术及开放手术技巧同样重要,二者结合,相得益彰。随着血管外科医师经验的积累及腔内介入器材的发展,越来越多的EVAR绝对禁忌证成为相对禁忌,将有更多的伴有复杂血管入路的腹主动脉瘤患者得到腔内治疗。
| [1] | GALLITTO E, GARGIULO M, FAGGIOLI G, et al. Impact of iliac artery anatomy on the outcome of fenestrated and branched endovascular aortic repair[J]. J Vasc Surg, 2017, 66(6): 1659–1667. DOI:10.1016/j.jvs.2017.04.063 |
| [2] | MOULAKAKIS K G, ANTONOPOULOS C N, KLONARIS C, et al. Bilateral endograft limb occlusion after endovascular aortic repair:predictive factors of occurrence[J]. Ann Vasc Surg, 2018, 46: 299–306. DOI:10.1016/j.avsg.2017.07.019 |
| [3] | VALLABHANENI R, SORIAL E E, JORDAN W D JR, et al. Iliac artery recanalization of chronic occlusions to facilitate endovascular aneurysm repair[J]. J Vasc Surg, 2012, 56(6): 1549–1554. DOI:10.1016/j.jvs.2012.05.089 |
| [4] | LIM J H, SUNG Y W, OH S J, et al. Successful endovascular management of intraoperative graft limb occlusion and iliac artery rupture occurred during endovascular abdominal aortic aneurysm repair[J]. Korean J Thorac Cardiovasc Surg, 2014, 47(1): 71–74. DOI:10.5090/kjtcs.2014.47.1.71 |
| [5] | FERNANDEZ J D, CRAIG J M, GARRETT H E JR, et al. Endovascular management of iliac rupture during endovascular aneurysm repair[J]. J Vasc Surg, 2009, 50(6): 1293–1299. DOI:10.1016/j.jvs.2009.06.020 |
| [6] | UHLMANN M E, WALTER C, TAHER F, et al. Successful percutaneous access for endovascular aneurysm repair is significantly cheaper than femoral cutdown in a prospective randomized trial[J]. J Vasc Surg, 2018. DOI:10.1016/j.jvs.2017.12.052 |
| [7] | ZENG Q L, HUANG L J, HUANG X Y, et al. Endovascular repair of abdominal aortic aneurysm with severely angulated neck and tortuous artery access:case report and literature review[J]. BMC Surg, 2015, 15: 20. DOI:10.1186/s12893-015-0005-5 |
| [8] | ETKIN Y, BAIG A, FOLEY P J, et al. Management of difficult access during endovascular aneurysm repair[J]. Ann Vasc Surg, 2017, 44: 77–82. DOI:10.1016/j.avsg.2017.03.190 |
| [9] | PAPAZOGLOU K O, SFYROERAS G S, ZAMBAS N, et al. Outcomes of endovascular aneurysm repair with selective internal iliac artery coverage without coil embolization[J]. J Vasc Surg, 2012, 56(2): 298–303. DOI:10.1016/j.jvs.2011.08.063 |
| [10] | NAUGHTON P A, PARK M S, KHEIRELSEID E A, et al. A comparative study of the bell-bottom technique vs hypogastric exclusion for the treatment of aneurysmal extension to the iliac bifurcation[J]. J Vasc Surg, 2012, 55(4): 956–962. DOI:10.1016/j.jvs.2011.10.121 |
| [11] | WANG G, ZHAI S, LI T, et al. Limb graft occlusion following endovascular aortic repair:Incidence, causes, treatment and prevention in a study cohort[J]. Exp Ther Med, 2017, 14(2): 1763–1768. DOI:10.3892/etm.2017.4658 |
| [12] | RONSIVALLE S, FARESIN F, FRANZ F, et al. A new management for limb graft occlusion after endovascular aneurysm repair adding a vollmar ring stripper:the unclogging technique[J]. Ann Vasc Surg, 2013, 27(8): 1216–1222. DOI:10.1016/j.avsg.2013.02.018 |
| [13] | VOURLIOTAKIS G, KATSARGYRIS A, TIELLIU I F, et al. A modified technique for Gore Excluder limb deployment in difficult iliac anatomy during endovascular abdominal aortic aneurysm repair[J]. Vascular, 2015, 23(1): 78–82. DOI:10.1177/1708538114529277 |
| [14] | TROISI N, PITOULIAS G, MICHELAGNOLI S, et al. Preliminary experience with the Endurant Ⅱ short form stent-graft system[J]. J Cardiovasc Surg, 2017. DOI:10.23736/S0021-9509.17.09862-7 |
| [15] | DEERY S E, SHEAN K E, POTHOF A B, et al. Three-year results of the endurant stent graft system post-approval study (ENGAGE PAS)[J]. Ann Vasc Surg, 2018. [Epub ahead of print]. DOI: 10.1016/j.avsg.2017.12.017. |
| [16] | CULVERWELL A D, KENT P, PUPPALA S. Iliac artery occlusion with "oxbow lake" formation following stent deployment in a tortuous external iliac artery during EVAR:a case report[J]. Vasc Endovascular Surg, 2011, 45(7): 668–671. DOI:10.1177/1538574411414922 |
| [17] | FRANZ R W. Unique operative approach for dealing with a tortuous external iliac artery during abdominal aortic aneurysm endografting[J]. Int J Angiol, 2009, 18(1): 49–51. DOI:10.1055/s-0031-1278324 |
| [18] |
李伦, 任为. 腹主动脉瘤中组织蛋白酶S以及NF-κB p65的表达及意义[J].
第三军医大学学报, 2014, 36(5): 483–486.
LI L, REN W. Expression and significance of cathepsin S and NF-κB p65 in abdominal aortic aneurysm[J]. J Third Mil Med Univ, 2014, 36(5): 483–486. |
| [19] | ARKO F R, FILIS K A, SEIDEL S A, et al. How many patients with infrarenal aneurysms are candidates for endovascular repair? The Northern California experience[J]. J Endovasc Ther, 2004, 11(1): 33–40. DOI:10.1177/152660280401100104 |
| [20] | KANG S H, BAE J M, YUN W S. Endovascular aortic aneurysm repair using a bifurcated stent graft in a patient with femoro-femoral bypass[J]. Ann Surg Treat Res, 2015, 89(2): 107–110. DOI:10.4174/astr.2015.89.2.107 |
| [21] | HOSSAIN S, STEINMETA O K, CORRIVEAU M M, et al. Patency of the contralateral internal iliac artery in aortouni-iliac endografting[J]. J Vasc Surg, 2016, 63(4): 974–982. DOI:10.1016/j.jvs.2015.10.056 |
| [22] | FUJIMURA N, HARADA H, YASHIRO H, et al. Endovascular repair of abdominal aortic aneurysm using bifurcatedstent-graft in a patient with complete occlusion from the common to the external iliac artery[J]. Ann Vasc Surg, 2014, 28(3): 740–741. DOI:10.1016/j.avsg.2013.07.007 |
| [23] | STRAJINA V, ODERICH G S, FATIMA J, et al. Endovascular aortic aneurysm repair in patients with narrow aortas using bifurcated stent grafts is safe and effective[J]. J Vasc Surg, 2015, 62(5): 1140–1147. DOI:10.1016/j.jvs.2015.07.050 |
| [24] | DORTCH J D, OLDENBURY W A, FARRES H, et al. Long-term results of aortouniiliac stent grafts for the endovascular repair of abdominal aortic aneurysms[J]. Ann Vasc Surg, 2014, 28(5): 1258–1265. DOI:10.1016/j.avsg.2013.12.026 |
| [25] | DURAN C, NAOUM J J, SMOLOCK C J, et al. A longitudinal view of improved management strategies and outcomes after iatrogenic iliac artery rupture during endovascular aneurysm repair[J]. Ann Vasc Surg, 2013, 27(1): 1–7. DOI:10.1016/j.avsg.2012.04.017 |
| [26] | JORDAN W D, NASLUND T C, ADELMAN M A, et al. Endovascular abdominal aortic aneurysm repair in patients with challenging anatomy:utility of the hybrid endograft[J]. Vascular, 2004, 12(2): 106. DOI:10.2310/6670.2004.20760 |
| [27] | VAN KEULEN J W, DE VRIES J P, DEKKER H, et al. One-year multicenter results of 100 abdominal aortic aneurysm patients treated with the Endurant stent graft[J]. J Vasc Surg, 2011, 54(3): 609–615. DOI:10.1016/j.jvs.2011.02.053 |
| [28] | RANCIC Z. Commentary on:"endograft limb occlusion in EVAR:iliac tortuosity quantified by three different indices on the basis of preoperative CTA"[J]. Eur J Vasc Endovasc Surg, 2014, 48(5): 534–535. DOI:10.1016/j.ejvs.2014.08.008 |
| [29] | FALKENSAMMER J, HAKAIM A G, ANDREW OLDENBURG W, et al. Natural history of the iliac arteries after endovascular abdominal aortic aneurysm repair and suitability of ectatic iliac arteries as a distal sealing zone[J]. J Endovasc Ther, 2007, 14(5): 619–624. DOI:10.1177/152660280701400503 |



