结外鼻型NK/T细胞淋巴瘤(extranodal NK/T-cell lymphoma,nasal type ENKL,NKTCL)作为非霍奇金淋巴瘤的一种特殊类型,发病率占全部恶性淋巴瘤的2%~10%[1]。流行病学调查示其发病具有明显的地域分布,亚洲及拉丁美洲较欧美国家明显多发[2],其发病机制尚不清楚。研究表明EB病毒(epstein-barr virus,EBV)感染与其发病机制有高度相关性,该病呈高度侵袭性进展,对化疗不敏感,预后差,生存期短,早期治疗常以单独放疗或联合化疗为主,进展期以化疗为主,化疗后部分患者可获短暂缓解却极易复发[3],故准确的预后评估对于NKTCL对于患者至关重要。本研究回顾性分析我中心85例NKTCL患者的临床随访资料,探讨NKTCL的临床特征、免疫组化、预后评估方式及其对预后与生存的影响。
1 资料与方法 1.1 一般资料收集2013年1月至2017年4月到我科就诊,根据初诊时鼻腔有明显新生物及颈部有伴有淋巴结肿大等临床特征并经病理确诊为NKTCL,电子资料完整的85例住院患者病例。本组患者中男性57人,女性28人,中位发病年龄46(20~83)岁,临床分期采用Ann Arbor分期标准,Ann ArborⅠ/Ⅱ分期占57.6%,分组、疗效评价标准参照张之南主编的血液病诊断及疗效第3版[4]。
1.2 治疗方式本组患者依据Ann Arbor标准选用单纯放疗、单纯化疗、联合放化疗3种治疗方式。Ⅰ/Ⅱ期患者多釆用放疗+化疗联合为主的治疗方式,部分行单纯放疗,Ⅲ/Ⅳ期则以化疗为主,少部分辅以姑息性放疗。85例患者中:单纯放疗6例(7.0%),放疗剂量45~50 Gy,中位剂量47 Gy,1.8~2.0 Gy/次。单纯化疗53例(62.4%),化疗方案主要以传统的CHOP(环磷酰胺+盐酸表柔比星+长春新碱+泼尼松)方案或现CR较高的MESA(甲氨蝶呤+地塞米松+足叶乙甙培门冬酶)方案为主:21 d为1个疗程,通常行4~6个疗程治疗。联合放化疗26例(30.6%),化疗2~3个疗程后即开始接受局部放射治疗,之后继续接受化疗治疗,直至化疗达6个疗程。
1.3 测量、评价指标收集85例患者首次治疗前实验室指标:乳酸脱氢酶(lactate dehydrogenase,LDH)、白细胞计数、血红蛋白和血小板计数。病理科调阅85例患者的详细病理诊断免疫组化分型指标:灶性CD20、T细胞内抗原-1 (T-cell intracellular antigen-1,TIA1)、颗粒酶B(granzyme B,GNB)、Ki67、EBV等指标。纳入研究影响因素指标有:临床特征、免疫组化特征、预后评估方式等。85例均行电话随访,随访截止日期为2017年4月1日。
1.4 统计学方法总生存时间(overall survival time,OS)的计算为疾病确诊时间至死亡或末次随访的时间间隔,应用SPSS19.0统计软件进行统计分析。预后影响因素的单因素分析采用Kaplan-Meier法,多因素分析采用Cox比例风险模型多因素分析,双因素相关性分析运用配对χ2检验。将单因素分析显示与预后相关的因素再纳入多因素分析。
2 结果 2.1 生存情况至随访截止日期,全组中位生存时间37个月,85例患者中生存39例,死亡46例,占全组的54.1%,经电话随访及回顾既往病例资料,其死亡原因均因疾病复发或进展。1、3、5年总生存率分别为68.2%、48.4%、32.7%;1、3、5年疾病无事件生存率(event-free survival rate,EFS)分别为56.0%、45.3%、31.8%。Ann Arbor分期Ⅰ/Ⅱ期者49例,占总病例数的57.6%,平均生存时间为56.9月,其1、3、5年生存率为87.3%、80.0%、52.0%,Ann Arbor分期Ⅲ/Ⅳ期者36例,占总病例数的42.4%,其1、3年存活率分别为30.6%、0%。
2.2 影响ENKL预后的单因素分析分析临床特征及实验室指标性别、年龄、ECOG(Eastern Cooperative Oncology Group)评分、Ann Arbor分期、国际预后指数(International Prognostic Index,IPI)及淋巴瘤B症状、LDH、血红蛋白、白细胞数、血小板数(表 1),免疫组化指标:CD20、TIA1、GNB、Ki65、EBV(表 2),表中P值代表各影响因素指标对NKTCL预后的总生存率是否具有统计学意义。结果表明:ECOG评分≥2分、Ann Arbor分期属于Ⅲ/Ⅳ、IPI≥3分、淋巴瘤B症状、高LDH、异常白细胞数、低血红蛋白水平、灶性CD20(-)、EBV(+)均是影响NKTCL患者的不良预后因素。
| 因素 | 百分比(%) | 总生存时间(月) | 3年生存率(%) | 5年生存率(%) | P* |
| 性别 | 0.905 | ||||
| 男 | 67.1 | 34.5 | 53.2 | 26.8 | |
| 女 | 32.9 | 38.1 | 55.7 | 46.2 | |
| 年龄 | |||||
| <60岁 | 84.8 | 36.7 | 53.9 | 40.8 | 0.822 |
| ≥60岁 | 15.2 | 35.3 | 50.5 | 36.7 | |
| Ann Arbor分期 | |||||
| Ⅰ/Ⅱ期 | 57.6 | 56.9 | 80.0 | 52.0 | 0.000 |
| Ⅲ/Ⅳ期 | 42.4 | 10.4 | 0.0 | 0.0% | |
| 国际IPI评分 | |||||
| 0~2分 | 68.2 | 51.2 | 72.5 | 44.6 | 0.000 |
| 3~5分 | 31.8 | 7.7 | 0.0 | 0.0 | |
| 淋巴瘤B症状 | |||||
| 有 | 61.1 | 47.3 | 10.6 | 2.1 | 0.000 |
| 无 | 38.9 | 17.7 | 68.3 | 58.0 | |
| 血清LDH | |||||
| 正常 | 68.2 | 50.6 | 70.7 | 50.3 | 0.000 |
| 升高 | 31.8 | 17.8 | 17.2 | 5.7 | |
| ECOG评分 | |||||
| 0~1分 | 69.4 | 50.5 | 72.8 | 42.9 | 0.000 |
| 2~4分 | 30.6 | 6.5 | 0.0 | 0.0 | |
| 白细胞计数 | |||||
| 4~10×109/L | 68.2 | 42.2 | 56.2 | 36.1 | 0.032 |
| 异常 | 31.8 | 24.3 | 23.6 | 13.5 | |
| 是否贫血 | |||||
| ≥11 g/L | 68.2 | 45.6 | 64.2 | 39.5 | 0.000 |
| <11 g/L | 31.8 | 15.8 | 21.2 | 6.2 | |
| 血小板计数 | |||||
| ≥100×1012/L | 88.2 | 39.1 | 56.7 | 46.1 | 0.067 |
| <100×1012/L | 11.8 | 24.8 | 30.0 | 15.0 | |
| 治疗方案 | |||||
| 单纯放疗组 | 7.0 | 32.5 | 66.7 | 47.5 | 0.611 |
| 单纯化疗组 | 62.4 | 34.7 | 48.2 | 25.6 | |
| 放疗+化疗组 | 30.6 | 37.1 | 51.9 | 30.5 | |
| *代表总生存率 | |||||
| 因素 | 百分比(%) | 总生存(月) | 3年生存率(%) | 5年生存率(%) | P* |
| 灶性CD20 | |||||
| 阳性(+) | 65.9 | 38.0 | 57.9 | 32.7 | 0.05 |
| 阴性(-) | 34.1 | 28.8 | 26.8 | 16.3 | |
| TIA1 | |||||
| 阳性(+) | 91.8 | 24.7 | 57.6 | 29.8 | 0.78 |
| 阴性(-) | 8.2 | 29.0 | 42.9 | 24.3 | |
| GNB | |||||
| 阳性(+) | 91.8 | 37.0 | 57.6 | 25.9 | 0.826 |
| 阴性(-) | 8.2 | 32.5 | 64.3 | 43.3 | |
| Ki67 | |||||
| 0~30 | 48.2 | 36.2 | 41.1 | 27.4 | 0.758 |
| 30~60 | 36.5 | 34.8 | 38.5 | 28.8 | |
| 60~100 | 15.3 | 31.0 | 34.6 | 20.1 | |
| EBV | |||||
| 阳性(+) | 77.6 | 29.8 | 48.2 | 26.4 | 0.010 |
| 阴性(-) | 22.4 | 52.9 | 70.1 | 43.7 | |
| *代表总生存率 | |||||
2.3 多因素分析
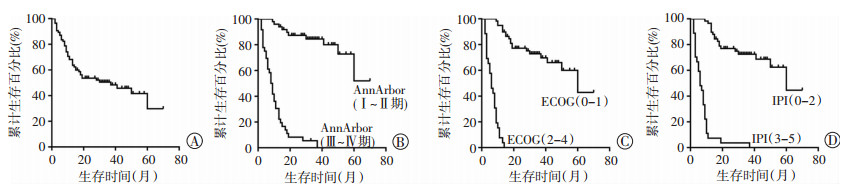
将单因素分析中显示与预后相关的因素纳入Cox比例风险模型进行多因素分析。结果表明:ECOG评分、Ann Arbor分期、IPI评分是NKTCL的独立预后因素(表 3),各独立预后影响因素的生存曲线图(图 1)。
| 因素 | B | SE | P | OR* | 95% CI |
| ECOG评分 | 2.215 | 0.547 | 0.000 | 9.165 | 3.135~26.792 |
| IPI评分 | 1.290 | 0.460 | 0.005 | 3.632 | 1.475~8.940 |
| Ann Arbor分期 | 1.635 | 0.586 | 0.005 | 5.130 | 1.626~16.187 |
| *相对危险度 | |||||
|
| A:总生存率;B:不同AnnArbor分期的生存率;C:不同ECOG评分的生存率;D:不同IPI评分的生存率 图 1 85例NKTCL患者总生存及各独立预后影响因素生存曲线图 |
2.4 NKTCL的治疗方式及疗效分析
85例NKTCL患者住院期间按Ann Arbor分期标准评估后行单纯放疗、单纯化疗、放疗+化疗治疗后,其中位生存时间分别为32.5、34.7、35.8个月,3年生存率分别为66.7%、48.2%、51.9%,5年生存率分别为47.3%、25.6%、30.5%,单因素分析中3组两两之间比较并无统计学差异(表 2)。
3 讨论NKTCL属侵袭性非霍奇金淋巴瘤,确诊依赖早期病理学、分子遗传学及免疫表型的检测[5]。近年来国内外研究者对NKTCL的预后因素进行了研究,如KOMABAYASHI等[6]发现EBV潜伏膜蛋白1(latent mem-brane protein 1,LMP1)可引起miR-15a的下调进而促进细胞增殖,并可作为NKTCL预后的不良因素。目前研究较多影响预后的因素包括性别、年龄、分期及EBV等。本研究通过一次性纳入临床特征、Ann Arbor分期、IPI、ECOG评分、EBV、LDH、病理免疫组化、治疗方案、疗效等对预后的影响因素,经多因素生存统计结果表明Ann Arbor分期、IPI、ECOG可作为NKTCL独立预后参考因素,单因素预后分析结果与国内外多数研究结论多数一致。而现有学者对IPI作为评价NK/T细胞淋巴瘤的预后提出质疑,如XU等[7]对170名ENKL的中国患者进行长期临床随访研究表明,外周T细胞淋巴瘤-非特异型预后指数(peripheral T cell lymphomas-unspecified prognostic index,PIT)相对于IPI对NKTCL预后表现更好,PIT显示年龄>60,LDH>正常,一般行为状态(performance status,PS)≥2分,骨髓受累4个独立因素有更好的预测能力,另外一项由日本学者报道在日本患有101例患者外周T细胞淋巴瘤-非特异型(peripheral T cell lymphomas-unspecified,PTCL-U)或者血管免疫母细胞性T细胞淋巴瘤(angioimmunoblastic T-cell lymphoma,AITL)研究预后中,也证明了上述观点[8]。
血液学指标对预后研究表明,白细胞数异常、贫血、LDH单因素分析中均有意义,但多因素分析中无意义。有研究表明贫血、LDH可作为NKTCL的独立预后因素[9-10]。本研究显示体能状态ECOG已作为独立因素影响该病预后,其中有贫血及淋巴瘤B症状患者若持续存在且进行性加重,本身就能直接影响患者的体能状况评估进一步影响预后,故认为贫血、淋巴瘤B症状可作为鼻型NK/T细胞淋巴瘤的高危预后参考影响因素,但不能作为独立预后因素。而LDH的持续性显著升高对预后有影响得到广泛认可,本研究显示LDH预后高LDH预示患者预后差,其5年总生存率仅有5.7%,特别是LDH数值高于正常高限1.5倍以上更具有评价预后意义,表明LDH在临床诊断NKTCL的分期及预后中具有重要的参考价值。
关于EBV感染与NK/T淋巴瘤的预后关系,多数文献研究报道EBV感染与NKTCL发病机制密切相关,发病机制尚不清楚,目前无大样本研究显示其可作为独立影响NKTCL的预后。本研究发现许多早期患者感染EBV经过治疗后,其预后生存率并非低于非感染EBV的患者,但仍有学者如KOMABAYASHI等[6]认为EBV的LMP-1定量检测可以代替EBV感染存在,而且其量的高低可作为NKTCL的预后影响因子,亦有研究者ITO等[11]认为EBV-DNA定量的高低也可作为NKTCL的预后评价指标,故EBV感染是否能纳入NKTCL的预后评价体系仍无定论。本研究>90%的NKTCL患者表达T细胞内抗原TIA1(+)及GNB,与NK/T淋巴细胞特性相符,而Ki67在Ⅰ/Ⅱ期及Ⅲ/Ⅳ期患者中负荷量相当,单因素分析无明显差异。HUANG[12]等将Ki67作为NKTCL的预后因素结果,认为Ki67是处于增殖周期中的细胞标记,其阳性率越高,肿瘤生长越快,组织分化越差,对化疗越敏感,一般来说预后较差。本研究纳入了NKTCL病理中灶性CD20(特指背景炎症B细胞表达而非肿瘤NK/T细胞本身表达)指标,发现病理灶性CD20(-)ENKT患者较灶性CD20(+)患者预后差,单因素统计中有明显差异性,提示灶性CD20(-)表达在其NKTCL预后起到一定作用。JIANG等[13]报道了NK/T淋巴瘤表达CD20(+)的患者,并追踪患者长期生存率情况发现其预后好、复发率低,可能考虑NK/T淋巴细胞肿瘤具有侵袭性,导致肿瘤及周围组织炎症反应,激活正常B淋巴细胞体液免疫应答并抑制侵袭及炎症。我们统计了EBV与灶性CD20二者表达之间是否具有一致性,运用配对χ2检验结论得出P=0.77>0.05,提示表达相关性上无明显统计学差异性,但两因素进行生存预后分析中发现,灶性CD20(-)和EBV(+)有22例患者其中19例死亡,1年、3年生存率为40.9%、0%,而灶性CD20(+)和EBV(-)有12例,其中6例发生死亡,1年、3年生存率分别为83.3%、56.9%,同时对比单EBV(+)1年、3年生存率分别为48.2%、26.4%,提示灶性CD20的表达与EBV感染有相关性,具有EBV(+)与灶性CD20(-)表达的患者预后较差,二者在NKTCL的发生发展机制中的作用有待研究。
NKTCL的治疗最佳方案迄今仍存于探索中,其原因在于NKTCL对常规化疗的疗效尚不理想,机制多数认为与p53、Fas/FasL基因突变、多重耐药基因(如P-糖蛋白)表达以及血管损害导致药物分部不均有关[14-15]。本文85例患者根据临床分期选择不同治疗方案,其分为单独放疗、单独化疗、放化疗联合三种方案,结果表明其三者的选择对预后没有明显影响,因本文为回顾性研究,结论尚需更多前瞻性研究证实,临床治疗方面亟需寻找更有效的治疗方法,如目前研究前沿的Car-T免疫疗法对于改善预后的作用值得期待。
| [1] | CHEUNG M M, CHAN J K, LAU W H, et al. Early stage nasal NK/T-cell lymphoma: clinical outcome, prognostic factors, and the effect of treatment modality[J]. Inte J Radia Oncol Biol Physic, 2002, 54(1): 182–190. DOI:10.1016/S0360-3016(01)01955-1 |
| [2] | AU W Y, WEISENBURGER D D, INTRAGUMTORNCHAI T, et al. Clinical differences between nasal and extranasal natural killer/T-cell lymphoma: a study of 136 cases from the International Peripheral T-Cell Lymphoma Project[J]. Blood, 2009, 113(17): 3931–3937. DOI:10.1182/blood-2008-10-185256 |
| [3] | MIYAKE M M, OLIVEIRA M V, MIYAKE M M, et al. Clinical and otorhinolaryngological aspects of extranodal NK/T cell lymphoma, nasal type[J]. Braz J Otorhinolaryngol, 2014, 80(4): 325–329. DOI:10.1016/j.bjorl.2014.05.013 |
| [4] |
张之南, 沈悌. 血液病诊断及疗效标准[M]. 3版. 北京: 科学出版社, 2007: 227.
ZHANG Z N, SHEN T. Diagnosis and treatment standards of hematopathy[M]. Third Edition. Beijing: China Science Publishing & Media Ltd, 2007: 227. |
| [5] | JEON Y K, KIM J H, SUNG J Y, et al. Epstein-Barr virus-positive nodal T/NK-cell lymphoma: an analysis of 15 cases with distinct clinicopathological features[J]. Human Pathology, 2015, 46(7): 981–90. DOI:10.1016/j.humpath.2015.03.002 |
| [6] | KOMABAYASHI Y, KISHIBE K, NAGATO T, et al. Downregulation of miR-15a due to LMP1 promotes cell proliferation and predicts poor prognosis in nasal NK/T-cell lymphoma[J]. Am J Hematol, 2014, 89(1): 25–33. DOI:10.1002/ajh.23570 |
| [7] | XU P P, WANG Y, SHEN Y, et al. Prognostic factors of Chinese patients with T/NK-cell lymphoma: a single institution study of 170 patients[J]. Med Oncol, 2012, 29(3): 2176–2182. DOI:10.1007/s12032-011-0011-0 |
| [8] | NIITSU N, OKAMOTO M, NAKAMINE H, et al. Clinico-pathologic features and outcome of Japanese patients with peripheral T-cell lymphomas[J]. Hematol Oncol, 2008, 26(3): 152–158. DOI:10.1002/hon.853 |
| [9] |
徐刚, 王槐富, 杜泽秀, 等. 鼻腔NK/T细胞淋巴瘤预后相关因素分析[J].
中国耳鼻咽喉头颈外科, 2007, 14(7): 393–396.
XU G, WANG H F, DU Z X, et al. Prognostic factors of nasal NK/T-cell lymphoma[J]. Chin Arch Otolaryngol-Head Neck Surg, 2007, 14(7): 393–396. DOI:10.3969/j.issn.1672-7002.2007.07.001 |
| [10] |
王存, 江波, 王瑜, 等. 血清LDH值与非霍奇金淋巴瘤临床关系分析[J].
中华肿瘤防治杂志, 2003, 10(7): 730–731.
WANG C, JIANG B, WANG Y, et al. Analysis of clinicaI relation between serum LDH level and NHL[J]. Chin J Cancer Prevent Treat, 2003, 10(7): 730–731. |
| [11] | ITO Y, KIMURA H, MAEDA Y, et al. Pretreatment EBV-DNA copy number is predictive of response and toxicities to SMILE chemotherapy for extranodal NK/T-cell lymphoma, nasal type[J]. Clin Cancer Res, 2012, 18(15): 4183–4190. DOI:10.1158/1078-0432.CCR-12-1064 |
| [12] | HUANG X, SUN Q, FU H, et al. Both c-Myc and Ki-67 expression are predictive markers in patients with extranodal NK/T-cell lymphoma, nasal type: a retrospective study in China[J]. Pathol Res Prac, 2014, 210(6): 351. DOI:10.1016/j.prp.2014.02.004 |
| [13] | JIANG Q, LIU S, YANG Y, et al. CD20-positive NK/T-cell lymphoma with indolent clinical course: report of case and review of literature[J]. Diagn Pathol, 2012, 7(1): 133. DOI:10.1186/1746-1596-7-133 |
| [14] | KIM K, CHIE E K, KIM C W, et al. Treatment outcome of angiocentric T-cell and NK/T-cell lymphoma, nasal type: radiotherapy versus chemoradiotherapy[J]. Japan J Clin Oncol, 2005, 35(1): 1. DOI:10.1093/jjco/hyi006 |
| [15] | LI T, HONGYO T, SYAIFUDIN M, et al. Mutations of the p53 gene in nasal NK/T-cell lymphoma[J]. Lab Invest, 2000, 80(4): 493. DOI:10.1038/labinvest.3780055 |



